TiO2@MOFs 光催化材料的研究进展与展望
2021-11-03胡金涛孙小卫邓佳乐
胡金涛,高 娟,孙小卫,邓佳乐,刘 美
(安徽理工大学 力学与光电物理学院,安徽 淮南 232000)
金属有机骨架(Metal-Organic Frameworks),简称MOFs,是由有机配体和金属离子或团簇通过配位键自组装形成的具有分子内孔隙的有机-无机杂化材料[1-2]。MOFs 具有广阔的比表面积、可调谐的孔径和结构以及丰富的活性中心等优点[3-5]。然而,MOFs 也存在不足之处,其结构易受环境中水、氧气或溶剂影响而发生坍塌,部分MOFs 的耐真空或低温能力差[6-7]。二氧化钛(TiO2)是最成熟的半导体光催化剂之一,作为光催化剂,TiO2由于其成本低,无毒,光催化活性高,是最有前途的光催化剂之一[8-10]。然而,由于纯TiO2纳米的团聚而对催化能力产生不利影响,此外,光生载流子的快速复合也阻碍了光催化活性的提高[10-11]。为了进一步提高TiO2与MOFs 的性能和实用性,科研工作者开始致力于TiO2@MOFs复合材料的探讨与研究[13-14]。本文探讨了由TiO2与MOFs 形成复合材料的研究进展,主要包括复合材料的制备方法、形貌结构,以及它们的应用。
1 TiO2@MOFs 复合材料制备的方法
1.1 水热法
水热法是合成TiO2@MOFs 材料常见的方法之一。高温高压的水溶液使那些在大气条件下不溶或难溶于水的物质通过溶解或反应生成该物质的溶解产物,并达到一定的过饱和度而进行结晶和生长的方法[15]。
He[16]等人通过一个典型的合成过程,首先将P25 与Fe(NO3)3· 9H2O 溶液混合加热处理,将FeOOH 转化为MIL-100(Fe),得到MIL-100(Fe)/P25 复合材料。研究表明原始P25 颗粒为单分散纳米晶,表面非常光滑直径约为25nm。并且随着Fe(NO3)3·9H2O 浓度的增加,使得FeOOH 棒越来越长。为进一步研究MIL-100(Fe)/TiO2类型复合材料,Wu[17]等人通过简单的两锅水热法成功地合成了一种类似鸡蛋的TiO2/MIL-100(Fe)复合纳米材料,其中锐钛矿型TiO2的{001}和{101}面共同暴露。该材料在相同的制备条件下比纯MIL-100(Fe)具有更高的比表面积和孔径。另外Duan[18]等人通过简单的水热法制备了PCN-222(Cu)/TiO2复合材料材料。将TiO2均匀的锚定在PCN-222(Cu)棒表面,其中PCN-222(Cu)和TiO2的结合可以有效地减少TiO2纳米粒子的团聚,改善了TiO2较宽的禁带宽度和光生载流子的复合。
综上所述,水热法是一种有效的,常用的制备TiO2@MOFs 复合材料的方法,并且实现了利用MOFs 的比表面积、平均孔径等优异特性。但该方法理论模拟与分析困难,重现性差,参量调节困难。
1.2 溶剂热法
溶剂热法是水热法的发展,它与水热法的不同之处在于所使用的溶剂为有机溶剂而不是水[19-21]。在溶剂热反应中,通过把一种或几种前驱体溶解在非水溶剂中。
Chang[22]等人基于MIL-101 材料作为核心模板,首先合成了单分散MIL-101,其晶体表面光滑,边缘清晰,再通过溶剂热法制备了TiO2@MIL-101 核壳结构,其中MIL-101 被TiO2纳米粒子均匀包覆。之后Chang[23]等人通过类似的合成流程,以简单的溶剂热法合成了以MIL-101 为支撑吸附多孔材料,TiO2为涂层光活性材料,成功制备出TiO2@MOFs 纳米复合材料,与MIL-101 相比,制备的TiO2@MIL-101 纳米复合材料具有较高的吸附性能和较大的比表面积,归因于TiO2晶体涂层对表面电荷的调节。Li[24]等人以一种方便的一步溶剂热法,加热MOFs 和TiO2前驱体的混合物制备出了锚定在NH2-MIL-88B(Fe)上的TiO2,其中柳絮状TiO2紧密附着在Fe-MOF 表面,异质结的形成大大提高了Fe-MOF 与TiO2之间的吸附容量,改善了催化剂的光催化性能。
溶剂热法作为合成方法,使得物相的形成、粒径的大小、形态能够控制,而且产物的分散性较好。在溶剂热条件下,溶剂的性质(密度、粘度、分散作用)相互影响,变化很大,且其性质与通常条件下相差很大,相应的,反应物(通常是固体)的溶解、分散以及化学反应活性大大的提高或增强[25-26]。
1.3 溶胶-凝胶法
溶胶(Sol)是具有液体特征的胶体体系,分散的粒子是固体或者大分子,分散的粒子大小在1-1000nm 之间。凝胶(Gel)是具有固体特征的胶体体系,被分散的物质形成连续的网状骨架,骨架空隙中充有液体或气体,凝胶中分散相的含量很低,一般在1%-3%之间[27]。
Tuncel[28]等人通过采用溶胶-凝胶法制备了以四异丙氧钛(Ti(OC3H7)4)和乙酸(CH3COOH)为前驱体的TiO2纳米粉末,之后成功地将TiO2光催化剂与Cu-BTC 金属有机骨架偶联,形成了杂化多孔纳米复合材料。研究表明杂化多孔结构建立的协同作用促进了辐射时电子空穴对的分离,并提高了光催化性能。
对于溶胶-凝胶法其优势有起始原料是分子级的能制备均匀纯度高的材料;组成成分较好控制,尤其适合制备多组分材料;可以控制孔隙度,容易制备出各种形状[29]。然而较长的反应时间,且有机溶剂对人体有一定的危害性。
1.4 其他方法
除了上述所介绍的合成方法,TiO2@MOFs 复合材料还可以利用其它方法复合。其中模板法是以模板为主体构型去控制、影响和修饰材料的形貌,控制尺寸进而决定材料性质的一种合成方法。如图1 所示,Zhang[30]等人首先以聚苯乙烯(PS)纳米球作为制备TiO2空心纳米球的合成模板,然后利用退火去除PS@TiO2核壳颗粒模板,得到了TiO2空心纳米球,再将ZIF-8 生长在TiO2空心纳米球的表面。其中可通过超声结晶抑制ZIF-8 的自核生长。最后成功合成了双壳层TiO2@ZIF-8 空心纳米球。

图1 双壳TiO2@ZIF-8 空心纳米球合成示意图[30]
钛及其合金的阳极氧化是一种重要的表面处理,特别是在附着力方面。其中二氧化钛(TiO2)纳米管阵列由Zwilling[31]等人在1999 年首次通过阳极氧化法制备。Xue[32]等人在此背景下,以钛箔为阳极,铂箔为阴极的两电极体系,两步阳极氧化法制备了TiO2纳米管阵列,再通过传统的溶剂热生长方法成功的制备出了MIL-125 和NH2-MIL-125修饰的TiO2纳米管阵列。Pipelzadeh[33]等人通过相对简单的制备方法,首先将TiO2(P25)分散在硝酸锌(100 mmol)溶液中超声处理5 分钟,悬浮液以4500 rpm 转速离心后洗涤,随后,在再分散的TiO2纳米粒子悬浮液中加入2-甲基-咪唑(100 mmol),在TiO2表面形成了ZIF-8 涂层,超声、洗涤、煅烧等操作后得到TiO2@ZIF-8 核壳型纳米复合材料。
2 TiO2@MOFs 复合材料的应用
2.1 光催化降解
随着社会的发展,工业上废水的排放,农业上的农药滥用等,使得水体中有害污染物对水生生物以及人类造成了极大危害,利用TiO2@MOFs复合材料能有效的降解污染物。Li[24]等人将TiO2锚定在MOFs(NH2-MIL-88B(Fe)上,制备出了一种新型光催化剂,并且借助可见光对有机染料亚甲基蓝(MB)进行了有效光催化降解。如图2(a)所示研究表明在吸附1.5 h,光降解2.5 h 后,样品SU-3 复合材料可以去除100%(31%的吸附和69%的降解)的MB。光催化活性的增强可归因于异质结的形成,从而有利于协同吸附和光催化降解。同时还研究了可见光、H2O2和光催化剂等不同参数的影响。如图2(b)所示当MB 只暴露在可见光下2.5 h 时,没有观察到分解,表明MB 在水中是稳定的。加入H2O2后,MB 的降解效率在2.5 h 内达到5%,表明用H2O2进行可见光照射导致MB 在没有催化剂的情况下适度降解。没有H2O2,仅在可见光照射下使用SU-3 复合材料,少量MB 被降解,这可能是由于通过空气中的氧形成的超氧自由基捕获电子。此外,在H2O2和不照射可见光的情况下,MB 的吸附和降解在SU-3 复合材料上可以达到45%,充分证明了SU-3 复合材料可以作为光催化剂来降解MB,类似于Fe2O3。相同的反应条件下降解5 次,降解效率也没有明显下降,表明SU-3 是稳定的和可回收的,这对于它在实际应用中是至关重要的。
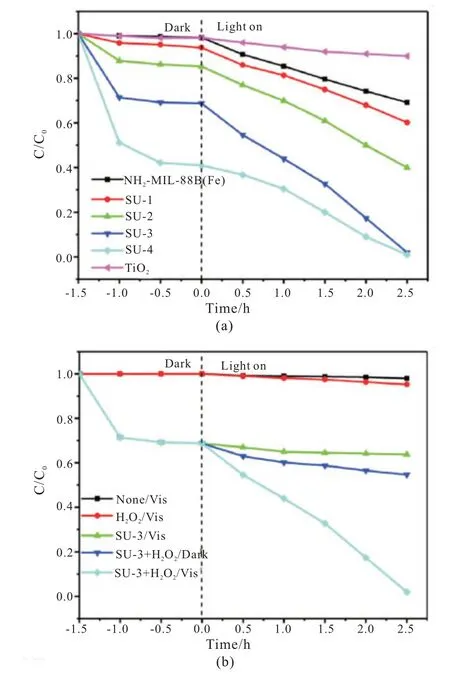
图2 (a)不同样品下MB 的降解(b)在不同条件下MB 的降解。(反应条件:50mL 的100mg/L MB 溶液,10mg 光催化剂(0.2g/L),100μL H2O2(20mM),pH 为7)[24]
Li[34]等人通过水热法制备了ZIF-8@TiO2微米复合材料,这是一种新型的高效光催化剂。在ZIF-8 表面均匀生长TiO2纳米球,其中ZIF-8@TiO2复合材料还保持了十二面体轮廓,具有相对钝的边缘和粗糙的表面,大大减弱了TiO2的团聚,提高了催化能力。通过对四环素(TC)的降解来评估催化剂的光催化性能。如图3(a)中所示在没有任何催化剂的情况下,TC 的降解很少,表明TC 在模拟太阳光照射下是稳定的,TiO2,ZIF-8 催化剂在黑暗中具有显著的吸附能力。其中ZIF-8@TiO2吸附率超过40%,ZIF-8 吸收率接近40%,这可能是由于它们具有较高的孔隙率和高比表面积。当辐照时间达到40 min 时,ZIF-8@TiO2复合材料的降解率近90%,而TiO2和ZIF-8 对TC 的降解率均小于70%。如图3(b)中所,其中ZIF-8@TiO2复合材料的光催化速率最高(k=0.034 min-1)),分别约为ZIF-8 的2.6 倍和纯TiO2的1.4倍。在相同的条件下进行了5 次光降解循环后,ZIF-8@TiO2复合材料在回收实验中具有良好的稳定性和可重用性,其内部的相互作用使其能够保持原来的高效率性能。Wu[17]等人通过水热法制备了蛋状的TiO2/MIL-100(Fe)复合材料,并研究了各个样品对亚甲基蓝(MB)的降解与吸附能力。与纯TiO2、MIL-100(Fe)相比不同摩尔比的TiO2/MIL-100(Fe)材料光催化性能明显改善,随着TiO2的加入,TiO2/MIL-100(Fe)复合材料的光催化MB降解效率明显高于MIL-100(Fe)。由于高的比表面积和大孔径有利于有机染料MB 的捕获发光体和提供反应位点,同时,TiO2共暴露的{001}和{101}晶面之间的协同作用也能有效地促进光载流子的分离,进一步提高光催化效率。Binh[18]等人制备了一种新型的基于Cu-MOF 的二氧化钛光催化剂,这种复合材料表现出较高的光催化分解MB 染料的性能,可归因于蓝色Cu-MOF 在可见光区域对TiO2的光谱敏化;具有较高的孔隙率和较大的比表面积;Cu-MOF 作为模板可以形成非常精细的TiO2纳米材料。Nguyen Thanh Binh[35]等人采用水热法合成了比表面积为1350m2/g 的Cu3BTC2金属有机骨架(MOFs),然后在水热条件下水解制得TiO2@Cu3BTC2光催化剂。并且通过紫外光-可见光照射MB 进行光催化降解,与掺杂TiO2的Cu3BTC2相比,纯Cu3BTC2的光催化活性可以忽略不计,而TiO2@Cu3BTC2几乎在暴露于光下1 分钟后立即观察到降解,可归因于材料的高孔隙率和大的比表面积。Okte[36]等人通过在Cu-BTC 和ZIF-8 表面负载TiO2,成功制备了负载型纳米复合材料,并研究了对亚甲基蓝(MB)和甲基橙(MO)的脱色作用。静电的相互作用和在载体和染料分子内的官能团的存在导致了复合材料对MB 和MO 的催化差异。
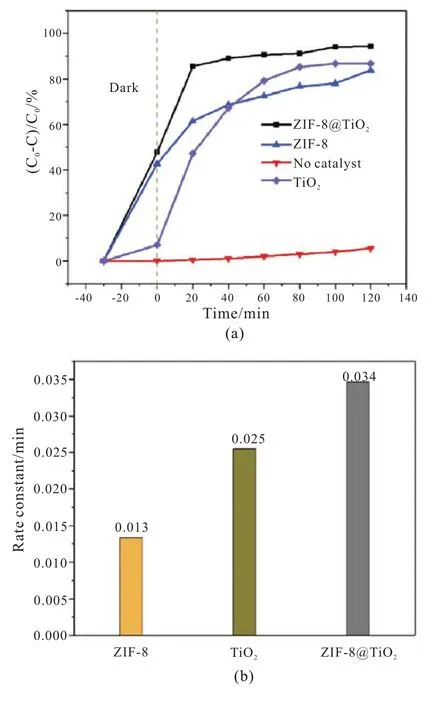
图3 (a)ZIF-8@TiO2、TiO2和ZIF-8 光催化降解TC 的效率;(b)制备样品的反应速率常数。[34]
2.2 CO2还原
近些年,化石燃料日益消耗使得大气中CO2含量增加,造成的环境污染等问题,推进实现CO2资源化转化的研究课题备受关注[37-38]。在解决温室效应等环境问题同时实现碳资源循环利用,对解决环境污染实现可持续发展具有十分重要的意义。Duan[19]等人通过水热法设计和构建了一种新型纳米棒PCN-222(Cu)/TiO2复合材料,其中TiO2均匀分布在PCN-222(Cu)表面,对于易团聚的TiO2纳米粒子,PCN-222(Cu)和TiO2的结合有效地减少TiO2纳米粒子的团聚现象。与TiO2相比,PCN-222(Cu)/TiO2纳米结构表现出更优异的催化性能。在300W Xe 灯下进行了光催化性能测试,
如图4(a)中所示不同比例的PCN-222(Cu)/TiO2复合材料表现出不同的CO2转化效率,呈现出先增加后降低的趋势,并且所有复合样品均比纯TiO2具有更高的CO2光催化还原活性。在所有制备的复合材料中,10%PC N-222(Cu)/TiO2的复合材料催化速率最好,从还原产物CO 的产率来看,10%PC N-222(Cu)/TiO2是TiO2的三倍。高的光催化活性主要是由于PCN-222(Cu)和TiO2的结合,提高了可见光吸收能力,加快了光生电子的传输效率,此外,复合材料的协同作用有效地提高了TiO2纳米粒子的分散性,为CO2和催化剂之间的接触提供了更多的反应位点。如图5(b)、(c)中所示在三次循环后,观察到的还原产物量基本保持不变,表明10%PC N-222(Cu)/TiO2复合材料光催化中的的稳定性更好,对催化剂进行了连续8h 的测试,CO 和CH4的产量增加,表明该光催化剂在整个试验过程中仍然具有催化活性。Angus Crake[39]等人通过溶剂热法制备了TiO2纳米片,再通过原位生长策略有效地耦合TiO2纳米片和金属-有机骨架(NH2-UIO-66),形成双功能材料,用于捕获和光催化还原在紫外光照射下的CO2,以H2为牺牲剂,在气相中只检测到CO 为产物。与纯TiO2相比,最佳的复合材料的CO 演化率增加了约1.9 倍。催化剂较好的催化活性可归因于复合材料的异质结构,并且较高的比表面积,可以抑制TiO2的团聚,暴露出更多的活性位点。由于MOF中孔隙度的存在,促进了CO2与催化剂中心的密切接触。之后Angus Crake[40]等人进一步研究气相CO2光还原的调控因素是较大的孔隙率的积累,异质结组分之间有大量的接触点,提高了电荷转移,利用多孔材料可以满足前者的要求,通过控制异质结组分的形貌来满足后者的要求。因此制备了TiO2和钛酸盐与MOFs 的复合材料。Wang[41]等人采用水热原位生长法成功地制备CTU/TiO2复合光催化剂,所得杂化物的光催化性能与TiO2和CTU 相比明显改善。并且光催化剂CTU/0.6TiO2的CO 产率为31.32μmol g-1h-1是原始TiO2的7 倍,主要是由于光生电荷的分离效率增强,其中MOFs 能够极大地改善TiO2颗粒的分散性,与原始TiO2相比,能够提供足够的反应位点,提高捕获CO2的能力。此外,异质结的形成使得复合材料在光催化CO2还原过程中显示出高度稳定性和可回收性。

图4 (a)在Xe 灯下TiO2和不同比例的PCN-222(Cu)/TiO2 1 小时内CO/CH4 释放总量(b)在10%PCN-222(Cu)/TiO2的基础上,CO2还原的三个循环。(c)在8 小时内用Xe灯测定10%PCN-222(Cu)/TiO2 CO/CH4的含量[19]
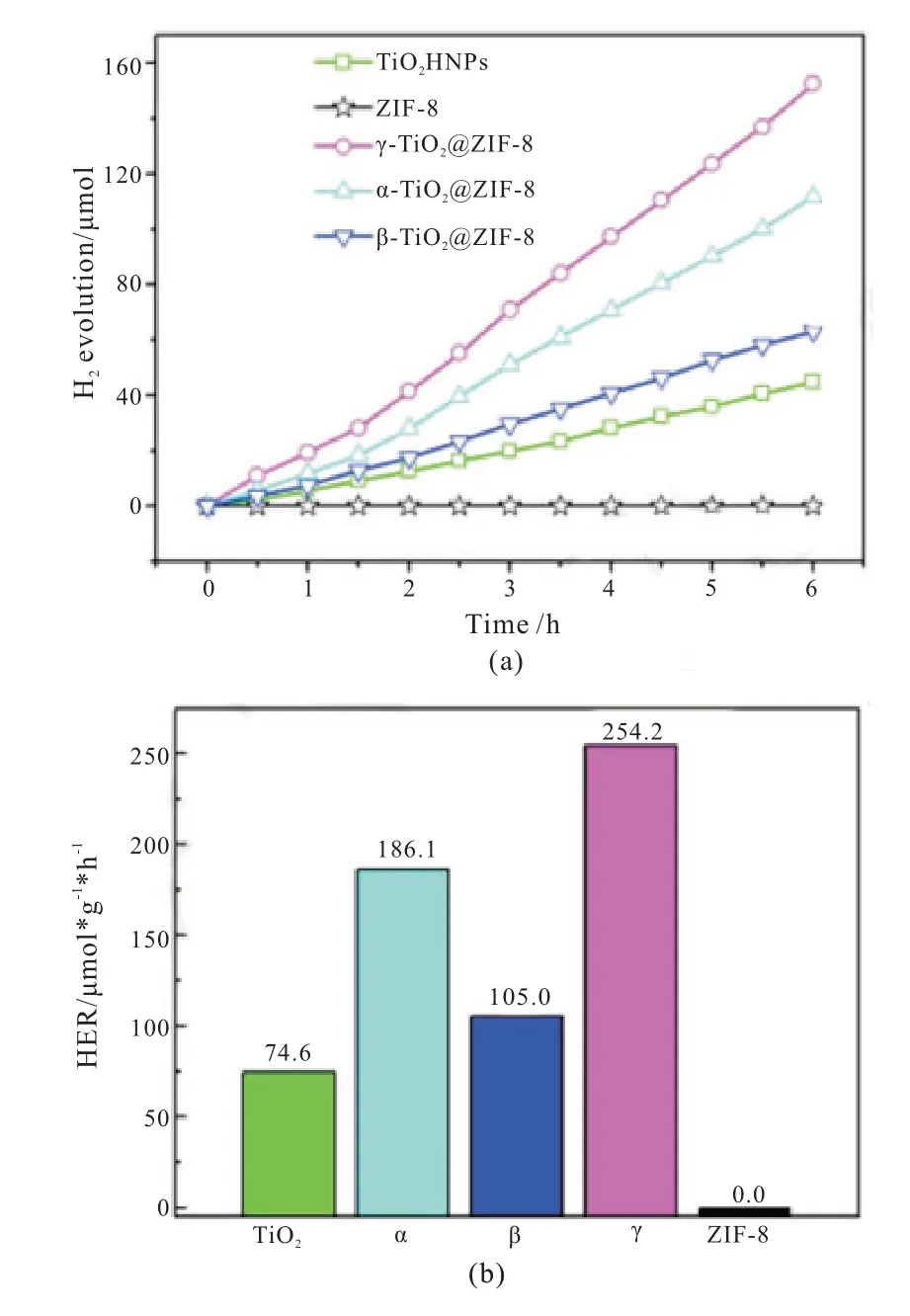
图5 (a)TiO2空心纳米球、ZIF-8 和α-/β-/γ-TiO2@ZIF-8 的光催化析氢性能;(b)H2演化速率。[30]
2.3 产氢
由于化石燃料的不可持续性,以及在燃烧中造成的环境污染,使得H2成为取代化石燃料的新型能源之一[42-43]。Stavroula Kampouri[44]等人通过温度控制二氧化钛的锐钛矿相和金红石相之间的组成,制备出不同的MIL-125-NH2衍生TiO2复合材料,并保留了MIL-125-NH2的晶体形状,衍生出的TiO2具有圆角矩形,其尺寸大小与温度有关。然后研究了MIL-125-NH2衍生TiO2 在水中光催化H2演化性能,组成为66wt%TiO2锐钛矿和34wt%TiO2金红石的样品的H2演化速率最高为1394μmol h-1g-1,具有更多TiO2金红石相的材料表现出其光催化性能的恶化。光催化活性的提高可归因于材料之间协同效应所致,大大增加了电荷载流子的分离,最终催化H2演化反应。
Zhang[30]等人通过聚苯乙烯纳米球为模板,设计并合成了双壳层TiO2@ZIF-8 空心纳米球。以甲醇溶液为牺牲量,在模拟太阳光照射下,用水析氢法评估了制备样品的光催化性能。如图5 所示,由于其可见光吸收能力差,在裸ZIF-8 存在下,不能检测到H2的演化。裸TiO2空心纳米球表现出较低的光催化性能,归因于其较小的比表面积和电荷载流子的快速复合,而γ-TiO2@ZIF-8 以152.54μmol g-1h-1表现出最明显的H2演化(HER 为254.2μmol g-1h-1),约为裸TiO2空心纳米球的3.4倍。对γ-TiO2@ZIF-8 的进行了5 次连续的光催化反应,第五次循环中的HER 值保持不变与第一个循环中的量几乎相同,证明了γ-TiO2@ZIF-8 的优异光催化稳定性。Wang[45]等人利用Cu 的有机骨架材料Cu-MOF(CuBTC)中金属离子高度有序的特性,基于高比表面的介孔TiO2载体,通过煅烧前驱体CuBTC-TiO2复合物制备纳米负载型CuOTiO2催化剂,平均产氢速率达到0.32 mmol/(g·h),在多次循环实验中产氢速率没有明显下降趋势,稳定性较好。Zhang[46]等人通过控制MOFs 前驱体分解的溶剂热路线,制备出MIL-125-NH2@TiO2核壳型纳米颗粒,具有与MIL-125-NH2光敏剂相互作用的高活性TiO2纳米片,大量的连接体缺陷和氧空位以及介孔结构有利于光催化活性。复合材料在可见光下的制氢活性比纯MIL-125-NH2高70 倍,此外,由于TiO2外壳对MIL-125-NH2的保护,大大提高了光催化剂的稳定性和可回收性。
2.4 其他
作为电池中最重要的三个部分,阳极、阴极和电解质。MOFs 材料在电池中作用越来越广泛,由于其高的比表面积和孔隙率有利于电子的迁移,同时良好的化学稳定性也促进了电池的循环使用[47-48]。Yoon[49]等人通过简单的水热反应将MIL(125)-NH2(Ti)[MOFs]层均匀地包覆在垂直有序的TiO2纳米棒(NRS)上作为光阳极,并研究了异质结光阳极在光电化学(PEC)水裂解中的性能。在模拟太阳光照下,MIL(125)-NH2/TiO2NRs在1.23 V 下的光电流密度达到1.63mA/cm2,约为原始的TiO2纳米棒的2.7 倍。复合材料通过有效的光吸收和电荷分离来促进水的氧化,半导体与MOF 之间异质结的合理设计,为水的裂解提供新的思路。Zhang[50]等人通过对Ti 基于金属-有机骨架模板进行退火,制备了多孔饼状TiO2。材料作为钠离子电池的阳极时,在电流密度为50mA g-1时,经过50 次循环后,最大充电容量为250mA g-1,在2500 次循环后,即使在1A g-1的大电流密度下,也能提供173m A g-1的非常稳定的可逆容量,其优异的电化学性能归功于独特的多孔结构和合适的孔径。之后Zhang[51]等人通过类似的方法制备了多孔饼状的锐钛矿型TiO2,并将其作为染料敏化太阳能电池(DSSCs)中的有效散射层。作为有效散射层的DSSCs 表现出光电效应转化率(PCE)为6.91%,大于单P25(TiO2)基DSSCs(3.89%)。其中光电转换效率的提高归因于多孔饼状TiO2在促进比表面积和入射光散射性能方面的关键作用。
利用MOFs 构建具有高表面积、可预测结构和可调谐孔径的多孔复合材料,以实现传感方面的应用[52-54]。Wang[55]等人通过简单的水热反应制备了UIO-66-NH2/TiO2纳米复合材料,应用于电化学生物传感器中。结果表明,UiO-66-NH2/TiO2晶体呈球状,两种纳米复合材料具有更明显、更好的分散性。利用UiO-66-NH2/TiO2纳米复合材料构建一种高选择性和灵敏的电极材料,用于检测水溶液中的绿原酸。最低检测限为7 nmol L-1,线性范围为0.01-15.0 μmol L-1,观察到的超低检测限可归因于UIO-66-NH2和TiO2的协同效应。此外,UIO-66-NH2/TiO2复合材料在至少90 个周期后和在酸性条件下,都具有良好的稳定性。
3 结论与展望
TiO2@MOFs 复合材料合理的利用二氧化钛的半导体性质和MOFs 高比表面积、可调孔径、良好热稳定性等性能而逐渐受到人们的关注。TiO2与MOF 之间形成的界面提高了光吸收性能,改善了电子空穴对的分离。此外,为了进一步提高光催化活性,研究人员通过设计合成特定的形貌,如空心纳米球、纳米棒、纳米片等形貌。从发展与应用前景来看,TiO2@ MOFs 复合材料在光催化降解、CO2还原、产氢等相关领域显示出了良好的应用前景,但是其工业应用仍然面临着一些挑战,首先在制备方法上,目前的方法步骤繁琐且仅限于实验室合成,因此开发简单高效的工业化生产制备方法具有重要意义。并且在功能材料选择上,二氧化钛和MOFs 仍存在一定的缺陷,使得复合材料的性能难以控制。最后相信经过国内外研究者的共同努力,TiO2@ MOFs 复合材料在工业上的应用能够尽快实现。
