一种8-羟基喹啉衍生物的制备及其对Mg2+的检测
2021-11-03付振海李志伟秦敬灿张志宏
付振海,王 敏,李志伟,秦敬灿,苏 彤,张志宏
(1. 中国科学院青海盐湖研究所,中国科学院盐湖资源综合高效利用重点实验室,青海 西宁 810008;2. 青海省盐湖资源化学重点实验室,青海 西宁 810008;3. 中国科学院大学,北京 100049)
Mg2+是人体细胞中含量最高的二价金属阳离子,在细胞中扮演着十分重要的角色。Mg2+能够参与核酸和蛋白质的合成及能量代谢,调控细胞的分化,增强酶的催化功能,影响Ca2+和K+的转运并在许多生理活动方面发挥着重要作用[1]。从健康角度考虑,镁离子摄取过量或者缺乏都会导致很多疾病,如:心脏病、神经病、糖尿病、心脑血管疾病及帕金森综合症等[2-3]。因此,开发对Mg2+的高效检测方法具有重要意义[4]。
荧光探针法因合成简单、使用方便、高灵敏度和高选择性等特点,成为近些年的研究热点[5-6]。目前,已报道的Mg2+荧光探针主要集中在希夫碱、香豆素、喹啉、冠醚、二酮等结构[7-11]。然而,由于同主族的Ca2+与Mg2+化学性质相似,导致Mg2+的检测易受到Ca2+的干扰[12-13]。因此,研究高选择性识别镁离子的荧光探针具有一定挑战性。
由于8-羟基喹啉及其衍生物具有较强的配位能力,其分子内光诱导质子转移效应(PPT,Intermolecular photoinduced proton transfer)使得分子无法发出荧光[14],而与金属离子配位后可消除该效应[15]。基于此,本研究首先根据Reimer-Tiemann 反应合成中间体8-羟基喹啉-5-醛,随后利用8-羟基喹啉-5-醛与苯甲酰肼反应制备出希夫碱化合物HQL,改善8-羟基喹啉荧光性能并用于识别Mg2+。
1 实验部分
1.1 试剂与仪器
1.1.1 试 剂 8-羟基喹啉、4-羟基-1-萘甲醛、丙酮、氯仿、石油醚、乙酸乙酯、苯甲酰肼、氢氧化钠均为市售分析纯试剂,未经处理直接使用。反应中所用的甲醇、乙醇等溶剂均为分析纯。测试中所用阳离子盐为氯化物或硝酸盐;测试及配制溶液所用乙醇和二甲基亚砜(DMSO)均为分析纯,未经处理直接使用;测试及配制溶液所用水为去离子水。
1.1.2 仪 器 JEOL JNM-ECS 400 MHz、INOVA 600 MHz 液体超导核磁共振波谱仪(1H 和13C NMR),Bruker microTOF(ESI-TOF MS)质谱仪,Hitachi F-7000荧光光谱仪,UV-VIS2600紫外吸收光谱仪,Seven Excellence Multiparameter pH 酸度计。
1.2 探针合成
1.2.1 探针HQL的合成 探针HQL的合成路线如下所示:

8-羟基喹啉-5-醛的合成:称取(14.5 g,0.1 mol)8-羟基喹啉置于500 mL的三口圆底烧瓶中,加入70 mL 无水乙醇并搅拌。同时称取37 g NaOH 溶解于63 g 去离子水中,将此NaOH 溶液滴加至烧瓶中,此时体系颜色迅速变为黄色,有部分固体产生。将三口圆底烧瓶置于油浴中加热至110 ℃回流几分钟至固体全部溶解,然后降温并保持在75 ℃左右。用注射器将30 mL 氯仿缓慢加入至体系中反应,此时溶液颜色由黄色逐渐变为黑色,保持温度70 ℃搅拌12 h。待温度降至室温,用稀释好的1.0 mol/L盐酸调至pH 中性,过程中有大量黄褐色沉淀析出,搅拌0.5 h 左右,抽滤,并用水进行洗涤,将分离得到的黄褐色固体室温下晾干。对固体进行硅胶柱色谱分离,淋洗剂为石油醚-乙酸乙酯体系(10∶1~5∶1,体积比),得到粉红色固体(3.57 g,产率20%)。1H NMR(DMSO-D6,400 MHz):δ11.17(s,1H),10.13(s,1H),9.55(dd,J=8.4,1.6 Hz,1H),8.97(dd,J=4.0,1.6 Hz,1H),8.16(d,J= 8.4 Hz,1H),7.78(dd,J= 8.8,4.4 Hz,1H),7.25(d,J= 8.0 Hz,1H)ppm;13C NMR(DMSO-D6,100 MHz):δ192.2,159.6,148.9,140.3,138.0,133.1,126.8,124.6,122.4,110.9 ppm;ESI-MS:m/z174.1[M+H]+。
荧光探针HQL 的合成:称取8-羟基喹啉-5-醛173 mg,置于50 mL 单口圆底烧瓶中,加入15 mL 甲醇,搅拌10 min后加入226.7 mg苯甲酰肼,将圆底烧瓶置于油浴中,调节温度至68 ℃回流过夜。观察有沉淀析出,过滤并用甲醇洗涤后得黄色粉末(169 mg,产率58%)。1H NMR(DMSO-D6,400 MHz):δ11.80(s,1H),10.42(s,1H),9.61(d,J= 8.8 Hz,1H),8.94(d,J= 2.8 Hz,1H),8.83(s,1H),7.95(d,J= 7.2 Hz,2H),7.78(d,J= 8.0 Hz,1H),7.74(dd,J= 8.8,4.0 Hz,1H),7.63-7.59(m,1H),7.57-7.53(m,2H),7.17(d,J= 8.0 Hz,1H)ppm;13C NMR(DMSO-D6,100 MHz):δ154.9,153.1,148.2,139.9,139.2,138.3,132.6,128.7,128.5(2C),126.3,122.7,122.4,120.4,119.8(2C),111.3 ppm;ESI-MS:m/z292.2[M+H]+。
1.2.2 分子HNL的合成 分子HNL的合成路线为:

HNL 的合成:称取4-羟基-1-萘甲醛258 mg,置于50 mL 单口圆底烧瓶中,加入20 mL 乙醇,搅拌10 min后加入265.5 mg苯甲酰肼,将圆底烧瓶置于油浴中,调节温度至78 ℃回流过夜。冷却至室温后有沉淀析出,过滤并用乙醇洗涤后得粉末(220.1 mg,产率50.5%)。1H NMR(DMSO-D6,600 MHz):δ11.90(s,1H),10.92(s,1H),9.07(s,1H),9.04(d,J=6.0 Hz,1H),8.34(d,J=12.0 Hz,1H),8.04(d,J= 6.0 Hz,2H),7.84(d,J= 6.0 Hz,1H),7.67-7.64(m,1H),7.57-7.52(m,4H),7.05(d,J= 12.0 Hz,1H)ppm;13C NMR(DMSO-D6,100 MHz):δ163.2,156.0,149.0,133.8,131.9,131.7,130.4,128.6(2C),127.8,127.7(2C),125.2,124.9,124.5,122.9,120.6,108.2 ppm。
1.3 荧光测试
测试所用金属离子Li+、Na+、K+、Rb+、Cs+、Mg2+、Ba2+、Ca2+、Sr2+、Cd2+、Zn2+、Mn2+、Ni2+、Cr3+、Cu2+、Fe2+、Fe3+和Co2+的储备液用去离子水配制,探针分子HQL和分子HNL 的储备液(10.0 mmol/L)用DMSO 配制。取2.0 mL 二甲基亚砜-4-羟乙基哌嗪乙磺酸(DMSO-HEPES)缓冲溶液(20 mmol/L,pH 7.0,95∶5,体积比,下同)作为测试溶剂。激发波长为420 nm,激发和发射狭缝均为5.0 nm。
2 结果与讨论
2.1 探针对Mg2+的荧光识别
首先研究了探针HQL 对金属离子的荧光光谱响应。如图1 所示,在420 nm 光照激发下,探针HQL 的溶液几乎没有荧光峰,这归因于探针结构中8-羟基喹啉的分子内光诱导质子转移效应。分别加入金属离子Li+、Na+、K+、Rb+、Cs+、Mg2+、Ba2+、Ca2+、Sr2+、Cd2+、Zn2+、Mn2+、Ni2+、Cr3+、Cu2+、Fe2+、Fe3+和Co2+,其中Mg2+、Cd2+、Zn2+的加入使得探针溶液荧光增强。当加入Mg2+后,探针体系在577 nm 处发出较强的荧光峰,加入Ca2+后荧光峰无显著变化,而已报道的Mg2+荧光探针主要在有机溶剂中使用,可能会受到Ca2+的干扰[3,13,16-18]。相比之下,探针HQL 在含5%水-有机溶剂(DMSO-HEPES 缓冲液)混合体系中对Mg2+表现出较好的选择性,具有较强的应用性能。此外,加入Cd2+和Zn2+后,体系分别在604 nm 和611 nm 处出现不同强度的荧光峰。这些变化表明探针HQL 能够以荧光增强响应模式,利用发射峰强度和波长区分识别Mg2+和Ca2+、Cd2+和Zn2+。
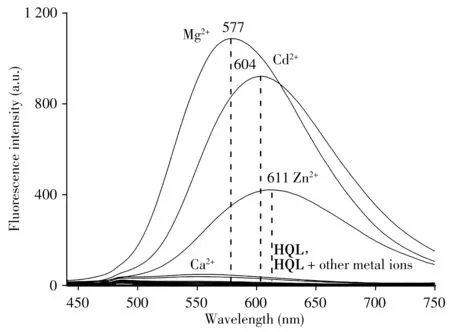
图1 探针HQL(10.0 μmol/L)对金属离子(1.0 mmol/L)的荧光响应光谱Fig.1 Fluorescence response of probe HQL(10.0 μmol/L)to various metal ions(1.0 mmol/L)
为进一步考察探针对Mg2+的选择性,进行了其他阳离子对HQL-Mg2+体系的竞争干扰实验。探针HQL 浓度为10.0 μmol/L,分别加入1.0 mmol/L 的金属阳离子后,再加入1.0 mmol/L 的Mg2+。如图2 所示,Li+、Na+、K+、Rb+、Cs+、Ba2+、Ca2+和Sr2+存在下,探针对Mg2+的荧光选择未受到明显干扰。然而在过渡金属离子共存的情况下,探针对Mg2+的荧光选择性会受到不同程度的影响,尤其是Ni2+、Cr3+、Cu2+、Fe2+、Fe3+和Co2+会严重破坏探针HQL 识别Mg2+,这主要是由于探针分子中的羟基喹啉与这些金属离子的配位能力较与Mg2+强所致。因此,在无过渡金属离子存在的情况下,探针HQL 对Mg2+具有选择性识别能力。

图2 其他阳离子对Mg2+的竞争干扰响应Fig.2 Selectivity of HQL toward Mg2+in the presence of various metal ions
2.2 Mg2+浓度对探针荧光光谱的影响
考察了探针HQL 溶液的荧光发射峰强度随Mg2+浓度的变化情况。如图3 所示,随着Mg2+在探针溶液中浓度的增加,577 nm 处的荧光发射峰强度逐渐升高。当Mg2+浓度达到1.0 mmol/L 时,荧光增强趋势出现拐点,继续增加Mg2+浓度,体系荧光发射峰强度缓慢升高。Mg2+浓度(x,μmol/L)在0~25 μmol/L 范围内与577 nm 处的荧光强度(y)呈良好的线性关系:y=16.876 67 + 2.757 99x,r2= 0.999 3。通过公式LOD =K×δ/S(信噪比K= 3,S为拟合直线的斜率,δ是10 次探针HQL 荧光强度的标准偏差)计算得到HQL 对Mg2+的检出限(LOD)为8.2 ×10-8mol/L。

图3 探针HQL(10.0 μmol/L)对不同浓度Mg2+的荧光响应Fig.3 Fluorescence responses of HQL(10.0 μmol/L)with variable Mg2+concentrations
2.3 探针与Mg2+之间的Job曲线
为确定体系中探针HQL 和Mg2+之间的化学计量比,保持探针和Mg2+的总浓度为1.0×10-4mol/L,调整两者之间的浓度比,基于577 nm 处的荧光发射峰强度得到工作曲线(图4)。可以看出,[HQL]/([HQL]+[Mg2+])=0.67处有一个交点,说明HQL与Mg2+之间是2∶1配位。

图4 探针HQL与Mg2+的Job工作曲线Fig.4 Job’s plots of HQL and Mg2+
2.4 探针对Mg2+的识别机理
为深入了解探针HQL 和Mg2+之间的相互作用,以4-羟基-1-萘甲醛和苯甲酰肼反应制备分子HNL,观察该溶液中加入Mg2+前后的荧光光谱变化。如图5 所示,加入Mg2+后,HNL 溶液的荧光峰强度无明显变化,表明探针HQL 分子中与Mg2+配位的是N和—OH。在此基础上,基于Gaussian09高斯软件,以B3LYP/6-31G(d)基组进行理论优化计算。如图6 所示,8-羟基喹啉和HQL 的能级差分别为4.51 eV 和3.72 eV,但是由于分子内光诱导质子转移效应,8-羟基喹啉和探针HQL 自身不能发出荧光。通过计算发现,当HQL 与Mg2+结合之后,其能级差进一步缩小,且电子云向Mg2+中心靠近,密度增大,并在荧光光谱中表现出荧光发射峰增强。这主要是由于探针与Mg2+形成配位后,抑制了分子内的光诱导质子转移效应。因此,根据上述实验结果和理论分析,可以推测其识别过程如图7所示。

图5 HQL和HNL对Mg2+的荧光光谱响应Fig.5 Fluorescence response of HQL and HNL toward Mg2+ion

图6 8-羟基喹啉、HQL与2HQL+Mg2+的HOMO与LUMO能级图Fig.6 HOMO and LUMO energy levels of 8-hydroxyquinoline,HQL and 2HQL+Mg2+
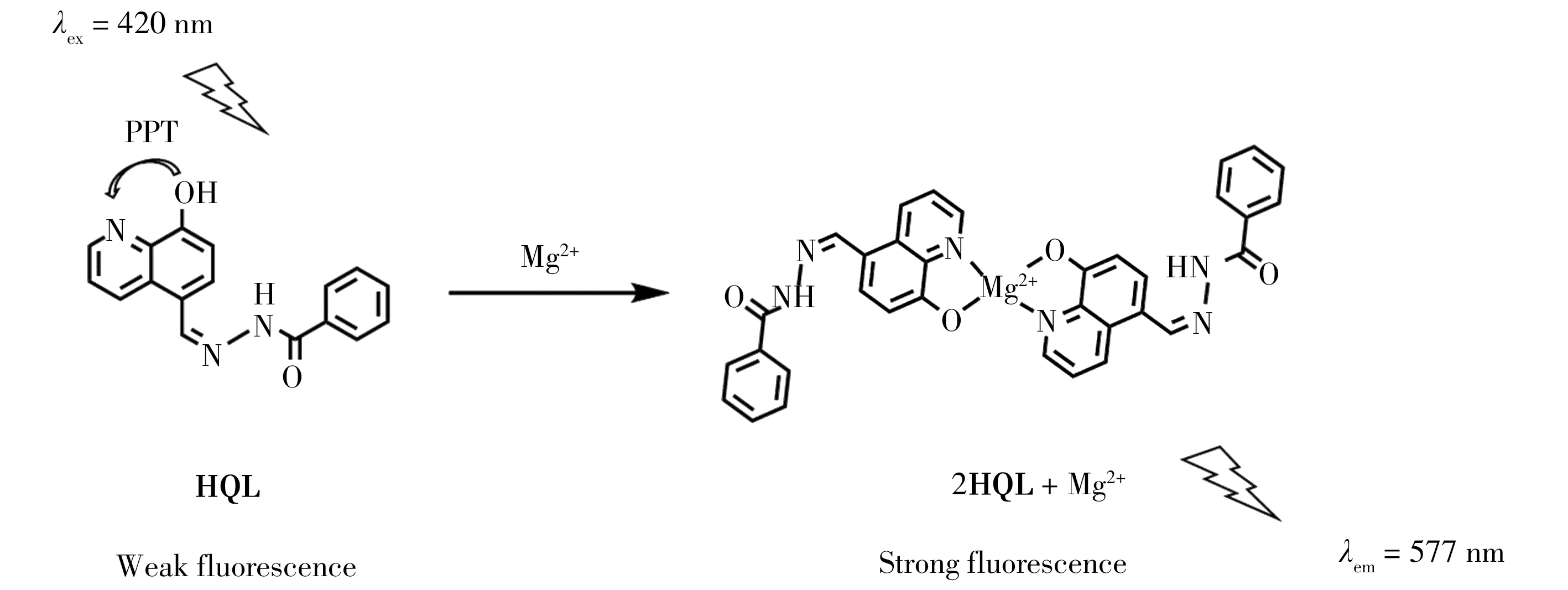
图7 探针HQL与Mg2+之间的作用关系Fig.7 Proposed interaction of probes HQL with Mg2+ions
3 结 论
本文基于8-羟基喹啉-5-醛与苯甲酰肼反应制备出荧光探针用于Mg2+识别,在含水5%的溶液中,该探针能够通过577 nm 处的荧光增强选择性识别Mg2+,还可以利用604、611 nm 处的荧光增强来区分识别Cd2+和Zn2+。探针结构中的N 和—OH 与Mg2+之间以2∶1 的比例发生配位,且配位后的体系能级差缩小,电子云密度增大,从而实现荧光增强对Mg2+进行检测。
