超高效液相色谱-串联质谱法测定鸡内金中9种磺胺类药物残留
2021-11-03许晓辉王小乔吴福祥杜锐浒朱仁愿石晓峰
许晓辉,王小乔,董 蔚,吴福祥,杜锐浒,朱仁愿,石晓峰
(1. 兰州市食品药品检验检测研究院,甘肃 兰州 730050;2. 甘肃省医学科学研究院,甘肃 兰州 730050;3. 兰州中检科测试技术有限公司,甘肃 兰州 730070)
鸡内金是一种动物源性中药材,也是药食同源的中药之一,其来源为雉科动物家鸡Gallus gallusdomesticus Brisson 的干燥沙囊内壁[1],具有健胃消食、涩精止遗、通淋化石等作用,主要用于治疗积滞(食积、石积、酒积和瘀血)、消渴、疮疡、遗尿等[2]。由于家鸡在饲养中使用饲料添加剂、抗生素等,严重影响了鸡内金的质量。其中化学合成的磺胺类药物因具有化学性质稳定、抗菌性能高效、价格低廉、使用简单、供应充足等优点被广泛应用于家禽养殖业,而含有该类药物的动物产品一旦被人长期摄入,会在人体内不断蓄积,产生肾毒性、耐药性及过敏反应,也可引起白细胞减少症和破坏胃肠道微生物平衡等[3-4]。为此我国发布的《食品安全国家标准食品中兽药最大残留限量》(GB31650-2019)中明确规定了动物产品中磺胺类药物的总残留量最高为100 μg/kg[5]。
有关动物性食品中磺胺类药物的检测方法主要有高效液相色谱法、液相色谱-质谱联用法、毛细管电泳法、放射免疫法、免疫传感器法和酶联免疫法等,样品前处理方法有液液萃取等传统方法和固相萃取法、固相微萃取法以及基质固相分散法等新方法[6-12],这些检测方法和样品前处理手段各具优势和缺陷。QuEChERS是一种广泛应用于动物源性产品中兽药残留检测的前处理技术,具有准确度高、样品制备时间短、分析速度快、溶剂用量小和操作简便等优势。目前,已有QuEChERS/高效液相色谱-串联质谱法测定鸡肉中磺胺类药物残留的报道[13-16],但有关鸡内金中磺胺类药物的检测方法尚无文献报道。为了评估鸡内金中磺胺类兽药残留风险,本研究采用QuEChERS 法提取鸡内金样品,以PRiME HLB 固相萃取柱净化提取液,基于超高效液相色谱-串联三重四极杆质谱(UPLC-MS/MS)技术,建立了鸡内金中磺胺甲噁唑等9种磺胺类药物的检测方法,并用于实际样品的快速筛查。
1 实验部分
1.1 仪器、试剂与材料
Agilent 1290-6460 超高效液相色谱-三重四极杆液质联用仪,配有电喷雾离子源(美国安捷伦有限公司);MS105DU 分析天平(美国梅特勒公司);Vortex-genie2 涡旋混合器(美国Scientific 公司);5810R 离心机(i国Eppendorf 公司);SBL-10DT 超声波清洗器(宁波新芝生物科技股份有限公司);Milli-Q超纯水系统(美国Millipore公司)。
对照品:磺胺甲噁唑(纯度99.5%,下同)、磺胺氯哒嗪(99.1%)、磺胺喹沙啉(98.9%)、磺胺甲基嘧啶(99.1%)、磺胺邻二甲氧嘧啶(99.1%)、磺胺间二甲氧嘧啶(99.5%)购于Dr. Ehrenstorfer GmbH 公司,磺胺二甲嘧啶(100%)、磺胺嘧啶(99.7%)购于中国食品药品检定研究院,磺胺间甲氧嘧啶(99.1%)购于Bepure公司。
乙腈、甲醇(色谱纯,i国Merck 公司);甲酸、乙酸铵(色谱纯,东京化成工业株式会社);其它试剂为分析纯;实验用水为自制超纯水;PRiME HLB固相萃取柱(6 mL/500 mg,美国沃特世公司)。
实际检测鸡内金样品均随机购于兰州市中药材市场和药店。
1.2 溶液配制
1.2.1 EDTA 缓冲液 称取柠檬酸8.4 g、磷酸氢二钠7.1 g、乙二胺四乙酸二钠19.5 g,溶于650 mL水中,超声溶解即得。
1.2.2 混合对照品溶液 精密称取9种磺胺类药物对照品各10.0 mg,分别置于10 mL棕色容量瓶中,用乙腈溶解并定容至刻度,配制成质量浓度均为1 mg/mL 的各磺胺类药物单一对照品溶液;分别精密吸取上述单一对照品溶液0.025 mL,置于同一25 mL 棕色容量瓶中,用乙腈稀释并定容至刻度,配制成各药物质量浓度均为1 μg/mL的混合对照品中间液;最后精密移取该混合对照品中间液1.00 mL,置于10 mL棕色容量瓶中,用乙腈稀释并定容至刻度,配制成各药物质量浓度均为0.1 μg/mL的混合对照品溶液,于4 ℃冷藏备用。
1.3 样品处理
1.3.1 试样制备 杀鸡后取出鸡肫,立即剥下内壁洗净,置于炒制容器用文火加热至鼓起的程度,取出放凉即得。称取干燥的空白或供试品鸡内金,分别粉碎过20目筛,备用。
1.3.2 提取与净化 准确称取干燥的鸡内金样品2.0 g 于50 mL 离心管中,加入3 mL EDTA 缓冲液,放入陶瓷均质子,涡旋混合1 min 后,加入10 mL 乙腈,涡旋混合1 min,在300 W 功率下超声提取5 min,加入1 g氯化钠和4 g硫酸钠,充分涡旋混合2 min,以5 000 r/min离心10 min,取1.5 mL上清液过PRiME HLB 固相萃取柱,保持1 滴/s 的流速,收集净化流出液,过0.22 μm 有机相滤膜,作为供试品溶液;取空白样品同法制成空白基质样品溶液;然后分别将供试品溶液和空白基质样品溶液转移至进样瓶中,待分析。
1.4 UPLC-MS/MS分析
1.4.1 UPLC 条件 色谱柱:ACQUITY BEH C18柱(2.1 mm × 100 mm,1.7 μm);流动相:A 为含0.1%甲酸和2 mmol/L 乙酸铵的水溶液,B 为含0.1%甲酸的乙腈溶液,梯度洗脱程序:0~2 min,15% B;2~3 min,15%~25% B;3~4 min,25%~35% B;4~5 min,35%~50% B;5~9 min,50%~90%B;9~11 min,90%~15%B;流速:0.3 mL/min;柱温:35 ℃;进样量:2 μL。
1.4.2 质谱条件 电喷雾离子源(ESI),正离子模式,动态多反应监测模式(d-MRM),雾化气(N2)流速为8 L/min,喷雾电压为500 V,气流温度为325 ℃,毛细管电压为4 000 V,鞘气流速为12 L/min,鞘气温度为350 ℃。磺胺类药物的质谱参数见表1。
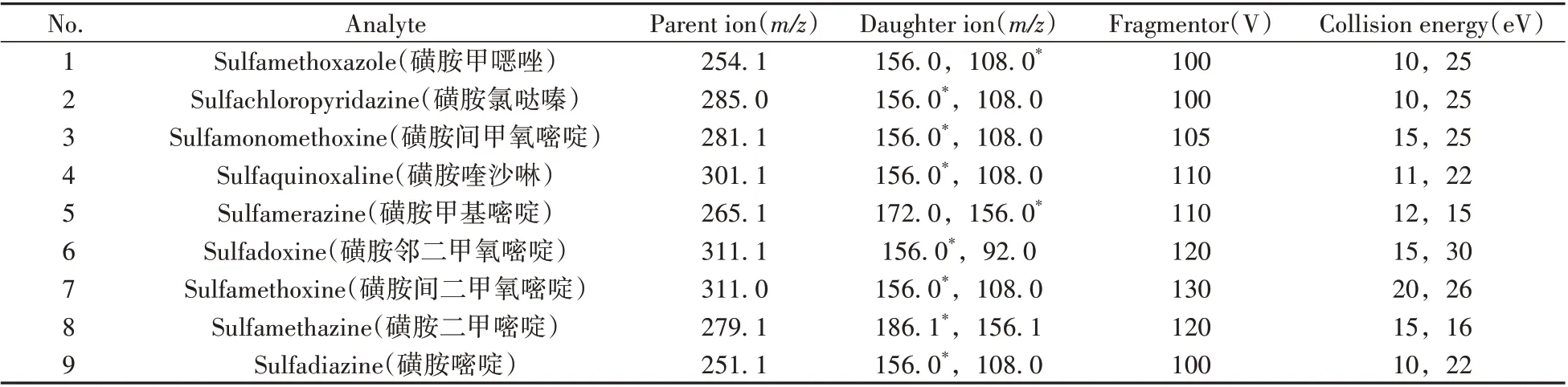
表1 9种磺胺类药物的质谱参数Table 1 Mass spectral parameters of nine kinds of sulfonamides
1.5 数据处理
采用Agilent MassHunter 工作站软件进行数据采集和分析,采用Excel进行数据统计与计算。
2 结果与讨论
2.1 样品前处理条件的选择
本研究的9 种磺胺类药物能够较好地溶解于甲醇和乙腈中,而乙腈为中等极性溶剂,与大多数待测化合物的极性接近,且能使蛋白质变性沉淀;另外,鸡内金中含有大量的蛋白质,可借助QuEChERS 萃取盐包(盐包内含4 g硫酸钠和1 g氯化钠)通过盐析使样品中蛋白质沉淀并通过离心去除,因此选择QuEChERS 法提取样品。在此基础上,选择PRiME HLB 固相萃取柱对提取液进行净化,可有效吸附去除鸡内金提取液中的磷脂等非极性干扰物,降低基质效应以增强质谱响应,同时该净化方法无活化、清洗和洗脱等传统固相萃取步骤,直接上样净化,简化了流程,节约了时间。实验还考察了提取过程加EDTA 与未加EDTA 的提取效果(见图1),结果显示加EDTA 提取可显著提高大部分磺胺类药物的回收率。优化的样品前处理条件如“1.3.2”所示。

图1 加入与未加EDTA缓冲液的提取结果对比Fig.1 Comparison of extraction results with and without EDTA buffer
2.2 色谱条件的优化
磺胺类药物大多数偏极性,因此实验选择适用于极性化合物的通用ACQUITY BEH C18超高效色谱柱(2.1 mm×100 mm,1.7 μm)。正离子模式下,在流动相中添加甲酸能够提高目标化合物的离子化效率,添加乙酸铵能够稳定水相和改善峰形,实验考察了乙腈-水、甲醇-水中添加不同量的甲酸和乙酸铵作为流动相时9 种磺胺类药物的分离效果和灵敏度。结果表明,在水相中加入0.1%甲酸和2 mmol/L乙酸铵可显著改善峰形、提高灵敏度,在有机相中加入0.1%甲酸可稳定保留时间、提高重复性。优化的色谱分析条件如“1.4.1”所示。
2.3 质谱条件的优化
将9 种磺胺类药物单一对照品溶液直接注入质谱仪,在正离子模式下进行全扫描(Scan)以确定母离子;进行选择离子扫描(SIM)确定碎裂电压;然后进行子离子扫描,选取丰度比最高且相对稳定的2 个碎片离子分别作为定性离子和定量离子;最后利用MassHunter 采集软件,以手动和自动两种方式同时优化定性和定量离子的碰撞能量,建立多反应监测(MRM)方法,并在MRM 方法下分析混合对照品溶液,再将采集的数据文件从安捷伦的MassHunter质谱采集工作站软件导入自动生成d-MRM方法。d-MRM 方法包含化合物名称、MRM 离子对、碎裂电压、碰撞能量、动态MRM 的保留时间和保留时间增量窗口,对于软件不能自动识别保留时间及保留时间增量窗口的化合物,可用安捷伦定性软件通过提取化合物的离子对手动识别。优化的质谱分析条件如“1.4.2”所示。
以d-MRM 模式测定9种磺胺类药物的定性和定量离子对色谱图,共有18个离子监测通道。混合对照品溶液(20 ng/mL)的总离子流图如图2所示,各目标化合物的峰形对称、响应良好、定量准确可靠。

图2 9种磺胺类药物对照品的总离子流图Fig.2 Total ion chromatogram of nine kinds of sulfonamides standards
2.4 基质效应考察
为明确鸡内金中9 种磺胺类药物检测时的基质效应(Matrix effect,ME),通过考察质量浓度为5 ng/mL 的各对照品溶液在空白样品基质与纯溶剂中信号强度的比值百分比评价ME,比值百分比越接近100%,表明基质效应越小;比值百分比大于100%,表明存在基质增强效应;比值百分比小于100%,表明存在基质抑制效应。结果显示:磺胺二甲嘧啶、磺胺甲基嘧啶、磺胺喹沙啉、磺胺邻二甲氧嘧啶、磺胺氯哒嗪、磺胺嘧啶的ME比值百分比均大于70%,表明存在弱的基质抑制效应;磺胺甲噁唑、磺胺间二甲氧嘧啶、磺胺间甲氧嘧啶的ME 比值百分比为60%~70%,表明存在中等的基质抑制效应。虽然9种磺胺类药物存在较弱或中等的基质抑制效应,但不影响分析检测结果。
2.5 方法学验证
2.5.1 线性关系、检出限与定量下限 精密移取混合对照品溶液适量,用空白样品基质溶液稀释配制成质量浓度分别为0、2、5、10、20、30、40、50 ng/mL的系列标准溶液,外标法定量,以各化合物的质量浓度(X,ng/mL)为横坐标,对应峰面积的积分值(Y)为纵坐标,绘制标准曲线。结果表明,9种磺胺类药物在0~50 ng/mL范围内呈良好的线性关系,相关系数(r2)均不小于0.996 0。将混合对照品溶液加入空白基质中,加标浓度逐级递减,按“1.3.2”进行样品前处理,以3 倍信噪比计算检出限(LOD),10倍信噪比计算定量下限(LOQ),并计算LOQ浓度水平的加标回收率和相对标准偏差(RSD)。结果显示,9种磺胺类药物的LOD为0.065 4~0.715 7 μg/kg,LOQ为0.212 2~2.478 μg/kg,LOQ浓度水平的回收率为63.1%~70.5%,RSD为2.8%~6.2%(见表2)。

表2 9种磺胺类药物的线性关系、检出限及定量下限Table 2 Linear relationships,LODs and LOQs of nine kinds of sulfonamides
2.5.2 回收率与相对标准偏差 在空白鸡内金样品中分别按15.0、25.0、50.0 μg/kg 3个浓度添加混合对照品中间液,每个加标水平平行制备6 份样品,经提取净化后上机测定,每份样品重复测定3 次,计算回收率和RSD。结果表明,9 种磺胺类药物的回收率为63.2%~88.7%,RSD(n=6)为0.90% ~7.1%(见表3)。
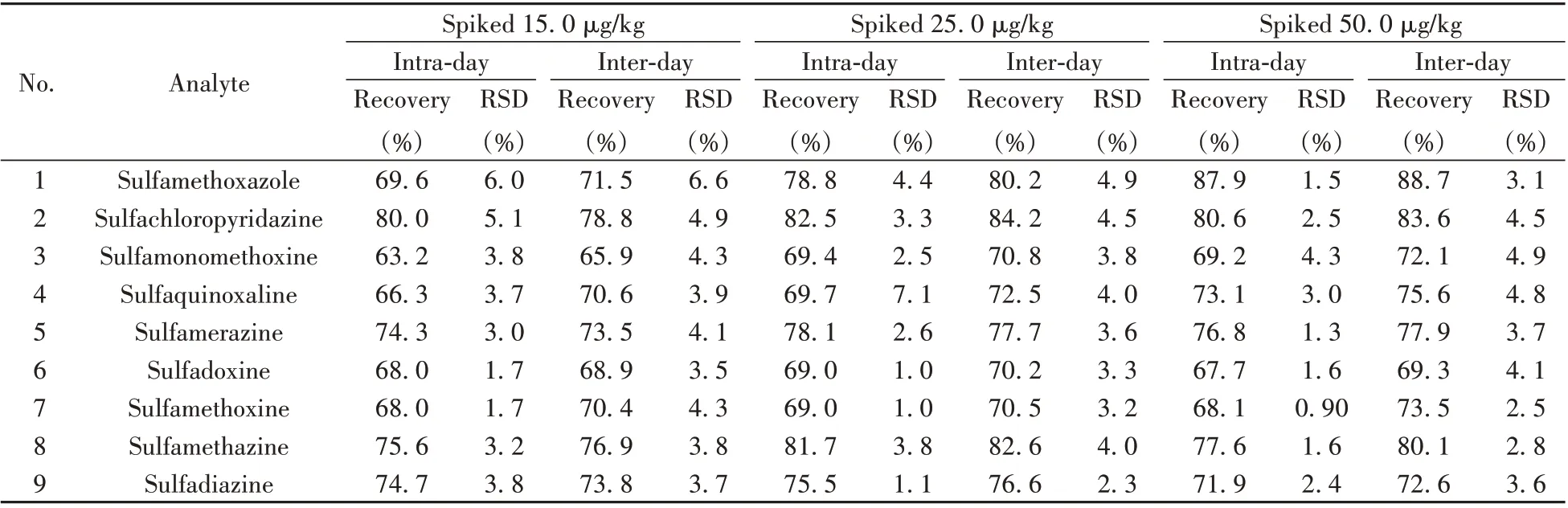
表3 9种磺胺类药物的回收率及相对标准偏差(n=6)Table 3 Recoveries and RSDs of nine kinds of sulfonamides(n=6)
2.6 实际样品测定
应用本方法筛查10 批鸡内金样品中9 种磺胺类药物残留,结果在1 份样品中检出磺胺甲噁唑,含量为0.88 μg/kg,其MRM 图如图3 所示。由于目前尚无动物源性中药中兽药残留的标准,参照现行的国家标准GB31650-2019进行判定,该阳性样品的磺胺甲噁唑残留量未超标。
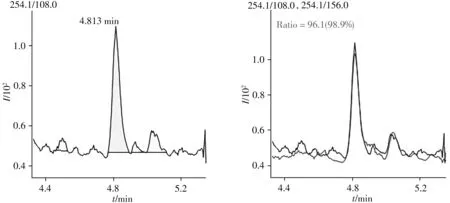
图3 磺胺甲噁唑阳性样品的MRM图Fig.3 MRM spectra of sulfamethoxazole for positive sample
3 结 论
本研究以QuEChERS法进行提取,PRiME HLB固相萃取柱进行净化,采用UPLC-MS/MS技术建立了药食同源中药鸡内金中9 种磺胺类药物残留的检测方法。该方法具有前处理步骤简单,净化效果显著,准确性好,检出限低等优点,适用于鸡内金中磺胺类药物残留的检测,可为降低药食同源中药的安全风险提供技术支持。
