采用焙烧-水浸法从报废锂离子动力电池中回收金属
2021-11-02王大辉陈怀敬刘振宁胡平平
王大辉, 张 珂, 陈怀敬, 刘振宁, 胡平平
(1. 兰州理工大学 省部共建有色金属先进加工与再利用国家重点实验室, 甘肃 兰州 730050; 2. 兰州理工大学材料 科学与工程学院, 甘肃 兰州 730050; 3. 兰州理工大学 理学院, 甘肃 兰州 730050)
车发展迅速,预计到2030年其销量占比将达汽车总销量的40%.而新能源汽车动力电池工作年限约为4~6年,且制造锂离子电池需要消耗大量的资源,如锂、钴、镍、铜、铝、石墨等,锂离子动力电池报废后的资源化循环利用正引起广泛关注[2-3].
锂离子电池中的有色金属分布具有规律性,如锂、镍、钴主要集中在其所使用的正极材料中.报废锂离子电池破碎-拆解后获得的正极材料中,金属的回收方法可分为湿法回收,火法回收和生物回收等[4-5]、原位还原焙烧法[6-7]、氯化焙烧法[8]、硫酸化焙烧法等[9-12].Lin J等[13]通过室温浓硫酸破坏正极材料晶体结构结合高温硫酸化焙烧回收锂的方法和He S等[14]将报废锂离子电池LiMn2O4与(NH4)2SO4低温焙烧回收其中金属元素的方法,分别产生毒害气体SO3与NH3,对环境及人体有害.湿法冶金通过H2SO4[15],HCl[16],H3PO4[17],以及柠檬酸等[18]对报废锂离子电池正极材料浸出回收有价金属元素的过程中存在锂的回收率低,回收成本高.原因在于:在酸浸过程中,锂将以离子形式与镍,钴和锰一起转移到酸浸溶液中,在随后的除杂及依次萃取分离镍、钴、锰的阶段,试剂的大量涌入将导致萃取镍、钴和锰后萃余液的体积扩大.随着酸浸液的进一步稀释,锂的浓度将降低.这种多阶段损失和稀释使锂的浓度降低,使得回收的经济成本更高,且锂的回收率通常约为80%~90%.如果能够在酸浸之前从废旧锂离子电池的正极材料中选择性提取锂,并对镍、钴、锰元素进行分步提取,则可以避免形成低浓度锂离子溶液和锂的损失,降低回收成本,提高锂的回收率.采用NaHSO4·H2O作为硫酸化焙烧过程的替代试剂可实现焙烧过程无有害气体产出且工艺更为简化,可实现锂的优先浸出,为后续锂的回收降低成本.
镍钴锰酸锂(LiNixCoyMn1-x-yO2)具有一系列突出的优点,包括LiNi0.5Co0.2Mn0.3O2、LiNi1/3Co1/3Mn1/3O2、LiNi0.8Co0.1Mn0.1O2等,在商业化锂离子动力电池产品中已获得广泛的应用.针对以LiNi0.5Co0.2Mn0.3O2为正极材料的报废锂离子动力电池中锂、镍、钴、锰的高效回收,开展LiNi0.5Co0.2Mn0.3O2-NaHSO4体系焙烧过程物相演变规律的研究,阐明影响金属元素赋存形式的主要因素,为锂、镍、钴、锰的差异性浸出行为提供理论依据.在此基础上,并提出了采用“焙烧-水浸出”工艺从报废锂离子动力电池中回收金属的工艺.
1 实验
1.1 材料和试剂
从中国兰州电子废品回收中心获得了以LiNi0.5Co0.2Mn0.3O2为正极材料的废锂离子动力电池.从废锂离子动力电池中经放电处理、破碎、筛分、干燥后获得LiNi0.5Co0.2Mn0.3O2.其他化学试剂均为分析纯,实验中的所有溶液、溶剂均为离子水.
1.2 实验步骤
锂离子动力电池完全放电后手工拆除,除去塑料和不锈钢外壳,分离正极极片和负极极片.正极极片在马弗炉(KSL-1100X-S)中于550 ℃煅烧0.5 h,随后将从正极极片上脱落下的LiNi0.5Co0.2Mn0.3O2粉末用去离子水洗涤,然后过滤并在真空烘箱中于80 ℃干燥10 h.将干燥后的LiNi0.5Co0.2Mn0.3O2粉末与一定质量比的硫酸氢钠水合物(NaHSO4·H2O)混合并充分研磨.将该混合物置于50 mL陶瓷坩埚中.将坩埚置于马弗炉中并以5 ℃/min的加热速率进行焙烧.焙烧后将焙烧产物自然冷却至室温,用去离子水浸出.水浸出的工艺条件为:反应器容积250 mL,搅拌速度为160 r/min,液固比为25 mL/g,浸出温度为60 ℃浸出时间0.5 h,之后,将其过滤获得滤渣和滤液,滤液中的金属离子可使用相关技术制备金属产品.使用ICP-OES(Pert-Pro MPD, Netherlands)检测滤液中的Li、Ni、Co和Mn元素含量,使用公式(1)计算Li、Ni、Co和Mn元素从LiNi0.5Co0.2Mn0.3O2中转移至水溶液的浸出率Li:
(1)
其中:mi是焙烧产物中元素“i”的质量;Vi和Ci是浸出液体积及元素在浸出液中的浓度.
图1是采用焙烧-水浸工艺从报废锂离子动力电池中回收金属的工艺路线图.依据式(2)配置LiNi0.5Co0.2Mn0.3O2与NaHSO4·H2O 摩尔比例分别为1∶1、1∶1.5、1∶2、1∶2.5、1∶3时对应选择的质量比1∶1.42、1∶2.14、1∶2.85、1∶3.57、1∶4.28.
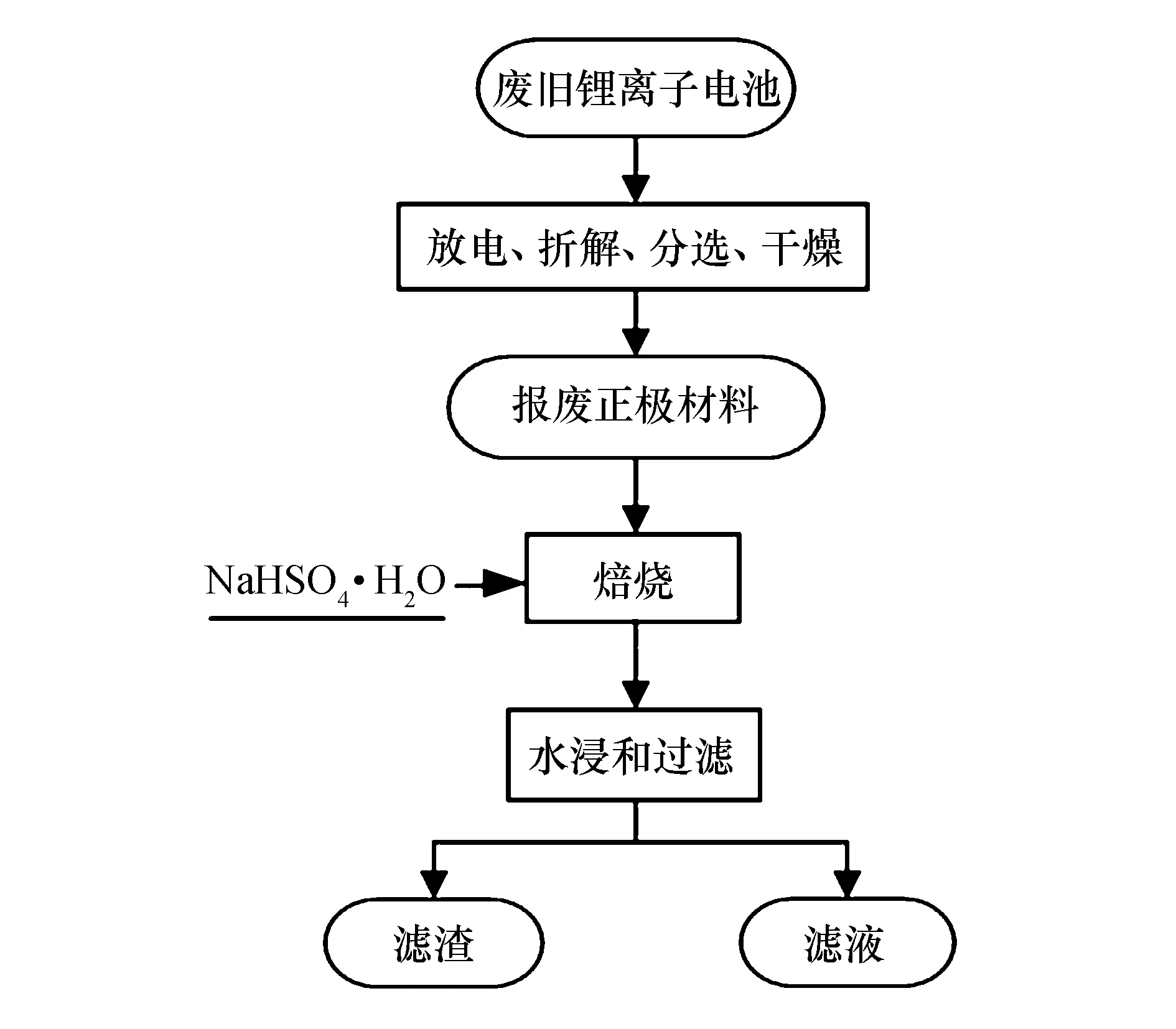
图1 采用焙烧-水浸工艺从报废锂离子动力电池中回收金属的工艺路线图Fig.1 Flow chart for metal recovery from spent lithium ion power batteries by roasting and water leaching process

5Li2SO4+15Na2SO4+5NiSO4+ 2CoSO4+
3MnSO4+5/2O2(g)+ 45H2O(g)
(2)
ΔrGθT=725.144-10.433 54T,kJ·mol-1
通过同步热分析仪(STA 449F3,Netzsch,Germany)以10 ℃·min-1的升温速率在25~600 ℃对混合物进行热重-差示扫描量热分析(TG-DSC).采用D/Max 2400型X射线衍射仪(XRD)分析物相组成(CuKα,λ=0.154 nm,U=40 kV,2θ=5°~90°),XRD数据通过MDI Jade 6.0软件进行分析.使用X射线光电子能谱仪(XPS,ESCALAB 250Xi,Thermo Fisher Scientific,America)通过单色Al Ka X射线测定焙烧后产品中O、Ni、Co和Mn的化合价态,并对所有光谱以284.8 eV的C1s峰值进行校准.采用HSC 6.0对LiNi0.5Co0.2Mn0.3O2-NaHSO4·H2O焙烧体系进行热力学分析.
2 分析与讨论
2.1 TG-DSC分析
为研究不同质量比例LiNi0.5Co0.2Mn0.3O2-NaHSO4·H2O体系在升温过程中发生的热重差异,对不同比例的混合物进行升温TG-DSC分析.
由图2a~e可见,TG曲线共有3个失重平台,第1个失重平台约为25~186 ℃,主要是LiNi0.5Co0.2Mn0.3O2及NaHSO4·H2O脱去吸附水以及NaHSO4·H2O脱去结合水,失重率6.75%~8.46%;第2个失重平台约为186~240 ℃,对应失重率2.12%~3.93%;第3个失重平台约为240~800 ℃,对应失重率3.1%~8.69%.对比图2a~e可以看出,图2a、b第二失重平台为180~240 ℃,而图2c~e则随着混合物中NaHSO4·H2O含量增大起始温度降低,且对应吸热峰温度逐渐从212 ℃降至168 ℃;图2a~d为240~800 ℃,对应失重率3.1%,图2e的第三失重平台为201~600 ℃,失重率8.69%, 且吸热峰在更低的温度点下出现,表明NaHSO4·H2O含量增加可以使物相转变在更低的温度下实现.
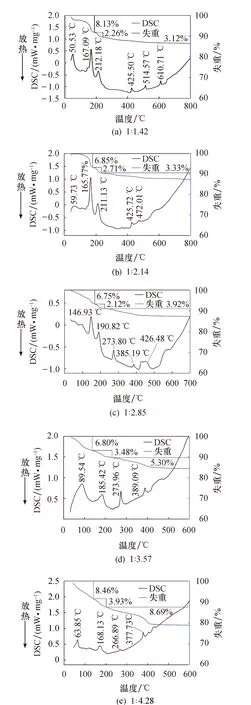
图2 不同比例LiNi0.5Co0.2Mn0.3O2材料与NaHSO4·H2O混合后焙烧的TG-DSC曲线
2.2 XRD分析
为研究硫酸化焙烧过程的物相转变规律,对温度230、350 ℃下的焙烧产物进行XRD分析.
图3a~e为质量比1∶1.42、1∶2.14、1∶2.85、1∶3.57、1∶4.28,在230 ℃焙烧后的XRD物相检测结果.可见,当混合物中LiNi0.5Co0.2Mn0.3O2和 NaHSO4·H2O比例为1∶1.42时,新的物相(Li0.45Ni0.05)(NiO2),LiNaSO4和Mn3O4开始出现,原有LiNi0.5Co0.2Mn0.3O2结构已经被破坏.当比例增大至1∶2.14时,焙烧产物物相组成为Li(Ni0.7Co0.3)O2、LiNaSO4和Mn3O4,说明随着Li的缺失,层状结构逐渐破坏.当比例继续增大至1∶2.85时,Li(Ni0.7Co0.3)O2的物相被LiMnO2取代,LiNaSO4的主峰(102)、(110)峰逐渐尖锐(1∶1.42~1∶2.85), 说明在这一比例区间,LiNaSO4生成量增多.当比例继续增大至1∶3.57时, Mn2O3和(Co, Mn)(Mn, Co)2O4开始出现,此时结构已由六方晶系转变为立方晶系.当比例继续增大时,Na6Ni(SO4)4、Na6Mn(SO4)4、Na2Ni(SO4)2出现,说明在同一温度下,LiNi0.5Co0.2Mn0.3O2和 NaHSO4·H2O混合物中NaHSO4·H2O含量增大对Li、Ni、Co、Mn形成各自的硫酸盐具有促进作用.
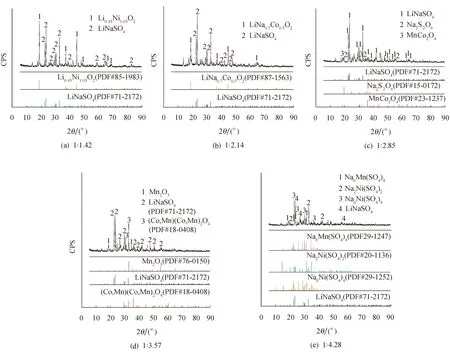
图3 230 ℃下不同质量比LiNi0.5Co0.2Mn0.3O2与NaHSO4·H2O混合后焙烧产物的XRD图 Fig.3 XRD patterns of roasting products after mixing LiNi0.5Co0.2Mn0.3O2 and NaHSO4·H2O at different mass ratio at 230 ℃
图4a~e为1∶1.42、1∶2.14、1∶2.85、1∶3.57、1∶4.28质量比下在350 ℃焙烧后的XRD物相.在1∶1.42质量比下的物相为LiNaSO4、LiNi0.7Co0.3O2和Co3O4;而当比例增大至1∶2.14时,物相为LiNaSO4和LiMnO4.随着比例继续增大,在1∶2.85、1∶3.57均出现了Na6Co(SO4)4、Na6Ni(SO4)4、Na2Ni(SO4)2物相,当比例增大至1∶4.28时,出现了Na6Mn(SO4)4物相.在350 ℃时开始出现硫酸复式盐的质量比例为1∶2.85,小于230 ℃下开始出现硫酸复式盐的比例1∶4.28,表明温度升高可以使LiNi0.5Co0.2Mn0.3O2和 NaHSO4·H2O生成硫酸复式盐的转变比例更小.
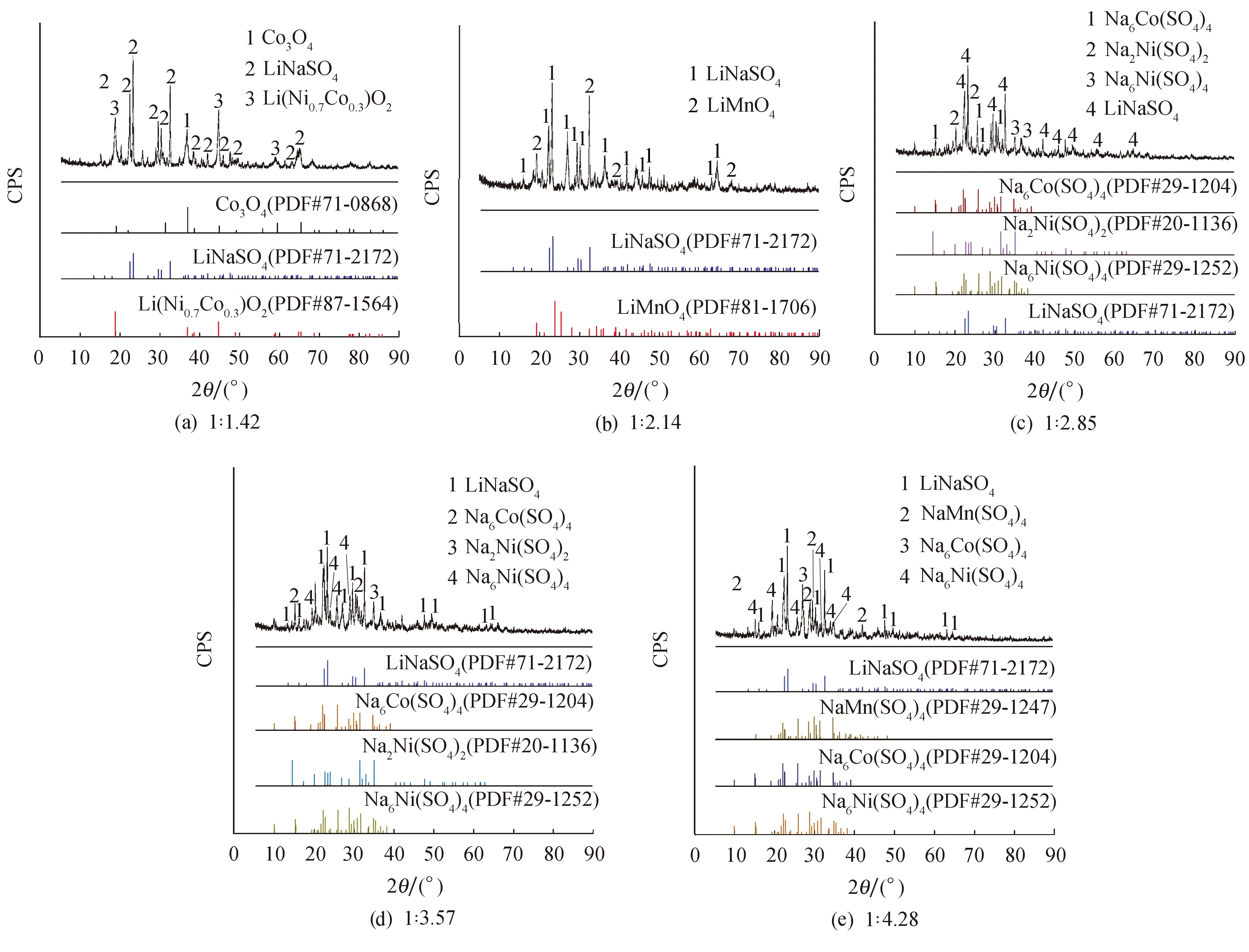
图4 350 ℃下以不同质量比将LiNi0.5Co0.2Mn0.3O2与NaHSO4·H2O混合后焙烧的产物XRD图 Fig.4 XRD patterns of roasting products after mixing LiNi0.5Co0.2Mn0.3O2 and NaHSO4·H2O at different mass ratio at 350 ℃
2.3 XPS分析
为研究焙烧产物随温度升高过程的价态转变规律,对1∶4.28质量比例下在230、350、470、590 ℃温度下的焙烧产物进行XPS分析.
图5为1∶4.28质量比下不同温度焙烧产物的XPS图谱.由O1s能谱,当温度升高至230 ℃时,晶格氧的结合能消失,出现了Na2SO4(531.30 eV)[19]、NiSO4(532.00 eV)[20]、MnSO4(532.40 eV)[21]叠加形成的宽峰, 温度继续升高,结合能基本保持不变.可见在230 ℃下Na2SO4已开始形成并伴随着金属硫酸盐的生成.Ni 2p谱图中,在230 ℃下2p3/2对应着结合能856.77 eV、2p1/2对应着874.69 eV,还有位于861.36、879.82 eV的两个卫星峰,与NiO的特征峰结合能一致[22],且NiSO4的2p3/2主峰856.80 eV与其重合[23],这是在230 ℃及更高温度下,Ni的赋存价态为+2价,存在形式为NiO和NiSO4并存.在Co 2p的图谱中,230、350 ℃下的峰结合能为2p3/2峰781.6eV、2p1/2峰797.78 eV、Sat.1峰785.74 eV、Sat.2峰802.29 eV, 这些与Co2O3的结合能一致.在470、590 ℃ 下,2p3/2峰、2p1/2峰、Sat.1峰及Sat.2峰与CoSO4的特征峰位一致,表明CoSO4为此条件下的主要存在状态.在Mn 2p的图谱中,原材料与LiNi0.5Co0.2Mn0.3O2中Mn的结合能一致,为+4价[24],可以看出,230、350、470、590 ℃下的主峰均一致,2p3/2峰642eV和2p1/2峰654 eV,这是由于MnO、Mn2O3和MnO2的峰位较为接近,需结合Mn 3s轨道进行分析,从Mn3s的图谱可以看出,其间距分别为5.55、5.8 eV,对应于Mn2O3的结合能间距,5.99、5.73 eV对应于MnO的结合能间距,则230、350 ℃下Mn2O3与MnSO4为主要存在形式,470、590 ℃温度下MnSO4为主要存在形式.

图5 1∶4.28质量比例在不同温度节点下的产物XPS谱图
2.4 金属提取率
为研究同一温度下比例的增大对Li、Ni、Co、Mn浸出率的影响,做出200、350、500 ℃下随质量比由1∶2.14升高至1∶4.28浸出率的变化图.由图6a可见,在200 ℃下,当质量比为1∶2.14时,Li的浸出率为67.91%,Ni、Co、Mn的浸出率分别为15.30%、21.26%、15.15%.Li、Ni、Co的浸出率均在1∶3.57质量比时出现转折,增速减慢.当比例继续增大至1∶4.28时,Li、Mn、Ni、Co略有增加.可见,这一温度下随着比例增大Li,优先浸出,其次为Ni、Co,而到达1∶3.57质量比时,浸出率不再增加,Mn相对Li、Ni、Co的浸出率变化较小.
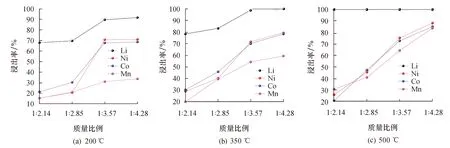
图6 Li、Ni、Co、Mn在不同温度下随质量比例增大的浸出率变化Fig.6 Li, Ni, Co, Mn leaching rate changes with increasing mass ratio at different temperature
在350 ℃下质量比1∶2.14时,Li的浸出率达到78.43%,Ni、Co、Mn分别为28.93%、30.32%、20.03%.当比例增大至1∶4.28时,Li、Ni、Co、Mn浸出率分别达到100%、79.39%、78.36%、59.43%,增幅分别为27.50%、174.42%、158.44%、196.70%,浸出率均为正向增长.这一温度下,温度升高与比例增大对Li、Ni、Co、Mn的浸出率为正向协同作用,且Li在1∶3.57质量比时已完全浸出,Ni、Co优于Mn浸出.
当温度为500 ℃时,Li的浸出率在1∶2.14时已达到100%,而后保持不变;Ni从1∶2.14时的浸出率25.84%增长至1∶4.28时的88.21%;Co从20.69%增长至85.14%;Mn从30.70%增长至83.80%.相比350 ℃时浸出率增幅,Li在这一温度下较小比例1∶2.14已完全浸出,Ni、Co随比例增长浸出率增幅较大,Mn的浸出率增幅相对比较小,说明温度的进一步升高对Co、Ni的浸出率增长是显著的.
综上所述,Li转化为可溶性硫酸盐优先于Ni、Co、Mn;在1∶2.14~1∶2.85质量比,Ni、Co、Mn 的提取率差异化较小,比例增大与温度升高对提取率正向增长有协同作用;在1∶3.57~1∶4.28质量比时,Ni、Co浸出优先于Mn,直至比例与温度分别达到1∶4.28与500 ℃时,Mn提取率达到83.80%,表明Mn 完全浸出对温度与比例要求较高.
2.5 焙烧过程热力学分析
LiNi0.5Co0.2Mn0.3O2-NaHSO4·H2O体系焙烧过程发生的反应如下,通过HSC 6.0软件计算了焙烧过程中发生的主要化学反应及其相应的Gibbs自由能.
LiNi0.5Co0.2Mn0.3O2-NaHSO4·H2O焙烧过程中可能发生的反应(2)~(18)的ΔrGθ与温度之间的关系如图7所示,温度均为273~1273 K.

(3)
ΔrGθT=65.468 8-0.166 52T,kJ·mol-1

(4)
ΔrGθT=177.838-0.385 74T,kJ·mol-1

(5)
ΔrGθT=154.724-0.236 94T,kJ·mol-1

(6)
ΔrGθT=407.390-0.337 09T,kJ·mol-1

(7)
ΔrGθT=111.968 8-0.214 166T,kJ·mol-1

(8)
ΔrGθT=157.788 42-0.164 594 9T,kJ·mol-1

(9)
ΔrGθT=395.366-0.252 878T,kJ·mol-1

(10)
ΔrGθT=-202.002+0.192 273T,kJ·mol-1
NiO+SO3(g)= NiSO4
(11)
ΔrGθT=-184.581+0.193 00T,kJ·mol-1

(12)
ΔrGθT=-228.442+0.203 71T,kJ·mol-1

(13)
ΔrGθT=-393.563+0.17936T,kJ·mol-1

2/3Co3O4+3MnO2+2/3O2(g)
(14)
ΔrGθT=3 319.108-3.077 3T,kJ·mol-1

(15)
ΔrGθT=-140.207+0.066 85T,kJ·mol-1

(16)
ΔrGθT=-199.360+0.136 7T,kJ·mol-1

(17)
ΔrGθT=-181.707+0.121 82T,kJ·mol-1

(18)
ΔrGθT=-164.960+0.100 1T,kJ·mol-1
式(3~5)表明,NaHSO4·H2O在373 K脱去结合水,NaHSO4在458 K脱去结构水,Na2S2O7在648 K开始产生SO3.式(6,8,9)在273~1 000 K温度非自发反应进行表明Co3O4、Mn2O3和Mn3O4具有高的热力学稳定性,并且难以分解为低价氧化物.式(13)和式(10,11,12)对比,表明Li2SO4的形成在热力学上比NiSO4,CoSO4和MnSO4的形成更为有利.从式(14,2)可以看出,当LiNi0.5Co0.2Mn0.3O2和NaHSO4·H2O一起焙烧时,LiNi0.5Co0.2Mn0.3O2的热力学稳定性急剧降低,常温下即可反应形成金属硫酸盐.在式(15~18)中,高价锰和钴氧化物转化为硫酸盐,这些反应自发发生在273~1 273 K.结合反应式(15~18)和式(10~12)可以看出,在温度高于450 K以后,Mn和Co的高价氧化物比低价氧化物生成硫酸盐摩尔反应的ΔrGθ更小,更容易发生硫酸盐转变反应.
3 结论
1)LiNi0.5Co0.2Mn0.3O2-NaHSO4·H2O体系中NaHSO4·H2O含量的增加可以促使LiNi0.5Co0.2Mn0.3O2转变为复式硫酸盐的反应在更低的温度下实现.
2) Li转化为可溶性硫酸盐优先于Ni、Co、Mn,比例增大与温度升高对提取率正向增长有协同作用.
3) 通过热力学理论,结合ICP-OES浸出结果,在质量比不小于1∶4.28的条件下,复式硫酸盐转变优于顺序为Li→Ni→Co→Mn;在质量比例小于1∶4.28条件下,复式硫酸盐转变顺序为Li→Ni→Co→Mn.综上所述,采用硫酸化焙烧-水浸工艺回收LiNi0.5Co0.2Mn0.3O2中的有价金属元素Li、Ni、Co、Mn是可行的.
致谢:本文得到沈阳材料科学国家(联合)实验室-有色金属加工与再利用国家重点实验室联合基金(18LHZD002)的资助,在此表示感谢.
