首诊非瓣膜性心房颤动患者E/e′及颈动脉粥样硬化斑块与缺血性脑卒中的关系*
2021-11-02雷玉华赵劲波
黄 锐,雷玉华△,赵劲波,严 莉
湖北省恩施土家族苗族自治州中心医院 1内科心血管病中心 2儿一科,恩施 445000
心房颤动(简称房颤,atrial fibrillation)是临床最常见的心律失常。与健康人相比,房颤患者血栓栓塞风险增加了5倍[1-3],由房颤导致的卒中占所有卒中的15%以上,因此预防血栓栓塞及脑栓塞是房颤治疗的主要目标之一。为减少脑栓塞的发生,临床上有多种血栓风险评估策略,其中最常用的是CHADS2评分系统(充血性心力衰竭1分,高血压病1分,年龄≥75岁1分,糖尿病1分,缺血性卒中/短暂性脑缺血发作2分)和CHA2DS2-VASc评分系统(充血性心力衰竭1分,高血压病1分,年龄≥75岁2分,糖尿病1分,缺血性卒中/短暂性脑缺血发作2分,血管疾病1分,年龄65~74岁1分,女性1分)[4]。
研究表明,与房颤相关的血栓多来自于左心耳,而左心耳的功能与左房的功能状态、左心房内压力、左心房血流情况密切相关。心室舒张功能不全时,左室充盈压升高,为了维持左心房搏出量,左心房会代偿性增大,这些改变会影响左心房功能和血流状态,从而增加左心房内血栓形成的风险[4-8]。众所周知,E/e′比值是评估心脏舒张功能的重要指标,因其容易获得、不受心搏节律的影响,在临床上应用广泛。研究发现,E/e′升高与心房颤动患者的不良结局如心衰、心肌梗死等有关,并可预测房颤患者在转复或导管消融后的复发[9-10]。有回顾性临床研究发现,E/e′与阵发性房颤合并脑梗死及左房重构相关,E/e′可作为房颤合并脑梗死的危险因素[7]。然而目前关于E/e′与房颤患者发生脑梗死关系的前瞻性研究甚少。此外,还有研究发现,颈动脉粥样硬化与房颤患者并发缺血性脑卒中有关,并且颈动脉硬化与CHA2DS2-VASc评分、心肌重构和舒张功能障碍显著相关[11-14]。因此,本研究进一步探讨了E/e′及颈动脉斑块与房颤患者并缺血性脑卒中之间是否存在相关性,以期为临床房颤患者管理及减少血栓栓塞事件提供指导。
1 资料与方法
1.1 研究对象
选择2013年1月~2015年12月在湖北省恩施州中心医院首次诊断为非瓣膜性心房颤动患者642例,所有患者心功能均为NYHA Ⅰ~Ⅱ级,在完善心电图或动态心电图或床旁心电监护等检查后,最终由心电图室专业医师诊断为房颤,房颤诊断标准符合2019年ACC/AHA/HRS房颤诊断及治疗指南[15]。在排除合并有重度二尖瓣环钙化、严重二尖瓣疾病、心包疾病、严重冠心病、节段性室壁运动异常、风湿性心脏病、心脏瓣膜置换术后等病理情况的患者后,剩余533例符合条件的患者。排除不愿配合的对象26例,纳入507例对象。所有纳入患者在入组时均行基线心脏超声心动图检查,并随访至2019年12月31日,最终排除在随访过程中行心房颤动导管消融的患者41例,剩余466例有效研究对象。研究对象的筛查流程见图1。本研究经过恩施州中心医院伦理委员会审查批准,所有患者均知情同意。

图1 研究对象筛查流程图Fig.1 Flow chart of research objects screening
1.2 研究方法
1.2.1 基线资料 记录研究对象的一般信息,包括姓名、年龄、身高、体重、体质量指数(body mass index,BMI)、房颤类型;收集相关危险因素,如吸烟史、高血压病(hypertension,HBP)、糖尿病(diabetes,DM)、高脂血症、冠心病、慢性肾功能不全(chronic kidney disease,CKD)、缺血性脑卒中(ischemic stroke,IS)、短暂性脑缺血发作(transient ischemic attack,TIA)、动脉硬化等病史及心功能情况;并记录患者的药物治疗情况,如β受体阻滞剂、抗血小板、抗凝、调脂、ACEI/ARB等用药情况。所有患者在入院后空腹采集静脉血完善相关生化指标,如谷丙转氨酶(glutamic pyruvic transaminase,ALT)、谷草转氨酶(aspartate transaminase,AST)、尿素、肌酐、尿酸、糖化血红蛋白(HbA1c)、NT-proBNP、肌钙蛋白T(Troponin T,CTnT)、C反应蛋白(C-reactive protein,CRP)等指标;按照Stevenson公式计算体表面积(body surface area,BSA),BSA=0.0061×身高(cm)+ 0.0128×体重(kg)-0.1529,单位为m2[16];行心电图及动态心电图检查,以记录房颤发生的情况;进行颅脑MRI或颅脑CT检查以明确颅脑是否存在缺血病灶。
1.2.2 心脏超声心动图 所有对象均在首次就诊24 h内完善心脏超声心动图检查,所用设备为飞利浦iu22。采用二维容积测量法中的单平面Simpson法测量左室舒张末期容积(leftventricular end diastolic volume,Vd)及左室收缩末期容积(leftventricular end systolic volume,Vs)。具体方法为沿左室长轴将左室切割成与长轴垂直的等厚切面,并对这些圆柱切面进行体积积分并得出左室容积,左室容积=(A1+A2+...An)×h,h=L/n,A为各圆柱体体积,h为各圆柱体厚度,L为左室长径,n为断面数。计算左室射血分数(left ventricular ejection fraction,LVEF)=(Vd-Vs)/Vd×100%。采用彩色多普勒超声在二尖瓣口测量充盈早期峰值血流速度即为E峰,采用组织多普勒于室间隔侧测量舒张早期二尖瓣环速度即为e′,并计算E/e′值。采用M型超声分别测量左室舒张末期内径(left ventricular end diastolic diameter,LVDd)、左室收缩末期内径(left ventricular end systolic diameter,LVDs)、左房前后径(left atrial diameter,LAD),连续测量3个心动周期,取平均值[17]。
1.2.3 颈动脉超声检查 颈动脉超声检测主要包括颈动脉内中膜厚度和颈动脉斑块的测定。颈动脉超声检测部位为左右颈动脉分叉近端1 cm处。最大颈动脉内中膜厚度定义为左或右颈动脉从球部延伸至颈动脉窦上方1 cm处的最大内膜中层厚度[18-19]。颈动脉斑块的定义为:①颈动脉壁厚度异常,内膜中层厚度大于1.5 mm;②侵袭动脉管腔至少0.5 mm的局灶性结构,或者其厚度比周围的内膜中层厚度≥50%以上[20]。颈动脉超声检测方法参考美国超声心动图学会的声明进行[21]。
1.2.4 随访 按E/e′三分位数将患者分为E/e′<8.8、8.8≤E/e′<13.5、E/e′≥13.5三组,对三组患者分别进行随访研究。对所有纳入研究的对象随访至2019年12月31日,排除随访过程中进行导管消融的对象41例。随访终点为:经颅脑影像学或相关医疗文件证实为新发脑梗死,或随访期间发生IS/TIA,或死亡,或新发心血管疾病如急性冠脉综合征、心功能衰竭等,或发生以上2种以上的复合终点事件。
1.3 统计学方法
应用SPSS 26.0版统计软件进行统计学分析。计数资料采用率表示,组间比较采用卡方检验或Fisher精确概率法检验。计量资料采用均数±标准差表示,对所有计量资料先进行正态分布性检验和方差齐性分析。对于符合正态分布的计量资料,多组间均数的比较采用One-way-ANOVA检验,后采取LSD法进行两两比较;两组间比较采用t检验。对于不符合正态分布的计量资料,多组间比较采用Kruskal-Wallis秩和检验,两组间比较采用Mann-Whitney U检验。采用相关与回归分析比较E/e′与CHA2DS2-VASc评分的关系。利用Kaplan-Meier法估计主要终点事件的累积发生率,并用Log-rank检验进行组间比较。利用COX回归分析首诊非瓣膜性心房颤动患者发生脑梗死的危险因素。在多因素COX回归分析中采用4种分析模型:模型一,调整CHA2DS2-VASc评分中的相关因子;模型二,包括模型一和其他心脑血管疾病危险因素如吸烟、高脂血症、BMI、慢性肾脏病、冠心病、颈动脉斑块、既往IS/TIA等;模型三,包括模型二和抗栓(含抗血小板、抗凝)及调脂治疗;模型四:包含模型三及心脏舒张功能相关指标如(LAVI、LAD、LVEF)。调整模型中的协变量采用逐步回归的方法确定。采用ROC曲线诊断分析确定E/e′预测房颤患者脑梗死发生的最佳截断值。以P<0.05为差异具有统计学意义。
2 结果
2.1 不同E/e′值患者基线资料比较
各组基线资料见表1。BMI、CHADS2、CHA2DS2-VASc、LAD、LVDd、EF三组间比较差异具有统计学意义(均P<0.05)。既往合并高血压病、糖尿病、IS/TIA、慢性肾功能不全等疾病,以及存在颈动脉斑块、持续性房颤的比例随E/e′的升高而升高,三组间差异具有统计学意义(均P<0.05)。而年龄、性别、BSA、AST、ALT、尿素、肌酐、尿酸、HbA1c、NT-proBNP、cTnT、CRP、高脂血症、心功能在三组间比较差异无统计学意义。

表1 不同E/e′值患者基线资料比较Table 1 Comparison of baseline data of the patients with different
2.2 E/e′与CHA2DS2-VASc评分的相关性分析
将患者根据CHA2DS2-VASc评分分值分为4组:0~1分组,2~4分组,5~7分组,8~9分组,比较各组E/e′。结果表明,随着CHA2DS2-VASc评分的增高,E/e′呈明显上升趋势[0~1分组:(9.7±8.6);2~4分组:(9.8±3.5);5~7分组:(13.1±3.7);8~9分组:(14.9±3.1);P<0.01]。通过相关与回归分析发现,E/e′与CHA2DS2-VASc评分呈显著正相关(r=0.213,P<0.01)。见图2、图3。

图2 CHA2DS2-VASc评分与E/e′的关系Fig.2 The relationship between CHA2DS2-VASc score and E/e′

图3 CHA2DS2-VASc评分与E/e′的相关性分析Fig.3 Correlation analysis between CHA2DS2-VASc score and E/e′
2.3 随访结果及生存分析
2.3.1 随访结果 在平均36.6个月的随访期内,共有17例患者出现新发缺血性脑卒中/短暂性脑缺血发作,13例新发急性冠脉综合征,14例出现急性心衰,6例死亡。新发缺血性脑卒中患者E/e′、LAD、CHA2DS2-VASc、既往合并IS/TIA病史和颈动脉斑块的比例明显高于非脑卒中患者,差异均具有统计学意义(P<0.05)。见表2。

表2 新发缺血性脑卒中及非脑卒中患者基线资料比较Table 2 Comparison of general baseline data between IS/TIA and non-IS/TIA
2.3.2 生存分析 进一步行Kaplan-Meier生存分析示:E/e′≥13.5患者缺血性脑卒中累计发生率(P=0.041)、心衰累计发生率(P=0.036)均明显高于8.8≤E/e′<13.5组及E/e′<8.8组。见图4、图5。而急性冠脉综合征(P=0.127)、全因死亡(P=0.420)的累计发生率在3组间比较差异没有统计学意义。
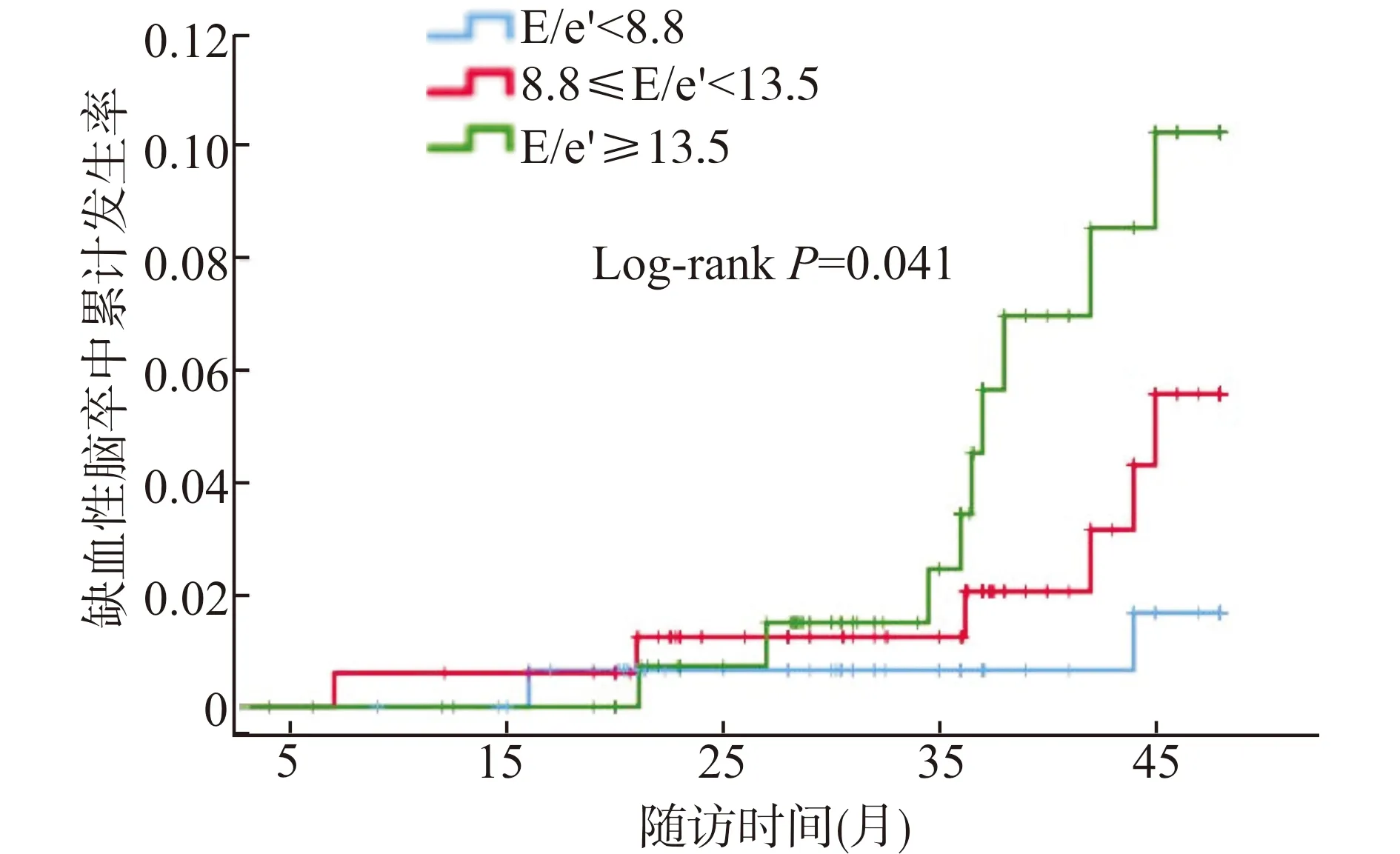
图4 缺血性脑卒中的累计发生率Fig.4 Cumulative incidence of IS or TIA
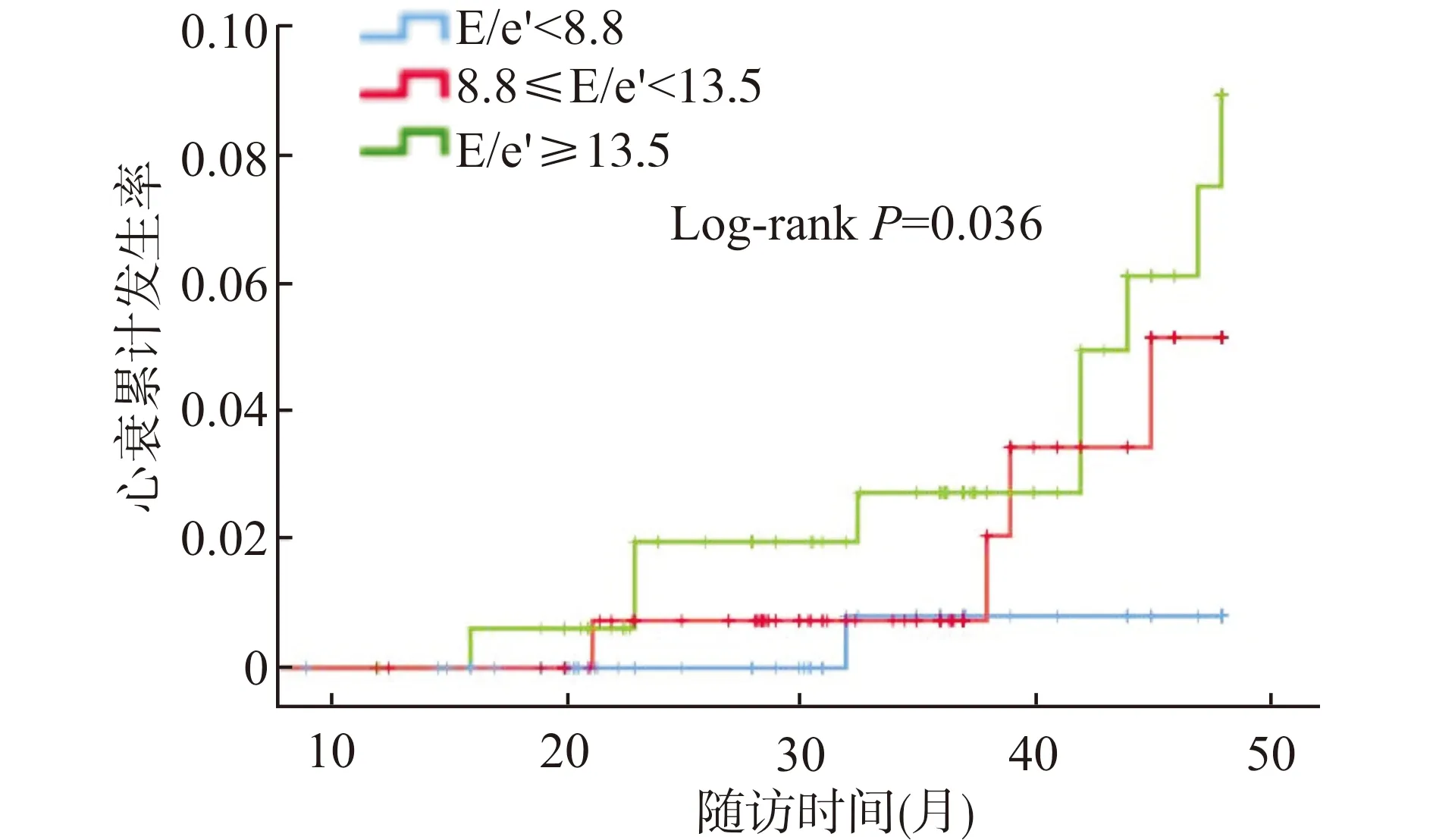
图5 心衰的累计发生率Fig.5 Cumulative incidence of heart failure
2.4 COX回归分析
为进一步分析房颤患者并发缺血性脑卒中的危险因素,我们分别进行了单因素和多因素COX回归分析。单因素COX回归分析结果提示:8.8≤E/e′<13.5、E/e′≥13.5、年龄≥75岁、吸烟、BMI、HBP、DM、既往IS/TIA、颈动脉斑块、抗血小板药、抗凝药、他汀类药物、LAD为房颤患者并发缺血性脑卒中的危险因素。在多因素回归分析中,采用了4种分析模型,调整模型中的协变量采用逐步回归的方法确定。结果显示:E/e′≥13.5是房颤患者发生缺血性脑卒中的危险因素(HR:2.103,95%CI:1.721~3.059,P=0.011)。此外,颈动脉斑块(HR:1.591,95%CI:1.041~3.125,P=0.008)、年龄≥75岁(HR:1.621,95%CI:1.351~2.868,P=0.035)、LAD(HR:2.057,95%CI:1.896~3.400,P=0.003)均为房颤患者发生缺血性脑卒中的危险因素。见表3、表4。
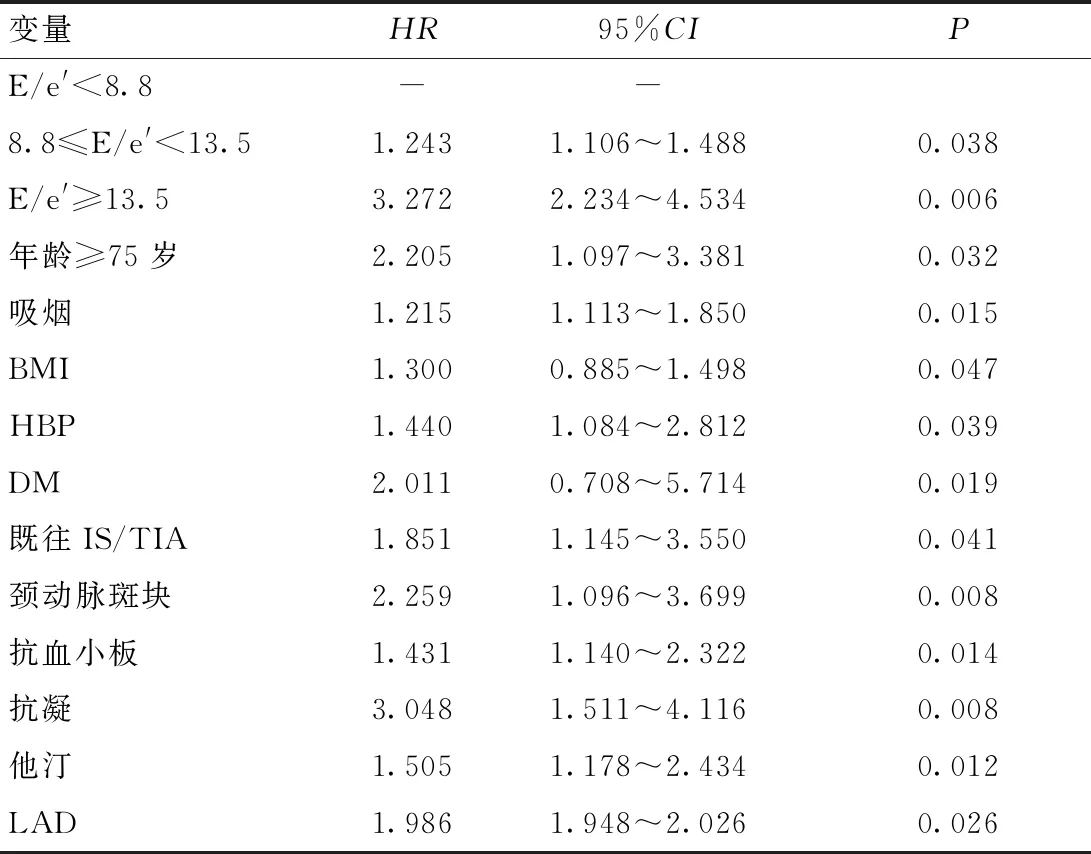
表3 单因素COX回归分析Table 3 Univariate COX regression analysis
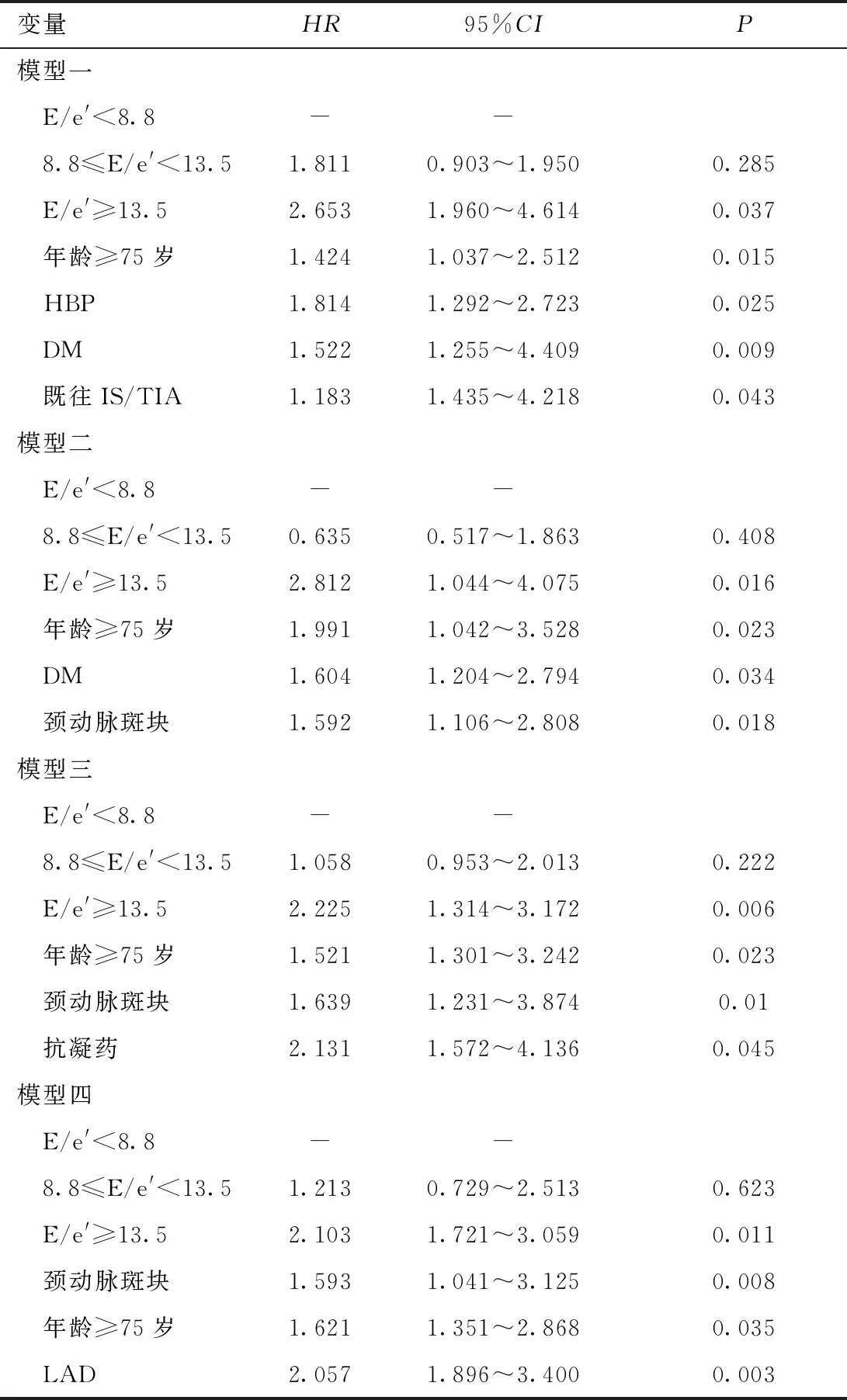
表4 多因素COX回归分析Table 4 Multivariate COX regression analysis
2.5 ROC曲线分析
ROC曲线分析示:E/e′诊断缺血性脑卒中的ROC曲线下面积为0.658(95%CI:0.537~0.779),最佳截断值为13.85,敏感度和特异度分别为70.6%和74.6%。
3 讨论
房颤是临床上常见的心律失常,其特点是左房不同步收缩导致心房的机械收缩功能丧失,从而使血液在心房内容易形成涡流,血液瘀滞,从而导致血栓的形成[4,6-7]。因此,房颤被称为隐形的杀手。临床上有多种评估房颤患者血栓栓塞风险的策略,其中,最常用的就是CHA2DS2-VASc评分系统[4]。
E峰为二尖瓣口心室舒张快速充盈早期峰值血流速度,e′为舒张早期二尖瓣环速度,E/e′是临床上评估心室充盈压力和心室舒张功能的有效指标,与多种心血管疾病有关[9,22-23]。近年来,有多项回顾性研究发现,心脏舒张功能不全是房颤患者并发脑栓塞的危险因素。例如,Kim等[7]的研究发现,E/e′估测的高左心室充盈压与阵发性房颤患者的左房排空速度和左房结构性重构有关,并与卒中或TIA的存在独立相关。而Park等[24]研究发现舒张功能减退与左房解剖重构程度及卒中风险相关。日本一项研究也发现,以E/e′比值升高来评价左室舒张功能受损与无症状性脑梗死的存在密切相关,并且独立于CHA2DS2-VASc评分[10]。此外,还有学者发现非房颤患者E/e′增高与缺血性脑卒中及远期发生房颤的风险相关[25]。本研究表明,房颤患者E/e′升高是发生缺血性脑卒中的独立危险因素。关于舒张功能减退与血栓风险增加可能的机制,考虑心室舒张功能减退时,为了维持左房的博出量,左房会代偿性增大,长期的左房压力和容量超负荷会引起的心房纤维化改变对左房顺应性和功能降低也进一步加重了血液瘀滞,从而增加血栓形成的风险[26-29]。
本研究还发现,E/e′与CHA2DS2-VASc呈明显正相关,这与Jang等[1]的研究结果一致。他们在研究中发现CHA2DS2-VASc评分增加与舒张功能受损、左室肥厚有关,并提示舒张功能减退可能代表高左房压力、并且有利于血栓形成。我们知道,CHA2DS2-VASc评分中的危险因素如高血压病、充血性心力衰竭、严重血管疾病如冠心病均可直接或间接影响左室舒张功能[4,30]。CHA2DS2-VASc评分是临床上一种简单易行的血栓风险评估系统,但CHA2DS2-VASc评分本身有其局限性,其并不能反映房颤患者心脏结构或功能的改变,而心脏结构功能的改变恰恰正是血栓形成的病理解剖学基础[1,3,31]。
此外,我们研究中还发现房颤患者颈动脉粥样硬化与E/e′比值密切相关,颈动脉斑块是缺血性脑卒中的独立危险因素,颈动脉粥样硬化增加了缺血性脑卒中的风险。这与前期多项研究结果相似[11,14,32-33]。Cho等[11]的研究对310例房颤患者进行了平均长达31个月的随访,他们发现颈动脉粥样硬化与缺血性卒中风险有关,是缺血性脑卒中的独立预测因子,颈动脉硬化与CHA2DS2-VASc评分、心肌重构和舒张功能障碍显著相关。颈动脉粥样硬化与心脏重构的关系提示全身动脉粥样硬化可能是房颤患者缺血性卒中发生的机制之一。关于颈动脉粥样硬化斑块与房颤及心脏舒张功能不全关联的可能机制如下:动脉粥样硬化尤其是全身动脉硬化可能通过减少对心房的冠脉供血、导致心肌细胞过早凋亡、纤维替代和增强折返过程而导致心房组织损伤。全身动脉粥样硬化后心肌缺血和后负荷增加可能引发心肌重构、心肌舒张功能障碍、左心房充盈压力增加和左心房增大[34]。
CHA2DS2-VASc评分系统中的血管疾病包括心肌梗死、外周动脉疾病和主动脉斑块,而不包括颈动脉粥样硬化[15,35-36]。然而,在常规临床实践中,主动脉斑块的诊断是很困难的,而颈动脉粥样硬化则可通过颈动脉超声易于评估。此外,颈动脉粥样硬化与脑血管系统在解剖和功能上更临近。因此,我们认为,在评估房颤患者发生缺血性脑卒中风险时,常规评估颈动脉硬化及颈动脉斑块具有重要意义。
综上,我们认为,在房颤的临床管理中,除了常规行CHA2DS2-VASc评分外,系统评估房颤患者心室舒张功能及颈动脉硬化斑块形成对减少栓塞事件具有重要临床意义。本研究也有一定局限性:①在评估舒张功能时应当考虑年龄因素。由于老年人舒张功能不全可能与心室僵硬度增加有关。②我们仍无法判断颈动脉粥样硬化和缺血性脑卒中之间的联系是由血栓栓塞还是动脉粥样硬化血栓形成引起的。③由于本研究是基于单中心队列,样本量相对较小,后续还需大样本量的多中心研究进一步验证本研究结果。
(2020-05-27 收稿)
