系统免疫炎症指数联合糖类抗原199在胆囊癌预后评估中的作用
2021-11-01任国亮李连生
任国亮,李连生,苏 伟,丰 帆
肿瘤年报数据显示,2018年全球新增恶性肿瘤约1810万,新增死亡病例960万,其中中国地区恶性肿瘤新发、死亡病例分别为380万、230万,均居全球首位[1]。胆囊癌是消化系统常见的恶性肿瘤之一,约占所有肿瘤的1%,也是胆道系统最常见、侵袭性最强的恶性肿瘤[2]。由于发病隐匿,胆囊癌的早期症状缺乏特异性,早期诊治率较低,多数患者确诊时已属于中晚期,预后较差。据调查显示,胆囊癌患者中,能行根治性手术者占22%~38%,多数患者不得不行姑息性手术或采用其他方案治疗,5年生存率较低[3]。近年来,虽然随着化疗药物的更新、新辅助放化疗的应用、免疫及靶向治疗的进步,胆囊癌患者术后生存期虽有一定延长,但尚不满意,尤其是进展性晚期胆囊癌患者[4-5]。早期预测胆囊癌患者预后状况,并及时采取个体化治疗策略对患者预后的改善至关重要。糖类抗原199(CA199)是常用的肿瘤标志物,在乳腺癌、胃癌、结直肠癌、胰腺癌等肿瘤的早期诊断与预后评估中具有一定价值[6-9]。有研究显示,CA199≥40 U/ml是胆囊癌患者预后不良的独立危险因素,但其敏感度不高(约70%),单独应用受限[10]。随着研究的不断深入,免疫炎症反应在肿瘤进展中的作用逐渐引起学者的关注。系统免疫炎症指数(SII)能综合反映炎症-免疫状况,在肺癌、肾细胞癌、结直肠癌等多种肿瘤的预后评估中有较高的应用价值[11-13],但其能否预测胆囊癌患者预后尚不清楚。本研究旨在探讨术前SII联合CA199在胆囊癌患者预后评估中的作用。
1 资料与方法
1.1一般资料 回顾性收集并分析2006年5月—2020年2月我院手术治疗278例胆囊癌的临床资料。其中男172例,女106例;年龄(60.23±9.80)岁;分化程度:中高分化119例,低分化159例;临床分期:Ⅰ~Ⅱ期86例,Ⅲ~Ⅳ期192例。①纳入标准:均行手术切除治疗,且经组织病理证实为原发性胆囊癌;术前未进行其他治疗;术后治疗按照《胆囊癌诊断和治疗指南(2019版)》[14]。②排除标准:合并其他肿瘤者;有血液系统疾病、慢性或急性感染性疾病者;长期使用免疫抑制剂者;术后失访,预后信息不完整者。
1.2方法
1.2.1基线资料收集:通过电子病历系统收集患者基线资料,包括一般资料(年龄、性别、手术方式等)、血清学(血常规、肝肾功能、肿瘤标志物等)、肿瘤特征(肿瘤直径、分化程度、临床分期、淋巴结转移情况等)。其中SII=中性粒细胞计数×血小板计数/淋巴细胞计数;临床分期的判定依据美国癌症联合委员会发布的第8版标准;分化程度依据组织病理结果判定。
1.2.2随访:手术治疗后采用门诊、电话或再入院的形式对患者进行随访,每3个月随访1次。随访时间为1~60个月,末次随访时间为2020年12月31日。记录患者生存情况,并依据患者末次随访时的生存情况分为存活组42例(15.11%)和死亡组236例(84.89%)。
1.3统计学方法 应用SPSS 22.0统计学软件进行数据分析。计数资料以率(%)表示,比较采用χ2检验;Kaplan-Meier法绘制生存曲线;多因素Cox回归分析胆囊癌患者死亡的危险因素;受试者工作特征(ROC)曲线分析SII、CA199预测胆囊癌患者死亡的效能。α=0.05为检验水准。
2 结果
2.1术前SII、CA199预测胆囊癌患者死亡的ROC曲线分析 CA199预测胆囊癌患者死亡的曲线下面积(AUC)为0.721(95%CI:0.641,0.802;P<0.001),敏感度为64.14%,特异度为78.57%,最佳截断值为116.25 U/ml。SII预测胆囊癌患者死亡的AUC为0.805(95%CI:0.740,0.871;P<0.001),敏感度为78.39%,特异度为76.19%,最佳截断值为635.38。SII联合CA199预测胆囊癌患者死亡的AUC为0.875(95%CI:0.821,0.930;P<0.001),敏感度为85.59%,特异度为80.95%。SII联合CA199预测胆囊癌患者死亡的AUC高于SII或CA199单独预测,且SII高于CA199(P<0.05)。见图1。
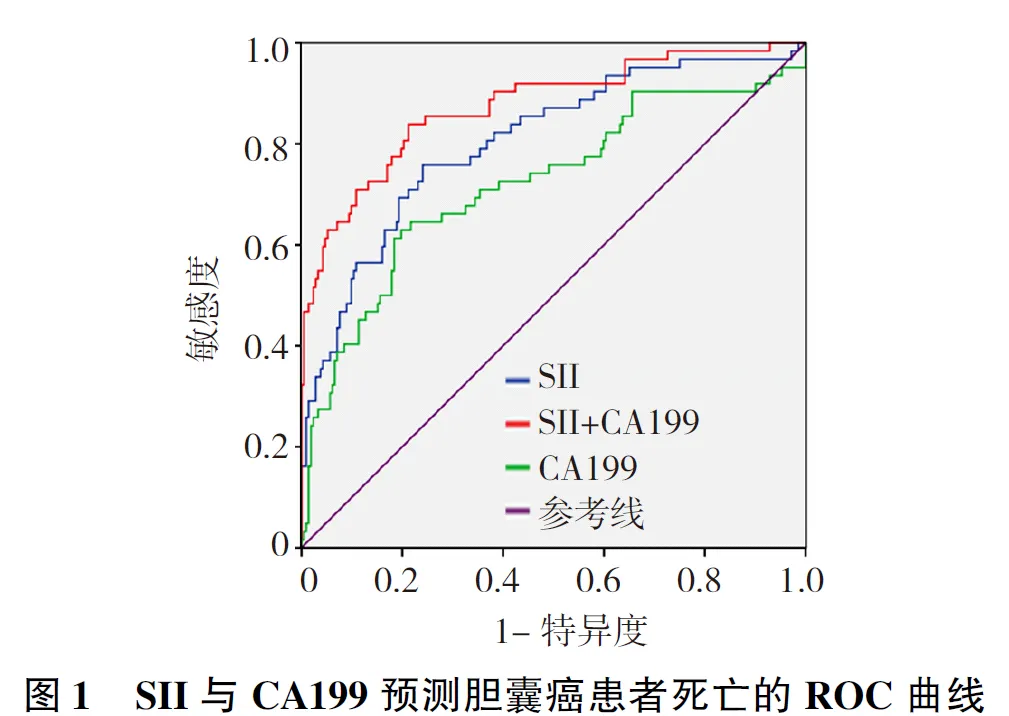
2.2单因素分析 死亡组行姑息手术、SII>635.38、癌胚抗原(CEA)>9.78 ng/ml、CA125>92.56 U/ml、CA199>116.25 U/ml、低分化、临床分期Ⅲ~Ⅳ期、有淋巴结转移比例高于存活组(P<0.05,P<0.01)。两组年龄、性别、总胆红素、血肌酐、肿瘤直径比较差异无统计学意义(P>0.05)。见表1。

表1 影响胆囊癌患者死亡的单因素分析(例)
2.3多因素Cox回归分析 以单因素分析中差异有统计学意义的指标为自变量,末次随访时生存状况为因变量进行多因素Cox回归分析,结果显示姑息手术、SII>635.38、CA199>116.25 U/ml、临床分期Ⅲ~Ⅳ期、有淋巴结转移是胆囊癌患者死亡的独立危险因素(P<0.05,P<0.01)。见表2。

表2 影响胆囊癌患者死亡的多因素Cox回归分析
2.4不同SII及CA199水平胆囊癌患者的预后分析 Kaplan-Meier生存曲线显示,SII高表达组(>635.38)、CA199高表达组(>116.25 U/ml)的5年生存率分别为11.32%(24/212)、11.29%(21/186),SII低表达组(≤635.38)和CA199低表达组(≤116.25 U/ml)分别为27.27%(18/66)和22.83%(21/92)。SII高表达组和CA199高表达组的5年生存率分别低于SII低表达组和CA199低表达组(P<0.05)。见图2。

3 讨论
胆囊癌早期诊治率低,病情进展迅速,肿瘤细胞极易发生远处转移,患者预后较差[15]。国外学者Ostwal等[3]研究显示,胆囊癌患者预后较差,在现有医疗条件下,及时采用标准方案治疗的患者,其5年生存率为2.7%~20.1%。鲍建亨等[16]对90例胆囊癌患者随访显示,其1年生存率为68.9%、3年生存率为23.1%、5年生存率仅为10.7%。温志坚等[17]对386例手术治疗的胆囊癌患者进行回顾性分析,发现其1、3、5年生存率分别为51.8%、25.2%、16.8%。本研究中,胆囊癌患者5年生存率为15.11%,符合上述报道范围,且与姚晶等[18]的报道结果相近。不同研究间胆囊癌患者预后存在差异的原因:①入组患者的基础状况、治疗策略不同;②样本量存在差异,检验效能不同;③不同的地区,医疗水平存在一定差异,导致患者预后不尽相同。由此可知,胆囊癌患者预后情况仍很严峻,亟待改善。
早期诊治、及时对预后情况进行评估,对改善胆囊癌患者的预后至关重要[19]。CA199为黏液性蛋白,正常人血液中含量极低,其作为常用的肿瘤标志物,在多种肿瘤的早期诊断及预后评估中发挥重要作用。张阳和杨清堂[20]研究结果显示,CA125、CA199联合CEA诊断胆囊癌的敏感度为93.33%。李晓洁等[21]研究发现,CA199>120.11 U/ml是肝内胆管细胞癌预后不良的独立危险因素。刘利民[22]在胆囊癌的研究中亦得出类似的结果,与术前CA199低表达组比较,CA199高表达组更易出现不良预后,生存期缩短的风险增加12.7%。以上研究结果均提示,CA199在一定程度上能够预测胆囊癌预后,但其也存在局限性,如单独用于胆囊癌早期诊断及预后评估的敏感度均较低。CA199为Lewis相关抗原的组成成分,部分人群缺乏此基因表达,此类胆囊癌患者检测CA199时为假阴性[20];另外,在部分良性疾病如肝实质损伤、梗阻性疾病中CA199也可升高,导致假阳性结果[23]。本研究结果显示,CA199升高是胆囊癌患者死亡的独立危险因素,且CA199预测胆囊癌患者死亡的AUC为0.721,提示其预测价值中等,单独应用受限,符合上述报道结果。
随着研究的不断深入,发现肿瘤的进展与侵袭不仅取决于肿瘤细胞的特性,也与肿瘤微环境关系密切。炎症细胞是肿瘤微环境的组成部分,其分泌的细胞因子如肿瘤坏死因子-α、血管内皮生长因子等不仅能促进新生血管的生成,而且能调节肿瘤细胞的增殖、侵袭活性,并影响肿瘤细胞的凋亡[24-25]。SII可综合反映免疫功能和炎症反应情况,其升高提示血小板及中性粒细胞增多,而淋巴细胞减少,机体处于炎症反应增强,免疫功能较弱的状态。中性粒细胞增多促进肿瘤发生及发展的机制:①中性粒细胞增多能释放更多的氧自由基,导致细胞DNA被破坏,抑癌基因失活,癌基因被激活,从而促进肿瘤的发生[26];②通过多种途径,如HMGB1/RAGE/IL-8轴增强肿瘤细胞的侵袭能力,促进肿瘤转移[27];③抑制T细胞活化,不利于机体免疫系统清除肿瘤细胞。血栓形成是肿瘤进展的重要机制,血小板增多一方面能增加血液的黏性,引起循环肿瘤细胞的边集化,进而穿透基底膜发生远处转移;另一方面,血小板增多会释放趋化因子和多种蛋白水解酶,增强肿瘤细胞的侵袭性[28]。淋巴细胞数目减少提示免疫监视功能降低,利于肿瘤的生长及侵袭。
SII在肿瘤患者预后评估中的作用,已得到广泛证实。在食管癌中,SII高表达组(≥686.9)预后不良的风险是SII低表达组的2.615倍[29]。SII高表达(≥570.5)是胃癌患者预后不良的独立危险因素[30]。还有meta分析显示,SII升高与胰腺癌患者的总生存期缩短有关[31]。在胆囊癌相关研究中,SII高表达组(>510.42)的1、3、5年生存率分别为27.9%、12.0%、9.6%,显著低于SII低表达组的65.7%、39.6%、30.2%[32]。本研究结果显示,SII高表达组(>635.38)的5年生存率低于SII低表达组,进一步多因素Cox回归分析在校正其他影响因素后显示,SII>635.38是胆囊癌患者死亡的独立危险因素,与上述报道相符。
本研究ROC曲线分析显示,SII预测胆囊癌患者死亡的AUC高于CA199,SII联合CA199预测的AUC最高,且敏感度和特异度均较高。提示SII对胆囊癌患者死亡的预测价值高于CA199,且二者联合的预测价值最高,可用于早期预测胆囊癌患者的死亡风险。
综上所述,术前SII、CA199升高是胆囊癌患者死亡的独立危险因素,二者联合检测对预测胆囊癌患者死亡具有较高的敏感度和特异度。本研究局限性为单中心、样本量小,且为回顾性分析,检验效能受限;此外,SII的临界值在临床工作中的实际意义,尚需进一步研究证实。
