钝性分离在儿童B超引导结合改良塞丁格PICC置管中的应用
2021-10-27范菊红吴菲菲
范菊红 谢 珺 宋 娜 吴菲菲
1.南京医科大学附属无锡儿童医院 无锡市儿童医院血液科,江苏无锡 214000;2.南京医科大学附属无锡儿童医院 无锡市儿童医院护理部,江苏无锡 214000
B超引导结合改良塞丁格技术(modified seldinger technique,MST)行经外周静脉穿刺中心静脉导管(peripherauy inserted central catheter,PICC)具有选择合适留置部位、合适血管通道、合适穿刺方法等优势,可提高护士对上臂血管的评估能力,使其在直视下穿刺,利于提高PICC置管成功率,减少静脉血栓等并发症的发生[1-2]。但在PICC置管过程中需应用手术刀扩皮,可对皮肤真皮层造成破坏,损伤淋巴管、血管、神经等,导致穿刺点渗血或渗液[3]。钝性分离为一种外科手术操作技术,指应用手术刀柄、止血钳等器械分离原本完整的软组织,避免应用刀与剪刀[4]。PICC置管中应用钝性分离可避免应用手术刀扩皮,通过扩张器扩张穿刺点,再将扩张器与外鞘组合送入血管内。有研究显示[5],B超引导下结合MST行PICC置管时应用钝性分离法,可有效减少出血量及穿刺点渗液。本研究将钝性分离用于儿童B超引导结合MST行PICC置管中,旨在评价其应用价值。
1 资料与方法
1.1 一般资料
选取2019年1月1日至2020年12月30日南京医科大学附属无锡儿童医院PICC置管患儿60例,根据不同扩皮方式分为观察组及对照组,每组各30例。观察组男17例,女13例,年龄2~14岁,平均(8.05±1.37)岁,置管部位:左上肢16例,右上肢14例,穿刺血管:贵要静脉13例,正中静脉9例,头静脉8例。对照组男18例,女12例,年龄3~13岁,平均(8.01±1.32)岁,置管部位:左上肢17例,右上肢13例,穿刺血管:贵要静脉12例,正中静脉10例,头静脉8例。两组患者一般资料比较,差异无统计学意义(P>0.05),具有可比性。
纳入标准:均符合PICC置管适应证[6];均为首次PICC置管;家属均知情并签订同意书;研究经医院医学伦理委员会批准。排除标准:合并局部皮肤感染、穿刺部位皮损者;合并其他系统严重疾病者;过敏体质、变态反应体质者;精神、意识等功能障碍者;置管前1周服用抗凝药物者;有PICC置管禁忌证者;置管依从性较差者。
1.2 方法
两组均行B超引导结合MST技术PICC置管,均采用美国巴德单腔三向瓣膜PICC,协助患儿取合适体位,教会其术中配合技巧。使患儿术侧手臂外展90°,扎止血带,于超声探头涂抹耦合剂,对双侧上臂进行查看,并选择合适的血管。通过超声评估选择穿刺静脉及部位后松止血带,对置管长度进行测量。抬高患儿置管侧手臂,以穿刺点为中心行环形消毒,助手无菌投递PICC套件、肝素帽、无针接头等,抽吸2%利多卡因(黑龙江哈尔滨医大药业有限公司,国药准字H20013390,规格5 ml∶50 mg)及生理盐水备用。按照无菌原则将三向瓣膜PICC穿刺套件打开,对管腔进行预冲,并用生理盐水浸润导管。
观察组行钝性分离送鞘技术,扎止血带,将导针架及穿刺针安装好,将超声置于目标血管行穿刺,穿刺成功后分离探头,降低穿刺针角度,将导丝置入,在体外保留10~15 cm,送止血带,将穿刺针退出。应用2%利多卡因0.2~0.4 ml在预穿处行局部浸润麻醉,不应用手术刀扩皮,分离导管鞘内外鞘,将穿刺针外套管与钢针分离,随后组装外套管与导管鞘内鞘,并穿过导丝,将穿刺点下方皮肤绷紧,沿导丝平行方向边扭转边递送该组件进入血管内。送鞘成功后撤出导丝及内鞘,将导管置入预定长度,并校对插管长度,外露导管保留约5 cm,抽回血后用20 ml生理盐水脉冲式冲管、封管,连接肝素帽,应用无菌纱布压迫止血,外贴透明敷料固定导管,行弹力绷带包扎,24 h后取下绷带。
对照组行传统手术刀扩皮送鞘技术,前面操作与观察组一致,行局部麻醉后,按预定长度修剪导管,应用扩皮刀沿导丝上方行纵行切开皮肤3 mm,注意不要切到导丝,沿导丝边推边扭转,送入插管鞘及扩张器,随后退出扩皮器及导丝,将导管融入血管至预定长度,应用无菌纱布压迫止血,外贴透明敷料固定导管,行弹力绷带包扎,24 h后取下绷带。
1.3 观察指标及评价标准
比较两组即刻出血量、置管后24 h PICC穿刺处出血量情况,出血量判断[7]:扩皮后2 cm×2 cm的16层无菌纱布置于穿刺点上方压迫止血,浸湿面积<50%为少量出血,≥50%或<1张纱布为中量出血,≥1块纱布为大量出血。记录两组置管后1、2、4、7 d渗液发生情况,渗液定义[8]:置管后穿刺处有黄色或无色液体渗出。记录两组一次性送鞘成功率(指一次性将导管送入血管视为成功,若需再次扩皮则为不成功)、总送鞘时间、一周内维护次数。
1.4 统计学处理
应用SPSS 19.0统计学软件进行统计分析,计量资料以(x±s)表示,采用t检验,计数资料以[n(%)]表示,采用χ2检验及秩和检验,P<0.05为差异有统计学意义。
2 结果
2.1 两组患者出血情况比较
观察组即刻出血量、置管24 h出血量与对照组比较,差异有统计学意义(P<0.05),见表1。

表1 两组患者出血情况比较[n(%)]
2.2 两组患者置管后渗液发生情况比较
观察组置管后1、2、4、7 d渗液发生率分别为3.33%、3.33%、0.00%、0.00%,明显低于对照组,差异有统计学意义(P<0.05),见表2。
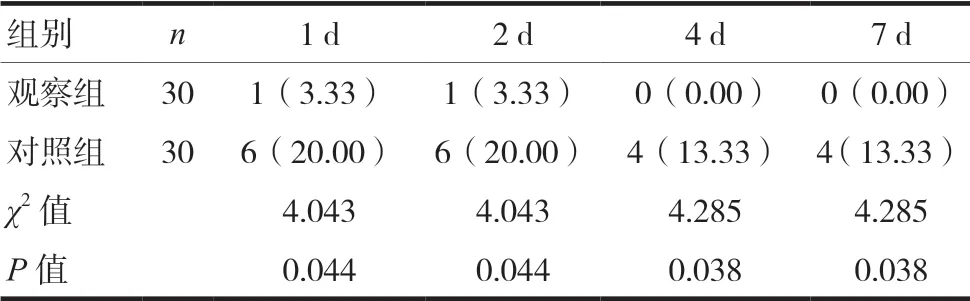
表2 两组患者置管后渗液发生情况比较[n(%)]
2.3 两组患者一次性送鞘成功率、总送鞘时间、一周内维护次数比较
观察组一次性送鞘成功率为93.33%,明显高于对照组的70.00%,观察组总送鞘时间、一周内维护次数均较对照组少,差异有统计学意义(P<0.05),见表3。
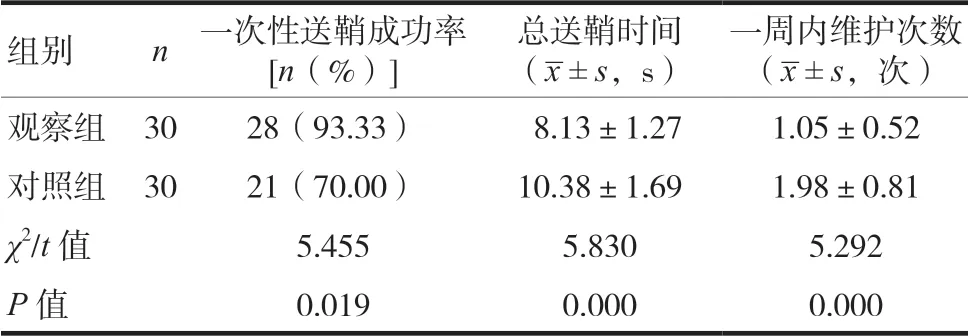
表3 两组患者一次性送鞘成功率、总送鞘时间、一周内维护次数比较
3 讨论
人体皮肤分为表皮层、皮下层及真皮层,真皮层及皮下组织血管较为丰富,且相邻血管网间有垂直交通支相连。在PICC置管过程中,传统扩皮主要应用刀片切开皮肤表皮、真皮层及皮下组织,可切断较多弹力纤维层,损伤组织及毛细血管,置管后可出现穿刺点渗血、伤口不易愈合等现象[9]。若患者皮肤组织较为疏松,置管后更易出现扩皮范围大、渗血多等情况。穿刺点出现渗血、渗液后可增加感染风险,且需频繁更换敷料,可给患儿带来不适与不便,容易引发医患纠纷[10]。
钝性分离法不需使用扩皮刀,可直接对穿刺点进行扩张,不会对淋巴管造成损伤,可降低穿刺点渗液发生风险[11]。钝性分离法沿着皮纹方向将组件送入表皮、真皮层,不会造成切割性损伤,与传统手术刀扩皮相比不依赖术者经验与技术,其扩皮范围、深度相对固定,可减少穿刺点皮肤的损伤,进而降低渗血、渗液发生风险[12]。但考虑操作部位的局限性,钝性分离法也存在着损伤毛细血管的可能。本研究结果显示,观察组即刻出血量、置管24 h出血量与对照组差异有统计学意义,提示钝性分离法用于B超结合MST技术PICC置管中可减少穿刺点出血量。李洪霞等[13]研究结果显示,干预组渗液发生率为7.5%,明显低于对照组的17.50%,本研究结果显示,观察组置管后1周内渗液发生率分别为3.33%、3.33%、0.00%、0.00%,均低于对照组,与李洪霞等[13]研究结果基本一致,提示钝性分离法还可减少穿刺点局部渗液。分析原因可能为钝性分离将插管鞘内鞘及盲穿针外套管进行组装,可避免扩皮刀切割带来的局部损伤,进而减少局部渗血、渗液发生[14]。观察组一次性送鞘成功率明显较对照组高,总送鞘时间较对照组短,分析原因可能为钝性分离外鞘管壁较薄,与扩张器贴合度较高,鞘前端与鞘身过渡约2 mm,在推进过程中可降低皮肤阻力,进而提高送鞘成功率,进而缩短送鞘时间[15]。观察组一周内维护次数较对照组少,分析原因可能为由于渗血、渗液减少,护士工作量减少,使得维护次数减少[16]。由于本研究选取样本量较少,结果可能存在一定偏差,今后还需进行大样本流行病学调查以提高结论可靠性。
综上所述,钝性分离在儿童B超引导结合MST行PICC置管中应用价值较高,可减少置管出血量及渗液,还可提高一次性送鞘成功率,缩短送鞘时间、减少维护次数,值得应用。
