煤系腐植酸磁性颗粒对水中Pb2+和Hg2+的选择性吸附
2021-10-26万克记范津津王国强许恩乐贺琼琼苗真勇张明亮
万克记,范津津,王国强,许恩乐,贺琼琼,苗真勇,,张明亮
(1.中国矿业大学 国家煤加工与洁净化工程技术研究中心,江苏 徐州 221116; 2.中国矿业大学 化工学院,江苏 徐州 221116; 3.内蒙古伊泰京粤酸刺沟矿业有限公司,内蒙古 鄂尔多斯 010300)
随着国家工业化进程的加快,采矿、氯碱化工、农药、有色金属冶炼、蓄电池制造等生产过程释放的大量重金属引发了严峻的水污染问题。以铅、汞等为代表的高毒性重金属具有难降解和生物体富集等特征,能够对人脑、肾脏、中枢神经造成极大的损伤[1],重金属环境污染正在引发人们的担忧。针对重金属废水的处置,离子交换、化学沉降、膜分离、电化学还原、生物法及吸附技术等被广泛采用[2-3]。而吸附作为一种低质量浓度重金属废水的深度净化方法,能有效避免过量化学沉淀剂导致的可溶性金属络合物的生成。
我国具有储量丰富的褐煤资源,弱化其化石能源属性,突出材料化应用,正在成为褐煤绿色化发展新趋势。腐植酸是褐煤重要的有机组分,具有丰富的羧基、酚羟基等活性基团[4-5],能够对金属阳离子产生强的络合作用,可作为廉价吸附材料用于废水中重金属的去除。为避免溶解,腐植酸的固化是其作为吸附材料应用的前提。近年来,磁性纳米颗粒(MNPs)类吸附剂,因其吸附速度快、易于固液分离、绿色环保等优势[6-9],正在成为废水中重金属吸附分离领域研究的热点。将腐植酸固化于Fe3O4表面形成腐植酸磁性颗粒(HA-MNPs)已经应用于废水中无机砷的去除[10]、海水中铀的提取[11]以及Cr(VI)的还原[12]。然而,OHA-MNPs对重金属的吸附选择性仍然较弱,难以在多金属共存溶液中实现对高毒性Pb2+和Hg2+的有效分离。
增加腐植酸表面基团密度,形成对重金属吸附稳定性和亲和度远高于单齿的多齿配位结构,可提高其对重金属的吸附选择性。煤系腐植酸分子中含有大量的酚羟基,能够通过给电子共轭效应,增加苯环电子云密度,使苯环易发生亲电取代。因而,以甲醛为氧化剂,在苯酚的邻、对位引入羟基,通过羟甲基化改性来提高腐植酸表面含氧基团密度,可为实现腐植酸对Pb2+和Hg2+的高效选择性吸附提供思路。
因此,笔者通过煤系腐植酸的羟甲基化改性来提高表面含氧基团密度,进一步共沉淀制备羟甲基化腐植酸磁性颗粒(OHA-MNPs),用于废水中Pb2+和Hg2+的吸附分离。考察了OHA-MNPs对单一Pb2+,Hg2+的吸附动力学、热力学、微观吸附机制以及多金属竞争下的Pb2+和Hg2+吸附选择性等方面。
1 实验部分
1.1 煤系腐植酸的提取与羟甲基化改性
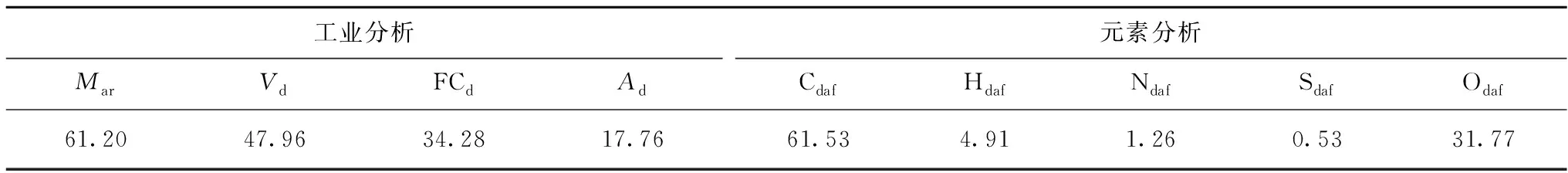
表1 昭通褐煤工业分析和元素分析Table 1 Proximate and ultimate analysis of Zhaotong lignite %
腐植酸的羟甲基化反应如图1所示。取2 g腐植酸溶于20 mL水溶液(pH=11.0)后加热至75 ℃,将1.20 mL 38%的甲醛溶液在1.5 h内分4次加入,反应2 h后,溶液冷却至室温,采用真空冷冻干燥获得羟甲基化煤系腐植酸(OHA)。
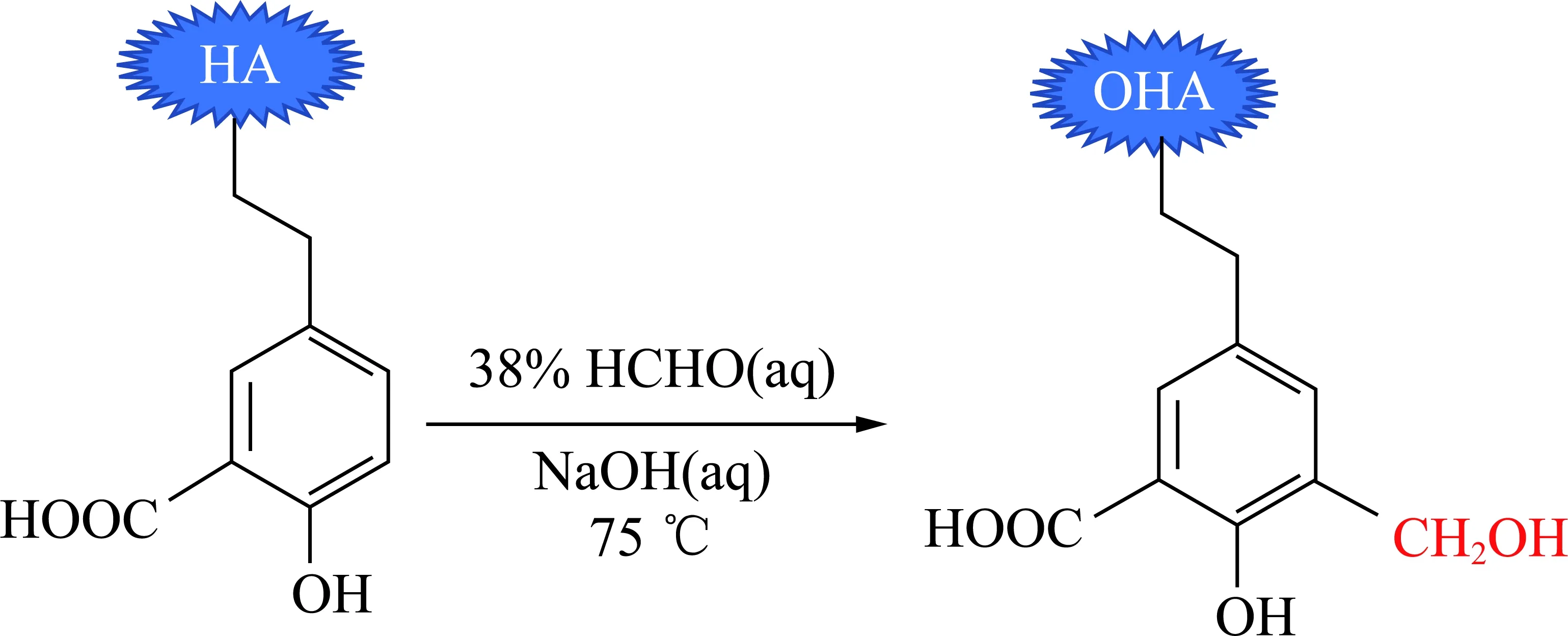
图1 腐植酸羟甲基化反应Fig.1 Hydroxymethylated reaction of HA
1.2 羟甲基化煤系腐植酸磁性纳米颗粒(OHA-MNPs)的共沉淀制备
6.0 g FeCl3·6H2O和3.0 g FeCl2·4H2O溶于100 mL去离子水后加热至90 ℃,取50 mL 1% 羟甲基化腐植酸钠溶液和10 mL 25%的氨水依次加入。在90 ℃条件下反应30 min后冷却至室温,所得黑色沉底物经去离子水洗涤,通过磁选分离、干燥后获得OHA-MNPs。采用热重分析仪(TGA),以15 ℃/min 升温速率,从室温升至1 000 ℃煅烧测定OHA-MNPs表面腐植酸含量。通过透射电镜(TEM)、X射线衍射仪(XRD)等对其表面形貌和组成进行表征。
1.3 OHA-MNPs对重金属的吸附实验
采用30 mL初始质量浓度为10 mg/L的含Pb2+或Hg2+的重金属溶液,进行吸附动力学实验。为避免pH过高引起Pb2+沉淀[13],溶液初始pH设定为5.0,吸附剂投加量控制在0.8~1.0 g/L。为维持吸附过程固液比恒定,采取多组平行吸附试验同时进行。在0~60 min内,选取不同时间节点依次终止各平行组吸附实验,最后通过磁选固液分离(图2)。借助等离子体电感耦合发射光谱仪(ICP-OES)和原子荧光光谱(AFS)测定残余溶液中Pb2+和Hg2+质量浓度。

图2 吸附剂快速磁选回收Fig.2 Rapid magnetic separation of adsorbent
取10 mg吸附剂加入30 mL含Pb2+或Hg2+的溶液,进行等温吸附实验。溶液初始pH设定为5.0。由于ICP-OES及AFS等都存在较低的质量浓度检出限,为避免初始金属质量浓度过高导致样品被过度稀释,扩大测量误差,本实验采用Hg2+初始质量浓度0~50 mg/L,Pb2+初始质量浓度0~130 mg/L。
25 mg吸附剂投加于30 mL初始质量浓度均为10 mg/L的Ni2+,Cd2+,Cu2+,Pb2+和Hg2+混合溶液中,用0.1 mol/L的HNO3和NaOH溶液调节pH,研究溶液pH对吸附过程的影响。吸附平衡后测定残余溶液金属离子质量浓度。
2 结果与讨论
2.1 OHA-MNPs吸附剂表征
图3(a)为OHA-MNPs的TEM 图及其200个颗粒的统计粒径分布。腐植酸表面大量含氧官能团,能够在水溶液中电离形成负电荷表面,颗粒间产生的静电斥力,使OHA-MNPs具有良好的溶液分散性,能够为金属离子的吸附提供较大接触面积。由图3(a)可知,OHA-MNPs颗粒粒径主要分布于7~11 nm,约占总粒度分布的67.41%。图3(b)为OHA-MNPs和MNPs的热重曲线。当加热到1 000 ℃时,MNPs失重5.19%,OHA-MNPs失重15%。因而,可计算得出附着于MNPs表面的腐植酸含量为9.81%。OHA-MNPs的XRD谱图如图3(c)所示,2θ为30.0°,35.4°,43.2°,53.5°和57.0°处分别对应OHA-MNPs中Fe3O4的(220),(331),(400),(422)和(511)晶面[14-15],这说明腐植酸的修饰并没有改变Fe3O4的晶体结构。而OHA-MNPs的XRD背景基线噪声较大,为吸附剂存在有机碳干扰。以上数据均说明,羟甲基化腐植酸成功负载于MNPs表面,形成了具有良好分散性的纳米颗粒吸附剂。

图3 OHA-MNPs吸附剂表征Fig.3 Characteristics of OHA-MNPs
2.2 吸附等温线
在pH=5.0时,OHA-MNPs分别对单一Pb2+和Hg2+的吸附等温线如图4所示(其中,qe为平衡吸附容量;Ce为吸附平衡质量浓度)。Langmuir 吸附等温模型[16]拟合系数(R2)均大于0.95,能够很好的描述OHA-MNPs对Pb2+或Hg2+的吸附热力学性质,表明以化学吸附为主的吸附过程。以Langmuir 吸附等温模型计算OHA-MNPs对Pb2+和Hg2+的最大吸附容量(qm)分别为89.05和90.09 mg/g,符合MNPs对重金属吸附容量范围[8,17-18]。
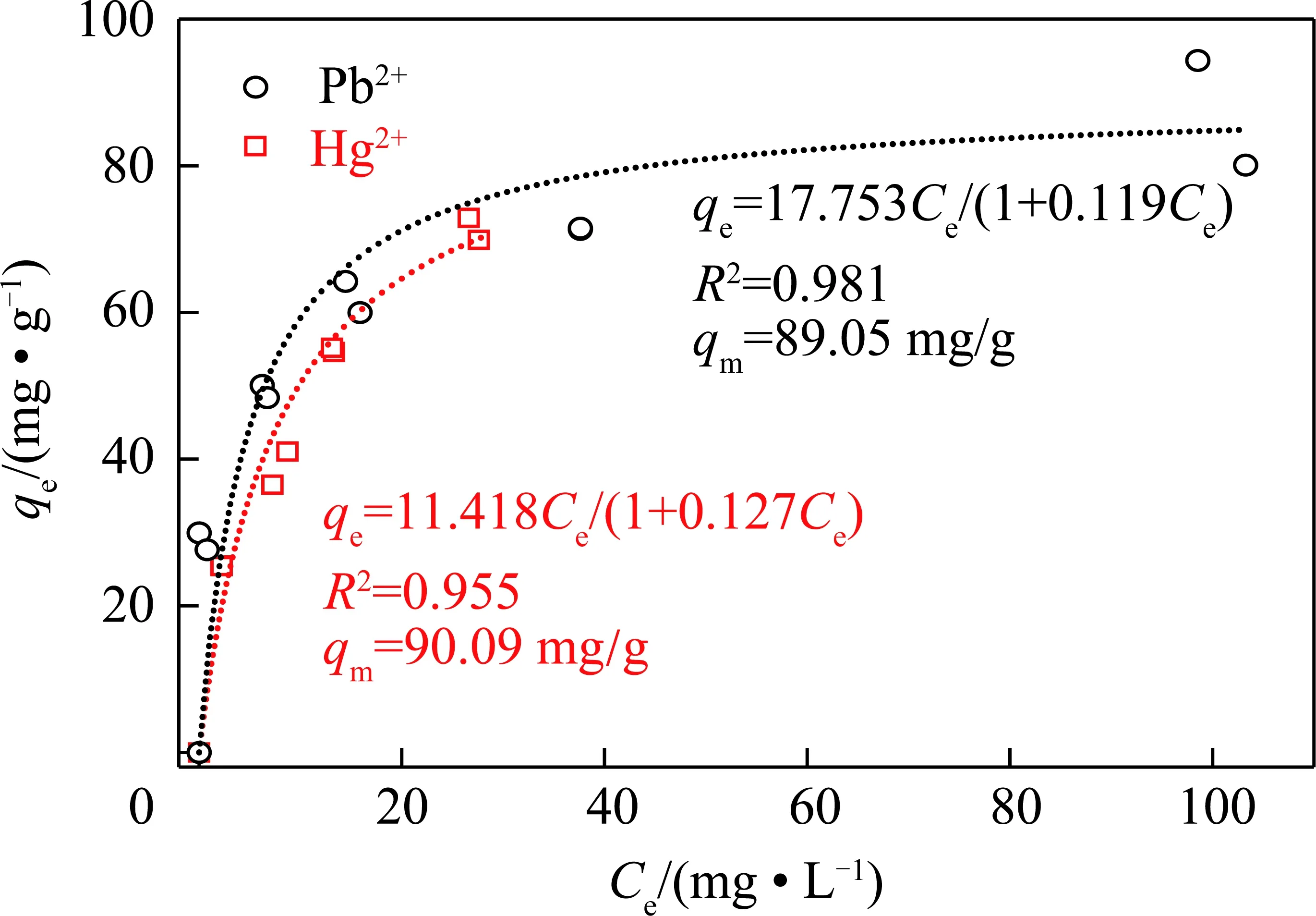
图4 Pb2+和Hg2+吸附等温线及Langmuir模型拟合Fig.4 Isothermals of Pb2+ and Hg2+ fitted by Langmuir model
2.3 OHA-MNPs对Pb2+和Hg2+吸附动力学
OHA-MNPs对单一Pb2+和Hg2+的吸附动力学曲线如图5所示。OHA-MNPs在t=5 min内将82%的Pb2+或94%的Hg2+快速去除,极高的吸附速率可归结于表面丰富的含氧基团和良好的颗粒分散性。随着吸附时间的增长,吸附速率逐渐降低,但总的吸附平衡可在30 min内达到。准一级和准二级吸附动力学模型对吸附曲线拟合结果如图6所示(其中,qt为t时刻吸附容量;k为模型常数)。准二级动力学模型能够更好的描述OHA-MNPs对Pb2+或Hg2+的吸附过程,其线性拟合相关系数R2值均达到0.999 9,远高于准一级动力学模型的0.759 4和0.831 1。这也说明络合配位、离子交换等的化学吸附是OHA-MNPs对Pb2+和Hg2+的主要作用机制[19]。
居民生活用水对管道材质要求高,引水管道全部采用PE 80级管,考虑到流量变化因素,蓄水池之前管道采用DN250PE管,蓄水池之后管道采用DN300PE管。根据各调压池之间的水头差,考虑到发生事故时水锤系数1.3的影响,引水管道压力等级在静水头差在 0~28 m 时取 0.4 MPa,28~45 m 时取 0.6 MPa,45~60 m 时取 0.8 MPa。

图5 OHA-MNPs 对Pb2+和Hg2+吸附动力学Fig.5 Adsorption kinetics of OHA-MNPs for Pb2+ and Hg2+
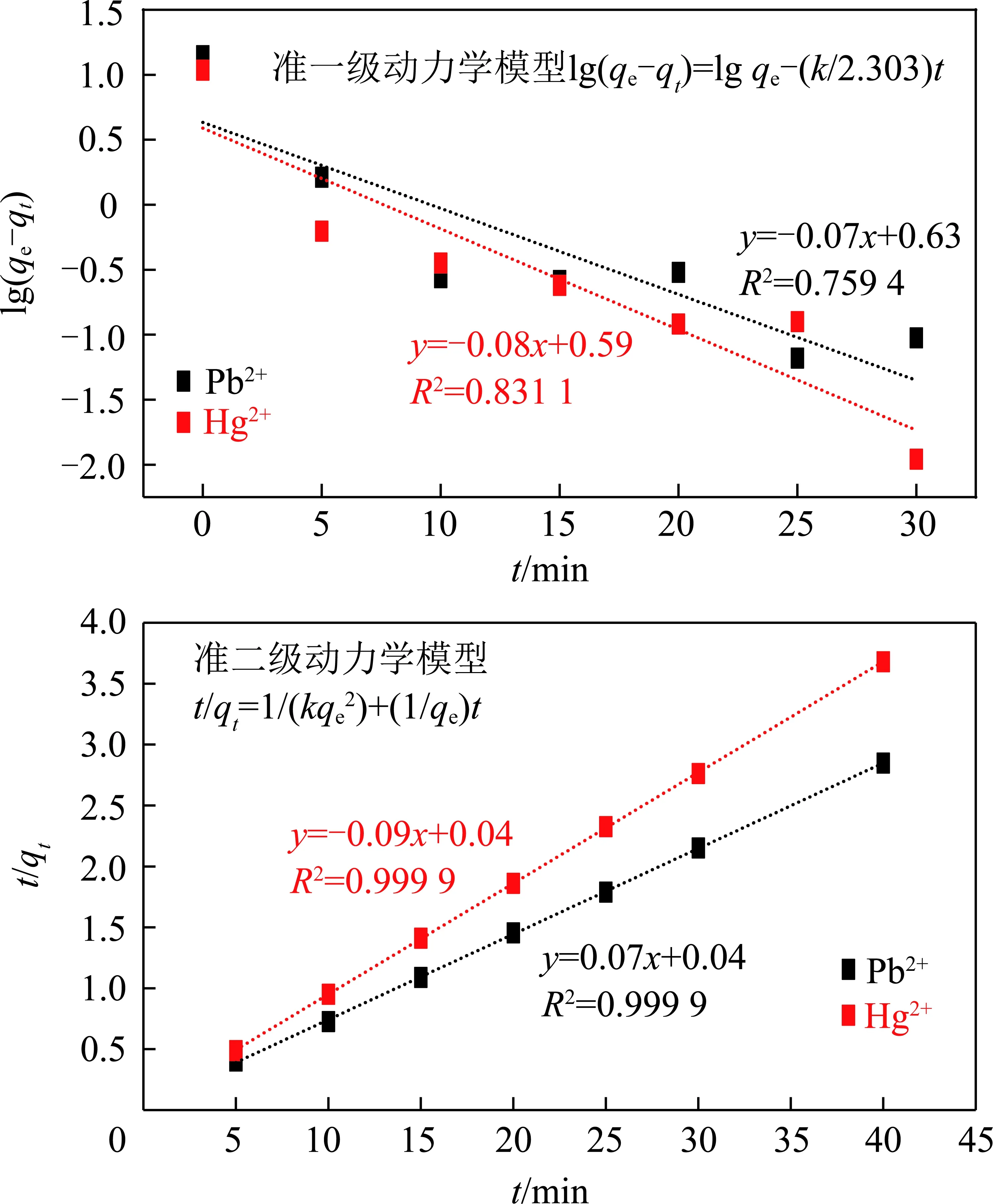
图6 Pb2+和Hg2+吸附动力学曲线线性拟合Fig.6 Linear fitting results of adsorption kinetics of Pb2+/Hg2+
2.4 吸附机制

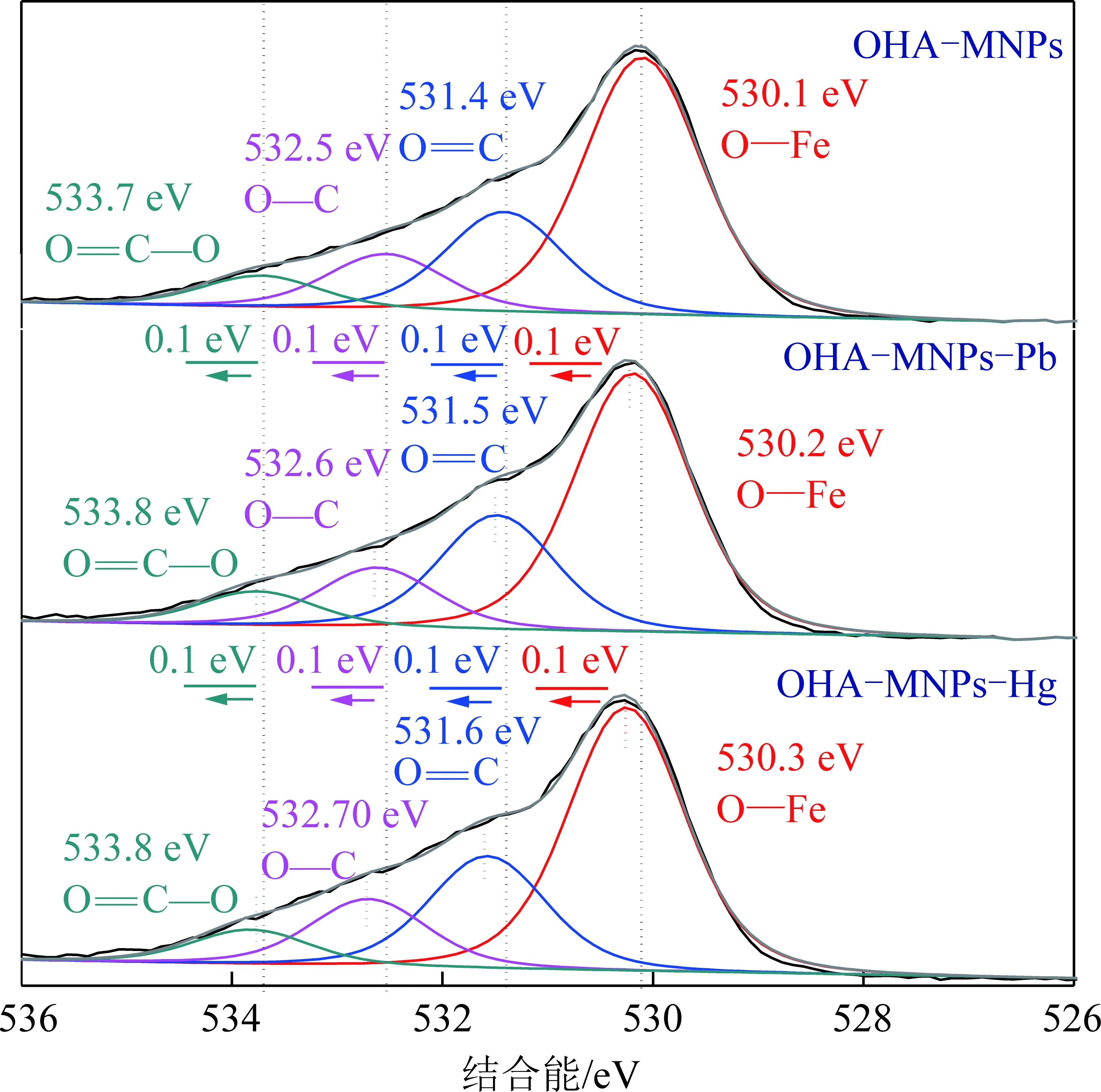
图7 OHA-MNPs吸附Pb2+或Hg2+前后O1s谱Fig.7 O1s spectra of OHA-MNPs after Pb2+ or Hg2+ adsorption
根据路易斯软硬酸碱理论[26],含硫元素对Pb2+或Hg2+具有很强配位能力。图8为OHA-MNPs对Pb2+或Hg2+吸附前后的XPS S2p精细谱。OHA-MNPs表面硫元素主要来自于煤系腐植酸,以磺酸基和C—S键形式存在。磺酸基(167~169 eV)在吸附Pb2+或Hg2+后峰位和强度变化不大,而C—S键只在吸附Hg2+后强度减弱,说明OHA-MNPs对Hg2+的吸附存在S—Hg配位。

图8 OHA-MNPs吸附Pb2+ 或 Hg2+后S2p谱Fig.8 S2p spectra of OHA-MNPs after Pb2+ or Hg2+ adsorption

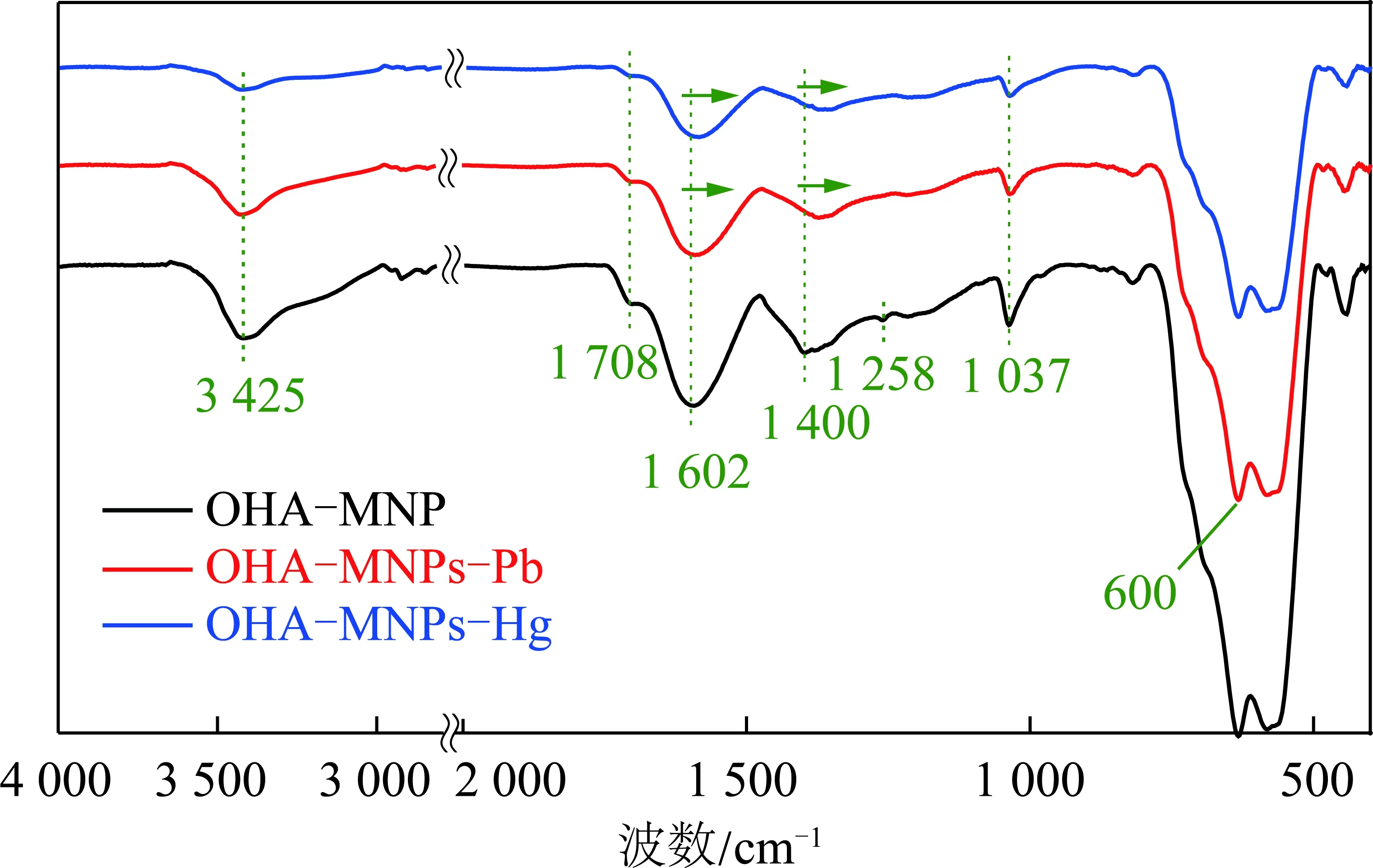
图9 OHA-MNPs吸附Hg2+或Pb2+前后红外光谱Fig.9 FTIR spectra of OHA-MNPs before and after Pb2+ or Hg2+ adsorption
随着溶液初始pH由低到高增加,OHA-MNPs对Pb2+或Hg2+吸附后的溶液pH由碱化向酸化转变,如图10所示。吸附前后溶液pH相等处可视为吸附剂OHA-MNPs的零电点[1],即pH=4.0。在pH < 4.0时,羧基、酚羟基等被大量H+包围,电离作用较弱,富集于吸附剂表面的H+导致溶液趋于碱化,吸附剂表面表现为正电,对金属阳离子存在斥力,限制了离子交换和静电吸附;当溶液初始pH > 4.0时,羧基等的电离能力增强[30],吸附剂表面负电势增加,金属阳离子对羧基、酚羟基中H+的离子交换能力增强,使得吸附后的溶液趋于酸化。上述过程证实OHA-MNPs对Pb2+或Hg2+的吸附除络合配位外还存在离子交换和静电吸附等作用。

图10 OHA-MNPs对Pb2+或Hg2+吸附前后溶液pH变化Fig.10 Variations of solution pH after Pb2+ or Hg2+ adsorption
2.5 OHA-MNPs对Pb2+和Hg2+吸附选择性
配制包含Ni2+,Cd2+,Cu2+,Pb2+,Hg2+五种重金属且初始质量浓度均为10 mg/L混合溶液用以模拟重金属废水,比较不同pH条件下的OHA-MNPs和HA-MNPs对Pb2+和Hg2+吸附选择性,结果如图11所示。随着溶液初始pH的升高,2种吸附剂对5种重金属的去除率均有不同程度的提高,这是由于吸附剂表面酸性基团电离强化了对金属阳离子静电吸附,同时,含氧基团的去质子化过程释放了更多位点。HA-MNPs对Cu2+,Pb2+,Hg2+有着较好的吸附亲和力,吸附选择性序列满足Hg2+/Pb2+> Cu2+≫ Ni2+/Cd2+。与HA-MNPs相比,OHA-MNPs在整个pH变化范围对Hg2+都表现出更好的选择性,去除率始终保持在85%以上,同时,对Pb2+的选择性也有较大提高,吸附亲和力序列为Hg2+>Pb2+≫Cu2+≫ Ni2+/Cd2+。在溶液初始pH=3.0时,85%的Hg2+和40%的Pb2+仍然附着于吸附剂,说明OHA-MNPs同Hg2+和Pb2+之间存在强烈的化学作用,且构成主要吸附机制。因而,OHA-MNPs表面较高的基团密度,有利于其对Pb2+和Hg2+吸附形成更稳固的螯合结构,从而提高吸附选择性。溶液pH对 Cu2+的吸附影响较大,pH=6.0时的Cu2+去除率约为pH=3.0时的8倍,说明吸附剂对Cu2+是以弱的配位和静电作用为主。

图11 OHA-MNPs 和HA-MNPs对模拟废水中多金属的 竞争吸附Fig.11 Competitive adsorption of OHA-MNPs for heavy metal ions
煤炭、有色金属矿开采过程中,在风化、雨水淋滤等作用下,矿物、矸石中的金属和硫化物会溶出进入周边环境形成酸性矿井废水(AMD)[31]。本研究所选AMD中关键金属离子组成及质量浓度如图12所示。Ca2+初始质量浓度是Pb2+的39.43倍,总阳离子质量浓度是Pb2+的44.78倍。以OHA-MNPs为吸附剂,采用0.80 g/L的投加量吸附后,废水中Pb2+质量浓度由6.34 mg/L降至0.39 mg/L,实现了93.76%的去除率。OHA-MNPs对AMD中Pb2+表现出极高的选择性,可用于AMD中Pb2+的资源化回收利用。
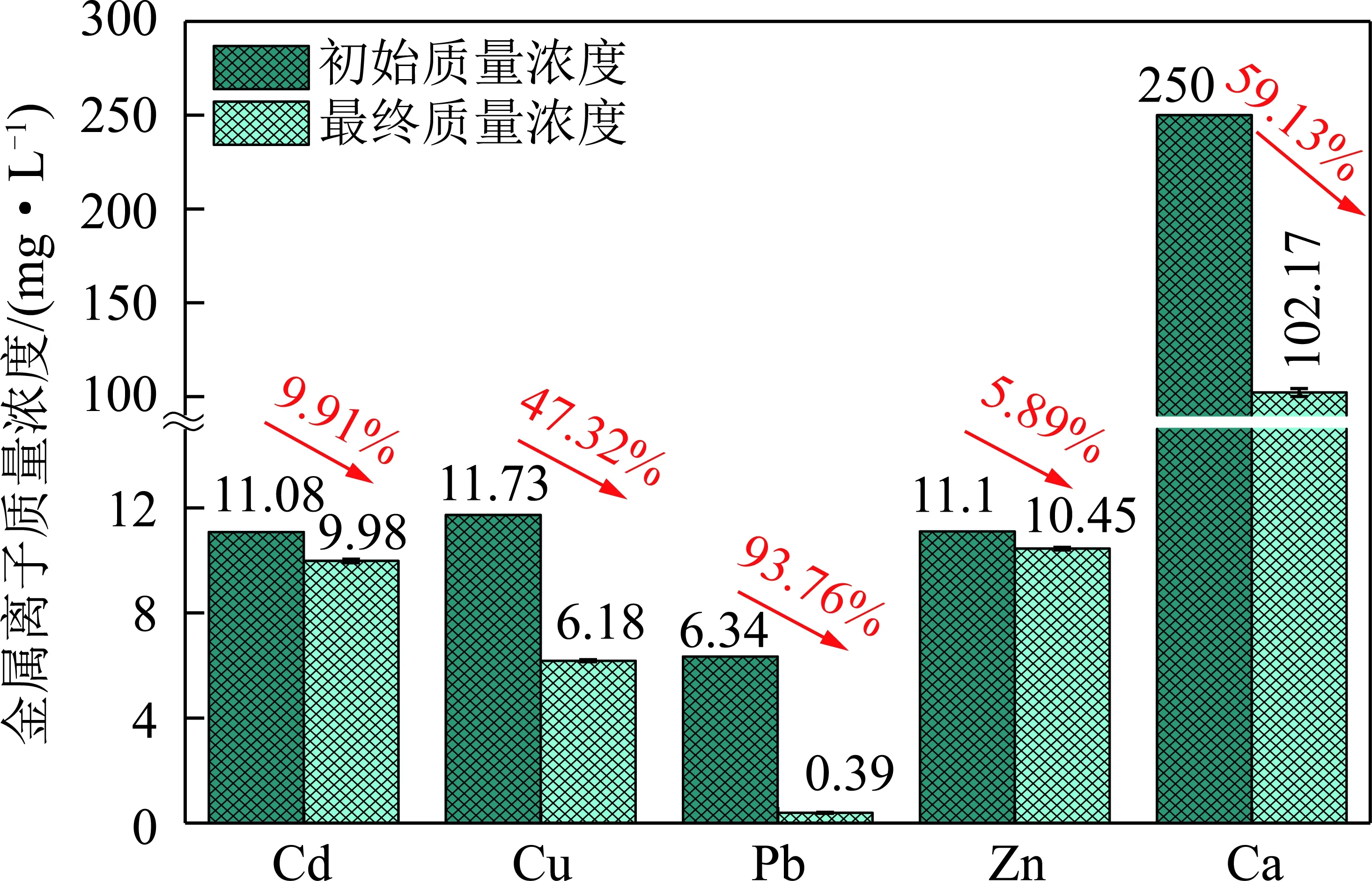
图12 OHA-MNPs对AMD中重金属的吸附Fig.12 Removal of Pb2+ in AMD using OHA-MNPs
2.6 吸附剂再生
将Hg2+或Pb2+吸附平衡后的OHA-MNPs浸泡于0.1 mol/L的乙二胺四乙酸(EDTA)溶液,充分搅拌,脱附时间为30 min。进一步用超纯水淋洗去除吸附剂表面残余EDTA,经低温烘干后进行再吸附。经过5次吸附-脱附循环后的吸附结果如图13所示。图13(a)为OHA-MNPs对Pb2+的循环再生结果,5个循环后OHA-MNPs对Pb2+吸附容量基本维持不变,吸附剂表现出良好的再生性。图13(b)为Hg2+的吸附再生,在3个循环后,OHA-MNPs对Hg2+的吸附容量明显下降,这可能是由于OHA-MNPs表面基团对Hg2+存在更加稳定的化学吸附作用,脱附剂EDTA同Hg2+的络合作用不足以挣脱吸附剂表面,使得部分Hg2+仍然占据吸附位点。
3 结 论
(1)OHA-MNPs表面腐植酸含量约为9.81%,颗粒粒径主要分布于7~11 nm,具有很好的溶液分散性。
(2)OHA-MNPs能够在5 min内对溶液中绝大多数的Pb2+或Hg2+快速去除,且能在30 min内达到吸附平衡;准二级动力学和Langmuir吸附模型能够很好的描述OHA-MNPs对Pb2+或Hg2+的吸附动力学和热力学。
(3)OHA-MNPs对Pb2+或Hg2+的吸附以高密度含氧基团多齿配位为主,并伴有酸性基团离子交换和静电吸附;此外,腐植酸中原生硫参与对Hg2+的络合配位。
(4)OHA-MNPs对Pb2+和Hg2+均表现出高的吸附选择性,在溶液pH=3.0~6.0时满足Hg2+>Pb2+≫ Cu2+≫ Ni2+/Cd2+选择性序列;在总阳离子质量浓度是Pb2+的44.78倍AMD实际废水中,可实现对93.76%的Pb2+选择性去除;0.1 mol/L的EDTA溶液可作为OHA-MNPs对Pb2+或Hg2+吸附后的再生脱附剂。
