C/EBPδ在结直肠癌中的表达及其对癌细胞增殖的影响
2021-10-20刘晶华余福兵冯程程赵霓姗
刘晶华 ,常 巍 ,余福兵 ,盛 娟 ,冯程程 ,赵霓姗
(1)云南大学附属医院消化内科,云南 昆明 650021;2)昆明医科大学统计教研室,云南 昆明 650500)
结直肠癌(colorectal cancer,CRC)是一种常见的致命性疾病,环境和遗传因素均可影响其发生风险,根据WHO的GLOBOCAN数据库,在全球范围内,CRC分别是男性和女性中最常见诊断的第三大和第二大癌症,2020年新发病例190万,死亡病例近93.5万。男性的发病率和死亡率显著高于女性[1]。
大多数CRC起源于腺瘤,腺瘤进展为癌,大概平均需要至少10 a[2]。其预后与临床病理学分期密切相关,早期CRC的5 a生存率高达90%,而晚期则不足10%[3]。肝脏是CRC最常见的转移部位,肝转移是CRC根治性切除后死亡的主要原因[4]。
C/EBP δ由CEBPD基因编码,是C/EBP转录因子家族的成员之一,它可以通过对靶细胞基因转录的调节,参与细胞周期调控、增殖与分化、肿瘤的发生与凋亡等重要生命活动[5]。有文献报道其在缺氧环境下能显著提高HIF-1α的表达,导致细胞异常增殖和肿瘤血管新生,从而促进肿瘤的进展和肝转移[6]。而E3泛素连接酶Siah2在低氧条件下,可通过Siah2/PHD/ HIF-1α信号通路使HIF-1α蛋白聚集来调控下游基因的表达[7]。C/EBPδ与Siah2在结直肠癌中的关系及相关机制尚不明确,笔者对此进行研究,现总结报道如下。
1 资料与方法
1.1 研究对象
选取云南大学附属医院普通外科2017年至2018年接受结直肠癌根治术的40例患者,其中12例同时伴有肝转移,男19例,女21例,年龄42~83岁,平均(65±13)岁。留取患者癌组织、对应的癌旁组织(踞肿瘤灶边缘 < 2 cm)以及正常肠组织(踞肿瘤灶边缘 > 5 cm),用于免疫组织化学以及免疫共沉淀检测。所有病例均由两名病理医师根据美国癌症联合委员会(AJCC)/国际抗癌联盟(UICC)结直肠癌TNM分期系统(第七版,2010年)[8],确定肿瘤的组织类型以及临床病例分期,其中Ⅰ期6例,Ⅱ期22例,Ⅳ期12例。纳入标准:所有患者均经电子结肠镜+病理检查确诊;均表现出结肠癌的临床特征;所有患者术前均未接受过放疗、化疗、生物治疗等其他治疗;既往无认知功能障碍;无精神类疾病。排除标准:伴有其它部位的重大疾病;伴有严重的肝肾功能损伤患者;病理学资料或基础资料缺失;研究中自动退出者。存在本研究经过云南大学附属医院伦理委员会审核批准,并经得患者及其家属的知情同意。
1.2 主要试剂
人结肠癌Caco-2细胞购于上海中国科学院细胞库,MEM培养基(Gibco,美国),胰蛋白酶(碧云天,中国),DMSO(Amresco,美国),PBS(北京中杉),免疫组织化学S-P检测试剂盒(PIERCE,美国)、ECL增强化学发光检测试剂盒(PIERCE,美国),兔抗人C/EBPδ抗体(rockland-inc,美国),兔抗人Siah2抗体(abcam,美国),HRP标记山羊抗兔抗体(abcam,美国)。
1.3 方法
1.3.1 人结直肠腺癌细胞Caco-2培养将Caco-2细胞培养于含20%胎牛血清和1%青霉素-链霉素双抗的MEM培养基中,2 d换液1次,待细胞80% 融合度按1∶3传代比例进行,于37 ℃,5%CO2及饱和湿度培养箱中培养。
1.3.2 C/EBPδ过表达及干扰慢病毒载体构建利用全基因合成方法得到C/EBPδ的ORF序列,构建其基因表达质粒载体。将构建好的慢病毒过表达及干扰质粒载体进行超纯去内毒素抽提,然后同慢病毒包装载体共同转染293T细胞,收集上清,纯化浓缩后即为pLVX-C/EBPδ-IRESZsGreen1、pLVX-CEBPδ-RNAi慢病毒。
1.3.3 C/EBPδ过表达和干扰慢病毒感染Caco-2细胞收集Caco-2细胞,将细胞密度调至1×105/mL,每孔200 μl细胞悬液,将4 ℃保存的病毒离心20 s,慢病毒使用量=MOI×细胞数目/慢病毒滴度,将病毒液加入细胞中,加入5 μg/mL的Polybrene助转染试剂,充分混匀后将24孔板放在37 ℃度培养箱中孵育,24 h后更换为新鲜培养基,48 h后,在荧光显微镜下观察,计算慢病毒感染目的细胞的效率,余样本留作后续实验。
1.3.4 CCK8检测C/EBPδ过表达和干扰对细胞增殖的影响取以上分组进行慢病毒感染后的细胞,将细胞浓度调整为1×105/mL,于96孔板上接种,每孔100 μL,每组设3个复孔,移入培养箱中培养(37 ℃,5% CO2),继续培养72 h,每孔加入10 μL的CCK8试剂,培养箱内孵育4 h,在酶标仪上450 nm处读取吸光度值,并绘制细胞生长曲线。
1.3.5 流式检测C/EBPδ过表达和干扰对细胞凋亡的影响收集细胞培养基的上清和沉淀,2 000 r/min离心5 min,PBS洗涤细胞3次,2 000 r/min离心5 min,收集3~5×105个细胞;在50 μL的Binding Buffer中加入5 μL 7-AAD染液,充分混匀;收集细胞后加入上述7-AAD染液;室温下避光反应5~15 min;反应完成后再加入450 μL 的Binding Buffer混匀;再加入1 μL AnnexinV-PE充分混匀;室温下避光反应5~15 min;1 h内,进行流式细胞仪观察和检测。
1.3.6 流式检测C/EBPδ过表达和干扰对细胞周期的影响参考上述步骤,在每管细胞样品中加入0.5 mL碘化丙啶染色液,缓慢、充分重悬细胞沉淀,37 ℃条件下避光温浴30 min,随后4 ℃避光保存。染色完成后24 h内完成流式检测。
1.3.7 平板克隆形成实验检测C/EBPδ过表达和干扰对细胞增殖的影响取正常及慢病毒感染后的细胞悬液做梯度倍数稀释,每组细胞每皿分别接种200个细胞于含预温培养皿中(10 mL,37 ℃),摇动使其分散均匀。于37 ℃细胞培养箱中培养2周。当出现肉眼可见的细胞克隆时,则停止培养。弃上清,PBS浸洗2次。使用结晶紫染色20 min,流动水漂洗,充分干燥,肉眼及低倍镜下计数大于10个细胞的克隆数。
1.3.8 免疫组织化学对切片进行双盲评价,高倍视野(×400)下选择阳性信号最强区域计数的150个肿瘤细胞中阳性细胞数,按C/EBPδ和Siah2表达百分率分为以下四个等级:< 1%为0分,1%~50%为1分,51%~75%为2分,> 75%为3分。根据染色强度分为三个等级:浅黄色计为1分,棕黄色计为2分,黄褐色计为3分。以阳性细胞率和染色强度的分值乘积作为每一例的积分,积分 < 4者判定为阴性,积分≥4为阳性。
1.3.9 免疫共沉淀用含有蛋白酶抑制剂和RNA酶抑制剂的裂解液充分裂解细胞,12 000 r/min转速离心15 min,取上清并加入相应的抗体(兔抗人C/EBPδ抗体、兔抗人Siah2抗体)及琼脂糖珠,在4 ℃条件下缓慢摇动4~5 h。用预冷的RIPA缓冲液洗3次,沉淀产物在SDS上样缓冲液中100 ℃煮沸10 min,进行免疫印迹并分析。
1.3.10 Western blot检测取结直肠癌组织裂解液上清,经电泳、转印,5%正常小牛血清封闭,抗C/EBPδ(1∶500)、内参一抗的稀释终浓度为1∶1 000,温育2 h,用TBST洗3次,每次5 min,用封闭液将二抗稀释成一定的浓度(1∶1 000),然后温育2 h。ECL曝光、拍照及计算机图像分析。
1.4 统计学处理
采用SPSS 13.0统计学软件,对C/EBPδ和Siah2在CRC组织中的表达及C/EBPδ在CRC中的表达与临床病例特征的关系进行χ2检验,P<0.05为差异有统计学意义。
2 结果
2.1 C/EBPδ和Siah2在CRC组织中的表达
免疫组织化学结果显示,在40例结直肠癌组织中,C/EBPδ呈包膜及胞质表达阳性(图1),阳性表达率在正常结直肠组织、癌旁组织以及癌组织分别为5%(2/40)、42.5%(17/40)和82.5%(33/40);Siah2呈胞核表达阳性,阳性表达率分别为2.5%(1/40)、25%(10/40)和75%(30/40)(图2)。C/EBPδ和Siah2在癌旁组织及癌组织中的阳性表达率差异无统计学意义(P> 0.05);从正常组织到癌旁组织再到肠癌组织中,C/EBPδ和Siah2的阳性率逐渐升高,差异均有统计学意义(均P< 0.05),见表1。

表1 C/EBPδ与Siah2在不同组织中阳性率比较n(%)Tab.1 Comparison of positive rates of C/EBPδ and Siah2 in different tissues n(%)
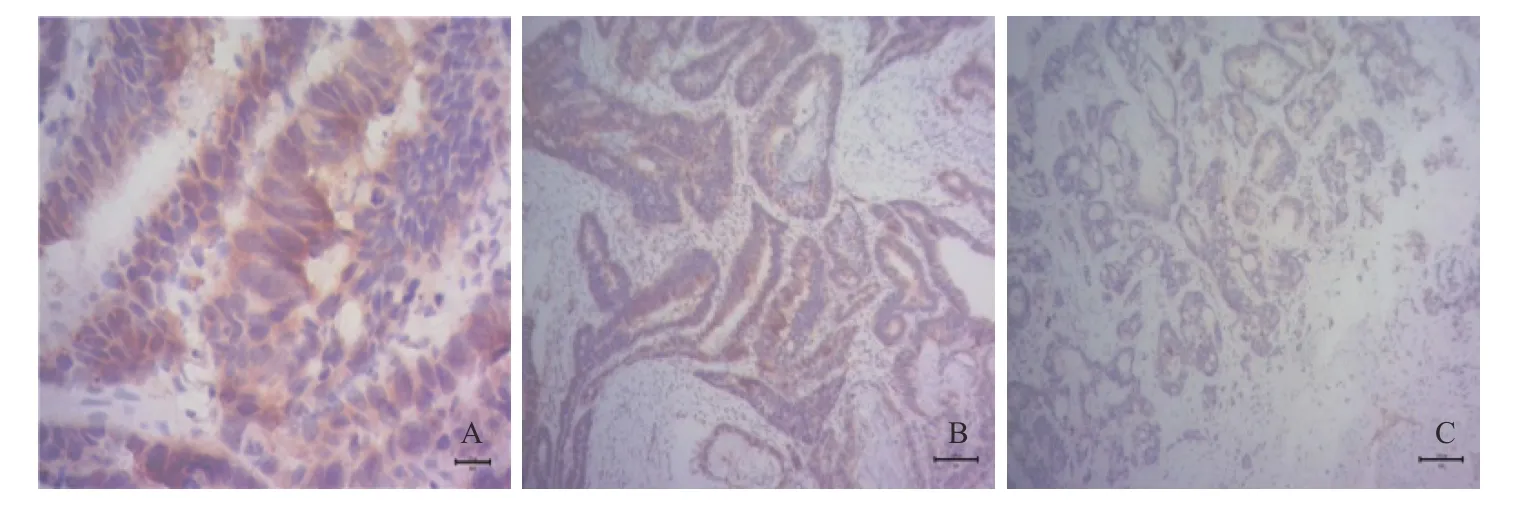
图1 免疫组化检测CRC癌组织、对应癌旁组织和正常肠组织中C/EBPδ的表达(×400)Fig.1 Immunohistochemical detection of C/EBPδ expression in CRC cancer tissues,corresponding adjacent tissues and normal intestinal tissues

图2 免疫组化检测CRC癌组织、对应癌旁组织和正常肠组织中Siah2的表达(×400)Fig.2 Immunohistochemical detection of Siah2 expression in CRC cancer tissues,corresponding adjacent tissues and normal intestinal tissues
2.2 C/EBPδ在CRC中的表达与临床病例特征的关系
C/EBPδ蛋白的表达与年龄、性别、癌胚抗原(CEA)、肿块大小均无相关性(P> 0.05),与TNM分期和伴肝转移有统计学差异(均P< 0.05),见表2。

表2 C/EBPδ在CRC患者癌组织中的表达与临床病例特征的关系Tab.2 The relationship between the expression of C/EBPδ in CRC and the characteristics of clinical cases
2.3 C/EBPδ与Siah2在CRC患者癌组织中表达的相关性
从免疫共沉淀结果可见,input检测人结肠癌细胞Caco-2 中C/EBPδ和 Siah2均有表达;IP检测显示C/EBPδ下拉成功,但C/EBPδ与 Siah2相互作用不明显,见图3。
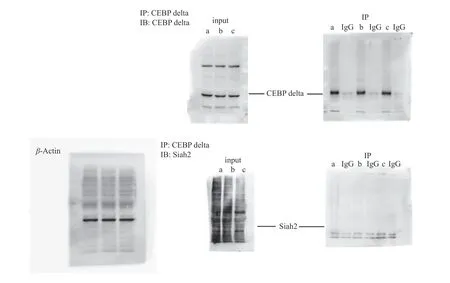
图3 免疫共沉淀检测C/EBPδ与Siah2在结直肠癌组织中的表达及相互作用Fig.3 Co-immunoprecipitation to detect the expression and interaction of C/EBPδ and Siah2 in colorectal cancer
2.4 C/EBPδ过表达和干扰对细胞增殖的影响
Cell Counting Kit结果显示,与正常对照组比较,过表达空载转染组、干扰空载转染组细胞增殖无明显变化;与过表达空载转染组比较,C/EBP δ过表达转染组细胞增殖能力增加;与干扰空载转染组比较,C/EBPδ干扰转染组细胞增殖能力降低(表3)。
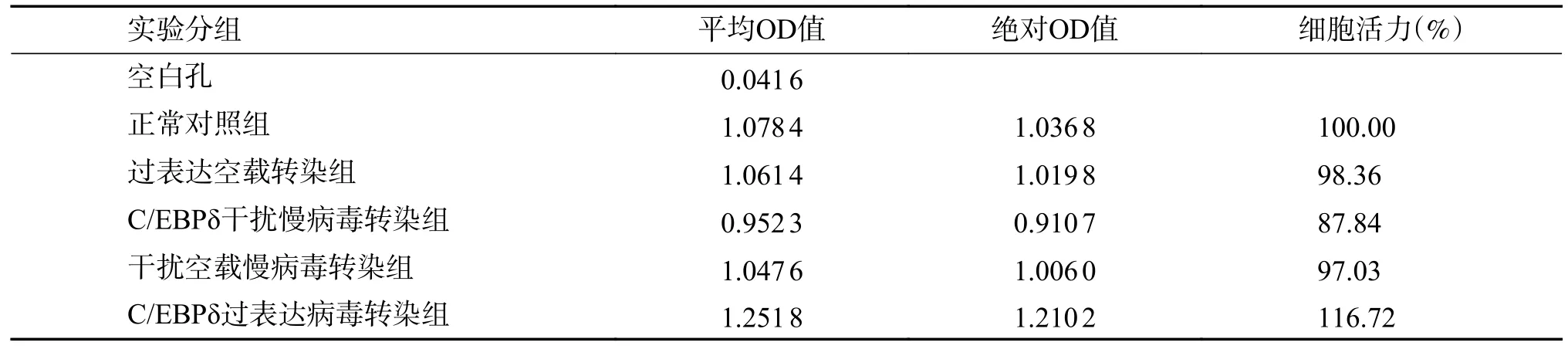
表3 CCK8检测C/EBPδ过表达和干扰对细胞增殖的影响Tab.3 CCK8 detects the effect of C/EBPδ overexpression and interference on cell proliferation
2.5 C/EBPδ过表达和干扰对细胞凋亡的影响
流式细胞仪检测结果显示,与干扰空载转染组比较,C/EBPδ干扰转染组S期细胞比例降低;与过表达空载转染组比较,C/EBPδ过表达转染组S期细胞比例增加(图4)。

图4 流式检测C/EBPδ过表达和干扰对细胞凋亡的影响Fig.4 Flow cytometric detection of the effect of C/EBPδ overexpression and interference on cell apoptosis
2.6 C/EBPδ过表达和干扰对细胞增殖的影响
平板克隆实验显示与干扰空载转染组比较,C/EBPδ干扰转染组细胞克隆形成能力降低;与过表达空载转染组比较,C/EBPδ过表达染组细胞克隆形成能力增加(图5)。

图5 平板克隆形成实验观察C/EBPδ过表达和干扰对细胞增殖的影响Fig.5 Plate clone formation experiment to observe the effect of C/EBPδ overexpression and interference on cell proliferation
3 讨论
C/EBPs是耐热转录调控因子中的一种,其生物作用多种多样,既参与正常的生理代谢过程,又与多种疾病(尤其是炎症和肿瘤)的发生和发展相关,其对转录的调控为双向性。C/EBPs的这种功能多样性是与其结构的特征性相联系的,它们属于bZIP蛋白家族,可以和含bZIP结构的应答元件蛋白(如Fos、Jun和cAMP)结合形成同源或异源二聚体来影响细胞的变化[9],从而极大的增加了其靶基因的多样性。有学者研究证实:C/EBPδ缺失小鼠表现出更高ERBB2-Neu诱导的乳腺癌发生率,但肺转移却减少[10],从而得出C/EBPδ做为肿瘤抑制因子和促癌转移因子的结论。然而,笔者在前期体外实验却发现C/EBPδ在大肠癌细胞中呈过表达,从而推测其与结直肠癌的发生、发展呈正相关。
本研究中,C/EBPδ蛋白质在结直肠癌患者癌组织中的表达水平高于癌旁组织,提示C/EBPδ的高表达可能与结直肠癌的发生、发展有密切关系。C/EBPδ蛋白质高表达与结直肠癌的TNM分期和肝转移呈正相关,与年龄、性别、病理分型、分化程度无关。为进一步明确C/EBPδ在结直肠癌中的功能,本研究构建了C/EBPδ过表达和干扰的结直肠癌细胞系,通过CCK8实验、流式细胞仪检测以及平板克隆形成实验证实,高水平的C/EBPδ加快结直癌细胞生长、提高其增殖能力、促进癌细胞的侵袭转移。为了深入探索C/EBPδ促进结直肠癌细胞侵袭转移的机制,本研究同时用免疫组织化学方法检测了结直肠癌组织中Siah2的表达,结果表明癌组织中Siah2蛋白含量较癌旁正常组织也有增加,提示二者之间存在某种联系。C/EBPδ长期以极低量存在于各种细胞中,可被许多刺激诱导而进一步增多,例如炎性细胞因子[11]。恶性肿瘤常伴随着大量的炎性因子[12],因此结直肠癌组织中检测出高表达的C/EBPδ。缺氧是促进肿瘤发生的另一个重要原因,其反应由缺氧诱导因子(HIF)所控制[13],C/EBPδ在缺氧环境下可以促进Siah2磷酸化,HIF-1α泛素依赖蛋白酶体降解通路受阻,HIF-1α得以稳定聚集,转入细胞核内与β亚基形成HIF-1,并与下游基因上的HRE序列结合,从而启动效应基因的转录[14]。血管内皮生长因子(vascular endothelial growth factor,VEGF)是HIF-1α最重要的靶基因之一,它可以促进肿瘤血管再生,从而影响肿瘤的进展和转移[15]。其次,Siah2还可能通过Siah2/PHD/HIF-1α通路来调控HIF-1α的作用。常氧情况下,脯氨酰羟化酶(PHD)可以将HIF-1α降解,破坏其稳定性[16-17]。在恶性肿瘤的缺氧环境下,Siah2的表达和活性增加,其通过泛素化降解途径促进PHD的降解,导致HIF-1α稳定性增加并且表达量增加。
本研究阐明了C/EBPδ与结直肠癌患者不良预后的关系,初步揭示了C/EBPδ在促进结直肠癌细胞侵袭转移中的作用机制,对寻找新的结直肠癌生物标志物和基因靶点、开发潜在的治疗策略、实现个体化治疗具有重要意义。
