ZnAlHo水滑石基复合氧化物的制备与光催化性能研究
2021-10-19张康丽徐敏虹钟馨奕支凤丽
张康丽,许 雯,徐敏虹,钟馨奕,支凤丽
(1.湖州师范学院 工学院,浙江 湖州 313000;2.湖州学院 浙江 湖州 313000)
0 引 言
随着染料工艺的发展,染料废水已成为重要的水污染源之一.对染料废水的降解和脱色是目前治理水污染的重要任务之一.近年来,类水滑石在光催化方面展现出优异的性能,不少学者对类水滑石的光催化性能进行了相关研究[1-4],促进了该类材料在光催化领域的应用前景[5].

1 实 验
1.1 实验试剂
硝酸锌(AR,成都市科隆化学品有限公司)、硝酸铝(AR,永华化学科技(江苏)有限公司)、硝酸钬(AR,上海阿拉丁生化科技股份有限公司)、氢氧化钠(AR,杭州萧山化学试剂厂)、碳酸钠(AR,太仓美达试剂有限公司)、亚甲基蓝(上海三爱思试剂有限公司)
1.2 ZnAlHo复合氧化物的制备
通过共沉淀法[8]制备三元类水滑石.分别称取0.06 mol Zn(NO3)3·6H2O、0.02 mol Al(NO3)3·9H2O溶解于50 mL去离子水中,为A液;称取0.16 mol NaOH、0.01 mol Na2CO3溶解于50 mL去离子水中,为B液;将A液和B液分别装入恒压滴液漏斗,打开磁力搅拌器,滴加溶液.搅拌过程要保持溶液pH值始终稳定在9~10之间,所得混合液置于晶化瓶中,在65 ℃烘箱中晶化24 h后洗涤、离心,再置于65 ℃烘箱中干燥24 h后取出,即得产品ZnAl-LDHs.
分别称取0.06 mol Zn(NO3)3·6H2O、0.019 mol Al(NO3)3·9H2O和0.01 mol Ho(NO3)3·5H2O溶解于50 mL去离子水中,为C液;称取0.16 mol NaOH、0.01 mol Na2CO3溶解于50 mL去离子水中,为D液;按照上述实验步骤,制备得到ZnAlHo水滑石,产物标记为ZnAlHo-LDHs.
将制得的ZnAl-LDHs置于马弗炉中高温煅烧,煅烧温度分别为300 ℃、400 ℃、500 ℃、600 ℃,煅烧4 h后分别标记为ZnAl-LDO-300 ℃、ZnAl-LDO-400 ℃、ZnAl-LDO-500 ℃、ZnAl-LDO-600 ℃.将ZnAlHo-LDHs 煅烧4 h后的产物分别标记为ZnAlHo-LDO-300 ℃、ZnAlHo-LDO-400 ℃、ZnAlHo-LDO-500 ℃、ZnAlHo-LDO-600 ℃。
1.3 表征测试
采用北京普析XD-6型X射线衍射仪分析样品的晶体结构(Cu靶,Kα射线,λ=0.154 nm,扫描速率为8 °/min,扫描范围为5°~70°,石墨滤波);采用日本日立S-3400N型扫描电镜观察样品的表面形貌;采用带积分球的Hitachi UV4100型紫外-可见光谱仪测试样品的紫外-可见漫反射光谱,以标准BaSO4作为参比.
1.4 光催化实验
称取0.05 g复合氧化物分散于25 mL亚甲基蓝溶液(5 mg/L)中,在可见光(150 W卤素灯)照射下,考察催化反应时间、催化剂用量对亚甲基蓝降解效果的影响.每隔10 min光照将溶液移入离心管中,离心分离5 min,离心机转速为8 000 r/min,用胶头滴管取上层清液,用722型可见分光光度计测量其吸光度,并利用以下公式计算亚甲基蓝的剩余率:
剩余率=Ct/C0×100%=At/A0×100%,
其中,C0为溶液的初始浓度,Ct为不同时间下的溶液浓度,A0为溶液在最大吸收波长处的初始吸光度,At为不同时间下的取样在最大吸收波长处的吸光度.
2 结果与讨论
2.1 XRD分析
由ZnAl-LDHs的XRD图(图1)可见,在2θ=11.5°、23.4°、34.4°、39.1°、46.6°、61.5°处出现的衍射峰分别对应(003)(006)(012)3个晶面特征衍射峰,以及(015)(018)(113)3个晶面微弱峰,这与标准PDF卡(PDF#38-0486)一致[9].由此表明,本实验制得的ZnAl-LDHs具有水滑石特有的层状结构[10].
由ZnAlHo-LDHs的XRD图(图2)可见,在2θ=11.3°、23.2°、34.4°、38.9°、46.6°处出现的衍射峰分别对应(003)(006)(012)3个晶面特征衍射峰,以及(015)(018)2个晶面微弱峰,这与标准PDF(PDF#38-0486)卡一致.由此表明,本实验制备的ZnAlHo-LDHs具有水滑石特有的层状结构.当加入Ho后,ZnAlHo-LDHs在(003)的衍射峰位置为2θ=11.3°,略小于ZnAl-LDHs(003)的衍射峰位置2θ=11.5°.通过布拉格方程2dsinθ=nλ(d为衍射面间距,θ为入射角弧度,λ为X射线波长)计算可知,ZnAlHo-LDHs的晶面间距d003为0.79 nm,而ZnAl-LDHs的晶面间距d003为0.77 nm,晶面间距变大,这是因Ho的原子半径比Al大,当取代部分Al原子后层间距变大.

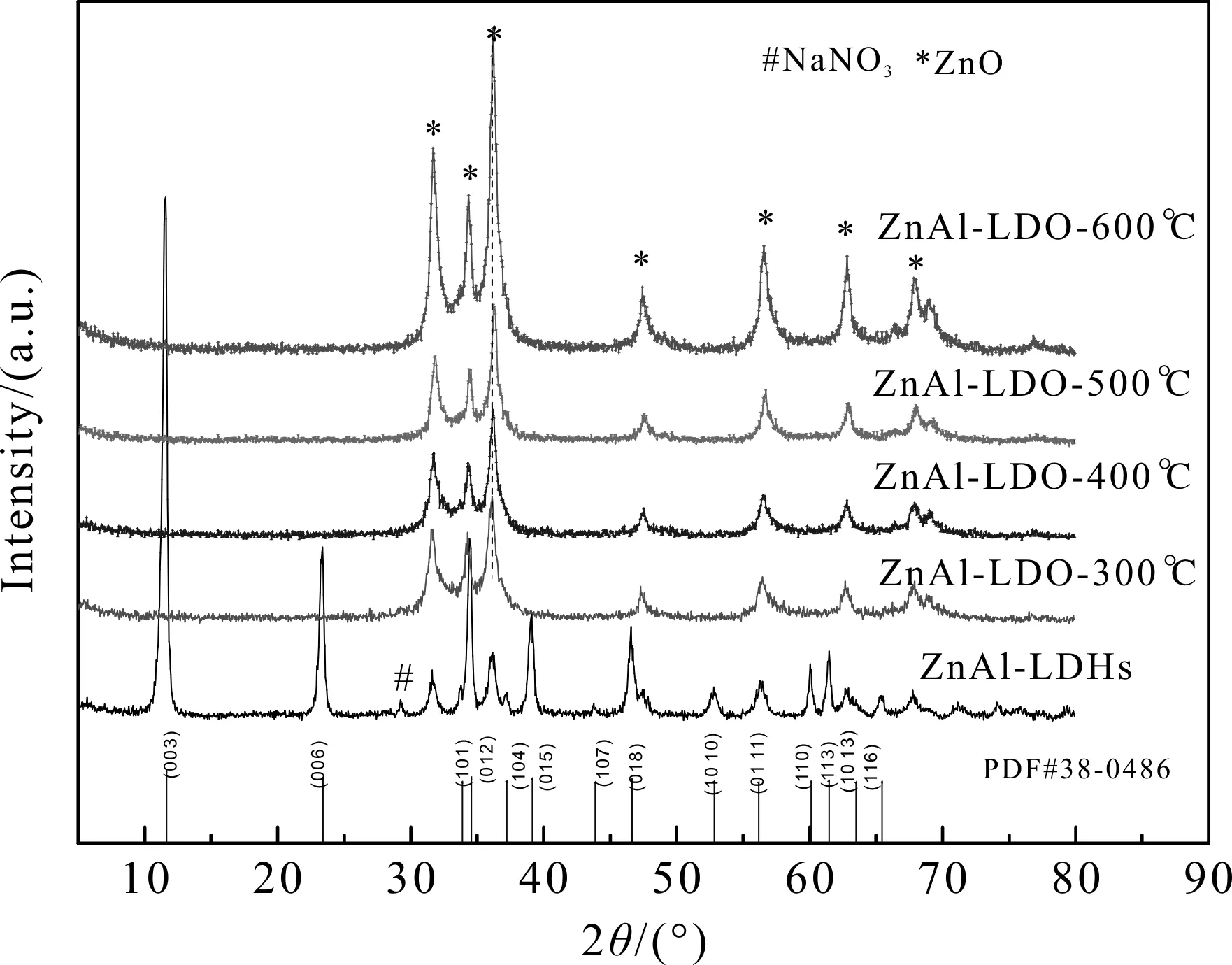
图1不同煅烧温度下ZnAl-LDHs的XRD图Fig.1 XRD patterns of ZnAl-LDHs calcined at different temperatures

图2 不同煅烧温度下ZnAlHo-LDHs的XRD图Fig.2 XRD patterns of ZnAlHo-LDHs calcined at different temperatures
2.2 SEM、EDX分析
图3的(a)(b)(c)(d)分别为ZnAl-LDHs、ZnAl-LDO-500 ℃、ZnAlHo-LDHs和ZnAlHo-LDO-500 ℃的SEM图.由图3可见:(a)中的ZnAl-LDHs颗粒尺寸在10~15 μm之间;(c)中的ZnAlHo-LDHs颗粒尺寸在20~25 μm之间;(b)中的ZnAl-LDO-500 ℃颗粒尺寸在25 nm左右;(d)中的ZnAlHo-LDO-500 ℃颗粒尺寸在20 μm左右.由此可见:在相同的放大距离下,ZnAlHo-LDHs没有破坏原有的水滑石层状结构;煅烧后,ZnAl-LDO-500 ℃和ZnAlHo-LDO-500 ℃两种复合氧化物呈现出薄片状结构,且结构更加紧密,ZnAlHo-LDO-500 ℃的颗粒尺寸相比ZnAl-LDO-500 ℃小,这与文献报道结果类似[12].从图4的EDX元素分析中可以看出,除水滑石中的Zn、Al元素外,还存在明显的Ho元素,这证明在ZnAl水滑石中确实有Ho掺入[13].

图3 ZnAl-LDHs煅烧前(a)和煅烧后(b),以及ZnAlHo-LDHs煅烧前(c)和煅烧后(d)的SEM照片Fig.3 SEM of ZnAl-LDHs before (a) and after calcination (b),ZnAlHo-LDHs before (c) and after calcination (d)

图4 ZnAlHo-LDHs的EDX图Fig.4 EDX spectrum of ZnAlHo-LDHs
2.3 复合氧化物的禁带宽度分析
由图5的(a)(b)可见,ZnAl-LDHs、ZnAl-LDO-300 ℃、ZnAl-LDO-400 ℃、ZnAl-LDO-500 ℃和ZnAl-LDO-600 ℃的边带吸收所对应的波长分别在396 nm、402 nm、410 nm、413 nm和415 nm左右.利用公式Eg=hv-(ahv)2(Eg为禁带能,h为普朗克常数=6.626×10-34,C为光速=3×108m/s,λ为波长)计算可知,ZnAl-LDHs的Eg为3.26 eV,ZnAl-LDO-300 ℃的Eg为3.19 eV,ZnAl-LDO-400 ℃的Eg为3.18 eV,ZnAl-LDO-500 ℃的Eg为3.16 eV,ZnAl-LDO-600 ℃的Eg为3.17 eV.可见,煅烧后禁带宽度明显减少,这是因煅烧后ZnAl-LDHs的结构发生变化所致.

图5 (a)为不同煅烧温度下ZnAl-LDHs的DRS曲线;(b)为不同煅烧温度下ZnAl-LDHs的Eg值; (c)为ZnAlHo-LDHs的DRS曲线;(d)为不同煅烧温度下ZnAlHo-LDHs的Eg值Fig.5 (a)DRS curves of ZnAl-LDHs,(b)Eg value of ZnAl-LDHs at different calcination temperatures, (c)DRS curves of ZnAlHo-LDHs,and (d)Eg value of ZnAlHo-LDHs at different calcination temperatures
由图5的(c)(d)可见,ZnAlHo-LDHs、ZnAlHo-LDO-300 ℃、ZnAlHo-LDO-400 ℃、ZnAlHo-LDO-500 ℃、ZnAlHo-LDO-600 ℃的边带吸收所对应的波长分别在406 nm、403 nm、409 nm、407 nm、400 nm左右.经计算可知,ZnAlHo-LDHs的Eg为3.21 eV,ZnAlHo-LDO-300 ℃的Eg为3.18 eV,ZnAlHo-LDO-400 ℃的Eg为3.18 eV,ZnAlHo-LDO-500 ℃的Eg为3.19 eV,ZnAlHo-LDO-600 ℃的Eg为3.20 eV.同样,煅烧后复合氧化物的Eg都小于ZnAlHo-LDHs.由此可知,煅烧能明显降低Ho掺杂水滑石的Eg,Eg越小电子容易被激发,越能从价带跃迁到导带产生光生空穴和光生电子[14],使得光催化活性也越好.
通过对图5的分析可知,煅烧前和煅烧后的ZnAl-LDHs、ZnAlHo-LDHs主要在400 nm波长内有强吸收[15].但Ho掺杂后在450 nm、550 nm和650 nm处有弱吸收,这些弱吸收可能使得ZnAl-LDHs的Eg略有降低.对比不同温度下Ho掺杂前后复合氧化物的Eg发现,在300 ℃和400 ℃煅烧下,Ho掺杂复合氧化物的Eg比未掺杂复合氧化物略低;在500 ℃和600 ℃煅烧下,Ho掺杂复合氧化物的Eg比未掺杂复合氧化物略高,但总的规律性不明显.
2.4 光催化性能分析
对比Ho掺杂前后ZnAl-LDHs的光催化性能(图6)可见:光照70 min后,在ZnAl-LDHs作用下,亚甲基蓝的剩余率为53%;在ZnAlHo-LDHs作用下,亚甲基蓝的剩余率为50%.由此说明,ZnAl-LDHs和ZnAlHo-LDHs都能通过光催化来降解亚甲基蓝,且ZnAlHo-LDHs光催化降解亚甲基蓝的效果略好于ZnAl-LDHs.

图6 ZnAl-LDHs(a)和ZnAlHo-LDHs(b)在不同煅烧温度下的光催化效果Fig.6 photocatalytic effect of ZnAl-LDHs (a) and ZnAlHo-LDHs (b) calcined at different temperatures
不同煅烧温度下ZnAl-LDHs的光催化效果见图6(a).由图6(a)可见,随着光照时间的延长,亚甲基蓝的剩余率减少.当光照70 min后,ZnAl-LDHs、ZnAl-LDO-300 ℃、ZnAl-LDO-400 ℃、ZnAl-LDO-500 ℃、ZnAl-LDO-600 ℃光催化亚甲基蓝的剩余率分别为53%、50.6%、51.3%、49.7%、34.9%.由此说明,ZnAl-LDHs及其复合氧化物都具有光催化性能,其中ZnAl-LDO-600 ℃光催化降解亚甲基蓝的剩余率最低,即去除率为65.1%.可见,ZnAl-LDO-600℃光催化亚甲基蓝的效果最好.
不同煅烧温度下ZnAlHo-LDHs的光催化效果见图6(b).由图6(b)可见,当光照70 min后,ZnAlHo-LDHs、ZnAlHo-LDO-300 ℃、ZnAlHo-LDO-400 ℃、ZnAlHo-LDO-500 ℃、ZnAlHo-LDO-600 ℃光催化降解亚甲基蓝的剩余率分别为50.1%、46.5%、45%、37.5%、27.8%.由此说明,ZnAlHo-LDHs及其复合氧化物都具有光催化性能,ZnAlHo-LDO-600 ℃光催化降解亚甲基蓝的剩余率最低,即去除率高达72.2%.
为更直观地对比Ho掺杂前后和不同温度煅烧对亚甲基蓝降解的效果,本研究选取光照50 min后亚甲基蓝的剩余率进行对比,结果见图7.由图7可见,ZnAlHo-LDO光催化降解亚甲基蓝的效果比ZnAl-LDO好,尤其在煅烧温度为500 ℃的条件下,ZnAlHo复合氧化物光催化降解亚甲基蓝的效果显著,ZnAlHo-LDO-500 ℃与ZnAl-LDO-500 ℃的对比结果更加明显,两者差距最大.

图7 不同水滑石光催化降解亚甲基蓝效果(光照50 min)Fig.7 Photocatalytic degradation of methylene blue by different hydrotalcites after 50 min
3 结 论
本实验采用共沉淀法制备ZnAlHo-LDHs三元类水滑石,其中Mg2+∶Al3+∶Ho3+的摩尔比为 6∶1.9∶0.1,并在不同温度下煅烧制备复合氧化物.利用X射线粉末衍射仪(XRD)、紫外-可见漫反射光谱(UV-Vis DRS)、扫描电镜(SEM)等对制备的水滑石进行表征,探讨掺杂Ho的复合氧化物在晶体结构和光催化方面的性能,从而得到以下结论:
(1) 通过XRD、SEM、DRS等的表征分析可知,ZnAlHo-LDHs具有典型的水滑石层状结构,且Ho的加入增加了水滑石的层间距,减小了禁带宽度,有利于提高光水滑石的催化活性.
(2) 在70 min光照下,ZnAlHo-LDO-600 ℃对25 mL、5 mg/L亚甲基蓝溶液的光催化降解效果最好;在50 min光照下,ZnAlHo-LDO-500 ℃与ZnAl-LDHs光催化降解亚甲基蓝的效果对比最明显.由此说明,Ho的加入及复合氧化物的生成能够增强水滑石光催化降解亚甲基蓝的性能.
