深共晶溶剂液液微萃取测定痕量苯系物的研究
2021-10-19周艳梅郭睿云吴少如谭晓红张茂升
周艳梅,郭睿云,吴少如,谭晓红,卢 姮,张茂升,2*
(1.闽南师范大学化学化工与环境学院,福建漳州363000;2.福建省现代分离分析化学科学与技术重点实验室,福建漳州363000)
苯系物作为一种芳香族化合物,对人类健康存在极大的危害[1-2].近年来,随着各行业对苯系物的应用和需求的不断加大,环境水体中苯系物的含量逐年增加[3-4].因此,建立精确、快捷、可靠的水体中的苯系物污染物分析检测方法具有十分重要的研究意义和实用价值.由于苯系物在水体中的含量很低,故对环境水样苯系物的前处理和萃取浓缩对准确测定其含量是十分必要[5].目前,常用的前处理方法主要有液液萃取法(LLE)[6]、固相萃取法(SPE)[7]以及后来兴起的各种微萃取方法,如固相微萃取(SPME)[8]、液相微萃取(LPME)[9],但这些方法依然存在许多不足,如操作繁琐、使用大量有毒有机溶剂、成本昂贵等问题.旋涡辅助分散液液微萃取(VALLME)[10-14]是近年来兴起的新型微萃取方式,因操作简单、设备便宜和分析灵敏度高等优势备受人们关注.然而,传统的VALLME 依然使用少量的有机溶剂作为萃取剂,对环境和分析人员的健康造成一定的影响.近年来,一种新型溶剂——深共晶溶剂(DES)[15]具有环保无毒、制备成本低廉、生物可降解性等优点,在分析化学、材料制备等各个领域引起了大家高度兴趣.DES通过两种或多种不同的氢键受体和氢键供体在一定温度下以一定的摩尔比混合,通过氢键作用而形成均一透明的液体,其还具备萃取效率高的特点[16-17],有望成为替代传统有毒的有机萃取剂的候选者.
本文中,我们采用麝香草酚、利多卡因单体制备疏水型深共晶溶剂(DES)作为萃取剂,建立VALLME-GC新方法,并用于环境水样中6种痕量苯系物的检测.新型萃取剂通过π-π共轭作用可快速富集水样中痕量的苯系物.实验结果表明,该方法在呈良好的线性和满意的检出限,可以用于环境水体中苯系物的检测.
1 实验部分
1.1 主要仪器和试剂
1.1.1 主要仪器
主要仪器见表1.

表1 实验所用主要仪器设备Tab.1 Main instrument and equipment used in the experiment
1.1.2 主要试剂
主要试剂见表2.

表2 实验所用主要试剂Tab.2 Main materials used in the experiment
1.2 色谱参数
主要色谱参数见表3.

表3 实验所用色谱参数Tab.3 Main chromatographic parameter used in the experiment
1.3 实验方法
1.3.1 DES萃取剂的制备
称取0.150 g麝香草酚、0.234 g利多卡因(n∶n/1∶1)于样品瓶中,30oC、500 rmp/min条件下搅拌1 h,通过氢键作用,粉末固体反应形成均匀透明的液体,室温保存以进一步实验和表征.
1.3.2 VALLME-GC程序
VALLME-GC主要流程如图1所示,将浓度为2.00×105μg/L标准样品用蒸馏水稀释定容至100 mL容量瓶中制备得2 000 μg/L标液,再移取7.50 μL 2.00×105μg/L标液至3.00 mL蒸馏水的离心管中,再加入1.00 mL 的DES 萃取剂,旋涡3.00 min,10 000 r/min 条件下离心10.0 min,取1.00 μL 上层清液至GC 进行分析.

图1 VALLME萃取、分析流程Fig.1 Extraction and analysis process of VALLME
1.3.3 实际水样分析程序
将环境水样用13 mm 水系性滤头过滤杂质,移取3.00 mL 过滤后水样至离心管中,加入1.00 mL 的萃取剂,旋涡3.00 min,10 000 r/min条件下离心10.0 min,取1.00 μL上层清液至GC进行分析.
2 结果与讨论
2.1 6种痕量苯系物色谱图
根据上述实验方法分析6苯物质,图2展示了2 000 μg/L苯系物标准溶液(a)以及通过VALLME-GC程序2.00 μg/L 加标水溶液(b)的色谱图.该方法下,6 种苯系物可以完全分离,加标水溶液的谱峰和标准溶液的谱峰完全对应.其中苯物质峰附近出现DES的特征峰(红色箭头),但不影响苯物质的正常出峰,实验结果表明DES萃取剂不影响6苯物质的正常出峰,该方法具有很好的可行性.

图2 VALLME-GC测定2 000 μg/L苯系物标准溶液(a)及2.00 μg/mL(b)加标水溶液的色谱图Fig.2 Chromatograms obtained by VALLME-GC of standard solution BTEX at 2 000 μg/L(a)and its spiked standard samples at 2.00 μg/mL(b)peak
2.2 萃取剂DES的红外表征
通过红外光谱对利多卡因(黑线)、麝香草酚(红线)、DES(蓝线)化学结构进行了表征和证实.如图3所示,3 252、1 665、1 494、1 290、2 970、1 088 cm-1分别对应利多卡因―OH,C=O,―NH,C―N,―CH的振动峰.3 223、1 620、1 423、1 244、2 960、1 087 cm-1符合了麝香草酚中的―OH,C=C,C―O,―CH 基团的伸缩振动峰.DES的谱图只是利多卡因和麝香草酚谱图的简单叠加,并没有出现新的特征峰,说明DES没有新的物质生成,进一步证明了利多卡因和麝香草酚单体之间通过分子间氢键作用成功制备了萃取剂DES.

图3 利多卡因(黑线)、麝香草酚(红线)、DES(蓝线)的FTIR图Fig.3 The FTIR patterns of lidocaine(black line),thymol(red line)and DES(blue line)
2.3 萃取条件优化
为了获得VALLME最佳萃取效果,本实验选取标准水溶液浓度为10.0 μg/L对萃取剂配比、萃取剂的用量、萃取时间参数进行了优化.
2.3.1 萃取剂配比的优化
如图4所示,本实验考察了麝香草酚、利多卡因配比(n∶n/3∶1,2∶1,1∶1,1∶2,1∶3)对苯系物的萃取影响.结果表明,配比为3∶1,2∶1时,固体无法全部溶解成透明溶液,配比为1∶1,1∶2,1∶3时,可生产均一透明溶液.图5展示了DES的摩尔配对苯系物峰面积的影响,随着利多卡因配比增加,苯系物峰面积逐渐减少,所以后面实验萃取剂配比采用1∶1.

图4 DES的摩尔配比示意图Fig.4 Picture of DES prepared as a 3∶1,2∶1,1∶1,1∶2 and 1∶3 mixture of thymol and lidocaine

图5 DES的摩尔比对苯系物峰面积的影响Fig.5 The effects of molar ratio of DES on the extraction of BTEX
2.3.2 萃取剂用量的优化
在萃取剂配比为1∶1条件下,本实验考察了萃取剂用量分别为,0.500、1.00、2.00、3.00 ml时DES对苯系物的萃取效果.如图6所示(其他萃取条件,漩涡时间:3.00 min;转速:10 000 r/min;离心时间:10.0 min),当萃取剂DES 用量从0.500~1.00 mL 且体积为1.00 mL 时,萃取量最大,随着萃取剂体积的增大,苯系物峰面积逐渐减少.故本试验萃取剂DES体积为1.00 mL.

图6 萃取剂用量对萃取效率的影响Fig.6 The effects of amount of DES on the extraction of BTEX
2.3.3 漩涡时间的优化
如图7所示,本实验考察DES 在最优配比、用量的条件下漩涡时间2.00、3.00、5.00、7.00、10.0 min对萃取效果的影响.结果可得,萃取时间小于3.00 min时,苯系物的色谱峰值增加至最大,旋涡时间大于3.00 min,苯系物的色谱峰值随着时间增加而减小.旋涡时间过长,由于水的强大极性干扰,萃取剂部分氢键脱落,导致萃取量减少,所以本实验萃取时间为3.00 min.

图7 漩涡时间对萃取效率的影响Fig.7 The effects of extraction time on the extraction of BTEX
2.4 标准曲线的绘制(n=5)
在最优的实验条件下,选取混合标准溶液浓度为0.500、10.0、50.0、100、500 μg/L,将峰面积与分析物浓度进行线性绘制.该方法的线性、RSD、LODs 等定量参数见表4、6 苯物质在范围0.500~500 μg/L 具有良好线性,相关系数(r2)≧0.997.同时,6种苯系物的LODs为1.80~28.0 μg/L(S/N=3).
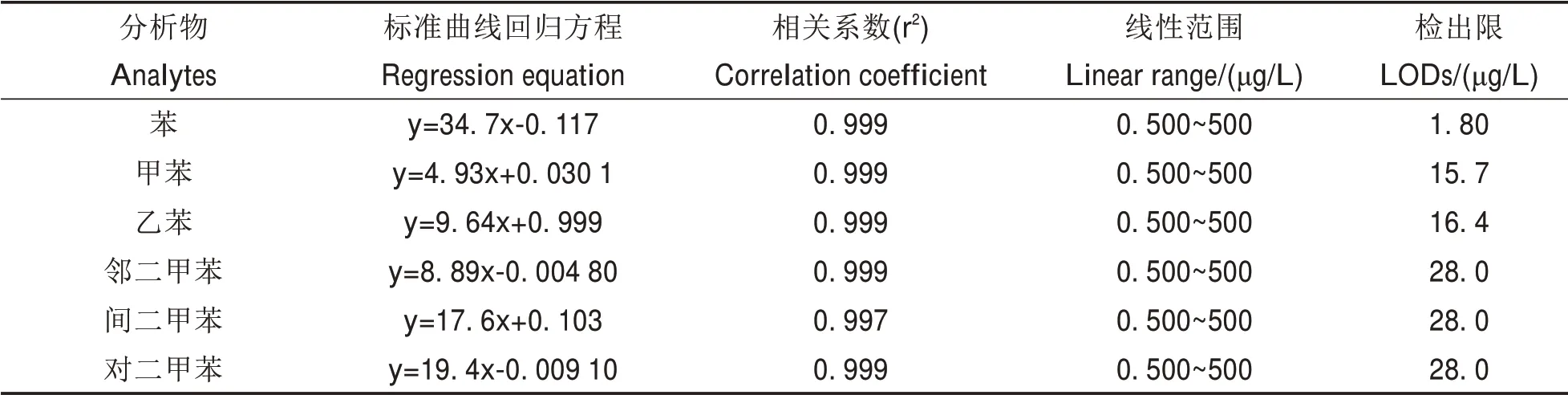
表4 VALLME-GC检测环境水样中的6种痕量苯系物的线性范围、回归方程、相关系数(r2)和LODsTab.4 Regression equation,linearity range,coefficient of determination(r2)and LODs of the VALLME-GC
由实验结果可见,6苯物质的回归方程的相关系数≧0.997;检出限为1.80 μg/L.表明该方法具有较高的稳定性和灵敏度.
2.5 实际水样测定分析
本实验选取福建省九龙江水(A 水样)和漳州市学校内湖湖水(B 水样)作为实际水样进行了VALLMEGC 分析检测.结果如表5所示,九龙江水检测出苯(2.50 μg/L)和乙苯(16.4 μg/L).学校内湖湖水检测到苯(1.80 μg/L)和甲苯(15.7 μg/L).通过分析50.0 μg/L 的加标样品,两个水样苯系物的回收率为78.9%~93.7%,RSD 小于7.74%,其空白及加标水样色谱图如图8、图9所示.综上所述,本文提出的VALLMEGC对检测水样中痕量苯系物具有较好的适应性.

表5 实际水样的测定结果Tab.5 Determination results of 6 BTEX in the water samples

图8 A水样6苯物质VALLME-GC测定色谱图Fig.8 Chromatograms obtained by VALLME-GC of the water sample A(black line)and its spiked standard samples(red line)

图9 B水样6苯物质VALLME-GC测定色谱图Fig.9 Chromatograms obtained by VALLME-GC of the water sample B(yellow line)and its spiked standard samples(red line)
从结果中可以看出,该实验方法适用于多种水体中痕量6苯物质的测定.
2.6 VALLME-GC与已报道的检测方法的对比研究
为了确认该方法可用于环境水样苯系物的分析检测,将其与已报道的检测方法进行了对比研究.从表6中可以看出,这种方法的LODs 低于其他报告的方法[6-9].此外,通过这种新方法在低的范围内获得了良好线性和满意的回收率.

表6 VALLME-GC与已报道的检测方法的对比结果Tab.6 Comparative study of VALLME-GC with the reported methods
3 结论
本实验中,采用麝香草酚和利多卡因单体制备新型深共晶溶剂作VALLME-GC 萃取剂,并应用于环境水样6 种苯系物的检测.麝香草酚和利多卡因通过π-π 共轭作用可快速富集水样中痕量的苯系物.实验结果表明,该方法在0.500~0.500 μg/L获得出色的线性,检出限为1.80 μg/L,相对标准偏差≦7.73%,回收率在78.9%~93.7%之间.该检测方法稳定性好,灵敏度高,可用于实际环境水样的检测分析.
