超高效液相色谱串联质谱法结合分散固相萃取技术快速测定化妆品中36种抗感染类药物残留
2021-10-15王庆龄裘钧陶詹越城叶磊海仰海清盛丽娜
王庆龄,裘钧陶,詹越城,叶磊海,仰海清,何 斌,盛丽娜
(1.浙江公正检验中心有限公司,浙江杭州310009;2.赞宇科技集团股份有限公司,浙江杭州310009)
随着经济的快速发展和生活水平的提高,人们对护肤也越来越重视。化妆品能够有效改善人们的生活质量,而人们也越来越认识和关注化妆品的功效和安全性问题。消费者希望化妆品在有足够功效性的同时也能兼顾产品的安全性。化妆品公司为了迎合消费者对功效的追求,会人为添加禁用或者限用成分,尤其是有功效成分的药物,比如在祛斑美白的化妆品中添加汞试剂制品、在抗衰老化妆品中添加禁用的激素类药品、在染发剂中加入化学试剂醋酸铅等[1-3]。
抗感染药物属于处方药,因具有杀菌抑菌的功效,因此会被违法添加到化妆品中,人体在使用时如果涂抹于面部、口唇等比较柔嫩且膜血管丰富的部位,会通过微血管和黏膜被人体快速吸收,从而破坏皮肤表面的正常菌群,最终导致皮肤发生皮疹发炎、过敏等不良反应。长期使用后更加会导致耐药性,后续治疗更加困难。抗感染类药物一般包括抗生素、磺胺类、喹诺酮类和四环素类等,但现行的相关检测标准仅能检测其中的几项,不能同时进行分析。目前,化妆品中抗感染类药物检测方法主要有气相色谱法、液相色谱法、气相色谱-串联质谱法和液相色谱-串联质谱法等。由于抗感染类药物种类繁多,而文献报道中的检测方法多为检查某一类抗感染药物,钱叶飞等人[4]运用HPLC-DAD法测定化妆品中非法添加的21种磺胺类抗生素;陈静等人[5]通过超高效液相色谱法同时测定化妆品中的19种喹诺酮类抗生素;赵晓亚等人[6]运用高效液相色谱-串联质谱法对化妆品中9种四环素类药物同时测定。对非法添加抗感染类药物的检测难点在于非法添加的药物种类具有不确定性,需要尽可能全面覆盖种类进行筛查,如何有效去除杂质而提高目标物的效应也成为研究的重点。对样品前处理效果影响最大的就是净化手段,化妆品含有大量的脂类和表面活性剂等杂质,因此如何有效去除杂质而不影响目标物的定性定量是评价所建立方法的重要因素。固相萃取技术是最常用的手段,一般包括极性萃取、离子交换萃取、共价萃取、高级聚合物萃取和专用固定相萃取等[7-8]。因此,旨在建立分散固相萃取法结合超高效液相色谱串联质谱法测定多种化妆品基质中可能添加的多种类型的抗感染药物。
1 试验部分
1.1 仪器与耗材
Agilent 1260 Series型超高效液相色谱仪(USA);Agilent 6470型三重串联四极杆质谱仪(USA);N-EVAPA 111型氮吹仪,美国Organomation associates公司产品;TGL-16G型高速离心机,上海安亭科学仪器厂产品;Milli-Q型纯水仪,美国Millpore公司产品;GX-274ASPEC型多通道固相萃取系统,美国Gilson公司产品。
甲醇、丙酮、乙腈、正己烷、乙酸乙酯、甲苯(色谱纯),美国Tedia公司提供;甲酸(优级纯),上海安谱科科学仪器有限公司提供;氯化钠、无水硫酸镁(分析纯)、十八弯基键合硅胶吸附剂(C18)、弗洛里硅藻土、N-丙基乙二胺吸附剂(PSA),杭州化学试剂有限公司提供;甲硝唑、磺胺吡啶、磺胺甲嘧啶、磺胺甲二唑、磺胺甲氧嗪、磺胺氯哒嗪、磺胺甲噁唑、依诺沙星等36种抗感染类物质(含量≥95%)(具体物质见表2,表4),Dr.Ehrenstorfer公司提供。除非另有要求,所有试剂均为分析纯,所用水为GB/T 6682规定的一级水。
标准储备溶液:分别精确称取除氯霉素外其他待测组分标准品各10.00 mg(精确至0.01 mg)置于100 mL棕色容量瓶中,氯霉素称取10 mg(精确至0.01 mg)置于10 mL棕色容量瓶中,加甲醇溶解(溶解性差的物质可加入少量甲酸或水促溶)后,定容至刻度,混匀,即得质量浓度为100.0 μg/mL(氯霉素质量浓度为1 000.0 μg/mL)的标准储备溶液,置于-20℃冰箱中保存。
1.2 试验条件
1.2.1 样品提取
准确称取化妆品样品0.2 g(精确到0.000 1 g)于15 mL的塑料离心管中,加入150 mg净化粉末(含有NaCl,C18和MgSO4)和含0.5%甲酸的乙腈溶液10.00 mL,涡旋30 s,涡旋混合摇匀,超声提取30 min后,以转速4 000 r/min离心5 min,取上清液置于新离心管中,重复提取1次,合并上清液。
1.2.2 样品浓缩净化
取上述离心后上清液,40℃水浴下氮吹至干,再加入2.00 mL的50%甲醇水复溶,经0.22 μm的有机微孔滤膜过滤后上机待测分析。
1.2.3 超高效液相色谱-质谱、质谱条件
(1)色谱条件。色谱柱:Agilent SB-C18型柱(2.1 mm×100 mm,1.8 μm,USA),柱温35℃,进样体积2 μL,流速0.3 mL/min;流动相A:0.1%甲酸水,流动相B:乙腈。
梯度洗脱程序见表1。
(2)质谱条件。离子源:电喷雾离子源(ESI),扫描方式:正/负离子,检测方式:多反应监测(MRM)方式采集,检测器:Agilent 6470型三重四极杆质谱仪配有ESI离子源。
36种抗感染类药物残留的质谱检测参数见表2。
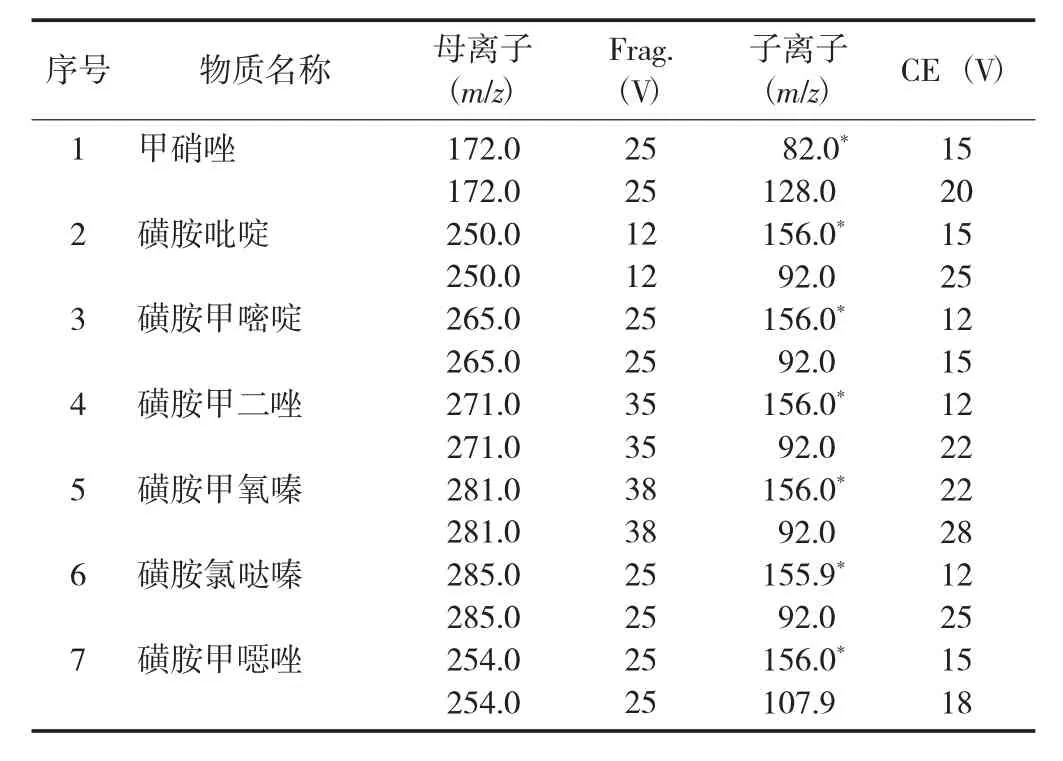
表2 36种抗感染类药物残留的质谱检测参数
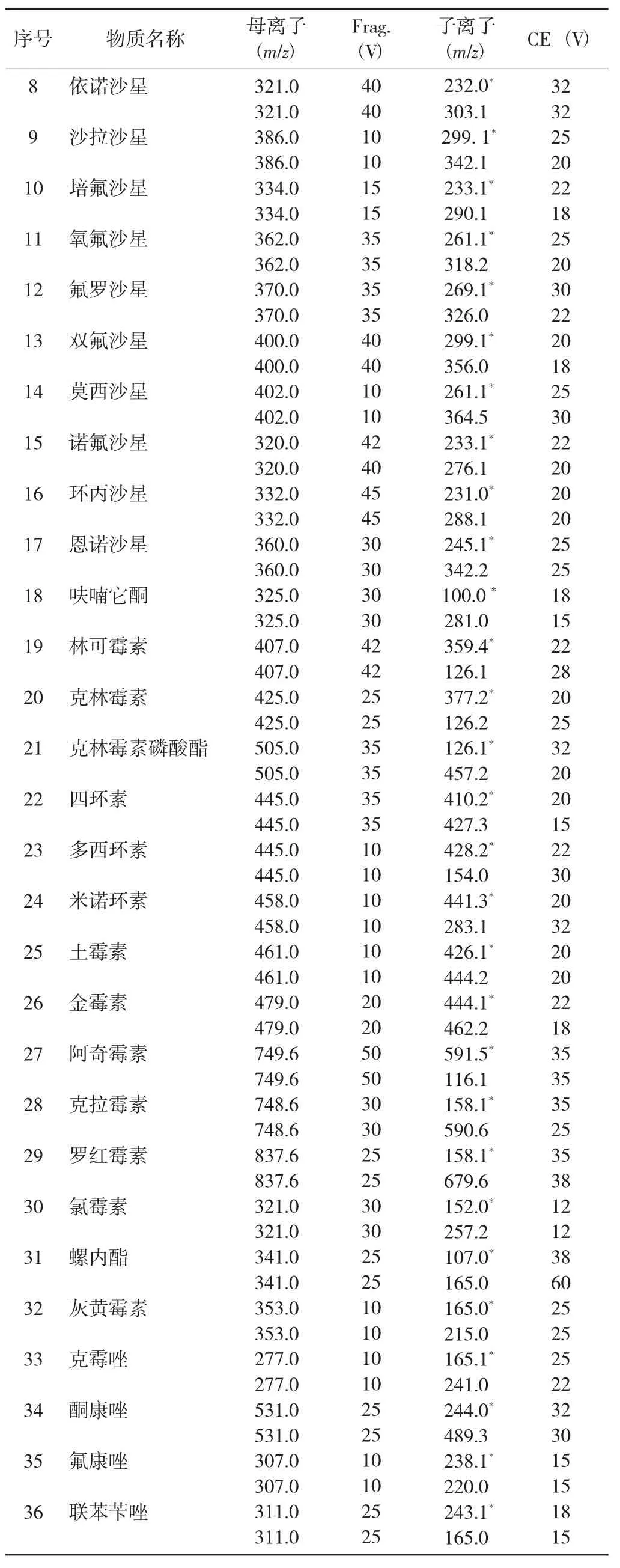
续表2
2 结果与分析
2.1 提取条件的优化
为了提高化妆品中目标物的提取率,根据抗感染类药物的分子性质,并总结文献资料中使用过的提取剂,分别以乙腈、0.5%酸化乙腈、乙酸乙酯和甲醇作为样品提取溶剂。
不同提取液测定结果见表3。
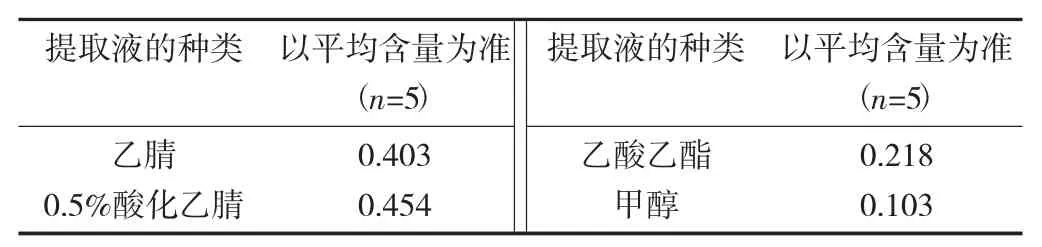
表3 不同提取液测定结果/mg·kg-1
由表3可知,当用乙腈提取目标物时,其极性较大并且分子较小,因此提取能力较强,能够将弱极性物质也提取出来,试验研究的抗感染类药物物质也能大部分被提取出来,所以可采用。0.5%酸化乙腈提取能力比乙腈较强,酸化过的乙腈能够更加亲和个别弱酸性的物质,研究涉及的抗感染类药物一般为酸性或弱酸性,提取率比乙腈更高。而乙酸乙酯非极性较大,可以溶解大多数抗感染类药物,同时能提取化妆品中的大部分油脂类,杂质成分太多影响准确定量。甲醇提取效果跟乙腈相比,因为其能够与水相溶,对一些水溶性的杂质和表面活性剂也会被提取。综合考虑到对目标物的溶解性和较高提取效率,选用酸化的乙腈溶液作为提取液。
2.2 分散固相萃取技术(dSPE)净化
由于化妆品种类繁多,大部分含有大量化工原料或者天然有机物质,成分复杂,因此如何有效去除这些杂质而不影响目标物的定性定量是研究的主要目的。在化妆品中多种药物筛查前处理中常用净化手段主要有固相萃取(SPE)和分散固相萃取(d-SPE)。王梦颖等人[9]使用Oasis PriME HLB固相萃取柱测定乳液类化妆品中的9种抗过敏违禁药物残留时,部分目标物回收率不超过70%,方法适应性不佳。王燕芹等人[10]使用Plexa PCX固相萃取柱结合超高效液相色谱-串联质谱法测定化妆品中9种抗过敏药物残留,其样品比较单一,所测药物种类单一,使其很难成为一个通用的多种药物检测方法。随着技术的不断发展和进步,对检测通量的要求越来越大,d-SPE作为简单便捷的净化方式被广泛应用于各种检测研究中[11-14],传统的d-SPE吸附材料有N-丙基乙二胺(PSA)、石墨化碳(GCB)、多壁碳纳米管(MWCNTS)和十八烷基键合硅胶(C18)等,C18和PSA能有效去除基质中的有机酸、糖类和脂肪,GCB和MWCNTS能吸附大部分色素。鉴于化妆品中杂质类型,考查几种特异性小柱,包括NH2柱、C18柱、非多孔性炭黑小柱、硅胶柱、佛罗里硅藻土小柱、PSA粉末和分散固相萃取粉末,优化最佳净化方案。
2.2.1 净化方式的选择
根据固相萃取柱所含有不同填料性质及参考部分文献,分别比较目前常用的不同填料的Sep-Park-C18,Sep-Park-Silica,Sep-Park-Florsi,Envi-Carb/GCNH2固相萃取柱,AOAC级别的PSA粉末和自制的净化粉末,通过试验,对空白样品加标(5.00 μg/kg)进行净化。
不同净化方式对回收率的影响见图1。
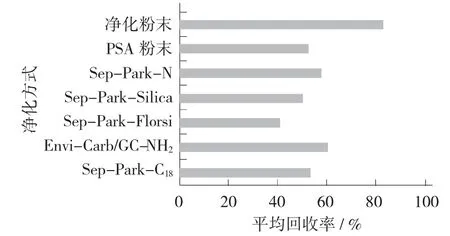
图1 不同净化方式对回收率的影响
由图1可知,自制分散固相萃取净化粉末的回收率最高。由于SPE小柱填料的选择性,同时能够检测的药物种类太少,而繁琐的操作步骤使得SPE小柱法前处理耗时较长,柱子筛板容易堵,很难作为一个通用的高通量多残留筛查检测的样品前处理方法。分散固相萃取经常作为最简单便捷的净化方式被广泛应用于各类目标物的检测中,传统的d-SPE能够去除各种基质中的有机酸、糖类、脂类、固醇和色素等杂质。可能36种抗感染类药物种类比较复杂,其他5种柱子只能对某一种或者几种物质有保留,容易造成其余目标物的损失甚至直接丢失,而自制粉末净化属于一种固液分配净化,只是吸附部分杂质,如脂质,对目标物的吸附能力不强,反而能保留大部分物质,因此回收率比较高。
2.2.2 绘制标准曲线
液相色谱-串联质谱中普遍存在基质效应,化妆品样品基质复杂,含有脂类和表面活性剂,因此基质效应也很严重。在最终优化后的试验条件下,空白样品经过处理吹干后,加入一定量标准溶液,制成基质标准曲线。与相应质量浓度的纯标准溶液比较后发现,基质效应明显,因此准备定量时采用基质匹配的标准曲线。
2.2.3 线性关系和检出限的考查
在所确定的试验条件、色谱和质谱条件下,对36种抗感染类药物进行测定,用空白基质配置一系列质量浓度范围为4.00~100.00 ng/mL,以目标物质量浓度为横坐标(X),对应的响应值为纵坐标(Y),进行线性回归。
36种抗感染药物的线性方程与线性范围与检出限见表4。
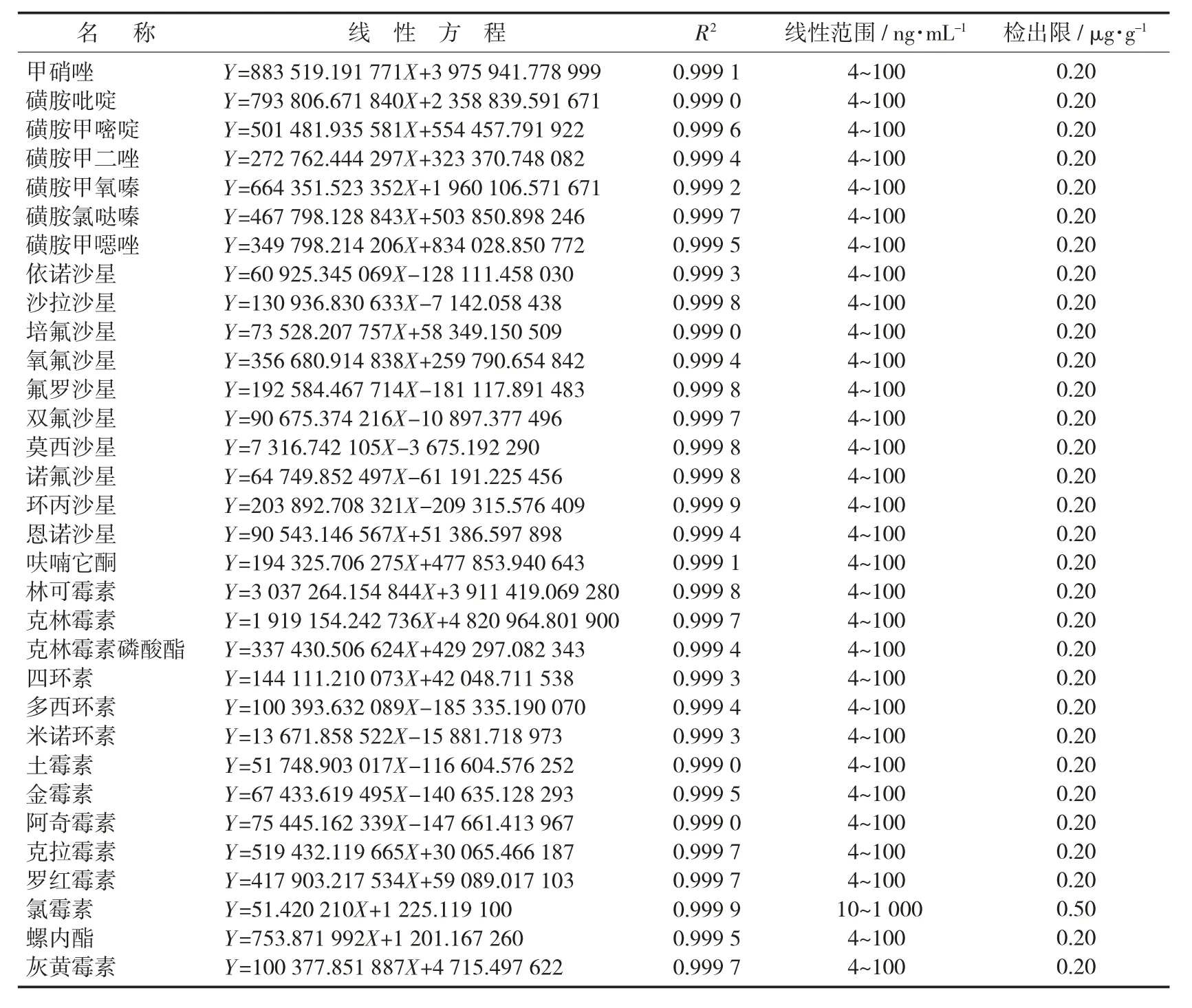
表4 36种抗感染药物的线性方程与线性范围与检出限
2.3 方法回收率和精密度验证

续表4
按液相色谱-串联质谱测定方法操作,实验室对阴性样品分别进行3次平行加标回收试验。
36种抗感染药物的加标回收见表5。
由表5可知,样品平均回收率为70.0%~120.0%,相对标准偏差均在10%以内,说明该方法具有较高的精密度和准确度。
3 结论
采用超高效液相色谱-四极杆串联质谱联用方法建立了化妆品中36种抗感染类药物残留含量的检测方法,36种药物均在除氯霉素外(氯霉素线性范围10.00~1 000.00 ng/mL,检出限为0.50 μg/g,加标量在1.00~10.00 μg/g内的乳液样品回收率均在85%~110%)线性范围4.00~100.00 ng/mL内检出限为0.20 μg/g,加标量在0.50~2.50 μg/g内的乳液样品回收率均在85%~110%,相对标准偏差均小于10%。因此,该方法能高效快速地用于化妆品中36种抗感染类药物残留含量的测定。
