CASH法制备高比表面积Mo-Al催化剂及其脱硫性能研究
2021-10-13周志伟武文良
秦 娟,周志伟,李 扬,武文良
(1.江苏省生产力促进中心,江苏 南京 210042;2.南京工业大学化工学院,江苏 南京 211816)
随着我国环保标准的提高,油品中硫含量的控制越来越严苛[1]。目前油品主要的脱硫方法有加氢脱硫(HDS)、吸附脱硫(ADS)、萃取脱硫(EDS)、生物脱硫(BDS)和氧化脱硫(ODS)[2]。其中ODS法因其反应条件温和、反应时间较短和较好的脱硫效果成为研究热点。但是,氧化后的砜类物质需进一步吸附、蒸馏及萃取等步骤才能脱除,增加了生产成本。而耦合EDS和ODS工艺的萃取催化氧化脱硫(ECODS)体系可将硫组分萃取进而催化氧化,一步法完成脱硫,已被证明是最优的脱硫手段之一。
复合金属氧化物因其制备简单及催化效果较好已被广泛应用到脱硫体系中,其中钼组分的脱硫活性最高[3-4],尤以MoO3/Al2O3催化剂最佳。但共沉淀法制备的催化剂因比表面积小,有效活性组分MoO3负载量过少(约为16%),导致反应效率不高。虽然硬模板法可以较好地克服以上缺点,但其制备方法苛刻,原料昂贵且模板剂难以脱除完全,影响其催化性能。
而软-硬模板(CASH)法可将软、硬模板法进行有效结合,制备的催化剂表现出更为优异的物化性质及催化性能,如:Lee等[5]采用CASH法制备出高比表面积和高热稳定性的TiO2材料,可以有效防止煅烧过程中孔隙的坍塌;Huang等[6]利用CASH法制备了载体Ce0.65Zr0.35O2,进而浸渍法获得了Pd/CZ材料。通过表征和反应测试发现,CASH法有利于提高载体中三价Ce的比例,增大了比表面积,活性组分分散更加均匀,颗粒尺寸更小,具有更高的催化活性。
本文利用CASH法首先合成出较大比表面积的Al2O3载体,进而采用浸渍法制备了Mo-Al催化剂;并将其应用于含DBT的ECODS催化体系中,考察其脱硫效果。
1 实 验
1.1 试剂及原料
异丙醇铝,化学纯,上海凌峰化学试剂有限公司;硝酸、氢氧化钠、正辛烷和乙腈,分析纯,上海凌峰化学试剂有限公司;三嵌段共聚物(EO20PO70EO20,P123),分析纯,西格玛奥德里奇(上海)贸易有限公司;钼酸铵、双氧水、γ-Al2O3,分析纯,国药集团化学试剂有限公司;二苯并哇噻吩(DBT),分析纯,阿拉丁试剂(上海)有限公司。
1.2 催化剂的制备
将一定量的异丙醇铝和水混合,80 ℃下搅拌1.5 h后,加入少量硝酸并搅拌2 h,记作A溶液;将一定量的P123和水混合,40 ℃下搅拌4 h,记作B溶液;随后,迅速将B溶液倒入A溶液中,并用1 mol/LNaOH溶液调节pH值至7.0,室温下老化48 h;过滤,洗涤,滤饼于100 ℃下干燥12 h,N2气氛下400 ℃焙烧3 h,最后400 ℃空气中焙烧2 h,得到γ-Al2O3。
称取一定量的钼酸铵配置成0.01 mol/L的溶液,加入不同质量的γ-Al2O3,室温下搅拌24 h,60 ℃干燥8 h,空气氛围中500 ℃焙烧4 h,得到xMo-Al试样,其中x指MoO3在催化剂中的质量分数(×100)。
采用空气焙烧和商用γ-Al2O3为载体,制得试样分别记为30Mo-Al-S和30Mo-Al-C催化剂。
1.3 催化剂的表征
采用Rigaku公司Smartlab型X射线衍射仪进行XRD分析,扫描范围2θ为10°~80°,管电压40 kV,管电流40 mA。采用Micromeritics公司Teistar300型N2吸附-脱附仪测定催化剂的比表面积和孔结构,试样先在N2气氛下200 ℃脱气2 h。H2-TPR测试在Autochem 2910型TPR仪器上进行,试样在Ar中250 ℃处理2 h,冷却至室温,5%H2/Ar气氛中保持2 h,以10 ℃/min升温至900 ℃,TCD检测。FT-IR表征采用Thermo Nicolet集团NEXUS FT-IR仪测试,以光谱级KBr为背景,4 000~400 cm-1范围扫描。采用ICP原子发射光谱仪(PerkinElmer Opyima 2100,USA)分析催化剂中各元素的实际量。
1.4 催化剂性能评价
先将含320×10-6(质量分数)DBT的正辛烷溶液与乙腈按体积比为3∶1加入三口烧瓶中,并加入适量催化剂,升温至指定温度后,用注射泵加入一定量H2O2,保持一段时间后,冷却至室温,静置0.5 h。油相经配有C18色谱柱和VWD3100紫外检测器的Thermo公司UltiMate 3000高效液相色谱分析,波长310 nm,柱温40 ℃。
2 结果与讨论
2.1 催化剂表征
2.1.1 XRD
图1为不同试样的XRD曲线。
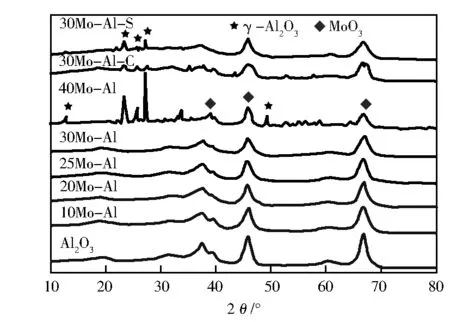
图1 不同试样的XRD分析
图1中,由CASH法制备的Al2O3分别在2θ为37.4°,45.8°和67.3°处出现了对应于γ-Al2O3的特征峰。随着MoO3负载量的增加,衍射峰强度逐渐减弱,可能主要是由于Mo和Al发生了强相互作用所致;当w(MoO3)=30%时,并未检测到MoO3的特征衍射峰,表明钼元素在γ-Al2O3表面高度分散。然而,当w(MoO3)=40%时,试样在2θ为12.6°,23.0°,25.7°,27.4°,33.8°和49.3°处出现了对应于MoO3的特征峰,表明钼物种已经团聚堆积[7]。与30Mo-Al试样相比,30Mo-Al-S和30Mo-Al-C两种试样均出现了明显的MoO3衍射峰,体现出CASH法的优势。
2.1.2 试样比表面积、孔结构及w(MoO3)
表1为应用N2等温吸附-脱附和ICP分析获得的试样数据。随着Mo含量的增加,试样比表面积和孔容均有所下降。与30Mo-Al-S和30Mo-Al-C试样相比,尽管MoO3负载量相同,但由于Mo和Al组分的相互作用,30Mo-Al试样的比表面积更大。由ICP结果可知,Mo组分实际负载量与投料量基本一致。

表1 试样表面积、孔结构及MoO3含量
2.1.3 拉曼光谱
图2是不同试样的拉曼分析曲线。Mo-Al催化剂随Mo含量的增加,在932 cm-1处逐渐出现对应于Al2(MoO4)3四面体吸收峰[8],表明钼铝之间发生了强相互作用;40Mo-Al,30Mo-Al-S和30Mo-Al-C三个试样均在818 cm-1处出现了对应于MoO3的吸收峰,表明已有部分MoO3颗粒的堆积团聚,与XRD一致。
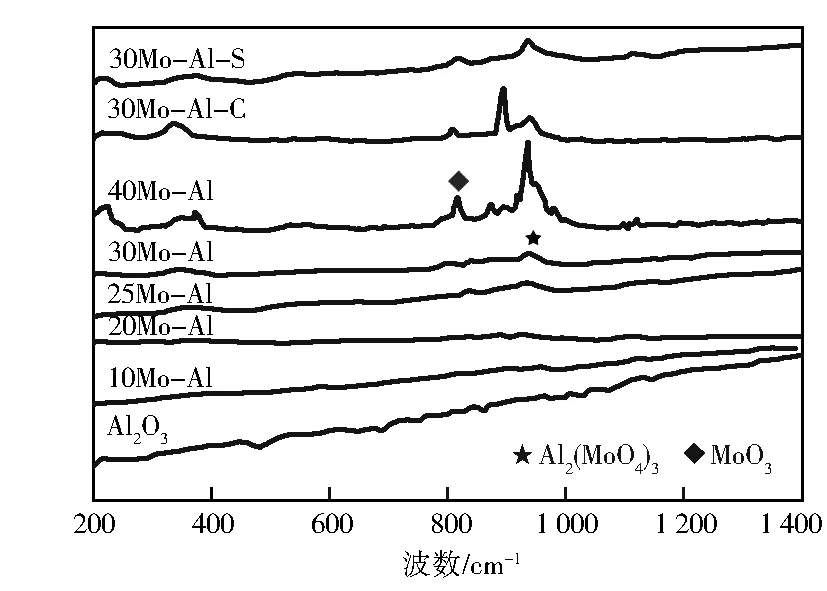
图2 不同试样的拉曼曲线
2.1.4 H2-TPR
图3为不同试样的H2-TPR谱。由图3可见,γ-Al2O3未出现明显的H2脱附峰;Mo-Al催化剂随着Mo含量增加,在450~550、800 ℃分别出现了对应于Mo氧化物的单层吸附和Al2(MoO4)3晶体还原的H2脱附峰,且强度有所增加;而40Mo-Al催化剂在550~650 ℃出现对应于MoO3晶体还原的H2脱附峰[9-10]。与30Mo-Al催化剂相比,30Mo-Al-S和30Mo-Al-C两种试样对应于Mo氧化物的单层吸附峰向低温方向偏移,表明其与载体作用力较弱;同时,在550~650 ℃出现了MoO3晶体的还原峰,归因于其表面出现的MoO3颗粒部分堆积团聚,这与XRD和Raman表征结果一致。
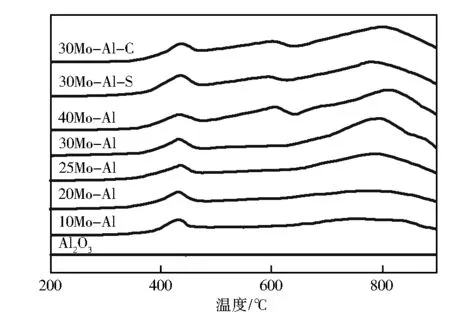
图3 不同试样的H2-TPR曲线
2.1.5 FT-IR
图4是不同试样的FT-IR图。与载体Al2O3相比,其余3个试样在560和1 000~700 cm-1处出现了分别对应于Mo=O和Mo-O的吸收峰[11-12];与30Mo-Al试样相比,30Mo-Al-C和30Mo-Al-S在700~1 000 cm-1处的吸收峰向高波数偏移,表明其出现了部分MoO3的堆积团聚[12],与XRD、拉曼及H2-TPR表征一致。
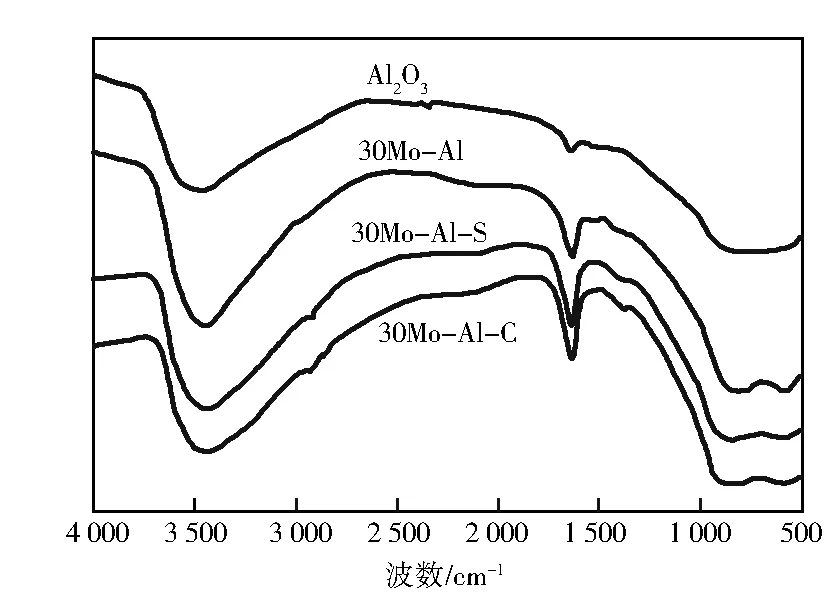
图4 不同试样的FT-IR谱
2.2 催化性能
2.2.1 不同催化剂的萃取氧化脱硫性能
图5是不同催化剂试样在DBT萃取催化氧化脱硫中的性能。由图5可见,纯Al2O3为催化剂时,DBT脱除率为51.0%。随着Mo含量由10%增加至30%,Mo-Al催化剂的DBT脱除率由89.7%提升至100.0%;进一步增加Mo含量至40%时,可能是由于其生成过多的MoO3,覆盖部分活性位点,堵塞孔道,催化活性下降[13-14]。与30Mo-Al催化剂相比,30Mo-Al-S和30Mo-Al-C催化剂的DBT脱除率分别仅为96.7%和87.8%,可同样归因于MoO3颗粒部分堆积团聚,从而体现出CASH法的优势。

图5 不同催化剂试样在DBT萃取催化氧化脱硫中的性能 n(H2O2)∶n(DBT)=2.3,催化剂用量=0.013 3 g/mL,在60 ℃下反应30 min。下同。
2.2.2 催化剂的稳定性
催化剂稳定性测试结果见图6。
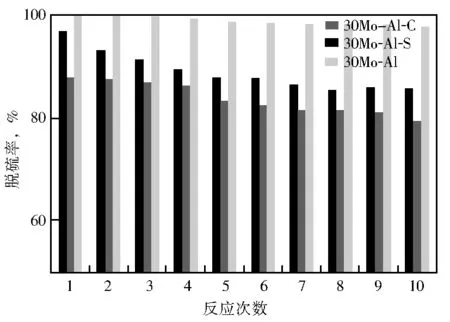
图6 不同催化剂试样的催化稳定性
由图6可见,随着重复使用次数的增加,三种催化剂的催化活性均有所下降。重复使用10次后,与30Mo-Al-S催化剂(降幅为10.4%)和30Mo-Al-C催化剂(降幅为13.9%)相比,30Mo-Al催化剂的DBT脱除率降幅仅为2.3%,可能是由于Mo与Al存在强相互作用所致;Mo组分流失率仅为7.34%(ICP),分别是30Mo-Al-S和30Mo-Al-C催化剂的83%和67%,表明其具有较好的催化稳定性和良好的应用前景。
3 结 论
a.与软模板法制备或商用Al2O3相比,CASH法制备的Mo-Al催化剂比表面积更大,Mo组分分散更为均匀。
b.当w(MoO3)=30%时,由于Mo与Al组分的强相互作用,形成了适宜的Al2(MoO4)3的活性位点,在ECODS反应中表现出最佳的催化性能,DBT脱除率可达100%。
c.与30Mo-Al-C和30Mo-Al-S催化剂相比,30Mo-Al催化剂的稳定性更佳,重复使用10次后,脱硫率仅下降2.3%。
