杯芳烃酚盐催化苯甲醛与丙酮的缩合
2021-10-13周海鹏
周海鹏,兰 鲲,陈 平
(辽宁石油化工大学化学化工与环境学部,辽宁 抚顺 113001)
杯芳烃(Calixarene)是继环糊精、冠醚后,被誉为第三代超分子化合物。常用的杯芳烃主要是含偶数个苯环的杯[4]、[6]、[8]芳烃。它们是由对叔丁基苯酚与甲醛在碱性条件下通过一步法缩合而成的环状低聚物,具有大小可调的刚性空腔,广泛应用于分子识别和自组装[1-2]、电化学应用[3]、荧光化学传感器[4-5]、配位化学[6]、手性合成[7]、杯芳烃的功能化[8-9]、超分子医学[10]等领域。但由于苯环的刚性结构导致杯芳烃的水溶性较差,应用范围受到限制。如果对杯芳烃的上下沿进行官能团修饰改性,可以降低其疏水性以改善其水溶性。如在上下沿通过磺化、酯化和胺化反应实现这一目的[11],但是合成方法复杂、成本高,影响了杯芳烃的使用价值。
近年来,杯芳烃及其衍生物作为有机合成催化剂的应用也取得了一些进展[12-13],主要是杯芳烃的酸性催化性能研究,如在杯芳烃的上沿引入磺酸基[14-15]。杯芳烃的下沿为酚羟基,酚羟基的氢具有一定的弱酸性,可以与强碱反应形成强碱弱酸盐而具有一定的碱性,可作为碱性催化剂。本文以杯芳烃为原料合成了具有弱碱性的杯芳烃酚钠(钾)盐,将其作为弱碱性催化剂,催化苯甲醛与丙酮发生克莱森-斯密特缩合(Claisen-Schmidt)缩合反应,并与传统的无机碱进行催化比较,以期获得杯芳烃酚钠(钾)盐作为催化剂的理论数据。
1 实 验
1.1 试剂与仪器
对叔丁基杯[4]、[6]、[8]芳烃和杯[4]、[6]、[8]芳烃,自制[11];乙醇、氢氧化钠、氢氧化钾、碳酸钠、氢氧化钡、苯甲醛、丙酮均为市售分析纯试剂,国药集团。
GC7890 Ⅱ气相色谱仪,上海天美科学仪器厂。
1.2 对叔丁基杯芳烃酚钠(钾)盐的合成
在100 mL烧瓶中,加入5 g对叔丁基杯芳烃,加入质量分数为15% 的NaOH(KOH)水溶液,磁力搅拌油浴加热至90 ℃,剧烈搅拌一定时间,当混合物转变成悬浊液,没有漂浮的杯芳烃时,取出少量悬浊液进行水溶性实验,完全溶于水后停止反应,趁热抽滤后用75%乙醇溶液洗涤2~3次,120 ℃干燥即可得到相应的杯芳烃酚钠(钾)盐,以杯芳烃酚钠盐合成为例的反应式如下。

1.3 苯甲醛与丙酮的缩合
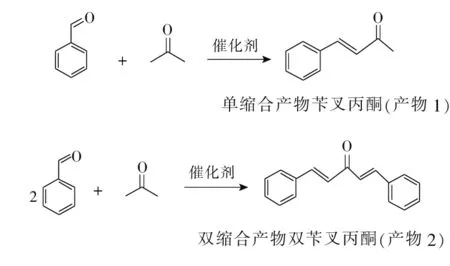
在100 mL三口烧瓶中加入对叔丁基杯芳烃酚钠(钾)盐作为催化剂,加入新蒸的苯甲醛,安装回流冷凝管和滴液漏斗,通过滴液漏斗向反应瓶内滴加丙酮,磁力搅拌,水浴控制反应温度。反应结束后趁热过滤,滤渣为催化剂。留少量滤液溶解于CHCl3中,通过色谱定性分析产物的组成,其余滤液冷却到室温后水洗,分离得到粗产物。用乙醇进行重结晶,抽滤、烘干、称重,计算产率。不同的反应条件下得到不同的缩合产物,主产物主要为苯甲醛与丙酮的单缩合产物苄叉丙酮(产物1)和双缩合产物双苄叉丙酮(产物2);副产物为丙酮自身缩合的产物。
1.4 催化剂的回收
上述缩合反应结束后趁热过滤反应液,滤渣为催化剂,用75%乙醇溶液洗涤2~3次后进行干燥,回收率90%;把上述反应混合物冷却到室温,有大量的产物析出,用水洗涤,洗涤液加入几滴盐酸,立即有少量的对叔丁基杯[4]芳烃析出,过滤后备用。
2 结果与讨论
2.1 产物表征
2.1.1 对叔丁基杯[4]芳烃酚钠盐
叔丁基杯[4]芳烃酚钠盐的1H NMR谱见图1。1H NMR(500 MHz,CDCl3),δ:1.24(m,36H)为对叔丁基的氢,3.99(m,8H)为连接杯芳烃苯环的亚甲基上的氢,7.00(s,4H)苯环上的氢,7.52(s,4H)苯环上的氢,与其结构基本吻合。

图1 对叔丁基杯[4]芳烃酚钠盐的1H NMR谱
2.1.2 苄叉丙酮和双苄叉丙酮
苄叉丙酮和双苄叉丙酮产物的1H NMR谱见图2。1H NMR(300 MHz,CDCl3),苄叉丙酮,δ:7.41(m,4H),7.61(m,3H),3.13(s,3H);双苄叉丙酮,δ:7.09(d,2H),7.42(m,6H),3.7.61(m,4H),7.61(m,4H),7.75(d,2H)。与相应的结构一致。

图2 产物的1H NMR谱
2.2 对叔丁基杯芳烃酚钠(钾)盐合成条件的影响
合成对叔丁基杯芳烃酚钠(钾)盐的反应条件列于表1。
由表1可见,不同的碱反应效果不同,其中以NaOH和KOH的反应效果比较好,Na2CO3反应不完全,始终有不溶的杯芳烃;与油浴相比,微波明显加快反应速度,温度越高,反应速率越快。杯[4]芳烃和杯[6]芳烃的反应速率相近,而杯[8]芳烃的反应速率很快。适宜的碱溶液的用量为质量分数15%。减少碱的用量,反应困难,碱溶液的质量为杯芳烃质量的5倍,量少搅拌困难。搅拌越剧烈越好,不搅拌则放置几天也没有产物。考虑到原料的成本,以下选择在微波条件下以NaOH为碱,合成对叔丁基杯芳烃酚钠盐作为碱性催化剂。

表1 合成杯芳烃酚钠(钾)盐反应的条件及产率
2.3 不同的碱催化苯甲醛与丙酮的反应
选择苯甲醛为50 mmol,苯甲醛与丙酮物质的量比为1∶1.4,催化剂用量为苯甲醛物质的量的1.2%,40 ℃下反应45 min,结果见表2。

表2 不同的碱催化苯甲醛与丙酮缩合的实验结果
由表2可知,上述各种碱催化苯甲醛与丙酮的缩合,并没有生成丙酮自身缩合的产物,表明滴加丙酮可以控制丙酮的自身缩合。苯甲醛在浓NaOH条件下能够发生自身的岐化反应生成苯甲醇和苯甲酸。但是在该条件下并没有岐化反应产物,说明碱的浓度不够,不足以发生苯甲醛的岐化反应。不同的碱催化效果也不同,Na2CO3没有催化效果,而NaOH作为传统的羟醛缩合反应的催化剂,催化效果良好,但选择性不佳;对叔丁基苯酚钠虽也有较好的催化效果,但不如对叔丁基杯[4]、杯[6]芳烃酚钠盐。对叔丁基杯[8]芳烃盐的催化效果较差,这是因为其催化效果取决于杯芳烃环的大小,因为环的大小可能会影响杯芳烃对反应物的作用。故选择催化效果良好的对叔丁基杯[4]芳烃酚钠盐作为苯甲醛与丙酮缩合反应的催化剂。
2.4 对叔丁基杯[4]芳烃酚钠盐催化苯甲醛与丙酮的缩合
2.4.1 催化剂用量的影响
以对叔丁基杯[4]芳烃酚钠盐为催化剂,苯甲醛用量50 mmol,苯甲醛与丙酮摩尔比为1∶1,在40 ℃下反应45 min,考察催化剂物质的量对苯甲醛转化率、产物收率的影响,结果见图3。

图3 催化剂用量对反应的影响
从图3可以发现,催化剂用量越多,苯甲醛的转化率就越高,最高可达99.1%,基本达到完全反应;催化剂对苄叉丙酮和双苄叉丙酮选择性的影响变化不大,催化剂极少时,只有苄叉丙酮生成;当催化剂用量增加时,使生成的单缩合产物会继续进行缩合,导致少量的双缩合产物生成。故适宜的催化剂用量为 0.75 mmol。
2.4.2 反应温度的影响
催化剂物质的量为0.75 mmol,苯甲醛用量50 mmol,苯甲醛与丙酮物质的量之比为1,反应时间为45 min,考察反应温度对苯甲醛转化率、产物收率的影响,其结果见图4。
从图4可以看出,苯甲醛的转化率随着温度的升高而提高。当温度达到40 ℃时,苯甲醛的转化率最高,达到99.1%,同时,苄叉丙酮的选择性也是最高的。故合成单缩合产物苄叉丙酮适宜的温度为40 ℃。

图4 反应温度对反应的影响
2.4.3 反应时间的影响
其他反应条件同上,选择反应温度为40 ℃,考察反应时间对苯甲醛转化率、产物收率的影响,结果如图5所示。

图5 反应时间对反应的影响
由图5可见,丙酮与苯甲醛在叔丁基杯[4]芳烃酚钠盐的催化作用下,反应速率比较快,随着反应时间的延长,苯甲醛的转化率明显提高,而反应时间的变化对产物的选择性影响不大。当反应45 min时,苯甲醛的转化率最高,同时单缩合产物苄叉丙酮选择性最好,故选择反应时间为45 min。
2.4.4 丙酮与苯甲醛物质的量之比对反应的影响
选择苯甲醛物质的量为50 mmol,催化剂物质的量为 0.75 mmol,40 ℃下反应45 min,苯甲醛转化率、产物收率的变化结果见表3。
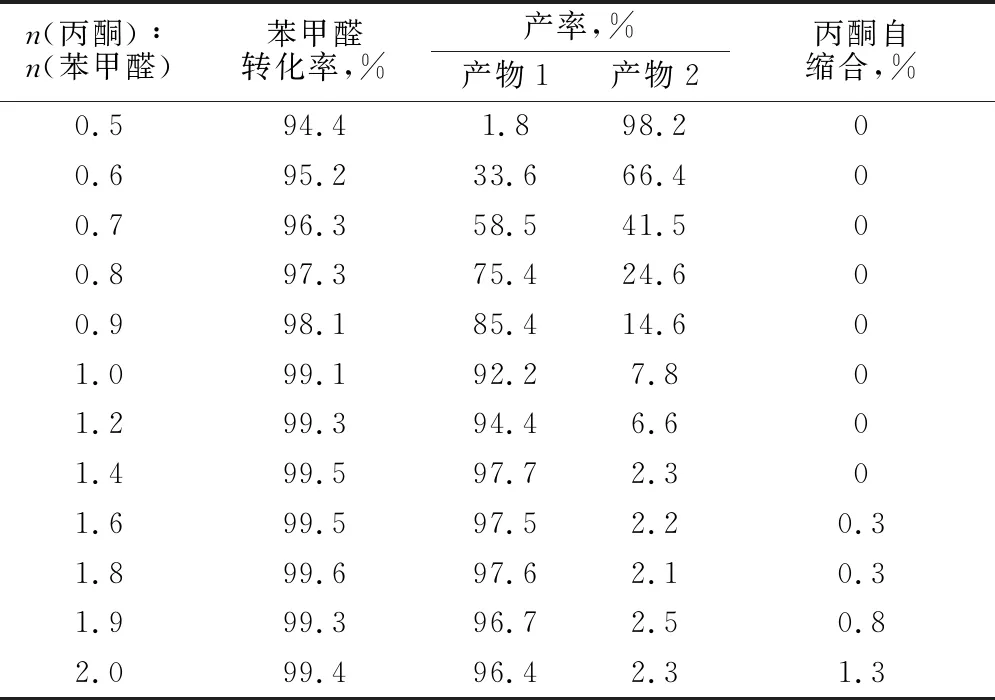
表3 原料物质的量之比对反应的影响
由表3可知,丙酮物质的量越大,苄叉丙酮产率越高,而苯甲醛的量越大,则双苄叉丙酮产率越高,这是由于苄叉丙酮的α-H活性要大于丙酮的α-H活性的关系,所以很容易合成双苄叉丙酮;另外,丙酮与苯甲醛物质的量比过1.4时,逐渐会有丙酮的自缩合产物生成,虽然丙酮的自缩合反应不及与苯甲醛的反应速度快,但是过量的丙酮也会有少量的自缩合产生,可见控制原料的配比是合成可选择产物的关键。
2.5 催化剂回收实验
将回收的催化剂应用于重复实验,结果如图6。

图6 催化剂回收再利用
回收催化剂的重复实验中苯甲醛转化率略有降低,催化剂的重复利用性较好。
2.6 反应机理初探
杯芳烃的酚羟基具有弱酸性,与强碱反应形成杯芳烃酚盐,具有一定的碱性,同时杯[4]芳烃酚盐的空腔能够对丙酮、苯甲醛等小分子具有包合能力,双重作用使其对羟醛缩合反应具有一定的催化作用,反应中丙酮的α-H与杯芳烃的酚氧负离子结合,生成丙酮的碳负离子,然后进攻苯甲醛的羰基碳,发生亲核加成,进一步产生缩合产物。
3 结 论
a.以对叔丁基杯[4]芳烃为原料,在微波条件下,与NaOH或KOH反应合成了对叔丁基杯[4]、[6]、[8]芳烃酚钠(钾)盐,合成产率较高。
b.以对叔丁基杯[4]芳烃酚钠盐为催化剂,催化苯甲醛与丙酮的缩合反应,当苯甲醛物质的量为50 mmol,丙酮与苯甲醛物质的量之比为1.4,催化剂物质的量为0.75 mmol,40 ℃下反应45 min,苯甲醛转化率达99.5%,单缩合和双缩合产物产物的选择性分别为97.7%和2.3%,对叔丁基杯[4]芳烃酚钠盐的催化效果良好,可作为碱性可回收的催化剂使用。
