盐度对厌氧消化脂肪酸的抑制研究
2021-10-12徐家英王楠楠
徐家英,王楠楠
(青岛市环境卫生发展中心,山东 青岛 266003)
餐厨垃圾具有有机质含量高、高盐高油脂、易腐烂变质而滋生病毒的特点[1-2]。随着垃圾分类的进行,越来越多的餐厨垃圾处理工程采用厌氧消化技术进行单独处理。在湿式厌氧消化处理过程中,餐厨垃圾的高盐度增加了发酵工艺稳定及高效产能的难度[3]。甲烷菌对盐类较为敏感,一定质量范围内,盐分属于有机物厌氧消化过程的毒性抑制剂,研究表明,餐厨垃圾中NaCl的存在影响了甲烷的最大产生量[4]。在运行过程中,循环水的使用和进料浓度的增高都会引起发酵过程中钠盐浓度的累计增加,厌氧消化的正常运行会受到冲击[5],因此钠盐对厌氧消化的影响引起了学术界的注意[6-8]。钠盐对甲烷化影响的研究表明,钠盐对甲烷化过程的抑制作用主要与阳离子有关而不是阴离子[9],对微生物具有毒性的主要是阳离子,Na+能够破坏细胞内外渗透压,甚至造成质壁分离。蒋彬[10]在探究Na+对餐厨垃圾厌氧消化的影响时发现Na+同样能够抑制甲烷产生,而且甲烷抑制效率与Na+质量浓度相关。本试验主要通过餐厨垃圾的盐度毒性抑制试验,探讨Na+对餐厨垃圾厌氧发酵过程的影响,从而为餐厨垃圾发酵过程的盐度抑制提供理论依据。
1 材料与方法
1.1 餐厨垃圾理化性质
试验所用餐厨垃圾取自青岛某大学学术交流中心,垃圾成分包括米饭、蔬菜、猪肉、鱼虾、贝类和油脂等。将垃圾中杂质(贝壳、骨头、纸巾、牙签等)剔除后,使用家用绞肉机粉碎打浆,所有垃圾打浆完毕后混合均匀,经测定,其总固体(TS)含量为19.2%,挥发性组分(VS)为18.6%。试验所用接种物为餐厨垃圾厌氧消化降解残渣,接种物固含率为6%,COD含量为6 288 mg/L,碱度含量为3 728 mg/L,pH为6.2。
1.2 试验装置
试验中使用2 000 mL储水瓶作为厌氧消化反应器,储水瓶带丁基橡胶塞,在橡胶塞原有两个孔的基础上再打一个孔,即每个橡胶塞上有3个孔。其中,第一个孔通入试剂瓶底部,用于通氮气,第二个孔通入试剂瓶中间位置,用于吸取液体,第三个孔通入试剂瓶上部空间,用于取气。
1.3 试验方案
将4个瓶子进行编号,分别是A反应器、B反应器、C反应器和D反应器;反应体系以有效体积1 500 mL计算,每个试剂瓶中加入900 mL已驯化好的接种物和133 g垃圾,使垃圾固含率达到2%;设置4个盐浓度,分别向4个试剂瓶中加入适量盐,调节至相应浓度,即A反应器是不加盐,只有900 mL接种物+133 g垃圾,B反应器是加灼烧后的NaCl 15.252 4 g,相当于加入4 g/L的Na+,C反应器是加灼烧后的NaCl 30.504 8 g,相当于加入8 g/L的Na+;D反应器是加灼烧后的NaCl 45.757 2 g,相当于加入12 g/L的Na+;加水至1 500 mL,通入氮气,将空气排净,封闭瓶塞,调节pH,进行驯化培养,每天测定一次pH,并取一定量的液体冷冻保藏,用于测定脂肪酸组分,每天测定一次气体浓度和气体成分;每个样品设置2个平行样,试验运行21 d,运行平稳,测定反应过程中物料pH、碱度、挥发性脂肪酸(VFA)和氨氮等。
1.4 理化指标及分析方法
化学需氧量(COD)测定使用标准重铬酸钾法,氨氮测定使用蒸馏和滴定法,挥发性脂肪酸测定采用气相色谱法,气体产量测定使用排水取气法,盐度测定使用盐度测定仪,pH测定使用精密pH试纸,碱度测定使用酸碱指示剂滴定法。
1.5 其他控制条件
本试验采用恒温箱来控温,反应温度设置为35 ℃±1 ℃。采用人工搅拌,每日运行时间歇搅拌2次,使发酵物料混合均匀,并使气体顺利产出。发酵接种物与底物比例为50∶50(VS比)。
2 试验结果与分析
2.1 盐度对发酵过程中氨氮的影响
不同的反应器类型、不同的微生物种群和不同的反应条件能够承受的氨氮抑制性浓度是不同的,一般说来,单相湿式系统容易受到氨氮的抑制[11]。在厌氧消化过程中,氨氮是微生物重要的氮源。对于一个长期运行的厌氧消化系统,其内部微生物群落经过长期驯化后,对氨氮的承受能力已趋于稳定与饱和,在氨氮浓度超过某一限值后,产甲烷菌的活性受到严重抑制[12]。研究表明,氨氮浓度为1 700 mg/L[13],系统的稳定性与产气能力开始降低。
从图1可以看出,虽然Na+的浓度不同,但到发酵期21 d结束时,4个反应器的氨氮浓度基本都保持在1 000~1 150 mg/L,差距不大,都低于1 700 mg/L。从试验结果来看,钠离子没有对氨氮产生明显的影响。

图1 不同盐度影响下氨氮浓度变化
2.2 盐度对发酵过程中pH的影响
pH强烈地影响酶的活性,每种酶都在一个特定和狭窄的pH范围内产生活性,并有一个最佳pH[14]。大多数产甲烷菌适合的pH范围为6.7~7.4,当pH低于6.3或高于7.8时,产甲烷效率会明显下降。图2显示不同盐度下的厌氧发酵过程pH变化,从图中可以看出,4个反应器开始时pH较高,调节pH到相同的值8.01,在启动阶段,反应器内的pH由启动时的8.01迅速下降,到第3天,4个反应器的pH都下降到最低值,然后呈现相同的变化趋势,开始逐渐回升,到发酵期21 d结束时,pH都恢复到大于7.0。
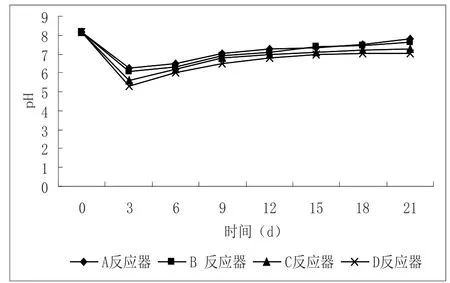
图2 不同盐度影响下pH变化
A反应器和B反应器的pH分别下降到6.2和6.1,而后开始逐步回升,试验期结束时,pH分别达到7.8和7.6。A反应器和B反应器的pH介于6.1~7.8,基本属于适合发酵的pH范围,对产气量没有明显的影响,也就是说,A反应器和B反应器没有明显抑制厌氧发酵的正常进行。
对于C反应器和D反应器,pH变化很大。C反应器pH在第3天降到5.59,然后缓慢回升,到反应期结束,pH恢复到7.3。D反应器pH在第3天降到5.30,而后缓慢回升,到反应期结束pH恢复到7.02。对于C反应器和D反应器,发酵过程已经开始出现抑制,发酵气体间断性出现,说明高浓度的盐已经开始抑制产甲烷菌的生长,发酵系统的pH急剧下降,回升缓慢。需要注意的是,虽然出现抑制现象,但发酵系统可以自行调节;虽然恢复缓慢,但可以慢慢恢复。
2.3 盐度对发酵过程中碱度的影响
有试验认为[15],餐饮有机垃圾处理宜采用间歇搅拌,碱度可大于5 000 mg/L,以确保体系的pH缓冲能力。图3反映了不同浓度Na+对发酵过程中碱度的影响,从图中可以看出,虽然Na+的起始浓度不同,但4个反应器的碱度都是从反应开始便呈现上升趋势。到发酵期21 d结束时,A反应器、B反应器、C反应器和D反应器的碱度分别为6 147.74、5 846.54、5 560.80、5 546.54 mg/L,4个反应器的碱度呈现逐渐递减的趋势,但总体来说差距不大,A反应器和D反应器的碱度仅差10%,很显然这样的碱度相对于高浓度的脂肪酸难以起到足够的缓冲作用。

图3 不同盐度影响下碱度变化
2.4 盐度对发酵过程中脂肪酸浓度的影响
挥发性脂肪酸是有机质经过水解和酸化形成的主要产物,主要成分为乙酸、丙酸、丁酸和戊酸等,这些酸化产物在产甲烷相作为甲烷菌的底物,最终降解转化为甲烷和二氧化碳[16]。因此,VFA的代谢平衡是厌氧反应器稳定运行的关键,当产生的挥发性脂肪酸不能及时转化为甲烷时,整个发酵系统就会出现VFA累积而受到抑制[17]。图4、图5、图6反映了不同盐度影响下的各脂肪酸变化状况。
图4显示了不同盐度对乙酸浓度的影响,4个反应器的乙酸浓度均呈现出先增加后缓慢降落的过程。其中,A反应器乙酸浓度增长平稳,但降解速度快,产甲烷量高。C反应器与D反应器的乙酸浓度增长迅速,浓度高,但降解缓慢,其中,D反应器到试验期结束,乙酸浓度仍然保持在1 633.24 mg/L。乙酸是厌氧发酵产气的底物,C反应器和D反应器乙酸浓度增加很快,但是引起累积,没有及时转化为甲烷,发酵系统产气量降低,说明高浓度的Na+抑制了乙酸的转化。

图4 发酵过程中乙酸的变化曲线
图5反映了不同盐度对丙酸浓度的影响,4个反应器的丙酸浓度呈先增长然后逐渐降低最后又上升的变化过程,整个过程的丙酸浓度增长平稳。C反应器、D反应器的丙酸浓度高于A反应器,到发酵期结束时,丙酸浓度最高分别可达1 121.5 mg/L和1 161.8 mg/L,表明高盐度对丙酸的转化有抑制作用,但是没有对乙酸的抑制明显。

图5 发酵过程中丙酸的变化曲线
图6反映了不同盐度对丁酸浓度的影响,A反应器和B反应器的丁酸浓度在发酵后第6天达到最高峰,但很快降解,到发酵期结束时,丁酸浓度分别达到50.6 mg/L和190.6 mg/L,基本降解。但是,C反应器和D反应器情况不同,到试验期结束时,丁酸虽然有降解,但浓度仍分别高达656.32 mg/L和838.7 mg/L,说明在高盐度影响下,丁酸明显出现积累。

图6 发酵过程中丁酸浓度的变化曲线
不同盐度对发酵反应系统各种脂肪酸的影响存在差异。当盐度从4 000 mg/L增加到12 000 mg/L时,脂肪酸浓度明显出现积累。主要原因是高盐度的抑制作用导致产甲烷菌丧失活性,但产酸细菌生长较快且对环境变化不敏感,造成脂肪酸积累,从而使C反应器和D反应器的pH长期处于酸性状态,到试验期结束时,pH都逐渐恢复,产气量有所增加,没有达到完全恢复。
3 结论
Na+浓度从1 000 mg/L逐渐增加到12 000 mg/L,到发酵期21 d结束时,4个反应器的氨氮浓度基本都保持在1 000~1 150 mg/L,差距不大,都低于1 700 mg/L,从本试验的结果来看,钠离子没有对氨氮产生明显的影响。从试验可以得出,高浓度的盐已经开始抑制产甲烷菌的生长,发酵系统的pH急剧下降,回升缓慢。需要注意的是,虽然出现抑制现象,但发酵系统可以自行调节;虽然恢复缓慢,但可以慢慢恢复。
由于高浓度Na+的抑制作用,4个反应器的碱度呈现逐渐递减的趋势,但总体来说差距不大,A反应器和D反应器的碱度仅差10%,很显然,这样的碱度相对于高浓度的脂肪酸难以起到足够的缓冲作用。在4个反应器中,乙酸含量最高,其次是丁酸和丙酸。在C反应器和D反应器中,高浓度Na+抑制了脂肪酸的转化,减少了甲烷气体的产生。Na+可以引起发酵系统的抑制,但Na+在没有达到完全抑制浓度时,系统可以再行缓慢恢复,产气量和对照组相比明显减少。在系统运行过程中,应加强盐度的监测和控制,减少和控制循环用水的使用。
