工业偏钛酸为原料制备H2TiO3锂离子筛及其吸附性能研究
2021-10-12蒲星宏杜新和王国传张云王倩吴昊
蒲星宏,杜新和,王国传,张云,王倩,吴昊
(四川大学材料科学与工程学院, 四川 成都 610064)
近年来,随着科学技术的全面发展,锂及其化合物在化工、冶金、玻璃、医药、核能,尤其是电池领域有着非常重要的应用,市场对锂资源的需求急剧增加[1]。然而,世界上锂资源总数的60%以上分布在卤水中[2],随着锂矿石资源的逐渐枯竭、开发难度增大,发展经济高效的液相提锂技术已迫在眉睫。目前,卤水提锂的方法主要有太阳蒸发法[3]、共沉淀法[4]、溶剂萃取法[5-6]、电化学法[7]以及吸附法[8]。吸附法因其操作简便、低污染、低成本等优点越来越受到人们的重视。其中,无机吸附剂基于记忆效应,经过特殊的离子交换过程,可以对锂离子进行选择性吸附,因此又被称为锂离子筛吸附剂。离子筛型吸附剂性价比高、稳定性好,近年来得到了广泛而深入的研究。该吸附剂主要分为铝系锂离子筛、锰系锂离子筛和钛系锂离子筛。其中铝系材料吸附容量低[9],锰系吸附容量高但酸洗过程中锰溶损严重,导致其循环稳定性差[10]。钛系材料因具有高的吸附容量、高离子选择性以及结构稳定而被广泛研究[11]。层状H2TiO3(HTO)作为钛系吸附剂中的一种,高的H/Ti比,赋予其高的理论吸/脱附容量(127.27 mg/g),更加稳定的Ti-O键,使得该材料溶损低,循环利用性能优异。目前HTO锂离子筛的合成主要以高纯、精细二氧化钛或钛酸四丁酯为原料[12-13],存在成本高等问题。为了更有利于工业化应用,本文选用工业偏钛酸为钛源,经简单的高温固相法一步合成HTO锂离子筛粉末。为追求高的吸脱附容量,通常要求粉末吸附剂具有较高活性表面、颗粒微小,达到纳米级别。但精细的粉末状吸附剂在固定床或吸附柱操作中对流动液体的阻力大,极易造成堵塞,降低工业生产效率,且在这个过程中粉末状吸附剂容易流失、回收困难,不利于工业上的连续和大规模生产。因此,针对以上问题,本工作将粉末吸附剂材料加工成条状,便于工业回收利用。
1 实验部分
1.1 HTO锂离子筛的制备
本实验主要原料为工业偏钛酸(TiO2含量为91.1%)、氢氧化锂、碳酸锂、醋酸锂、盐酸均为分析纯。将一种锂源(LiOH·H2O、Li2CO3或C2H3LiO2·2H2O)加入到研钵中,加入适量无水乙醇研磨形成悬浮液,将研钵放入到烘箱,60℃加热30 min成熔融态,然后将钛源(工业偏钛酸)按摩尔比Li:Ti=2.02:1加入到研钵中混合均匀后常温下干燥,在一定温度(550 ~ 850℃)下烧结后得到锂离子筛前驱体LTO。将前驱体放入一定浓度的盐酸溶液中常温搅拌反应24 h,然后过滤并用去离子水洗涤、干燥后得到HTO锂离子筛。
1.2 条形HTO锂离子筛(PVDF-HTO)的制备
通过反溶剂法制备条形PVDF-HTO,简要地,将0.35 mL的PEG-600加 入5mL的NMP中。然后通过搅拌将0.25 g的PVDF完全溶解在溶液中。最后,添加1.0 g的LTO前驱体粉末并均匀地混合以形成浆料,用移液枪将浆料快速挤入去离子水中以形成直径约为1 mm、长度为1 ~ 2 cm的条状PVDF-HTO。随后,将这些材料在60℃下用盐酸溶液处理约24 h,以获得条状PVDF-HTO吸附剂。
1.3 实验测定及计算方法
(1)吸附动力学测试:将0.3 g的HTO锂离子筛加入到100 mL的模拟卤水(C0=1000 mg/L)中,常温下磁力搅拌一定时间。每隔一段时间用离心机离心后取上层清液,去离子水稀释后用火焰光度计(FP)测得剩余的锂离子浓度(Ct)。根据式(1)计算t时刻的吸附容量(qt),吸附后的锂离子筛经0.25 mol/L HCl酸洗后即可再生。

其中qt(mg/g)为t时刻的吸附容量;C0(mg/L)为离子的初始浓度;Ct(mg/L)为时间t(h)时的离子浓度;V(L)为模拟卤水的体积;m(g)为HTO锂离子筛的质量。
(2)循环性能测试:将0.3 g的HTO锂离子筛加入到100 mL的模拟卤水(C0=1000 mg/L)中,常温下磁力搅拌至平衡后收集上清液,采用火焰光度计进行Li+浓度分析,剩余吸附剂用去离子水洗涤、干燥后用0.25 M HCl进行Li+解吸,监测此过程中Li洗脱率,然后将再生的吸附剂应用于下一次吸/脱附循环。根据式(2)、(3)和(4)计算平衡时脱附容量(qde)、脱附效率(Ede)和Ti溶损率(Tiloss)[14]:
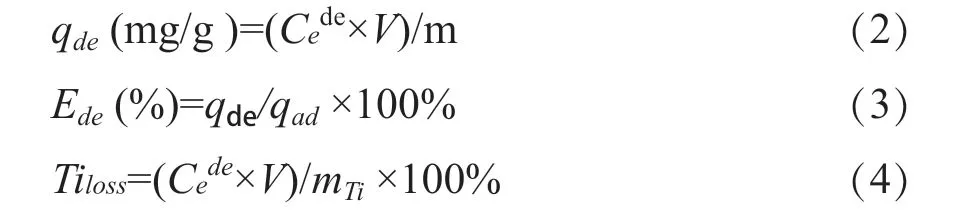
其中qde(mg/g)为表示脱附容量;(mg/L)为对应脱附平衡时溶液中金属离子的浓度;Ede(%)为平衡脱附效率;Tiloss(%)为Ti溶损率。
2 结果与分析
2.1 不同锂源制备LTO前驱体的形貌表征
采用不同锂源(LiOH·H2O、Li2CO3和C2H3LiO2·2H2O)分别作为原料合成的单斜偏钛酸锂LTO前驱体,其微观形貌有较大差异,见图1。

图1 不同锂源制备LTO的SEM图像Fig. 1 SEM images of LTO precursor obtained using
(a)、(b)和(c)分别为用LiOH·H2O、Li2CO3和C2H3LiO2·2H2O作为锂源合成的LTO前驱体的SEM图像。从图1(a)可以看出,用LiOH·H2O作为锂源合成的LTO呈较为规则的立方体形貌,粒径分布在约300 ~ 400 nm,结构致密,颗粒团聚较为严重;从图1(b)可以看出,用Li2CO3作为锂源合成的LTO每个晶粒形貌相似,晶体的粒度分布也较为均匀(200 ~ 300 nm),但同样颗粒团聚严重;从图1(c)可以看出,用C2H3LiO2·2H2O作为锂源合成的LTO与用Li2CO3作为锂源合成的LTO晶粒形貌相似,但粒径更小(~ 200 nm),并且结构较为疏松多孔。将不同锂源制备的锂离子筛前驱体用0.25 mol/L的盐酸酸洗脱锂后进行吸附试验实验,见图2。
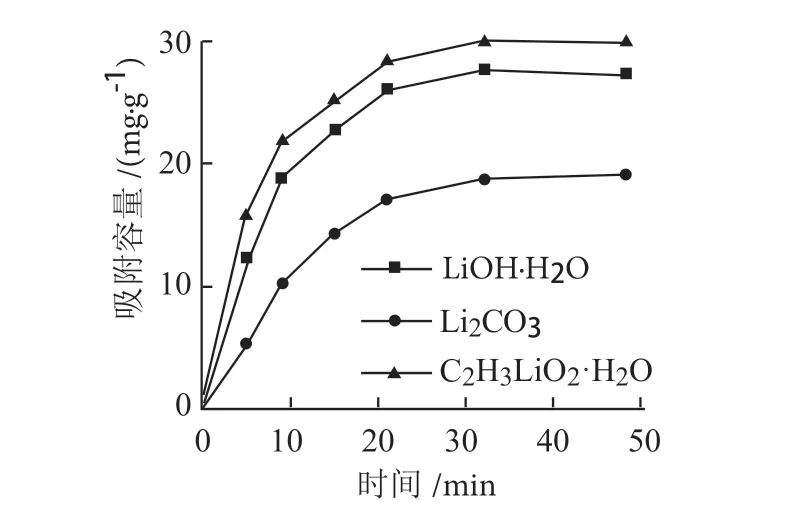
图2 不同锂源制备HTO的时间-吸附容量曲线Fig. 2 Li adsorption capacity-time curves of HTO obtained from different Li sources
2.2 不同煅烧时间制备LTO的结构与形貌表征
用C2H3LiO2·2H2O作为锂源,工业偏钛酸为钛源,在不同煅烧温度下得到前驱体LTO的XRD见图3。

图3 不同煅烧温度得到的LTO的XRDFig. 3 XRD patterns of LTO precursors obtained under different calcination temperatures
与单斜偏钛酸锂LTO标准PDF卡片(JCPDS33-0831)相对比,三种煅烧温度下均生成了单斜LTO晶相。但在550℃时,合成的LTO前驱体中不仅仅有Li2TiO3晶相,还存在一些TiO2杂相,因而550℃不是煅烧最佳温度。当温度升高到700℃时,衍射峰强度明显强化且无杂相生成。继续升高温度到850℃,其衍射峰变细且变尖,说明其结晶度更高。
由图4可知,较高的煅烧温度也加剧了颗粒的团聚,降低其比表面积,进而影响吸附性能。根据谢乐公式,衍射峰变细其平均晶粒尺寸也更大。因而,将制备LTO的较佳煅烧温度确定为700℃。

图4 不同煅烧温度制备LTO的SEM图像Fig. 4 SEM images of LTO precursor obtained under different calcination temperatures
三种锂离子筛在1000 mg/L的锂溶液中吸附32 h左右达到平衡,用LiOH·H2O作为锂源合成的HTO锂离子筛平衡吸附容量为27.64 mg/g,用Li2CO3作为锂源合成的HTO锂离子筛平衡吸附容量为18.75 mg/g,用C2H3LiO2·2H2O作为锂源合成的HTO锂离子筛平衡吸附容量为29.98 mg/g,结果表明,用C2H3LiO2·2H2O作为锂源合成的HTO锂离子筛平衡吸附容量较高,这得益于该材料疏松多孔的结构有利于吸附过程中的Li+的快速液相传输扩散。因此,选定C2H3LiO2·2H2O作为锂源。
2.3 盐酸浓度对吸附剂吸附容量的影响
单斜偏钛酸锂离子筛前驱体LTO成功制备后,通过酸洗将前驱体中的锂离子洗脱出来,从而留下尺寸与锂离子(0.076 nm)相匹配的空穴,这个空穴只能容纳尺寸小于或等于锂离子半径的金属离子。盐湖卤水与锂离子共存的金属离子主要为K+(0.138 nm)、Ca2+(0.100 nm)、Na+(0.102 nm)、Mg2+(0.072 nm),K+、Ca2+与Na+由于其较大的离子半径不能进入HTO晶格内,而Mg2+由于其水合能较大,脱去身边的水分子进入晶格也很困难,因此HTO锂离子筛对锂离子具有高的离子选择性。酸洗是为了将LTO中的Li+洗出之后留下空位进而容纳尽可能多的锂离子,空穴的多少直接影响着吸附剂后续吸附容量的大小。本实验主要探究了酸洗用盐酸浓度对LTO前驱体脱锂量和酸洗后形成锂离子筛结构稳定性的影响。
由图5可知,将1 g锂离子筛前驱体加入到不同浓度的盐酸中,常温下搅拌24 h,离心取上清液测其中锂离子与钛离子浓度。脱锂率越高,意味着其吸附容量也会越高,然而高的钛溶损会严重破坏其结构稳定性,影响其长期循环性能,因而我们需要选出一个合适的盐酸浓度使得其脱锂量足够高,但其钛溶损相对较小。从图中可以看出随着盐酸浓度的增加,其脱锂率急剧增加,随之增加的还有钛溶损率。当盐酸浓度为0.25 mol/L时,其脱锂率达到93.38%,此时钛溶损为0.52%;继续增加盐酸浓度,其脱锂率与钛溶损也相应增加,盐酸浓度为0.5 mol/L时脱锂率达到98.35%,此时钛溶损为3.38%;盐酸浓度为1 mol/L时脱锂率达到99.78%,此时钛溶损为15.71 %。因此,综合考虑选择盐酸浓度为0.25 mol/L。
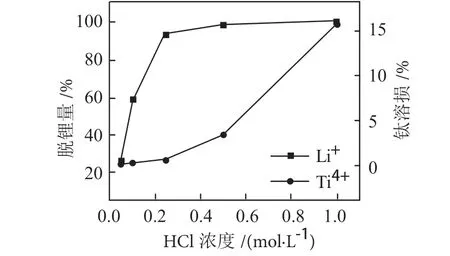
图5 盐酸浓度对脱锂量和钛溶损的影响Fig. 5 Effect of HCl concentration on the lithium removal and titanium dissolution
2.4 酸洗转型前后吸附剂结构对比
用X射线衍射(XRD)和场发射扫描电子显微镜(SEM)对LTO前驱体以及HTO吸附剂(C2H3LiO2·2H2O作为锂源,700℃,4 h,0.25 mol/L HCl酸洗)进行了表征,见图6。

图6 酸洗前后形貌变化Fig. 6 SEM images of morphology changes before and after pickling
HTO样品很好地继承了LTO前驱体的形貌特征,纳米颗粒分布均匀,没有明显的团聚现象。
从图7可以看出,酸洗之后,HTO的XRD谱图与LTO前驱体相比发生了显著变化,(002)和(131)的衍射峰略微右移,表明了酸洗过程中的晶胞收缩。此外,酸处理后(133)、(206)和(062)晶面也随之消失。
2.5 pH值对吸附容量的影响
由图8可知,将0.3 g HTO锂离子筛加入到100 mL浓度为1000 mg/L不同pH值的模拟卤水中,搅拌32 h之后,离心取其上清液测锂离子浓度。可以看出,吸附剂的吸附容量受到模拟卤水中pH值的显著影响。随着pH值的增加,其吸附容量也随之上升,pH值大于10之后,吸附容量急剧上升,pH值为12时吸附容量达到最大,当pH值超过12.5后,吸附容量反而降低。因此,确定吸附溶液pH值在12 ~ 12.5之间。
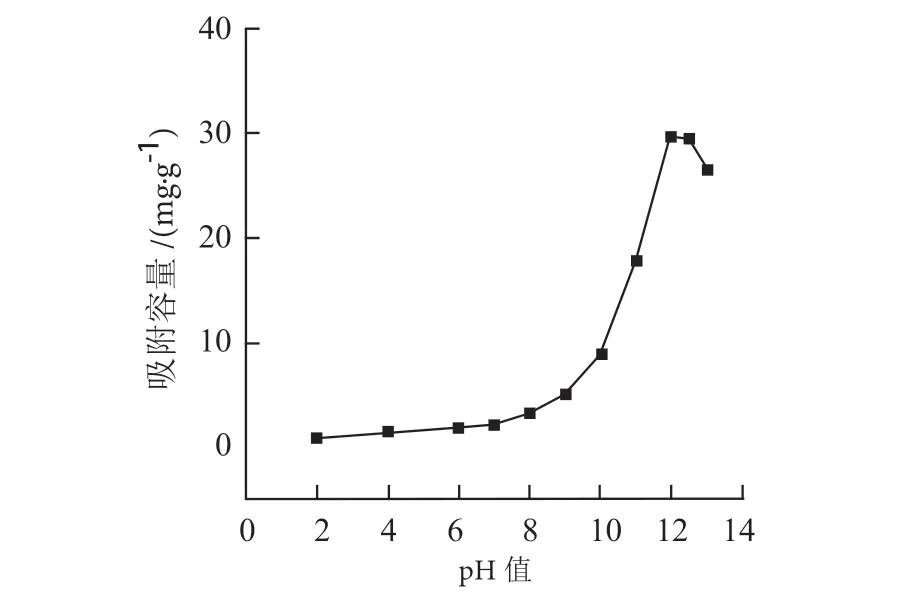
图8 pH值对吸附容量的影响Fig. 8 Effect of pH value on adsorption capacity
2.6 HTO锂离子筛循环性能
2.6.1 粉末HTO锂离子筛循环性能
根据上述讨论,以C2H3LiO2·2H2O为锂源、工业偏钛酸为钛源合成的HTO锂离子筛显示了较高的平衡吸附容量。对吸附剂来说,回收特性也是决定吸附剂能否实际应用的关键性能。为此,本文研究了该样品的吸/脱附循环性能(0.3 g HTO锂离子筛加入100 mL模拟卤水中,C0≈1000 mg/L,pH=12.43),见图9。

图9 粉末HTO锂离子筛的循环性能Fig. 9 (a) Cycling adsorption/desorption capacities, and (b)desorption efficiencies of powder HTO lithium ion sieve
对于每个循环,吸附平衡后,将粉末HTO锂离子筛过滤、干燥并用0.25 M HCl洗脱再生。图9(a)中的结果表明,首次吸附容量为29. 92 mg/g,在5个循环之后几乎没有容量衰减,且Li+脱附效率稳定在94.08%以上(图9(b))。优异的吸脱附性能均显示了HTO锂离子筛骨架具有极好的的稳定性,有利于其多次循环利用。
2.6.2 条形PVDF-HTO锂离子筛循环性能
为了实现工业上的连续和大规模生产,粉末HTO锂离子筛需进行造粒处理。其造粒后的光学照片和SEM见图10。

图10 条形PVDF-HTO吸附剂Fig. 10 SEM image of the striped PVDF-HTO LIS
粉末HTO锂离子筛经造粒制备成条状大颗粒。条状PVDF-HTO的吸附循环性能(0.3 g HTO锂离子筛加入100 mL模拟卤水中,C0≈1000mg/L,pH=12.43)见图11。
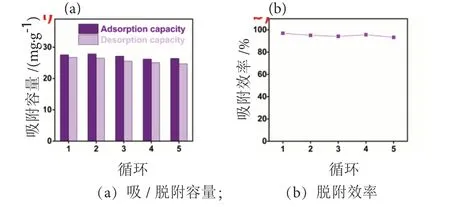
图11 条形PVDF-HTO吸附剂的循环性能Fig. 11 (a) Cycling adsorption/desorption capacities, and (b)desorption efficiencies of the striped PVDF-HTO LIS.
每个循环达到吸附平衡后,将条状PVDF-HTO吸附剂过滤、干燥并经0.25 M HCl洗脱再生。图11(a)中的结果表明,首次吸附容量为27.56 mg/g,在5个循环过程之后容量衰减较小,并且Li+脱附效率稳定在93.3%(图11(b))。
3 结 论
采用C2H3LiO2·2H2O为锂源、工业偏钛酸为钛源,通过高温固相法合成的HTO锂离子筛结构最为疏松多孔。因此,在该体系下对实验条件进行探索。结果表明,其最佳合成温度为700℃,煅烧时间4 h,洗脱用盐酸浓度为0.25 mol/L,吸附溶液环境较佳pH值范围为12 ~ 12.5。较佳工艺条件下得到的HTO锂离子筛平衡吸附容量较高为29.98 mg/g,经造粒成条形后其平衡吸附容量仍然可以达到27.56 mg/g,与粉末状锂吸附剂接近。粉末和条形造粒吸附剂都表现出优异的循环性能。综上,该材料具有制作工艺简单、原材料成本低廉、且造粒后仍具有可观的吸附性能,因此,具有巨大的实用化潜力。
