龙骨风HPLC 指纹图谱建立及5 种成分测定
2021-09-27卢汝梅张进燕杨新洲韦建华
卢汝梅,张进燕,王 肖,杨新洲,韦建华,李 兵*
(1.广西中医药大学药学院,广西 南宁530200; 2.中南民族大学药学院,湖北 武汉 430074)
壮药龙骨风为桫椤科植物桫椤Alsophila spinulosa(Wall.ex Hook.)Tryon 的茎干,具有祛风除湿、活血散瘀、清热解毒、止咳平喘、强筋骨、杀虫等功效[1⁃2],主要分布在中国南部、南亚和东南亚等地[3⁃4],具有一定的抗肿瘤、抗菌和镇痛作用[5⁃7],主要含黄酮、三萜、甾体、酚酸等成分[8⁃12]。药材中化学成分种类及含量可能会随着其地理来源、物种和收获季节的不同而产生变化[13⁃14]。龙骨风来源广泛,规格等级复杂,仅凭TLC 或单一成分含量测定难以全面反映其质量。近年来,越来越多的学者采用指纹图谱结合多成分定量分析的方法进行药材质量评价[15⁃18],故本实验建立11 批龙骨风HPLC 指纹图谱,并对其中5 种成分含量进行测定,以期为其科学鉴定和质量控制提供依据。
1 材料
Agilent 1260 高效液相色谱仪(美国安捷伦公司);UV⁃1780 型紫外分光光度计[岛津(中国)有限公司];CPA225D 型电子天平[十万分之一,赛多利斯科学仪器(北京)有限公司];KQ5200B型超声清洗器(昆山市超声仪器有限公司)。
甲醇为色谱纯[赛默飞世尔科技(中国)有限公司];其他试剂均为分析纯;水为超纯水。原儿茶酸(批号110809⁃201205)、原儿茶醛(批号110810⁃201608)对照品均购自中国食品药品检定研究院;其余对照品为2018 年广西中医药大学中药化学课题组从龙骨风中分离得到,分别为咖啡酸、反式对羟基肉桂酸、阿魏酸,质量分数均大于98.0%。
11 批龙骨风采自国外内各地,信息见表1,经广西中医药大学壮医药学院韦松基教授鉴定为桫椤科植物桫椤Alsophila spinulosa(Wall.ex Hook.)Tryon 的茎干。
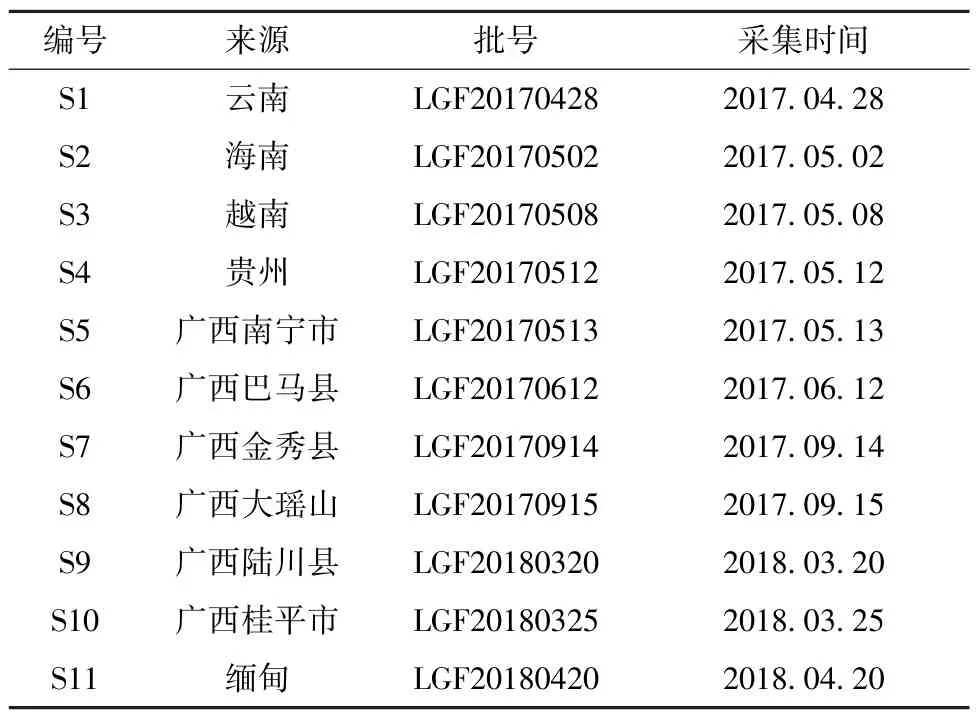
表1 样品信息Tab.1 Information of samples
2 方法与结果
2.1 色谱条 件 COSMOSIL 5C18⁃PAQ 色谱柱(250 mm× 4.6 mm,5 μm);流动相甲醇(A)⁃0.1%磷酸(B),梯度洗脱,程序见表2;体积流量1.0 mL/min;柱温35 ℃;检测波长280 nm;进样量15 μL。
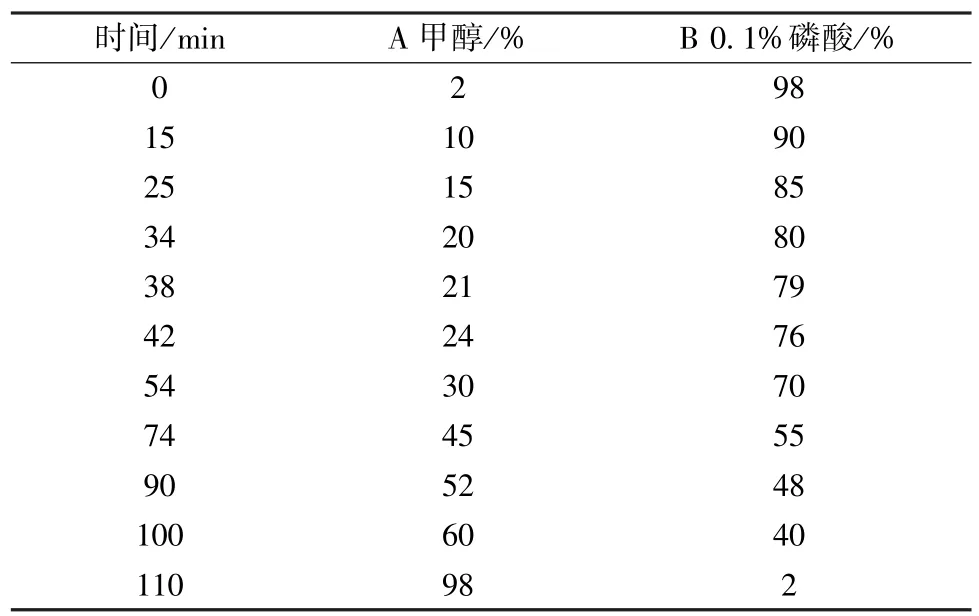
表2 梯度洗脱程序Tab.2 Gradient elution programs
2.2 溶液制备
2.2.1 对照品溶液 精密称取各对照品适量,置于2 mL 量瓶中,甲醇溶解并定容,制得贮备液,取适量置于同一量瓶中,加甲醇稀释,制成分别含原儿茶酸、原儿茶醛、咖啡酸、反式对羟基肉桂酸、阿魏酸0.187 9、0.371 0、0.170 4、0.023 5、0.019 8 mg/mL 的对照品溶液。
2.2.2 供试品溶液 取龙骨风粉末(50 目)5 g,精密称定,置具塞锥形瓶中,精密加入甲醇⁃1%冰醋酸(70 ∶30)混合液25 mL,称定质量,超声45 min,放冷,甲醇⁃1%冰醋酸(70 ∶30)混合液补足减失的质量,摇匀,滤过,挥干溶剂,甲醇⁃1%冰醋酸(70 ∶30)定容至5 mL,0.22 μm 微孔滤膜过滤,即得,4 ℃保存备用。
2.3 方法学考察
2.3.1 精密度试验 取药材(LGF20170428),按“2.2.2”项下方法制备供试品溶液,在“2.1”项色谱条件下进样6 次,测得各共有峰相对保留时间及相对峰面积RSD 均小于3.0%,表明仪器精密度良好。
2.3.2 稳定性试验 取药材(LGF20170428),按“2.2.2”项下方法制备供试品溶液,在“2.1”项色谱条件下于0、2、4、8、12、16、24 h 测定,测得各共有峰相对保留时间及相对峰面积RSD 均小于3.0%,表明溶液在24 h 内稳定性良好。
2.3.3 重复性试验 取药材(LGF20170428),按“2.2.2”项下方法制备供试品溶液6份,在“2.1”项色谱条件下进样,测得各共有峰相对保留时间及相对峰面积RSD 均小于3.0%,表明该方法重复性良好。
2.4 指纹图谱建立 取11 批样品,按“2.2.2”项下方法制备供试品溶液6 份,在“2.1”项色谱条件下进样。
2.4.1 共有峰确定 根据11 批样品HPLC 色谱图,并比对15 个共有峰,构建其特征指纹图谱。由于原儿茶醛在各批样品中均出现,分离度良好,峰面积较大,故选择其(5 号峰)作为参照峰。
2.4.2 共有峰归属 通过对照品比对,确定5 个共有峰代表的成分,其中4~5 号峰分别确定为原儿茶酸、原儿茶醛,9 号峰为咖啡酸,11 号峰为反式对羟基肉桂酸,15 号峰为阿魏酸,见图1。

图1 各成分HPLC 色谱图Fig.1 HPLC chromatograms of various constituents
2.4.3 相似度计算及对照指纹图谱生成 11 批样品指纹图谱见图2,将其AIA 数据文件导入中药指纹图谱相似度评价系统研究版(2012)进行相似度计算,设置样品S1 图谱为参照图谱,对照图谱生成方法采用中位数法,时间窗宽度为0.1,自动匹配,生成对照指纹图谱,见图3,相似度见表3。
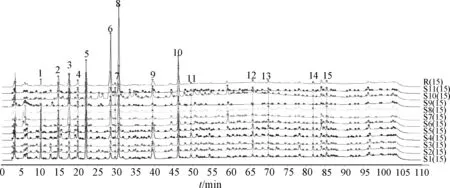
图2 11 批样品HPLC 指纹图谱Fig.2 HPLC fingerprints of eleven batches of samples
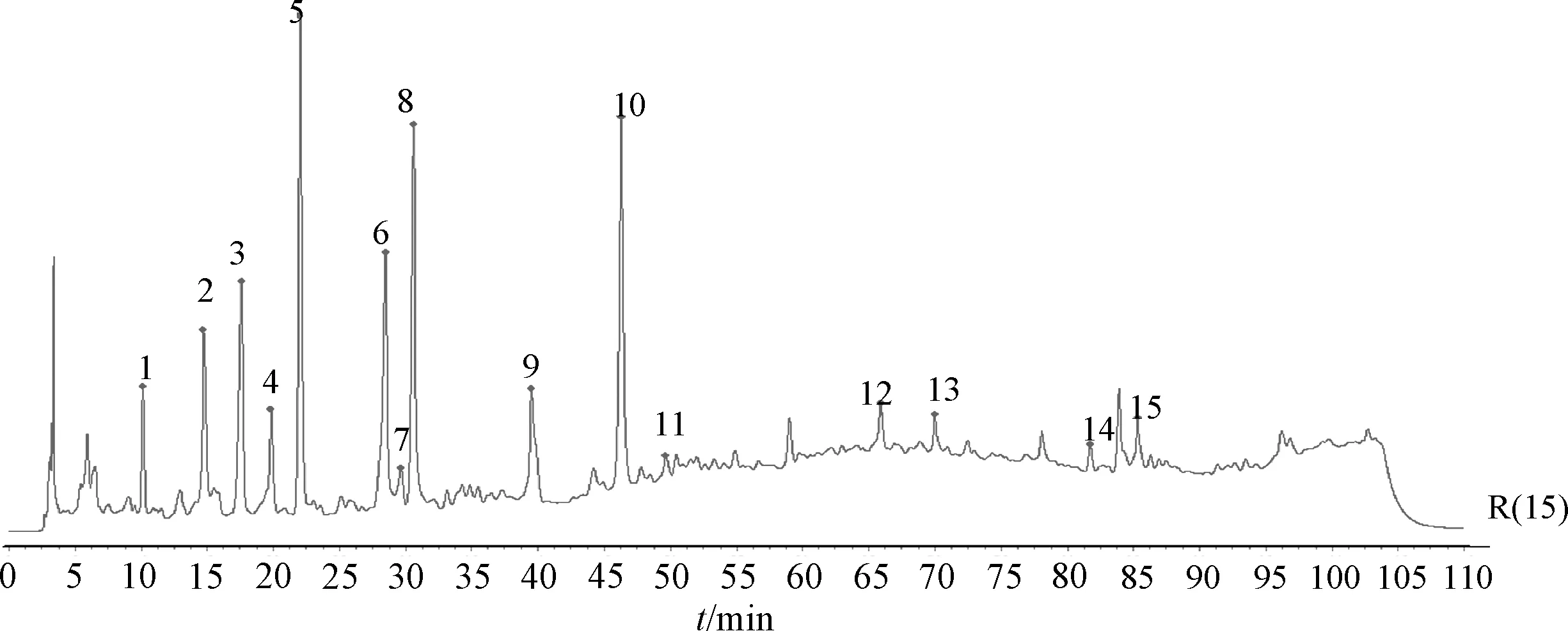
图3 11 批样品HPLC 指纹图谱共有模式Fig.3 Common pattern of HPLC fingerprints of eleven batches of samples
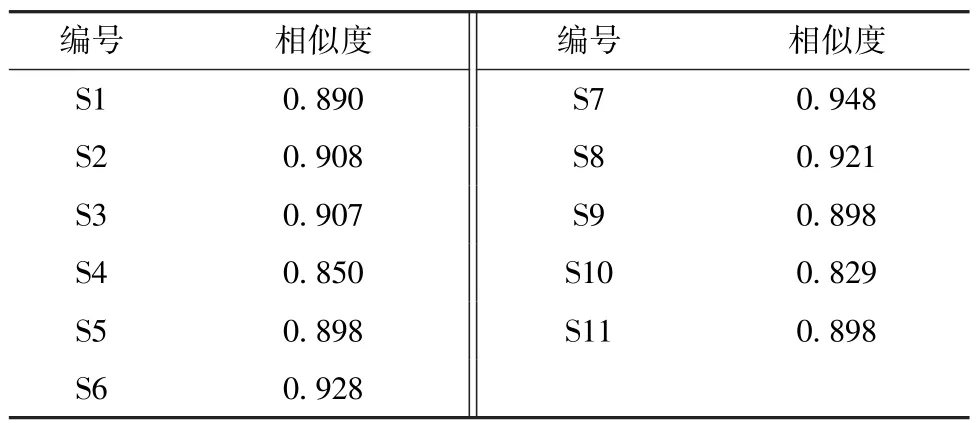
表3 11 批样品相似度Tab.3 Similarities of eleven batches of samples
2.4.4 相似度分析 与对照指纹图谱比较,各批样品相似度在0.829~0.948 之间,90.9%在0.850以上,表明不同产地药材成分相似度高,但仍然存在一定差异。另外,S4、S1、S5、S11、S9、S10相似度较低,其他样品较高,其中S10 与共有模式图谱的相似度最低,仅为0.829。
2.4.5 聚类分析 运用SPSS Statistics 22.0 软件对11 批样品的共有峰面积进行系统聚类分析,采用组间连接法,以平方Euclidean 距离为度量标准,标准化范围0~1,结果见图4。在距离10 内,11批样品聚为3 类;样品S1~S5、S8、S11 产地、共有峰面积相近,因此聚为一类;S6~S7、S9 聚为一类;S10 的差异性最大,聚类距离最远,聚为一类,与相似度评价结果基本一致。

图4 11 批样品聚类树状图Fig.4 Dendrogram of eleven batches of samples
2.4.6 主成分分析 在聚类分析的基础上,运用SPSS Statistics 22.0 对样品进行主成分分析,主成分的特征值及贡献率作为主成分选择的依据。根据降维结果,共挑选出2 个主成分因子,各主成分因子方差贡献值分别为81.869%、8.253%,累积贡献值达到90.122%,见图5,与聚类分析的结果一致。
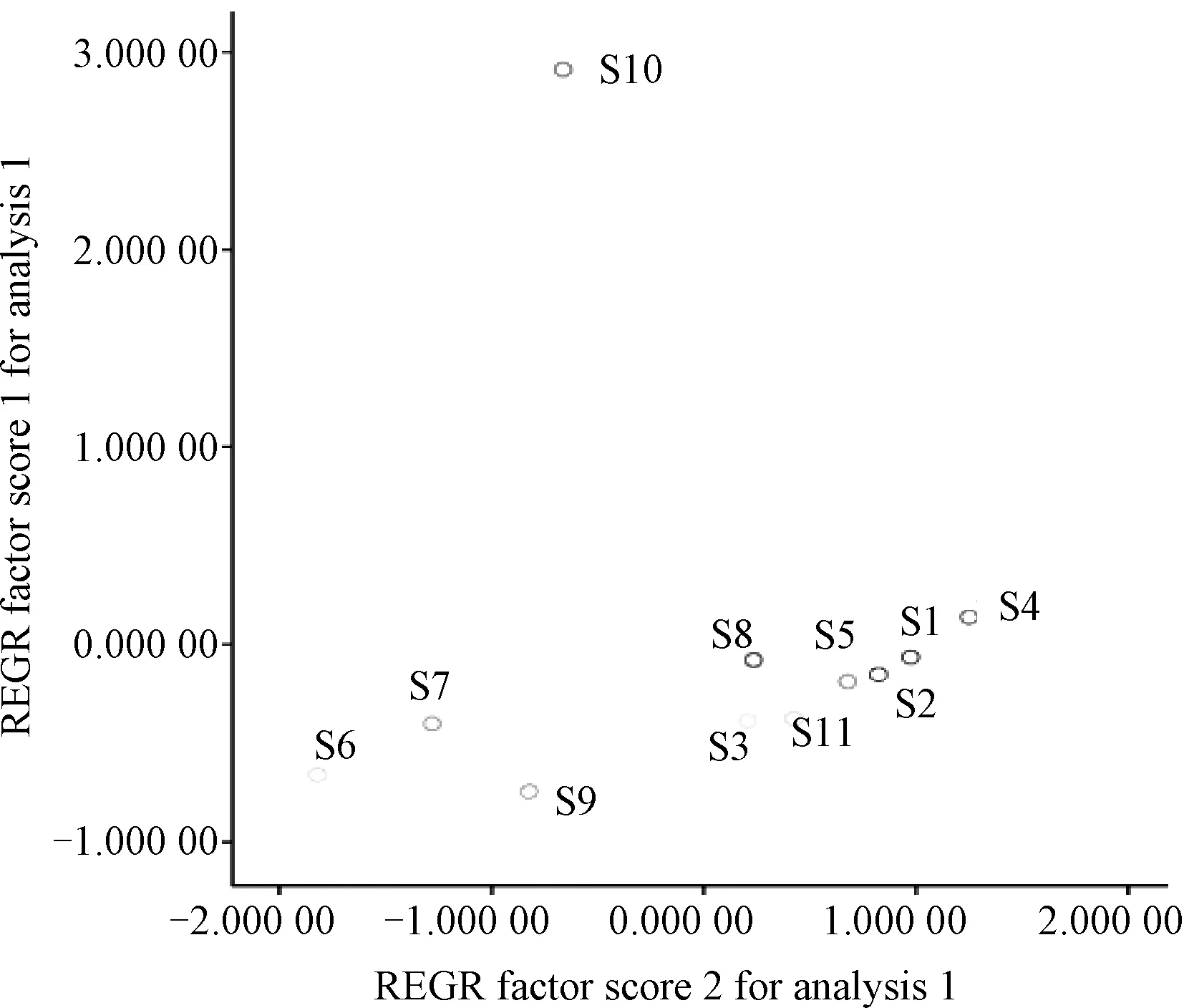
图5 11 批样品主成分分析图Fig.5 Principal component analysis plot for eleven batches of samples
2.5 5 种成分含量测定
2.5.1 线性关系考察 取对照品贮备液适量,逐级稀释,制成对照品溶液,分别精密吸取15 μL,在“2.1”项色谱条件下进样测定。以峰面积为纵坐标(Y),质量浓度为横坐标(X)进行回归,发现各成分均呈良好的线性关系,见表4。
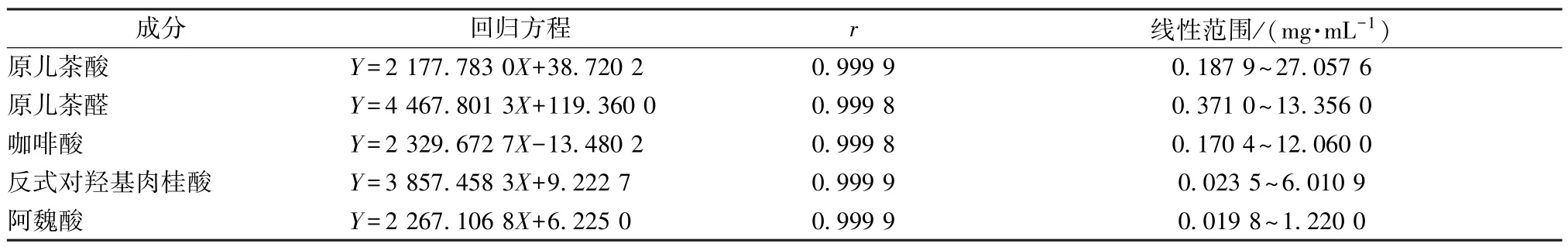
表4 各成分线性关系Tab.4 Linear relationships of various constituents
2.5.2 精密度试验 取药材(LGF20170428)粉末5 g,精密称定,按“2.2.2”项下方法制备供试品溶液6 份,在“2.1”项色谱条件下进样6 次,测得原儿茶酸、原儿茶醛、咖啡酸、反式对羟基肉桂酸、阿魏酸峰面积RSD 分别为0.72%、0.52%、0.53%、0.40%、0.21%,表明仪器精密度良好。
2.5.3 稳定性试验 取药材(LGF20170428)粉末5 g,精密称定,按“2.2.2”项下方法制备供试品溶液6 份,于0、2、4、6、8、12、24 h 各精密吸取15.0 μL,在“2.1”项色谱条件下进样,测得原儿茶酸、原儿茶醛、咖啡酸、反式对羟基肉桂酸、阿魏酸峰面积RSD 分别为1.55%、1.28%、0.97%、0.60%、0.31%,表明溶液在24 h 内稳定性良好。
2.5.4 重复性试验 取药材(LGF20170428)粉末5 g,精密称定6 份,按“2.2.2”项下方法制备供试品溶液,各吸取15.0 μL,在“2.1”项色谱条件下进样,测得原儿茶酸、原儿茶醛、咖啡酸、反式对羟基肉桂酸、阿魏酸峰面积RSD 分别为0.27%、0.32%、0.74%、0.63%、0.32%,表 明该方法重复性良好。
2.5.5 加样回收率试验 精密称取药材(LGF20170428)粉末2.5 g,共6 份,精密加入含原儿茶酸(0.177 mg/mL)、原儿茶醛(0.410 mg/mL)、咖啡酸(0.511 mg/mL)、反式对羟基肉桂酸(0.061 mg/mL)、阿魏酸(0.147 mg/mL)的对照品溶液1.00 mL,按“2.2.2”项下方法制备供试品溶液6 份,在“2.1”项色谱条件下进样15 μL,计算回收率,结果见表5。
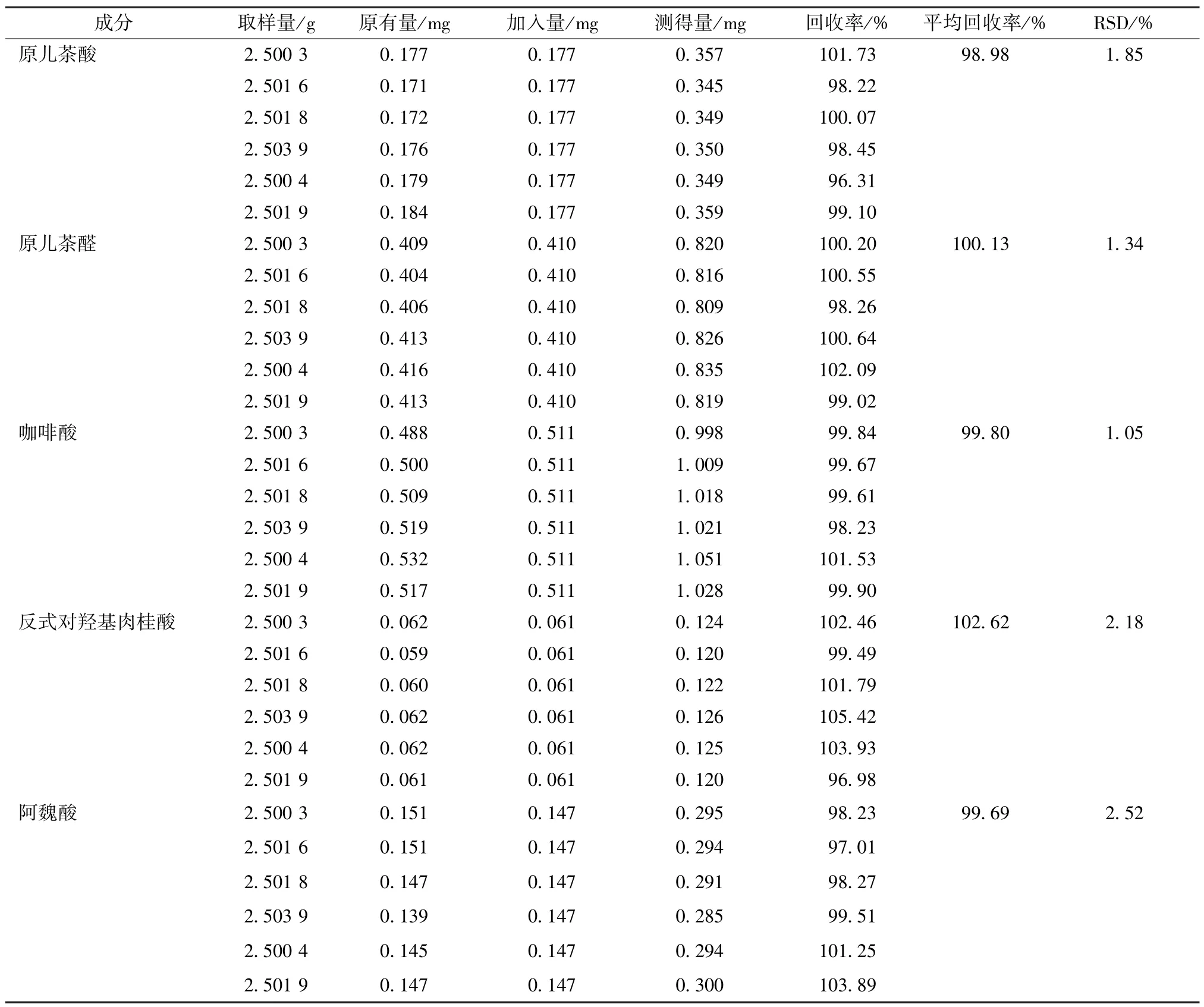
表5 各成分加样回收率试验结果(n=6)Tab.5 Results of recovery tests for various constituents(n=6)
2.5.6 样品含量测定 取不同产地药材各5 g,精密称定,按“2.2.2”项下方法制备供试品溶液6份,精密吸取15.0 μL,在“2.1”项色谱条件下进样,外标法计算含量,结果见表6。
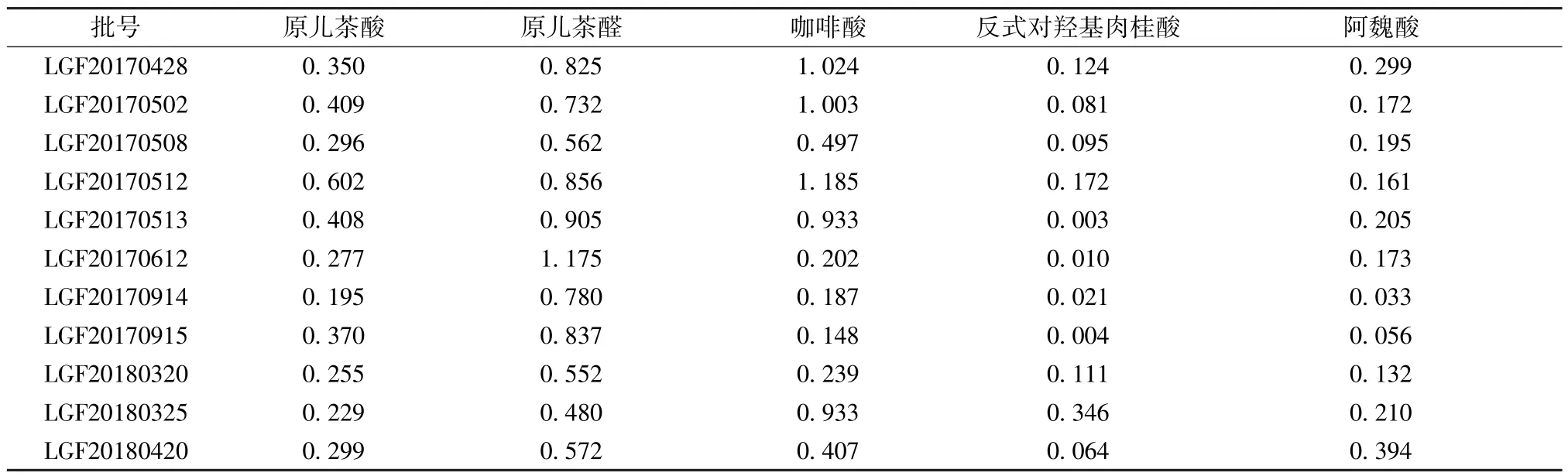
表6 各成分含量测定结果(mg/g)Tab.6 Results of content determination of various constituents(mg/g)
3 讨论
本实验分别对不同提取方法、溶剂种类、提取次数、提取体积、流动相、检测波长、色谱柱、柱温、流速等条件进行考察。结果表明,在“2.1”项色谱条件下进样时,所得色谱图峰形较好、分离度高,重复性好,因此选择其作为色谱条件。
本实验运用HPLC 法建立了11 批样品的指纹图谱,并采用中药指纹图谱相似度评价系统(2012 版)建立了共有模式,结果显示各批样品相似度为0.829~0.948,表明其指纹图谱基本一致,品质较稳定。再采用中位数法,经多点校正、自动匹配后共生成了15 个共有峰,指认了其中5 个,分别为原儿茶酸、原儿茶醛、咖啡酸、反式对羟基肉桂酸、阿魏酸。药理研究表明,酚酸类成分具有消除自由基、抗炎、抗病毒、抗氧化等[19⁃20]活性,也与龙骨风功效相关,故本实验选取这5 种成分作为指标进行含量测定,结果表明同一成分在不同批次样品中存在较大的差异,可能受药材生长的地理环境、生长年限、采收季节、储存条件等因素的影响。
4 结论
本研究首次采用HPLC 指纹图谱结合聚类分析、主成分分析、含量测定对11 批龙骨风进行研究,所建立的方法准确可靠,重复性好。通过对龙骨风药材指纹图谱的初步研究,可为其质量控制提供依据也能为探索谱效关系、明确其主要有效成分奠定基础。
