食品中丙烯酰胺抑制策略的研究进展
2021-09-27汪腾飞孙大文蒲洪彬韦庆益
汪腾飞,孙大文,蒲洪彬,韦庆益*
(华南理工大学食品科学与工程学院,现代食品工程研究中心,广东省冷链食品智能感知与过程控制工程技术研究中心,广东 广州 510006)
随着人们生活方式的改变,食品营养和安全问题受到广泛的关注。在获得诱人风味和香气的同时,食品原材料在热加工过程中所发生的化学反应也会导致一些有毒物质的产生。其中,丙烯酰胺(acrylamide,AM)是热加工食品中最为常见的危害物之一。早在1994年,AM就被国际癌症研究机构列入“可能的人类致癌物(2A组)”[1]。后续的研究证明,AM严重危害人体的遗传物质、神经系统、免疫功能等方面,并且还具有潜在的致癌性,因此科研人员对食品中AM的形成、毒性、抑制以及检测方面都进行了广泛的探索。研究表明,在超过120 ℃的条件下加热土豆等富含还原糖和天冬酰胺(asparagine,Asn)的食品时会发生美拉德反应,而AM就是该反应的重要产物之一[2]。鉴于AM对人体的潜在危害,在保证热加工食品品质的同时,选择合适的抑制策略来缓解食品中AM的形成也是十分必要的。因此,本文将从食品原材料选择、预处理到热加工得到最终产品的整个过程出发,结合具体的反应过程,从机理的角度对食品中AM形成和抑制策略进行系统的归纳。
1 AM在食品中的含量及毒性
1.1 AM在食品中的含量
AM主要通过饮用水、食品以及皮肤接触进入人体,其中最重要的途径是通过食品摄入。目前已有学者对不同热加工食品中的AM含量进行了检测和统计,结果如表1所示。其中,薯片中所检测到的AM含量最高,然后依次分别为面包、咖啡和饼干。考虑到AM在人体中大量累积必然会对生命健康造成有害影响,因此对AM的毒性及其毒性机理的研究显得尤为重要。
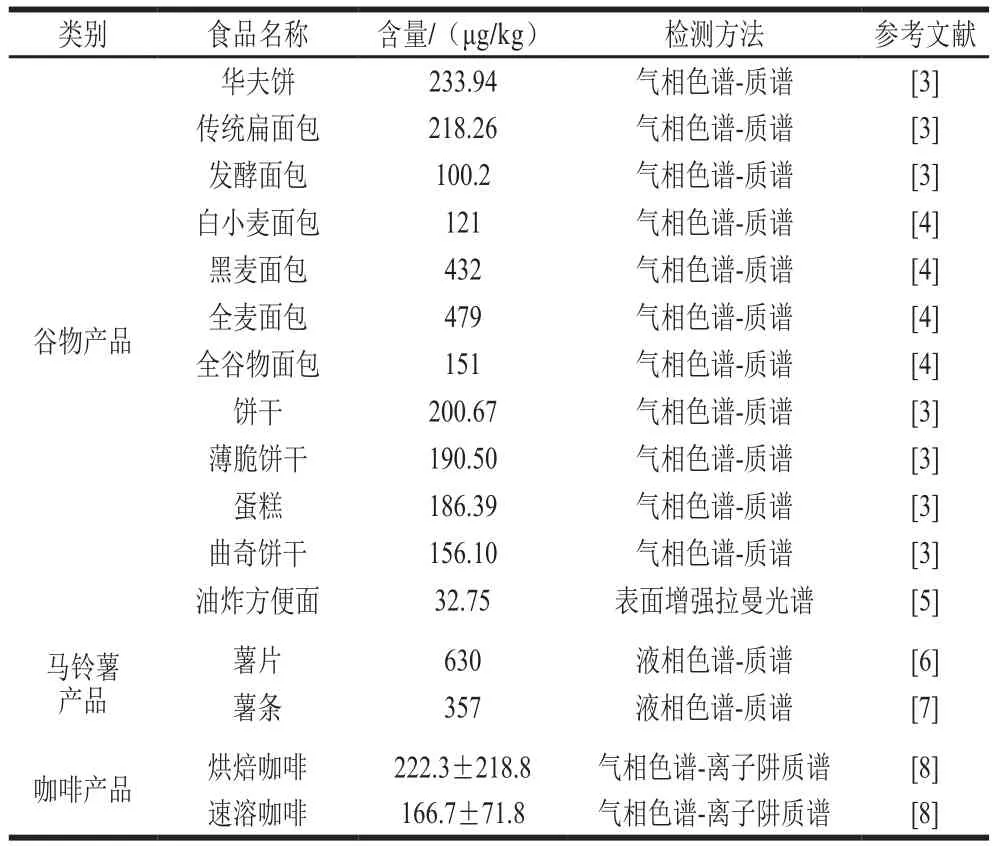
表1 AM在不同食品中的含量Table 1 Contents of AM in different food matrixes
1.2 AM的毒性作用机理
AM的毒性主要体现在对人体免疫功能、遗传物质、神经系统等方面的损伤以及潜在致癌性,并且上述毒性都已通过动物实验或者体外细胞实验所证实。虽然学界对于AM的毒性作用机理尚无统一定论,但仍有众多的研究结果可供参考。就AM的神经毒性而言,离子作用、与蛋白结合、能量代谢、氧化应激和细胞凋亡与自噬被认为是AM诱发神经毒性的主要途径。潘校琦等[9]发现,AM可以使PC12细胞中活性氧化物和脂质过氧化物的水平提升,同时使抗氧化物的水平降低,最终由于生物大分子发生过氧化进而损害细胞正常功能。而AM的致癌性则被认为与多种癌症相关蛋白数量的减少有关。许义[10]发现经过AM处理的HepG2细胞中多种基因表达的蛋白数量减少,这些蛋白涉及的代谢通路与病毒致癌、转录失误调控、肝癌化等息息相关,实验结果能够从转录组学的角度证明AM的致癌性。此外,AM经人体内代谢时,如果浓度过高,会在细胞色素的作用下生成活性环氧丙酰胺,二者都可以与遗传物质中的鸟嘌呤结合,从而损伤人体遗传物质[11]。当人体中的AM积累到一定水平,同样会对人体的免疫系统造成损伤。刘东敏等[12]报道了AM能够通过氧化应激途径对小鼠体内的免疫细胞造成损伤;此外,还发现AM能够抑制巨噬细胞正常增殖并降低淋巴细胞转化率,表明AM对非特异性免疫和细胞免疫都有抑制作用。考虑到AM广泛存在于多种食品中,因此有必要采取相应的措施降低食品中AM的毒性或者含量。
2 食品中AM的形成途径
由表1可知,对同一原料采用不同的加工方式也会导致食品中的AM含量差异较大。因此,了解AM的形成机理对于减少食品中AM的产生具有重要的意义。食品中的AM有多种生成途径,其中主要的途径有3 个(图1)。
一般认为,Asn-还原糖途径(即美拉德反应)是最关键的一条AM形成途径[14-16]。具体反应过程如图1所示,以Asn和还原糖作为反应物,经过脱水和N-糖基化共轭产生席夫碱。一方面不稳定的席夫碱经过分子重排形成糖胺化合物,在脱羧之后发生β-消除反应从而生成AM[17];另一方面,席夫碱也可通过甜菜碱途径或者恶唑烷-5-酮途径脱羧形成甲亚胺鎓内盐,并发生水解反应生成3-氨基丙酰胺(3-aminopropionamide,3-APA),然后继续脱氨之后形成AM[18-19]。此外,除了含有α-羟基羰基的还原糖外,其他含有α-二羰基或α、β、γ、δ-二不饱和羰基的还原糖也可以经由这一途径与Asn反应生成AM[13]。

图1 AM的形成途径[13]Fig.1 Formation pathways of AM[13]
第二种途径是丙烯醛途径。首先,油脂被降解成甘油后脱水形成丙烯醛和丙烯酸,随后其与Asn降解释放出的氨气反应可直接生成AM。此外,当加热的温度较高时,该途径中产生的丙烯醛可能会直接与Asn反应,为美拉德反应提供羰基从而加速AM的产生[20]。
第三种途径是Asn分解途径。虽然该途径形成的AM较少,但分解过程中产生的反应性羰基可以加速美拉德反应的发生[21]。在此途径中,Asn经由热脱羧和脱氨两步反应直接分解成AM,但是在单独加热Asn时,该途径的主要产物可能由AM转变为马来酰亚胺[22]。
除了上述3 种关键途径外,AM的形成还与其他途径有关:1)在酶催化下Asn发生脱羧基和脱氨基反应合成AM[23-24];2)D-葡萄糖经过一系列烯醇化和异构化反应生成L-脱氧-2,4-二酮,然后进一步分解为甲醛和乙醛并最终生成丙烯醛[25];3)通过水解肽产生的丙氨酸可与Strecker降解反应释放的氨作用生成AM[18]。
在复杂的食品基质中,AM的形成方式多种多样,因此下面将进一步总结食品中影响AM形成的主要因素。
3 影响AM形成的因素
热加工食品中AM主要是通过美拉德反应产生的。因此,前体物水平、加工温度、时间以及美拉德反应产物等均可影响食品中AM的含量。
一般认为,Asn和还原糖是AM合成的重要前体物质[26]。Rommens等[27]研究表明经过基因改性的马铃薯在4 ℃下贮藏3 个月后,其葡萄糖含量与对照组相比降低了80%,并且热处理后的AM含量较对照组也减少了80%左右。此外,加热时间和温度同样影响AM的形成。Morales等[28]证实了加热过程中温度的升高和时间的延长会促进AM的形成。然而,上述规律并不适用于所有食品,Şenyuva 等[29]发现当烘焙时间较长时,咖啡豆中的部分物质在加热过程中与AM发生了反应从而使得其含量下降。除了AM之外,在美拉德反应过程中形成的其他产物如呋喃、5-羟甲基-2-呋喃(5-hydroxymethyl-2-furan,HMF)、糠醛等也会影响AM的合成。例如,HMF在加热条件下与Asn反应生成3-氨基丙酰胺,该物质可以加速AM的形成[30]。Lachenmeier等[31]发现烘焙后咖啡种子中的AM含量与呋喃、糠醇、羟甲基糠醛等其他美拉德反应产物含量呈正相关。虽然美拉德反应会产生AM等有害副产物,但其在提升加工食品色泽、香气等方面具有重要意义[32]。因此需要对美拉德反应进行有效控制,以期获得AM浓度更低、品质更好的食品。
4 食品中AM的抑制策略
食品从原材料到最终产品的每个阶段都可以采取不同的策略降低AM的最终水平。如图2所示,缓解薯片生产过程中的AM水平大致上可分为3 个阶段:农业生产阶段(第一阶段),通过选择植物品种、改良种植方法和改善贮藏环境来减少AM前体物质含量;预处理阶段(第二阶段),通过漂烫或者添加不同类型物质的溶液进行浸泡等处理手段来减少AM形成;热处理阶段(第三阶段),通过将真空油炸、射频加热等新技术与传统加工技术相结合的方式达到预期的产品质量。下面将分别阐述各阶段中可利用的AM抑制策略。
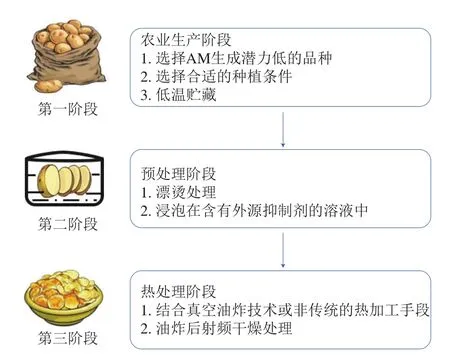
图2 热加工食品中各个阶段可采用的AM抑制策略Fig.2 Strategies available to inhibit AM formation at different production stages of thermally processed foods
4.1 农业生产阶段
在农业生产阶段,通过将还原糖或Asn控制在一定的水平就能获得低AM形成潜力的原料。Novy等[33]发现了一种名为‘Payette Russet’的低还原糖和Asn含量的马铃薯品种,经过热加工后该品种的AM含量较一般马铃薯降低了81%。除此之外,还可通过基因改造或常规育种等方式培育低还原糖和Asn含量的品种[20]。此外,土壤条件和贮藏环境也会影响还原糖和Asn水平,进而影响AM的合成[20]。de Wilde等[34]的研究表明,减少氮肥的施用会增加马铃薯块茎的糖浓度,而对Asn的影响却完全相反。原因在于施用氮肥的量减少会促进马铃薯还原糖的合成,从而导致Asn合成可利用的碳源不足并最终造成Asn含量减少[28]。Gerendas等[35]发现生长在高氮低钾土壤中的马铃薯AM及其前体的含量最高。此外,马铃薯生长的最适温度是15~20 ℃,当温度低于8 ℃或高于25 ℃时,可能会造成马铃薯中淀粉被分解从而引发还原糖的积累[36]。因此,一般选择还原糖含量较低的马铃薯品种贮藏在8 ℃左右的环境中[37]。
4.2 预处理阶段
除了选择AM形成潜力低的原料外,一些简单的预处理方法也可以抑制加工食品中AM的合成。其中,漂烫处理和利用含有外源添加剂的溶液浸泡处理是食品生产中最主要的选择。
4.2.1 漂烫处理
目前,有多种漂烫技术可供选择,如超声波、蒸汽和沸水漂烫处理等。Antunes-Rohling等[38]证实了与直接油炸相比,经过高强度超声波漂烫处理的油炸土豆中AM含量降低90%,与仅浸泡在水中的对照样品(42 ℃、30 min)相比,AM含量降低50%。原因在于漂烫不仅可以通过较高的温度使褐变反应所涉及的一系列酶失活,还可以使表面淀粉发生糊化,从而抑制热加工过程中马铃薯对油的吸收[39]。此外,漂烫会稀释原料表面AM前体的浓度,从而减少AM的形成[40]。
4.2.2 溶液浸泡处理
在热加工(烘烤或油炸)之前,通常会将食品材料浸泡在含有不同添加剂的溶液中以缓解AM的生成。一般常用的添加剂可分为三大类,即植物源添加剂、微生物源添加剂和金属离子添加剂。
4.2.2.1 植物源添加剂
植物源添加剂中以天然抗氧化剂及其衍生物在降低AM生成方面应用最为广泛。由于结构的多样性及其参与美拉德反应的复杂性使得天然抗氧化剂及其衍生物对AM形成可能产生截然不同的影响。植物多酚对AM的影响可分为两种——促进型和抑制型(图3),其涉及美拉德反应的不同阶段。Hamzalioğlu等[41]研究发现,在长时间加热过程中,姜黄素所含的羰基可以与Asn直接反应形成AM,如图3中第一类反应过程所示。除了姜黄素之外,其他包含活性羰基结构如α、β、γ、δ-二不饱和羰基的天然抗氧化剂也可以与Asn的氨基反应,从而促进AM的形成[41]。此外,某些植物多酚还可以促进美拉德反应中间体转化成AM。Cai Yun等[42]通过测定不同温度下的美拉德反应速率发现绿原酸可以降低3-APA向AM转化的活化能,从而加速AM的合成,具体如图3中第二类反应过程所示。然而,某些植物多酚也发挥着抑制AM形成的作用,如黄酮类抗氧化剂可以有效地捕获美拉德反应中间体中的活性羰基和二羰基,具体如图3中第三类反应过程所示。Cheng等[43]的研究表明柑橘中的黄酮类化合物柚皮苷能够与AM前体反应生成8-C-(E-丙酰胺)柚皮苷和6-C-(E-丙酰胺)柚皮苷,造成AM含量较对照组减少20%~50%。就富含脂肪的食品而言,长时间加热会使食品中的脂质发生氧化而产生大量的丙烯醛,该物质可通过一系列反应形成AM。一些植物多酚还可以作为断链抗氧化剂,通过与脂质自由基发生反应从而抑制脂质氧化[44],具体如图3中第四类反应过程所示。Toro-Uribe等[45]发现原花青素和可可多酚均可在pH 3.0或pH 5.0时降低过氧化氢、己醛等脂质氧化产物的含量,并且随着抗氧化剂聚合度的增加,其抑制效果更加明显。

图3 不同植物多酚对AM生成的影响[21]Fig.3 Effects of different plant polyphenols on AM formation[21]
除植物多酚外,部分维生素也有利于抑制美拉德反应产生AM。例如,抗坏血酸可以通过与其他添加剂(如过硫酸钾)的协同作用来减少AM的生成[46]。Kamkar等[47]通过气相色谱-质谱联用技术发现添加烟酸和吡哆胺后,薯片中的AM含量分别降低了58%和50%。在此基础上,Zeng Xiaohui等[48]发现烟酸可以直接捕获AM而使其含量下降(图4A)。
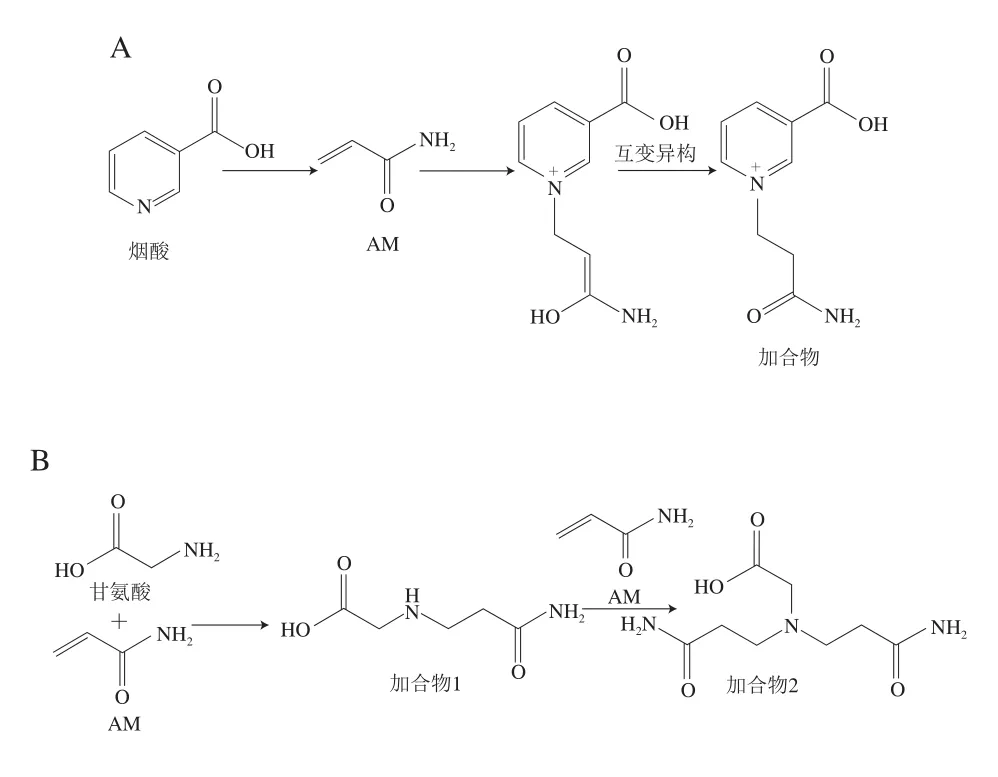
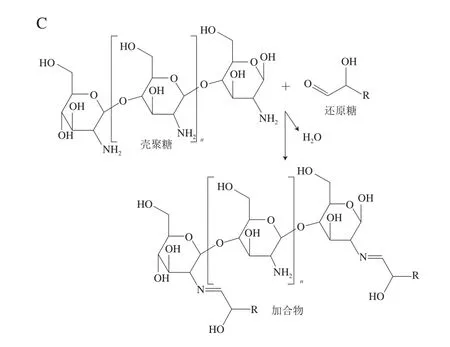
图4 部分添加剂对于AM形成的影响[48-50]Fig.4 Effects of some additives on AM formation[48-50]
4.2.2.2 微生物源添加剂
为了减少AM前体的形成,适当地在食品配方中添加天冬酰胺酶、葡萄糖淀粉酶等酶类也是一种有效手段。其中,天冬酰胺酶抑制AM形成的机制主要有两种:一种是通过水解反应将Asn转化为氨和天冬氨酸;另一种是通过乙酰化反应将Asn转化为N-乙酰-L-Asn[51]。在工业应用中,为了获得最佳的抑制效果,天冬酰胺酶通常与热烫工艺相结合。Zuo Shaohua等[52]报道了在80 ℃条件下经过耐热的L-天冬酰胺酶溶液热烫处理后,薯条中的AM含量减少了80.5%。除了天冬酰胺酶外,添加葡萄糖淀粉酶、利用乳酸菌和酵母菌进行发酵也被认为是降低AM含量的有效手段。总地来说,葡萄糖淀粉酶更适用于谷类产品,通过减少发酵过程中还原糖的含量来抑制AM的形成[53]。乳酸菌和酵母菌协同发酵的手段则适用于面包食品,研究表明以该种方式发酵的面包中AM含量(6.9~20 μg/kg)相较于仅用酵母发酵的面包(47.6 μg/kg)有明显的降低[54]。
4.2.2.3 金属离子添加剂
金属阳离子不仅可以增加食品中的无机盐含量,还能抑制AM的合成。其中,NaCl可以促进AM发生聚合反应从而加速其消除,而钾、钙、锌、铝、铁等阳离子则通过与Asn发生螯合反应从而抑制AM的合成,并且在这一过程中还会对其他美拉德反应副产物产生影响[37]。以Asn-葡萄糖模型为例,Wen Chao等[55]发现钾、钙、锌、铝、铁等阳离子添加剂在最适浓度下对AM的抑制率分别为47%、71%、55%、57%、61%,并且在165 ℃下加热35 min后发现另一种美拉德反应产物——羟甲基糠醛的含量增加。因此使用金属离子添加剂还需要根据不同的情况对具体浓度加以研究。
4.2.2.4 其他添加剂
酸性环境对热加工食品中AM的浓度也有一定的影响,因此可以通过添加不同的物质调节溶液的pH值,如磷酸和柠檬酸缓冲溶液。Jung等[56]通过气相色谱-质谱联用测定了煎炸马铃薯中的AM含量,发现经过质量分数2%柠檬酸溶液浸泡对马铃薯中AM形成的抑制率可达79.7%。一般认为AM形成的最适pH值为8左右,当环境pH值较低时,质子化反应使得自由基团的活性降低,从而缓解了AM合成反应的发生,例如Asn中的—NH2被转化成不参与反应的—NH3+[57]。同时,将食品材料浸泡在不含Asn的氨基酸溶液(丙氨酸、谷氨酰胺、甘氨酸、赖氨酸和半胱氨酸)中也可以达到同样的目的,机制在于:一是在合成其他物质的过程中与Asn竞争消耗外源氨基酸;二是氨基酸的亲核基团会与AM的碳碳双键发生反应[58-60]。例如,当加热至160 ℃时,甘氨酸可以与AM形成加合物从而降低其含量[49](图4B)。
水溶交涂层和亚硫酸盐的使用同样影响AM的合成。作为一种改善含水食品功能特性的食用涂料,一些水交体既可以通过包裹食品从而显著减弱油炸食品的吸油能力,还可以促进水交体与AM前体的相互作用来抑制AM的形成[61]。以壳聚糖水交体为例,它可以与还原糖发生反应从而阴止AM的积累[50](图4C)。此外,Alasmar等[62]证明不同的水交体包覆液对薯条中AM的抑制率分别为果交48%、壳聚糖38%、草豆粉31%。虽然亚硫酸盐也具有抑制AM形成的作用,但由于其与过敏、硫胺素吸收不足和碳水化合物代谢损伤等疾病密切相关,因此作为食品添加剂的使用仍然受到严格的管制[46]。
4.3 热处理阶段
除了必要的预处理之外,加工食品还必须经过一定程度的热处理,而AM的累积主要发生在此过程中。目前,已经开发了多种新型热处理技术,例如真空加热、射频加热和辐照消解技术,其与传统工艺相结合同样可以降低AM的水平。
真空加热是在低于常压的封闭系统中对食品进行加热的一种技术,在显著降低加热温度的同时也能在一定程度上延缓AM的产生[63]。Mariotti-Celis等[63]研究发现,与常压油炸相比,真空油炸薯片中呋喃、AM的含量分别下降了81%、58%。在饼干生产中,利用先真空加热后传统烘焙的方法得到的饼干中没有观察到AM的形成[20]。此外,射频加热一般被视作是一种后干燥的技术,它通过将电磁能直接传递给食品而产生热量[64]。这种后处理过程可以在降低水分的同时,避免由于余热引起的AM含量急剧增加,一般适用于大规模处理饼干和薯片等形状较薄的食品[65]。Palazoğlu等[66]研究发现,射频加热干燥后,曲奇中的AM含量较对照组降低了30%。由此可见,通过对传统的烘焙条件进行重新设计,并与新型加工工艺相结合,可以实现食品中AM的含量大幅降低。同样,AM在辐照的作用下会发生聚合反应,生成无毒的AM聚合物,从而降低食品中AM的含量。王倩倩[67]发现在3 kGy辐照消解的条件下,油炸薯条样品中AM消解率达到53.13%,并且证明了芝麻酚、苹果酸、碳酸钠等多种添加剂可以有效提升AM消解效果,其中芝麻酚溶液对AM抑制率可达60.49%。辐照消解处理方式的优点在于对食品的风味基本没有影响且成本较低,但考虑到目前相当一部分消费者对于“辐射”一词尚抱有抗拒心理,因此选择该技术还面临市场接受度的问题。
5 抑制策略的比较
降低AM形成的策略多种多样,但并不是所有的选择都能满足工业应用的期望。目前所报道的方法各有优缺点,表2列出了抑制AM形成的多种策略,其各有不同的特点。
将AM前体物质含量较低的品种在初期作为优先选择的品种,并贮存于适当的环境中可获得理想的原料。虽然前期的品种改良可以使炸薯条中的AM抑制率达到81%[33],但在农业种植阶段仍然存在由于季节和气候变化造成的原料差异[37]。在预处理过程中,用含有关键添加剂的溶液热烫或者浸泡是抑制AM形成的另一种有效方法,但同时也要尽量避免食品原材料如土豆出现完整性、苦味等感官品质缺陷[73]。对于植物源添加剂,一些天然提取物和维生素可能有利于食品颜色和亮度的提升,但同时也会影响气味、质地等感官指标[68-69]。相反,微生物源的天冬酰胺酶不会影响食品的感官品质,且容易处理,但存在产量低和成本高的缺点,并且这一方法对于天冬酰胺酶的用量有严格的要求,用量过多可能会导致Asn在水解过程中产生过量的氨并形成异味,从而影响食品品质[74]。乳酸菌也被广泛用于减少面包中AM的合成,但乳酸菌在长时间的发酵过程中可能会生成3-氯丙二醇副产物[75]。金属离子作为一种营养补充剂能够在很大程度上抑制AM的形成,尤其是NaCl和CaCl2,但过度的添加也可能导致其他有害物质的形成,如羟甲基糠醛和糠醛[76]。此外,Ca2+浓度过高时还会产生异味,过量添加氨基酸也会造成同样的结果。例如,由于含硫基团的存在,半胱氨酸和还原型谷胱甘肽会产生带有异味的物质[77]。另外,通过降低pH值来减少AM在食品中的含量也是一种可行的方法。但是,当柠檬酸等有机酸的浓度超过一定限度时,会造成食品发酸、质地较硬的品质问题[62]。在热处理阶段,通过结合真空油炸、射频干燥和辐照消解等新技术可以抑制食品中50%以上的AM产生(表2)。真空油炸对最终产品感官没有显著的影响,而射频干燥则会导致轻微的褐变[54]。
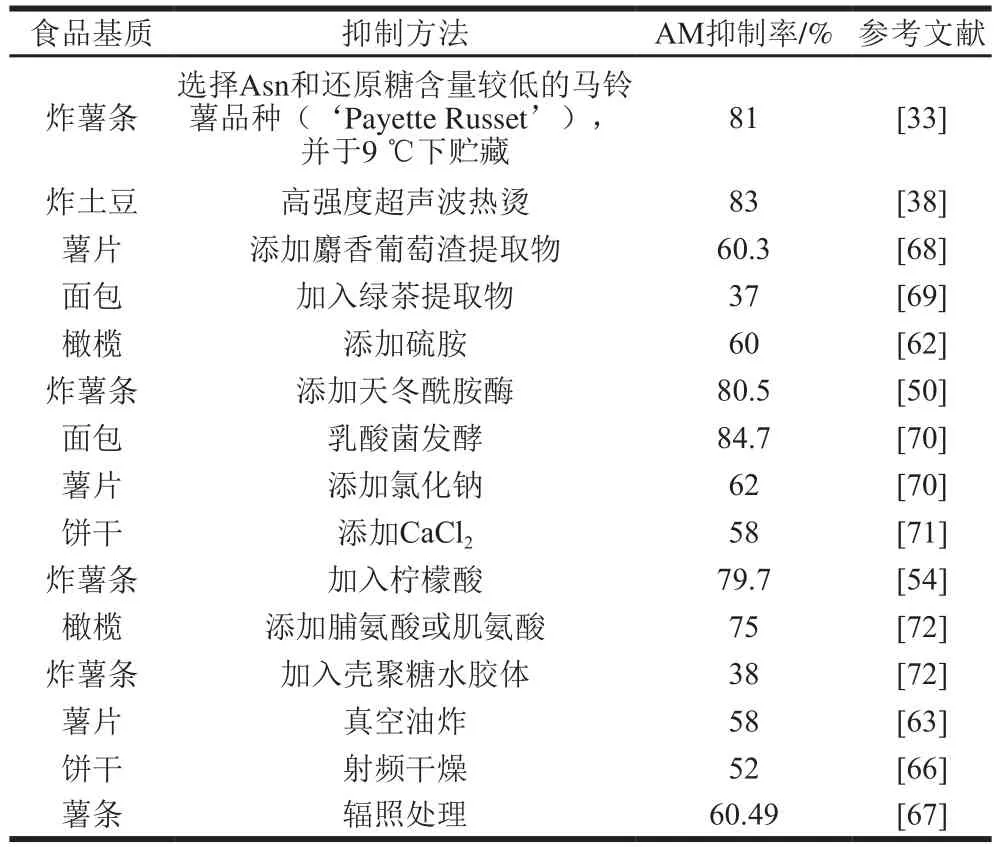
表2 不同可减少AM形成的抑制策略Table 2 Different inhibition strategies on reducing AM formation
如何平衡AM抑制策略及其副作用之间的关系是加工食品中亟待解决的问题。因此,为了在降低AM生成量的同时避免可能产生的有毒副产物和感官品质缺陷,需要对抑制策略进一步优化,并研究不同抑制策略的联合使用。
6 结 语
本文主要综述了在食品加工的3 个阶段中可用于减少AM生成的多种策略,具体可以概括为:1)在农业生产阶段选择AM生成潜力较低的原料,并对种植条件进行相应改进;2)在预处理阶段对原料进行烫漂或使用外源添加剂进行处理;3)在热处理阶段,通过结合新的加工工艺减少AM的合成。此外,对AM抑制策略中可能涉及的具体反应过程也进行了系统的归纳,但从目前的研究成果来看,由于食品基质复杂,食品中AM合成可能涉及多种途径,同时添加剂的抑制机理还未完全阐明;因此在许多文献中也只是简单加入相应的添加剂来研究其抑制AM合成的结果,而很少提及可能涉及的具体反应过程。此外,在高温加热至一定程度后,食品中可能会合成一些未知的化合物,特别是在加入添加剂后。因此,大多数抑制策略仍处于实验室研究阶段,尚不能适应于工业中的大规模应用。将来,随着新技术(比如表面增强拉曼光谱以及针尖增强拉曼光谱技术)的出现,可以使用简单的Asn-还原糖模型来模拟美拉德反应,并且可以在控制温度、湿度、pH值等基础上进一步探索合成反应和抑制策略的机理。当采用上述方法抑制AM形成时,利用超快拉曼光谱可以实现对整个反应过程的动力学监测。同时,时间分辨拉曼光谱可以用来识别反应过程中的各种中间产物(电子激发态),特别是在加入外源抑制剂前后。此外,电化学针尖增强拉曼光谱可以从分子尺度上研究AM抑制过程的具体反应机制。随着对食品中AM合成及抑制机理的进一步探索,将获得更有效的抑制方法,且不造成有毒副产物的产生和感官品质缺陷。
