肺移植术后排斥反应的影像学检查方法现状及展望
2021-09-24徐琳严浩吉王俊杰唐宏涛李偲涵陈婷婷张涵付思怡田东
徐琳 严浩吉 王俊杰 唐宏涛 李偲涵 陈婷婷 张涵 付思怡 田东
肺移植是临床治疗终末期肺病的有效方法,全球每年约有4 600例患者接受肺移植,术后1年和3年生存率分别为84.8%和70.3%[1]。我国肺移植手术量呈逐年上升趋势,截止至2019年12月31日,中国每年超过400例患者接受肺移植,术后1年和3年生存率分别为70.11%和61.16%[1-2]。随着肺移植手术及术后管理技术的发展与完善,受者术后早期预后明显改善,但其生活质量及远期生存仍无明显提升[3]。究其原因,肺移植术后排斥反应是影响受者预后的主要因素,主要包括急性排斥反应(acute rejection,AR)和以慢性移植肺功能障碍(chronic lung allograft dysfunction,CLAD)为表现的慢性排斥反应。约有28%的肺移植受者会在术后1年内发生AR,50%的受者在术后5年内发生CLAD,而10年后CLAD的发生率约为75%[4]。早期诊断排斥反应是改善肺移植受者远期生存的关键。目前,经支气管镜肺活组织检查(活检)是诊断肺移植术后排斥反应的金标准,但存在采样误差且为有创检查。因此,寻找准确且无创的排斥反应诊断方法至关重要。近年来,关于影像学检查用于肺移植术后排斥反应的报道逐渐增多。通过影像学检查早期监测排斥反应可提高肺移植受者生存质量并降低病死率。本文通过复习既往文献,对肺移植术后AR和CLAD的影像学检查方法进行综述,为各种影像学方式在检测肺移植术后排斥反应中的应用提供理论依据,进而提高肺移植受者预后及生活质量。
1 肺移植术后排斥反应的临床特征
肺移植术后排斥反应是肺移植受者对同种异体移植肺抗原发生的细胞和(或)体液免疫反应,可导致移植肺失功,主要包括AR和以CLAD为表现的慢性排斥反应[5]。AR多见于肺移植术后早期,表现为无症状或发热、呼吸困难、胸闷气急、胸痛等非特异性症状。AR的发生和严重程度是导致CLAD的主要危险因素,AR的发生预示着排斥反应增强以及远期预后恶化[6]。CLAD主要分为以慢性小气道阻塞性改变为特征的闭塞性细支气管炎综合征(bronchiolitis obliterans syndrome,BOS)和以限制性通气障碍、周边肺纤维化改变为特征的限制性移植肺综合征(restrictive allograft syndrome,RAS),其中BOS和RAS分别占70%~85%、25%~35%,诊断为BOS和RAS后,受者中位生存期分别为3~5年、6~18个月[7]。
2 肺移植术后排斥反应的影像学检查
目前已报道的影像学检查手段较多,包括胸部X线、CT、MRI、正电子发射计算机体层显像仪(positron emission tomography and computed tomography,PET/CT)、超声等,不同的检查方式在诊断肺移植术后排斥反应中各有利弊(表1)。
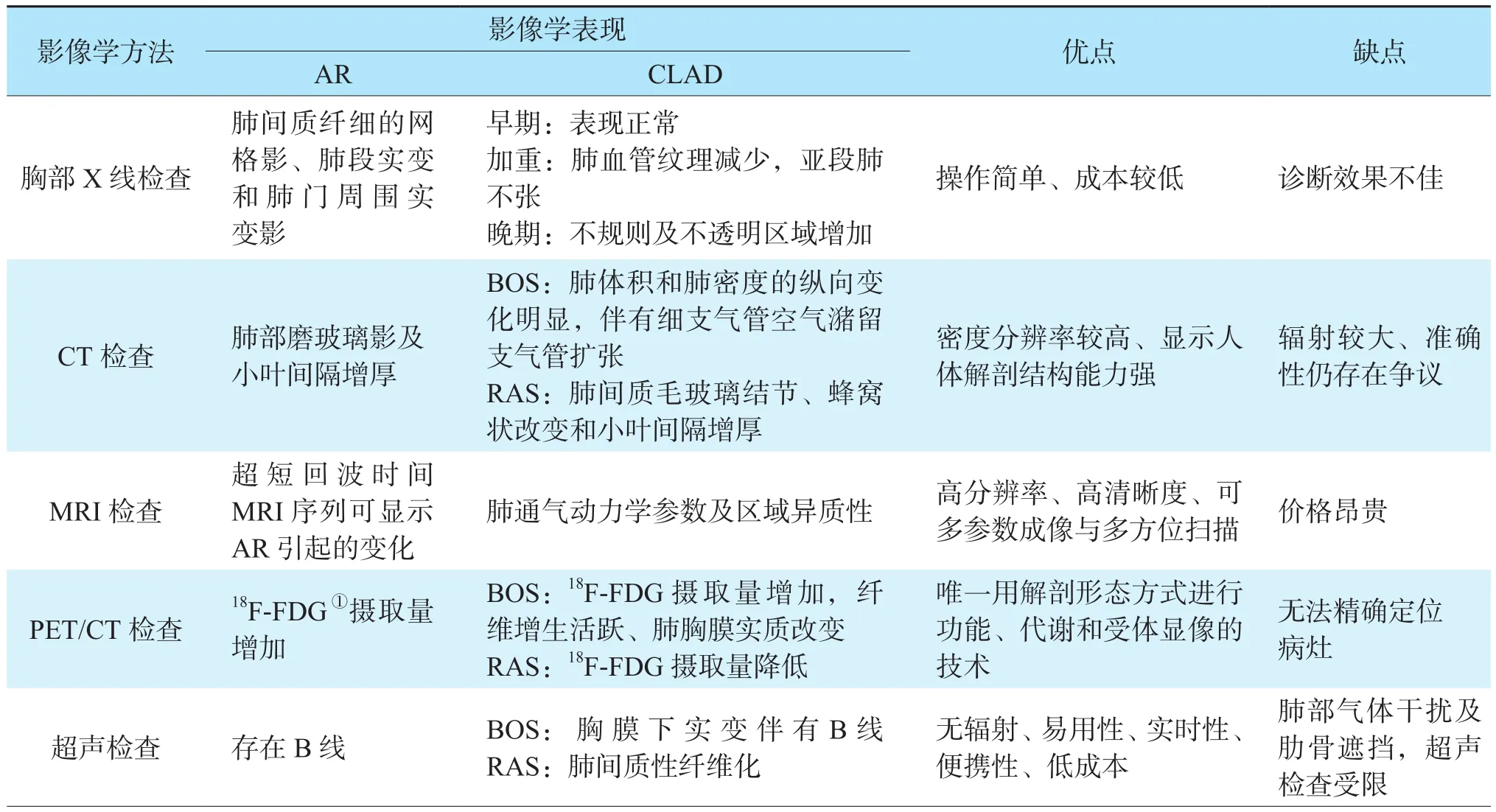
表1 肺移植术后排斥反应影像学检查方法Table 1 Imaging methods of rejection after lung transplantation
2.1 胸部X线检查
胸部X线检查是肺移植术后随访的重要检查手段之一,其操作简单、成本较低,对肺移植术后排斥反应的早期筛查具有一定意义。AR受者的X线胸片表现为肺间质纤细的网格影、肺段实变和肺门周围实变影。早期CLAD受者的X线胸片表现正常,随着CLAD加重,其X线胸片表现为肺血管纹理减少,亚段肺不张,晚期CLAD受者的X线胸片可观察到不规则及不透明区域增加。Bergin等[8]分析X线胸片结果发现,AR受者间隔线增厚和胸腔积液增加,不伴有心脏大小或血管蒂宽度增加及血管重分布,其灵敏度、特异度、准确率分别为0.68、0.90、83%。但该研究仅纳入83例受者,样本量较小,这一结果需要更多数据佐证。同时,肺移植术后排斥反应的X线胸片表现与其他疾病相似,且X线胸片密度分辨率较低,导致其对肺移植术后排斥反应的诊断效果不佳。Kundu等[9]对25例肺移植受者行经支气管镜活检,在确诊为AR的病例中仅有50%左右的受者X线胸片表现异常,表明胸部X线检查诊断AR的价值有限。
胸部X线检查诊断肺移植术后排斥反应效果不佳,不是一种理想的诊断方法,但其可用于肺移植术后早期排斥反应的辅助筛查。
2.2 CT检查
CT密度分辨率较高、显示人体解剖结构能力强,在肺移植术后排斥反应的临床诊断方面应用广泛,是肺移植术后随访的重要诊断工具。随着影像技术的发展,螺旋CT、多排CT、定量CT、高分辨率CT的出现进一步提高了CT的诊断价值。
AR在高分辨率CT图像中表现为肺部磨玻璃影及小叶间隔增厚,其灵敏度、特异度分别为0.500、0.975,准确率高达89.6%[10]。Gotway等[11]回顾性分析64例肺移植受者的低剂量薄层CT扫描结果发现,其诊断AR的灵敏度、特异度分别为0.35、0.73,准确率仅为53%。Di Piazza等[12]通过多因素回归分析78例肺移植受者的CT扫描与组织学诊断结果,发现CT检查结果与肺移植术后AR无相关性。CT检查诊断AR的准确性仍存在争议,未来需要更多数据以探讨其应用价值。
CT检查在早期预测CLAD方面具有积极意义。Horie等[13]对137例肺移植受者进行支气管镜、肺功能和定量胸部CT(quantitative chest CT,QCT)检查,结果显示CT扫描的定量密度指标(quantitative density metrics,QDM)预测CLAD的受试者工作特 征(receiver operating characteristic,ROC) 曲线下面积(area under the curve,AUC)为0.63,合并分析QDM、第1秒用力呼气容积(forced expiratory volume in 1 second,FEV1)及毛玻璃样不透明影后AUC增加到0.74,即在FEV1下降早期,QCT得到的QDM可预测肺移植术后CLAD。通过受者的CT检查结果可区分BOS和RAS。BOS受者的CT图像显示肺体积和肺密度的纵向变化明显,随着肺的膨胀,肺体积增大,肺密度减小,且伴有细支气管空气潴留支气管扩张,RAS受者的CT表现为肺间质毛玻璃结节、蜂窝状改变和小叶间隔增厚[14-15]。此外,CT还可引导支气管镜检查、经支气管活检和支气管肺泡灌洗,有助于及时诊断肺移植术后CLAD[16]。Philippot等[17]回顾性分析51例肺移植受者的资料发现,CT评分和CT体积测量能比肺功能检测更早识别或预测肺移植术后RAS的发生。CT在肺移植术后CLAD方面的应用价值高于AR,运用机器学习算法可进一步提高定量CT指标预测CLAD发病的能力,进而优化肺移植受者的疗效[18]。CT在预测肺移植术后CLAD方面具有一定价值,但其诊断AR的准确性仍存在争议。
2.3 MRI检查
MRI具有高分辨率、高清晰度以及多参数成像与多方位扫描等优势,但高昂的价格限制了其在临床上的应用。Guo等[19]通过MRI测量小鼠肺体积、肺实质信号和肺顺应性,证明纵向MRI可监测肺移植术后排斥反应。Kanno等[20]于2000年首次提出MRI结合超小超顺磁性氧化铁(ultra-small superparamagnetic iron oxide,USPIO)纳米颗粒可用于诊断肺移植术后AR,但USPIO纳米颗粒主要由巨噬细胞摄取,感染和排斥反应均涉及巨噬细胞,尚不清楚该技术能否区分感染和排斥反应,因此该研究存在一定局限性。由于正常肺组织与病变肺组织的弛豫特性不同,超短回波时间MRI序列可较清晰地显示肺移植术后AR引起的变化[21]。一项动物研究表明,超短回波时间MRI序列可用于区分肺移植术后原发性移植物功能障碍和AR[22]。
同时,MRI检查也可作为诊断肺移植术后CLAD的辅助手段,具有较高的准确性。Moher Alsady等[23]回顾性分析62例肺移植受者的MRI扫描结果,发现MRI扫描得到的肺通气动力学参数及区域异质性对诊断肺移植术后早期CLAD较敏感。此外,MRI还可利用肺内氧分压的不同诊断BOS及评估BOS分期[24]。Voskrebenzev等[25]评估62例肺移植受者的傅里叶分解 MRI(Fourier decomposition MRI,FD-MRI)参数发现,FD-MRI在诊断和评估双肺移植术后CLAD方面展示出较大潜力。FD-MRI可在正常呼吸期间快速采集图像以提取通气和灌注相关信息,便于计算区域通气变化。该研究表明FD-MRI对CLAD的预后价值较高,后续可采用大样本量前瞻性研究进一步验证该技术在CLAD方面的应用价值。因此,MRI可较胸部X线和CT更早、更精确地反映肺移植术后排斥反应[26]。
2.4 PET/CT检查
近年来,正电子发射体层仪(positron emission tomography,PET)作为目前唯一用解剖形态方式进行功能、代谢和体层显像的技术被广泛运用于临床诊疗过程,但其无法精确定位病灶。为提高病灶定位的准确性,以达到更好的鉴别和定位,同时缩短图像采集时间,将PET功能成像与CT解剖成像同机融合为PET/CT[27]。18F-氟代脱氧葡萄糖(18F- fluorodeoxyglucose,18F-FDG)是临床中常用的葡萄糖代谢显像剂,结合临床全面分析及PET/CT检查表现,有利于提高诊断的准确率,通常用于测定代谢活性、炎症部位和监测围手术期的治疗效果。目前,18F-FDG PET/CT检查在其他(心脏、肾、肝)移植领域可用于排斥反应的早期预测或随访,但在肺移植方面的研究尚少。PET/CT检查可通过18F-FDG局部标记快速鉴别感染及炎症[28]。此外,采用18F-FDG PET检查评估体内中性粒细胞活性可区分肺移植术后感染及排斥反应[29]。通过18F-FDG PET/CT检查无创鉴别排斥反应及感染,可减少肺移植受者支气管活检次数,改善其预后。
Chen等[30]通过18F-FDG PET检测移植物中T细胞的18F-FDG摄取量,发现18F-FDG摄取量的增加往往伴随AR的发生,即18F-FDG PET检查可能有助于诊断AR。Verleden等[31]回顾性分析肺移植受者的PET/CT检查结果,发现RAS受者的18F-FDG摄取量明显高于BOS受者。18F-FDG PET/CT检查可无创鉴别肺移植术后BOS和RAS,其灵敏度和特异度分别为0.76、0.87。PET检查在鉴别CLAD的两个亚型方面展示出了其优势和潜力,且对AR的检查也具有一定价值。
2.5 超声检查
肺部超声检查是一种重要的影像学诊断方法,其因易用性、实时性、便携性和低成本等优势广泛应用于临床。超声检查可用于监测心脏移植术后排斥反应的发生及评估排斥反应的分级(无、轻度、中度、重度),且可在肺移植术后早期检测出肺部病理性并发症,但其在肺移植术后排斥反应中的应用还不够成熟[32]。Bensted等[33]分析165例肺移植受者的超声检查结果得出,超声检查诊断肺移植术后气胸的灵敏度和特异度分别为0.75、0.93。此外,超声检查也可用于肺移植术后移植物功能的监测和评估[34]。Narula等[35]前瞻性研究119例肺移植受者,结果显示超声检查诊断AR的灵敏度为0.852,但特异度仅为0.250。超声检查诊断AR的灵敏度较高,但关于超声检查诊断肺移植术后CLAD的研究尚少。Davidsen等[36]结合高分辨CT、超声检查及肺部生理学特征诊断1例肺移植术后RAS,结果表明超声检查可作为诊断RAS的辅助手段。相对于CT和MRI等成像方式,超声检查无辐射,但由于肺部气体干扰及肋骨遮挡,超声检查可能受限。超声检查可用于无创诊断AR,且灵敏度和阴性预测值较高,是诊断肺移植术后AR的辅助手段之一,但超声检查早期诊断肺移植术后CLAD的应用价值还需更多研究验证。
3 小结与展望
目前,排斥反应仍是肺移植术后的主要并发症之一,尽早诊断出排斥反应有利于改善肺移植受者的预后。活检是肺移植术后排斥反应的金标准,但其难度及风险较大,且频繁活检不利于受者术后恢复。虽然影像学检查不能代替活检,但其可作为诊断肺移植术后排斥反应的辅助手段。综上所述,胸部X线、CT、MRI、PET/CT、超声等影像学检查可辅助其他检查无创监测肺移植术后排斥反应。应用计算机辅助的影像组学与机器学习方法将推动影像学检查诊断向更精准的方向发展,从而提高诊断肺移植术后排斥反应的准确性,进一步推动肺移植的发展。
