直肠癌并巨块型肝转移瘤同期行腹腔镜右半肝切除的治疗策略▲
2021-09-24陈永军靳小建蔡小勇
赵 波 陈永军 靳小建 蔡小勇
(广西医科大学第二附属医院微创外科中心,广西南宁市 530000)
结直肠癌是我国常见的消化道恶性肿瘤之一,而肝脏是结直肠癌最常见的远处转移器官。在临床诊疗过程中约20%的结直肠癌患者可能出现肝脏转移,即同时性肝转移[1]。对于可切除结直肠癌肝转移(colorectal liver metastasis,CRLM)患者,手术切除是能够根治CRLM 的治疗手段,治疗目标是达到肿瘤完全切除。相关研究显示,约25%~50%的CRLM患者经根治性手术切除后生存期可达5年以上[2]。近年来,随着治疗理念及外科技术的提高以及多学科诊疗模式的运用,越来越多的患者通过综合治疗方法达到了更好的生存获益甚至治愈的目标。肝转移灶同期根治性切除是获得长期生存机会的治疗方式,目前对于结直肠癌并巨块型肝转移瘤且同期行腹腔镜右半肝切除的案例国内尚无临床报道。现报告1例直肠癌并巨块型肝转移患者同期行右半肝切除的治疗策略。
1 临床资料
1.1 病例简介 男性患者,61岁。2019年3月23日因“发现肝右叶占位3 d”入院。患者诉3 d前因反复右上腹疼痛至当地医院行CT检查,显示肝右叶占位性病变,大小约10 cm×8 cm。无皮肤黄染、无恶心呕吐、无腹泻、无便秘、无黏液血便等不适,当地医院予止痛对症治疗(具体不详),余未予特殊处理。随后至我院就诊,门诊拟“肝占位性病变”收住入院。患者无乙肝病史。查体:体温36.5℃,脉搏90次/min,呼吸20次/min,血压100/65 mmHg。腹壁稍紧张,右上腹部轻压痛,无反跳痛。肝脾肋缘下未触及、胆囊肋缘下未触及,Murphy征阴性,双肾未触及,未触及腹部包块,未触及波动感,叩诊呈鼓音,肝浊音界大小正常,无肝区叩击痛,无移动性浊音,脊肋角无叩痛,肠鸣音4次/min,未闻及血管杂音。
1.2 影像学检查 CT检查显示肝右叶团块状低密度影,边界模糊,大小约9.1 cm×7.8 cm×10.2 cm。增强扫描动脉期较肝实质明显强化,门脉期、平衡期强化程度低于肝实质,部分坏死液化始终未见强化。考虑肝右叶巨块型肝癌并肝门淋巴结转移。见图1、图2。

图1 术前CT评估肝
1.3 其他检查 患者CEA 16.74 ng/mL,CA199 45.84 U/mL,AFP 6 ng/mL。同时完善电子肠镜检查,发现距肛缘8 cm见大小约3 cm×3 cm的溃疡型肿物,肠腔无狭窄,肠镜病理提示直肠中分化腺癌。临床诊断为直肠癌并肝转移。
1.4 术前诊疗及评估 根据病例情况对患者进行多学科会诊讨论,明确诊断。建议术前化疗或化疗联合靶向方案治疗:CapeOx(卡培他滨+奥沙利铂)或CapeOx联合贝伐珠单抗。因患者经济原因最终选用CapeOx方案行术前化疗4个疗程(奥沙利铂130 mg/m2、卡培他滨1 000 mg/m2,每3周重复1次),复查肿瘤未见明显缩小、疗效欠佳,患者拒绝进一步化疗,要求手术治疗。
用三维重建评估患者的肿瘤大小及残肝体积:肿瘤病灶670.97 cm3、体积比37.37%,右半肝切除方案剩余肝体积率约52.79%。见图3。
1.5 手术方法 充分评估后行腹腔镜直肠癌切除同期行解剖性右半肝切除、降结肠单腔造口术。采用全身麻醉方式,手术体位为平卧分腿位,术者站于患者两腿中间,腹腔镜下解剖性右半肝切除包括了多个环节:腹腔镜下分离右肝蒂予右半肝阻断,同时下腔静脉预置阻断带等措施防止术中出血,这些步骤均是腹腔镜右半肝切除的安全保障。首先用超声刀切断肝圆韧带,分离肝镰状韧带、右三角韧带、右冠状韧带,充分游离右半肝脏。然后显露第一肝门,锐性解剖右肝蒂,腔镜下血管阻断器阻断右半肝入肝血流,显示右半肝缺血线,以电凝于膈面标记肝切线,游离出下腔静脉,预留血管阻断带(见图4、图5)。沿肝切线用超声刀离断肝实质,直至第一肝门水平切断右肝蒂,至右肝静脉根部予游离后离断,将右半肝完整切除。随后再行直肠癌根治切除并左下腹降结肠单腔造口。术后注意观察肝功能及腹腔引流情况。

转移瘤(横断面)图2 术前CT评估肝

转移瘤(冠状面)图3 三维重建评估肿瘤大小及残肝体积
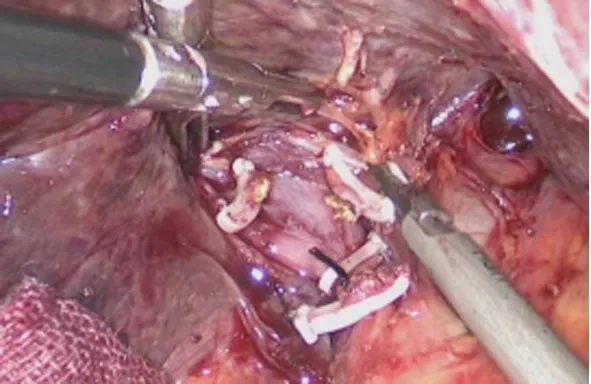
图4 术中行右半肝阻断
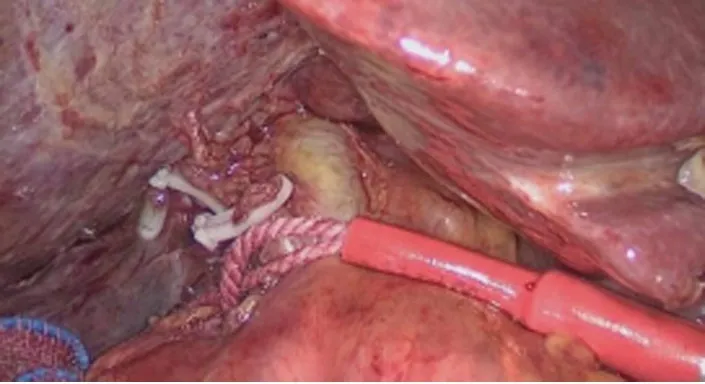
图5 术中预置下腔静脉阻断带
1.6 术后观察及处置 术后严密监测生命体征,密切观察腹腔引流液性状及引流量,尽早下床活动,促进早期康复,随访6个月。术后规律行FOLFOX(奥沙利铂85 mg/m2、亚叶酸钙400 mg/m2、氟尿嘧啶400 mg/m2,每2周重复1次)方案化疗。
2 结 果
术后第6天患者造口见排气排便,无腹胀腹痛不适,引出少量腹水,术后第10天予以出院。术后病理:直肠中分化腺癌(见图6),累及肠壁全层并肠周癌结节形成,13枚淋巴结中仅3枚出现转移,肝脏肿瘤符合肠癌肝转移。术后半年复查CT,肝肺未见明显复发转移病灶。
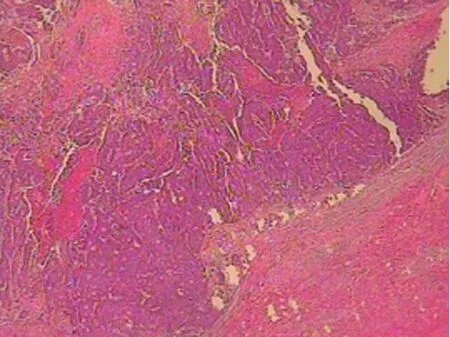
图6 术后病理显示为直肠中分化腺癌
3 讨 论
肝脏是结直肠癌最常见的远处转移器官,结直肠癌肝转移是导致患者死亡的主要原因之一。转移分为同时性肝转移与异时性肝转移两种形式,约25%的结直肠癌患者可同时性肝转移、20%~30%的患者出现异时性肝转移[3]。结直肠癌同时性肝转移瘤行同期切除的患者,其5年生存率达到31%~58%[4]。
3.1 结直肠癌肝转移的诊断 对于结直肠癌患者推荐完善胸部/全腹/盆腔 CT 增强扫描或肝脏增强MRI检查,其诊断并不困难,通常可以兼顾癌肿本身及转移瘤好发部位肝脏的检查。同时影像医生可以评价结肠癌的TNM分期及有无壁外脉管癌栓的情况。然而本例患者首发症状仅为右上腹胀痛不适,肿瘤标记物CEA、CA199升高但AFP正常,结合影像学资料易误诊为原发性肝肿瘤,故对类似病例建议完善电子肠镜排查结直肠肿瘤。
3.2 CRLM同期切除的手术适应证 对于可切除的转移性结直肠癌,同期外科手术切除是根治的有效方法[5]。CRLM的手术适应证:(1)结直肠癌原发灶能够根治性切除;(2)达到足够的剩余肝体积(剩余肝脏容积≥40%); (3)患者全身状况允许,没有肝外转移病灶[6]。评估肝功能及剩余肝体积在结直肠癌同期肝切除中尤为重要,研究表明当计划同期肝切除时最重要的因素之一就是术后需保留有功能的肝实质的量[7]。因此,对于结直肠癌肝转移患者建议多学科团队参与对患者诊治的全程讨论,根据患者临床表现、影像学、病理及分子生物学资料对患者一般状况及分期、发展演变、手术治疗及预后进行全面评估。多学科团队一般由结直肠外科、肝胆外科、肿瘤内科、放射治疗科、病理科及影像科组成,以充分评估患者的整体治疗策略。对于可切除的CRLM患者肝功能A级、肝转移灶小于5个,根据原发灶和转移灶的切除顺序不同,我们建议同期或者分期切除,目前手术方式的选择尚无定论,同期切除术理论上避免了二次手术等待时间、降低了肿瘤进展发生的概率等。CRLM患者的同期切除与分期切除相比,术后并发症发生率和远期的生存时间无明显差异,但行同期切除患者的术后住院时间明显缩短[8]。然而,研究显示相比于同期原发灶联合大范围肝切除(≥3个肝段),分期肝切除组的术后并发症高于同期切除组,术后住院时间亦明显增加[9]。对于肝转移性结直肠癌,手术治疗选择以原发灶优先还是转移灶优先的先决条件是哪个因素更能影响患者生存及生活质量,如转移灶是主要因素可先切除转移病灶再切除原发病灶。因此,应选择合适的CRLM患者进行同期切除和制订最佳的治疗方案。关于CRLM患者的预后评估应根据原发肿瘤的淋巴结情况、无病生存时间、肝转移瘤数目、术前癌胚抗原水平及转移瘤直径等相关指标参数进行复发风险评分,评分越高预后越差[10]。
3.3 CRLM同期切除的手术方式 随着腹腔镜技术的发展,对CRLM行腹腔镜同期切除的应用日益增多[11]。对可切除的CRLM尤其是巨块型右肝转移瘤患者(≥3 个肝段),应先行三维重建评估残余肝体积后再行腹腔镜右半肝切除。由于肝脏及肠道同期手术,有学者认为手术创伤大、腹腔感染概率增高,半肝切除手术创伤大、肝功能受损也会增加吻合口相关并发症的发生。对于直肠癌同期行半肝切除,建议采用Hartmann术式,不建议一期吻合,以免吻合口漏并导致严重腹腔感染的发生。
3.4 CRLM同期切除的手术要点或注意事项 在腹腔镜直肠癌切除同期行解剖性右半肝切除手术中,腹腔镜解剖性右半肝切除具有手术难度大、风险较高的特点。在充分的术前评估与准备后,右半肝游离、肝门部解剖及肝实质离断均是手术的难点。我们的经验是腹腔镜下分离右肝蒂并结扎,予右半肝阻断同时予下腔静脉预置阻断带,这些措施可防止或减少术中出血,也是腹腔镜右半肝切除的安全保障。然而腹腔镜下对第一肝门的精细解剖并选择性对右侧入肝血流阻断最为关键,接下来的断肝过程中精细解剖第二肝门应显露腔静脉窝。肝右静脉血管壁薄,分离过程中容易造成血管损伤,有时易导致难以处理的大出血,故处理需十分小心谨慎。因此在半肝切除过程中下腔静脉预置阻断带及肝实质离断过程中降低中心静脉压,也是减少术中出血的重要举措。
3.5 CRLM同期切除并发症的防治 随着手术技术的提高及医疗设备的发展,同期手术的并发症及死亡率能得到较好的控制。肝肠同期切除的手术中,切除肝体积较多者的术后并发症发生率为33%~55%[12],术后总体死亡率低于5%。围术期内应积极预防肝功能衰竭、出血、胆漏和感染的发生。
对于结直肠癌可切除肝转移瘤患者,术前应充分评估肿瘤浸润的范围及解剖学上的可行性手术、剩余肝体积能否维持正常的功能;对于不可切除的肝转移瘤可选择肝动脉栓塞、微波消融技术或者转化治疗后分期行转移瘤切除。目前认为,转移性结直肠癌的一线姑息治疗中,强烈治疗可以带来更多的生存获益,不但体现在抗血管内皮生长因子靶向治疗的策略中,也体现在抗表皮生长因子受体的靶向治疗中。因此,Ⅳ期结直肠癌诊治方案和策略的优化、精准化将给这部分患者带来更大的生存获益。总而言之,可切除CRLM的治疗策略是以手术切除病灶为基础,术前进行多学科讨论,充分评估患者的状况和手术风险,术中谨慎操作、精细解剖,术后辅助其他可靠有效的综合治疗措施。
