儿童肝脏未分化胚胎性肉瘤的MSCT 表现
2021-09-18王攀鸽苏晓然陈晓云陈志平
王攀鸽,郑 彬,苏晓然,陈晓云,陈志平
(郑州大学附属儿童医院/河南省儿童医院放射科,河南 郑州 450000)
肝脏未分化胚胎性肉瘤(undifferentiated embryonal sarcoma,UES)是一种罕见的起源于肝原始间叶组织的恶性肿瘤,多见于儿童,居儿童肝脏原发恶性肿瘤第3 位,恶性程度高,预后差[1]。因其临床表现、实验室检查无明显特异性,临床医师对该病常认识不足,极易误诊,影响预后。现对我院2015—2020 年收治的8例肝脏UES 患儿的临床及影像资料进行回顾性分析,以提高临床医师对该病的诊断正确率。
1 资料与方法
1.1 一般资料 8例中,男5例,女3例;年龄10 个月至8岁,中位年龄5岁11 个月;临床多以发热、腹痛、腹胀及发现腹部包块就诊。实验室检查乳酸脱氨酶(LDH)均不同程度升高(范围284.0~937.4 U/L),甲胎蛋白(AFP)正常或轻度升高(14.59 μg/mL)、癌胚抗原(CEA)未见异常。8例均行腹部超声检查,表现为肝脏囊实性肿物,其中5例以高回声实性成分为主。
1.2 仪器与方法 采用Philips 256 排螺旋CT 扫描仪,患儿均行全腹平扫加多期增强扫描。范围从膈顶至盆腔入口水平。扫描参数:100~120 kV,100~200 mAs,层厚5 mm,迭代重建层厚1 mm。对比剂采用非离子型对比剂碘海醇(碘含量300 mg/mL),剂量1.5~2.0 mL/kg 体质量(最大剂量60~80 mL),采用高压注射器经肘静脉注射,流率1.5~2.5 mL/s,对比剂注射后18~25、55~60 s 及3 min 行肝动脉期、门脉期、延迟期扫描。
1.3 图像分析 由2 名高年资诊断医师采用盲法分析肝脏UES 影像表现,包括病变部位、累及肝段、密度、形态、边界、大小、CT 强化特征及转移情况等。
1.4 手术及病理 4例化疗后手术切除,4例行半肝切除手术。切除标本先行大体观察,后石蜡包埋切片行常规HE 染色和免疫组化分析。
2 结果
2.1 CT 表现 8例均表现为肝内单发囊实性肿物,其中实性成分为主2例(图1a),囊性成分为主6例(图2);肿块位于肝右叶4例,肝左叶1例,左右叶均累及3例;病灶大小7.9 cm×7.8 cm×8.5 cm~15.3 cm×10.8 cm×20.3 cm,最大径8.9~21.4 cm;病灶呈分叶状3例、椭圆形或类圆形5例;病灶内均可见厚薄不均软组织分隔。2例实性为主病灶边缘无假包膜,边界不清,病灶中心见多发小囊变坏死;余6例囊性为主病灶边缘可见完整假包膜,边界清楚,内见大片出血、坏死,其中3例出血形成阶梯状液-液平面(图2),1例病灶内可见点状钙化。增强扫描5例肿瘤血管丰富(图3a),内分隔及实性成分呈中度延迟渐进性强化(图3b,3c);余3例囊性为主病灶肿瘤血管少、纤细,内分隔及少量实性成分呈轻度强化。8例均未见癌栓及转移灶。
2.2 病理结果 大体肿瘤切面呈灰黄灰白或灰红,质韧或质软,大部分见完整假包膜。4例化疗后呈广泛坏死;2例呈实性,外观黏稠样,与正常肝组织分界不清;2例囊性为主,切面见大量暗红黏稠液体及败絮状物。镜下见未分化的不规则梭形或星形肿瘤细胞散布于黏液基质中(图1b),可见形态怪异的多形性或瘤巨细胞,异型性明显,间质可见黏液样变性,部分见嗜酸性小体,PAS 染色阳性。免疫组化示波形蛋白(Vimentin)(+)8例(8/8)(图1c)、平滑肌肌动蛋白(SMA)(+)5例(5/7)、α1-抗胰蛋白酶(α1-AT)(+)3例(3/3)、结蛋白(Desmin)(+)3例(3/6),AFP(-)7例(7/8)。
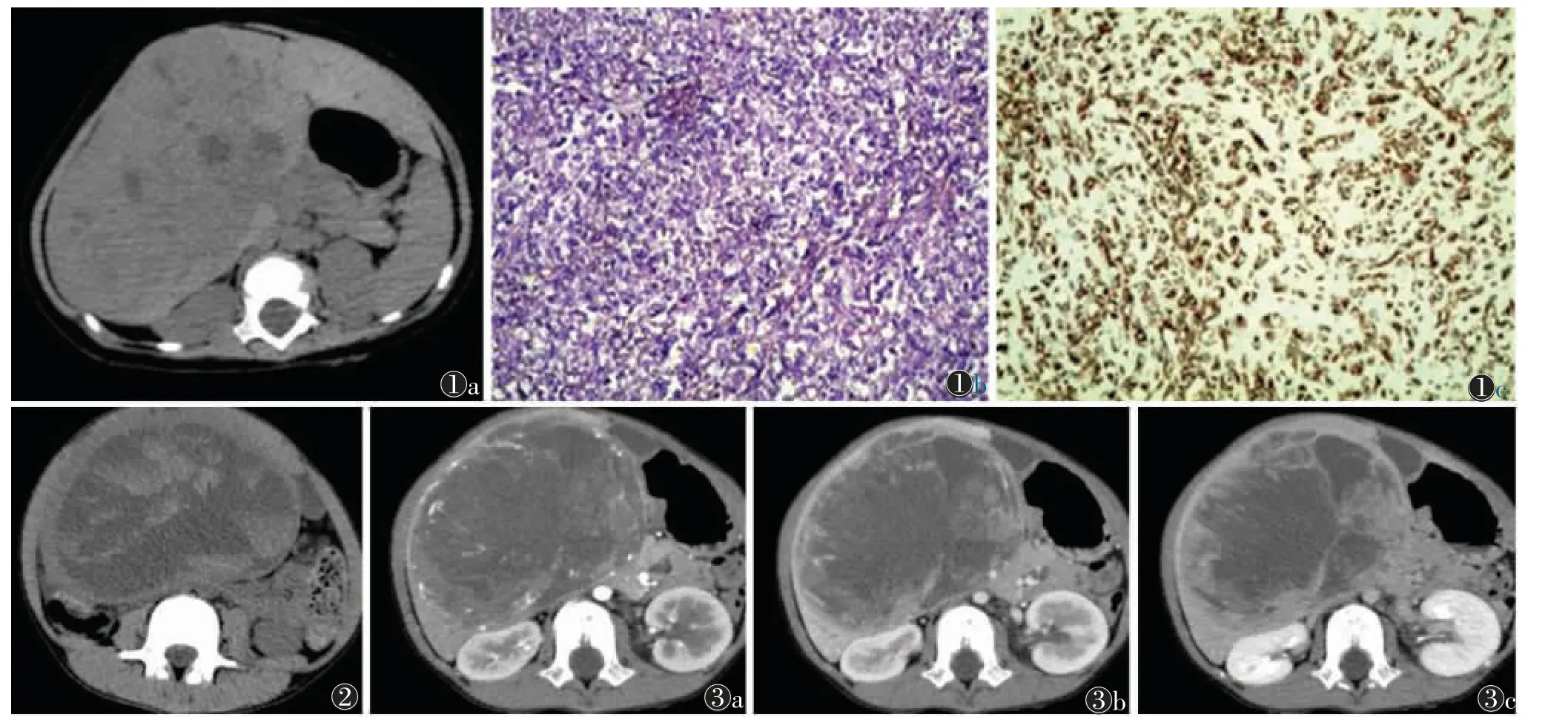
图1 男,10 个月,肝脏未分化胚胎性肉瘤(UES)图1a CT 平扫示累及左右叶、边界不清、分叶状囊实性占位性病变,实性成分为主,中心见多发小片状囊变、坏死 图1b 镜下肿瘤细胞呈圆形、不规则形、多边形,胞浆内有空泡,间质内见轻度黏液样变性(HE 染色,低倍放大)图1c免疫组化Vimentin 染色(阳性,低倍放大)图2 女,5岁10 个月,肝脏UES,CT 平扫示累及左右叶、边界清晰、类圆形囊实性占位性病变,囊性分成为主,内见大范围坏死、出血,形成阶梯状液-液平面图3 男,6岁,右叶肝脏UES 图3a CT 增强扫描动脉期见丰富肿瘤血管,周边为主 图3b,3c 门脉期及延迟期示肿瘤内多发分隔、边缘实性成分渐进性强化
3 讨论
3.1 临床及病理特点 肝脏UES多见于6~10岁儿童,偶可见于成人及新生儿,男女比例相当[2],本组1例为10 个月婴儿,余均为学龄前及学龄期儿童。临床主要表现为发热、右上腹不适、腹痛腹胀、腹部包块,血清AFP多正常[3]、LDH 升高。本组1例血清AFP 轻度升高,结合术后病理考虑为含肝脏间叶性错构瘤(hepatic mesenchymal hamartoma,HMH)成分所致;血清LDH 均不同程度升高,提示肝功能损害。肿瘤早期仅限于肝内生长,呈结节状及巨块状,晚期可穿破假包膜,向周围浸润、转移,治疗以外科手术为主,联合介入、化疗可提高患者生存率[4]。本组4例化疗后手术切除,切除标本见肿瘤组织大片坏死;4例行半肝切除术,其中2例肿块边缘与正常肝组织分界欠清,1例与周围肠管、肠系膜轻度粘连,均未见转移、癌栓形成,随访预后均较好。
肝脏UES 镜下见未分化的不规则梭形或星形肿瘤细胞散布于黏液基质中,异型性明显,可见形态怪异的多形性或瘤巨细胞,部分见特征性嗜酸性小体,PAS 染色阳性。多数免疫组化Vimentin、α1-AT 见阳性表达[2],部分可有Desmin、SMA 表达,而AFP 常为阴性。本组8例Vimentin 均为阳性,所检测3例α1-AT 均阳性表达,Desmin、SMA 部分表达,而AFP几乎阴性,支持肿瘤为间质起源。因部分肝脏UES中可观察到类似HMH 区域,且HMH 发病年龄早于肝脏UES,因此有学者认为肝脏UES 可能是HMH恶变的结果[5]。本组1例10 月龄肝脏UES 患儿,镜下见局部分化较好的区域其组织学结构类似HMH,提示此区域与肝脏UES 之间存在一定的过渡。
3.2 CT 表现与病理基础 结合相关文献分析,笔者认为儿童肝脏UES 的CT 表现有以下特点:①巨大单发囊实性肿块,囊性为主多见,可见大范围囊变坏死、厚薄不均软组织分隔,实性成分呈结节状、乳头状分布于病灶边缘[6-7]。本组6例以囊性为主,与文献相符,其中3例CT 示囊性而超声示实性成分为主,表现不一致,病理上超声示实性区为黏液样基质及疏松分布于其中的肿瘤细胞,由于黏液样区域不断吸收水分,故在CT 上表现为液性水样密度,两者影像不一致性被认为是肝脏UES 的重要诊断特征[8-9]。②实性为主肿块,少见,通常体积相对较小,中心见多发小囊变、坏死。③瘤内出血,较常见,其密度可因出血时间、多少而表现混杂。本组6例肿瘤内可见出血,其中3例出血较多,形成阶梯状液-液平面,具有一定诊断特征。④瘤内钙化,极少见,多为病灶边缘针尖样钙化。本组仅1例出现点状钙化灶,此特点可与其他富钙化肿瘤相鉴别。⑤血供,肿瘤血管多为少血管或无血管型,肿块以囊性为主,而多血管型少见,肿块以实性为主。有学者认为肝脏UES 病灶早期血供丰富,以实性为主,肿瘤生长迅速致其血供相对不足,实性成分坏死且不断扩大而渐呈囊实性[10],因此肝脏UES在MSCT 上表现为实性为主还是囊性为主可能与本病的发展阶段有关,与肿块的血供及生长速度密不可分。⑥强化特点,肿块分隔及边缘实性成分轻中度、持续渐进强化,常见较完整的假包膜[11-12]。本组6例可见假包膜,病理为肿瘤与正常肝组织间的纤维分隔,含受压肝索、胆管及小血管;8例均见实性成分渐进性强化,其中3例分隔少,实性成分少、模糊,呈轻度强化,5例肿瘤内多发厚薄不均的分隔及实性成分呈渐进性强化,囊性区域不强化,与术后病灶呈囊实性肿块相一致。
3.3 鉴别诊断 肝脏UES 需与以下疾病相鉴别:①肝母细胞瘤,是儿童最常见的肝脏恶性肿瘤,多发生于3岁以下婴幼儿,血清AFP 升高;有学者总结在CT 上有“十多一低”的典型影像表现[13],即右叶多、单发多、圆形多、实性多、钙化多、假包膜多、外生型多、跨叶生长多、新鲜出血灶多、中央坏死囊变多,以及肝硬化少见。肝脏UES多以囊性为主,易误诊为囊性肝母细胞瘤,但肝母细胞瘤多钙化、增强扫描动脉期多明显强化,门脉期及延迟期强化减弱的特点,可有助于鉴别,另外患儿年龄、病史及AFP值对两者鉴别极有帮助。②HMH,是仅次于血管瘤的儿童第二常见肝脏良性肿瘤,多发生于2岁以下婴幼儿,CT常为囊实性肿块,表现为大囊套小囊,囊壁光整,分隔较薄,间隔及实性部分强化[14];③肝寄生虫病,多见于牧区,为单囊或多囊,囊内囊及囊壁环形、弧形钙化、内外囊分离形成“套囊征”或内囊塌陷卷曲形成“飘带征”为其特征性CT 表现[15]。此外,应注意与肝细胞癌、肝囊肿、肝脓肿、肝转移瘤、肝囊腺瘤或癌等鉴别。
