CexZr1-xO2 储氧材料制备方法研究进展
2021-09-16孟玲
孟玲
(矿冶科技集团有限公司,北京 100160)
0 引言
汽车尾气主要包括未完全燃烧的碳氢化合物(HC)、不完全燃烧生成的CO、反应生成的NOx以及烟尘颗粒、硫化物和甲醛等,汽车尾气控制和治理长期以来都是社会关注的热点和难点问题,不断严格的排放标准对汽车尾气催化器提出了更高的要求。三效催化剂(Three Way Catalysts,TWCs)是尾气催化器的核心部件,能使尾气中的CO、HC和NOx转化为N2、CO2和H2O等无害物质,转化率达到90%以上,是目前最有效的尾气治理措施。汽车尾气催化剂既要实现NOx的还原反应,同时也要实现CO 和HC 的氧化反应,要使这三种污染物的转化率达到最佳,则要求反应体系中的氧含量处于化学反应计量系数。典型三效催化转化效率(HC、CO 和NOx)随空燃比(空燃比:A/F=发动机消耗的空气质量/发动机消耗的燃油质量)变化如图1 所示,当空燃比为14.63 时,恰好能完全燃烧;如果A/F<14.63,燃油发生不完全燃烧,为富燃状况;如果A/F>14.63,空气过量,为贫燃状况[1]。
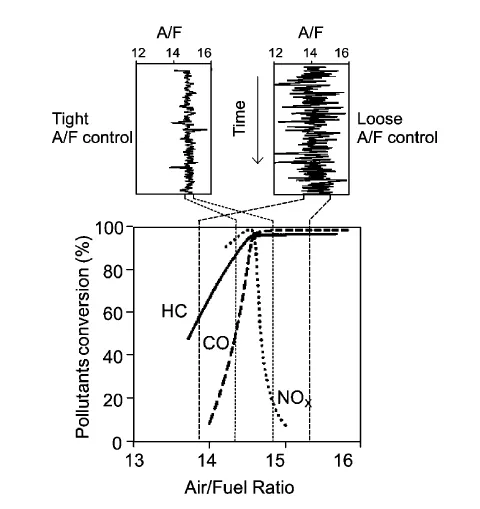
图1 典型三效催化转化效率(HC、CO 和NOx)随空燃比变化曲线[1]Fig.1 The curve of TWCs conversion efficiency(HC, CO and NOx) with air-fuel ratio
三效催化剂的转化效率受空燃比影响较大,控制反应体系空燃比一般有以下两种方法:(1)“工程控制”,即使用氧传感器提供空燃比反馈信号的闭环控制系统,提高空燃比的控制精度;(2)“化学控制”,即通过在催化剂中加入储氧材料来控制空燃比的波动。尽管采用“工程控制”的方法可以将发动机空燃比的变化控制在非常狭窄的范围,但是由于汽车的加、减速以及路况的复杂多变,仍然使得发动机的空燃比在14.63 左右以一定的频率和幅度振荡,从而使实际的尾气组成往往超出催化剂窗口的浓度范围,因此,寻找满足要求的储氧材料一直是三效催化剂的研究重点。另外,随着越来越严格的汽车尾气排放法规的出现,要求使用密偶催化剂以满足尾气排放标准,因此,汽车尾气催化剂除了具有低温下的高活性和选择性以及起燃速度快(<10-20s)之外,还必须具有高的热稳定性和氧存储释放能力。
1 储放氧原理及CeO2-ZrO2 材料
1.1 储放氧原理
储氧材料能够调节汽车尾气中的氧含量,极大提高三效催化剂的催化效果。在贫氧条件下,CeO2通过反应提供氧来去除CO 和HC,反应方程式如(2-1)、(2-2)、(2-3)所示;在富氧条件下,可以吸附和存储O2、NO 和H2O 的氧,从而提高尾气波动下三效催化剂的使用效率的稳定性,反应方程式如(2-4)、(2-5)、(2-6)所示。
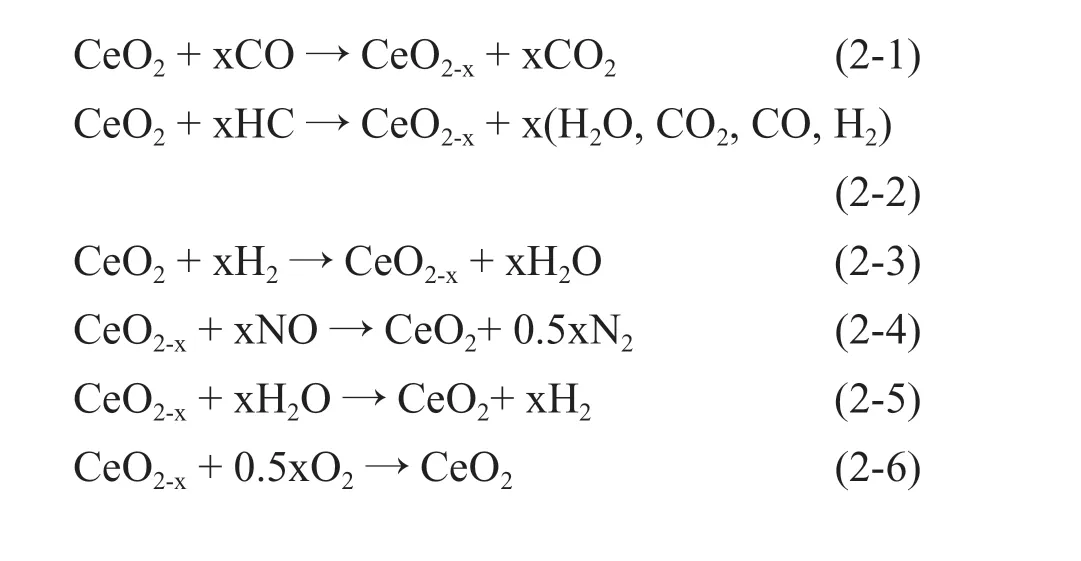


1.2 CeO2-ZrO2 材料
与CeO2相比,铈锆固溶体具有如下优点:(1)ZrO2的加入使铈锆晶胞扭曲和收缩,增加了铈锆固溶体内的结构缺陷,提高了氧空穴浓度,促进了氧的迁移和扩散;(2) CeO2的储氧以表面氧为主,受比表面积的影响较大,高温下CeO2的烧结会导致储氧能力大幅度下降,而铈锆固溶体的储氧以体相氧为主,对比表面的依赖程度减小,高温烧结对铈锆固溶体储氧能力的影响也减小;(3)Ce4+和Ce3+的离子半径分别为0.097 nm 和0.114 nm,在Ce4+向Ce3+的转化过程中,由于CeO2体积增大产生的膨胀会抑制此转变过程,Zr4+(0.084 nm)可以减弱体积膨胀的影响,促进氧化还原的进行[8-9]。
越来越严格的汽车尾气排放法规要求使用密偶催化剂,致使催化剂的使用温度高达1100℃,使用寿命也是一个很重要的问题,这就要求CeO2-ZrO2储氧材料具有更高的热稳定性。提高CeO2-ZrO2储氧材料热稳定性的方法有以下两种:(1)通过采用合适的制备方法来设计改善CeO2-ZrO2微结构;(2)通过掺杂其它的离子来进一步提高CeO2-ZrO2的热稳定性能。
2 CeO2-ZrO2 复合氧化物制备方法
制备方法对铈锆固溶体的纯度、晶相、晶粒大小、颗粒形貌、比表面积有显著的影响,从而影响CeO2-ZrO2复合氧化物的氧化还原性能、储放氧性能和热稳定性。目前,CeO2-ZrO2复合氧化物的制备方法主要有共沉淀法、溶胶-凝胶法、微乳法、水热合成法、固体合成法等。
2.1 共沉淀法
共沉淀法是用可溶性的铈锆混合盐与沉淀剂混合沉淀将其转化为难溶的铈锆化合物,经抽滤、洗涤、干燥、焙烧等工序得到铈锆复合氧化物。常用沉淀剂包括氨水、碳酸氢铵、碳铵-氨水混合沉淀剂、氢氧化钠、草酸等。
Sellick 等[10]分别以碳酸钠和尿素为沉淀剂,共沉淀合成了不同铈锆比的复合氧化物,结果表明,采用碳酸钠为沉淀剂制备的CeO2具有较低的活性,这是由于高浓度碳酸盐覆盖在产物表面,抑制了反应的进行;而采用尿素为沉淀剂得到的CeO2,其活性远高于以碳酸钠为沉淀剂得到的CeO2。随着Zr 含量增加到1%,活性大大增强,当超过1%时,催化活性有所降低。
Lan 等[11]采用常规共沉淀方法制备了Ce0.2Zr0.8O2、Ce0.5Zr0.5O2和Ce0.8Zr0.2O2, 分 别 标记为CZ1、CZ2 和CZ3;采用改性共沉淀法合成Ce0.5Zr0.5O2(CZ4), 即 分 别 溶 解Ce(NO3)3和ZrO(NO3)2得到一定浓度的溶液,再通过一定配比确保Ce:Zr=1,最后用氨水沉淀。所有样品在1000℃下热处理5 h后测试其催化性能。结果表明,Ce0.5Zr0.5O2具有最好的氧化还原性能和热稳定性,并且改性的铈锆复合物催化性能明显优于传统法得到的样品。岳等[12]以碳酸氢镁和碳铵-氨水混合液为沉淀剂,通过控制工艺条件,得到了铈锆复合氧化物。研究表明,部分Mg2+进入铈锆复合氧化物的晶格内部,提高了产物体相氧的活动性,改善了其低温还原性能,800℃下的储氧量可达到567 μmol/g。
Li 等[13]分别研究了共沉淀和络合-共沉淀法制备铈锆储氧材料,络合共沉淀法先加柠檬酸与Ce/Zr 络合,然后用氨水调节pH 值到3 左右,再加入PEG2000 作为表面活性剂,搅拌、干燥、焙烧得到CexZr1-xO2。在微观形貌上,共沉淀法得到的样品呈现出随机颗粒的聚集,在1100℃条件下老化6h,晶粒烧结长大成块,样品孔体积仅为0.216 cm3/g,比表面积61.4 m2/g;络合-共沉淀法得到的样品具有空洞和颗粒零星分布,老化处理后,空洞变大且趋于均匀,样品晶粒小且均一,样品-孔体积达到0.79 cm3/g,比表面积136 m2/g。共沉淀和络合-共沉淀法制备铈锆储氧材料储氧性能也有很大差别,未经老化的样品储氧量分别为874 μmol/g 和1205 μmol/g,经1100℃老化6 h 后,储氧量分别达到320 μmol/g 和615 μmol/g。研究结果表明,络合-共沉淀法制备铈锆储氧材料具有较好的抗高温烧结性能和储氧性能。
Cui 等[14]通过反滴定法研究了不同温度下(10℃、20℃、30℃、50℃、70℃、80℃)析出对CexZr1-xO2的性能影响。研究结果表明,相对高的析出温度(70℃)有利于在析出开始阶段形成大的晶粒,大的晶粒能提高孔的半径和扩大孔的尺寸分布,这有利于老化处理后保持高的比表面积,同时也能有效维持焙烧后氧化物的尺寸。而且,在70℃时锆易进入二氧化铈晶胞中,形成的锆复合氧化物更加均匀,同时提高了热稳定性。
2.2 溶胶-凝胶法
溶胶-凝胶法是目前低温制备氧化物超细粉末最常用的方法之一。溶胶凝胶法是在Ce/Zr 不同比例的溶液中加入柠檬酸盐或其它有机酸化合物,经搅拌、恒温蒸发等处理成为凝胶后高温分解即得CexZr1-xO2复合氧化物。通常合成的CexZr1-xO2粒度比较均匀、比表面积较大,但制备时间长,高温易引起团聚。制备过程中,溶液的pH 值、凝胶温度以及水解时水的添加量对固溶体的性能有着明显的影响。
方 等[15]用Ce(NO3)4·6H2O 和Zr(NO3)4·5H2O为铈锆原料,以丙烯酰胺(C3H5NO)、N'N 亚甲基双丙烯酰胺(C7H10N2O2)和过硫酸铵((NH4)2S2O8)作为高分子凝胶剂,制备出高分子凝胶改进铈锆复合氧化物。研究结果表明,高分子用单体与网络剂的三维聚合网络,分散固溶体的粉体颗粒,煅烧高分子后形成多孔结构,上述两因素的协同作用促进了多孔纳米铈锆固溶体的形成。表1 为单体与网络剂质量比对凝胶及平均粒径的影响,当C3H5NO 与C7H10N2O2的质量比为5:1、混合溶质的溶度为0.04 mol,经合适的热处理可以得到粒径为10~20 nm 的铈锆固溶体。Ce/Zr 摩尔比为6: 4 时,Ce0.6Zr0.4O2固溶体具有优异的比表面积和孔结构,其比表面积达到120.5 m2·g,孔径达8.12 nm,孔容高达0.22 cm3/g。Alifanti 等[16]用Ce(NO3)3和ZrO(NO3)2为铈锆原料,以柠檬酸为络合剂,反应完成后,在40℃下离心脱水得到无色胶状物,该凝胶材料在70℃真空干燥12h,最后通过在450℃或700℃下焙烧3h。研究表明,当二氧化铈含量低时,溶胶凝胶法能得到组分均一的铈锆复合氧化物;当CeO2>20%时,会出现分相,得到的是Ce0.5Zr0.5O2和CeO2。

表1 单体与网络剂质量比对凝胶及平均粒径的影响[15]Table 1 Effect of monomerand network agent mass ratioon gel and average particle size
2.3 水热法
利用水热法可合成各种形貌的铈锆复合氧化物,不同形貌的CeO2能暴露不同的晶面、增强氧缺位浓度或提高其储氧能力等,使其具有独特的物理和化学特性。
许等[17]采用水热法制备了棒状和球状的Ce0.8Zr0.2O2-δ复合氧化物,将溶解的形貌控制剂添加到溶解的Ce(NO3)3·6H2O 和ZrO(NO3)2·xH2O 的混合溶液中,搅拌30min 后,将尿素溶液滴入混合液中,搅拌直至透明,再将其转入高压反应釜中反应,离心、洗涤、干燥得到白色前驱体,最后将前驱体在500℃煅烧5h 得到淡黄色样品。棒状复合氧化物采用十六烷基三甲基溴化铵(CTAB)作为形貌控制剂,样品表明光滑、致密,宽约2 μm,长约14 μm;而球状复合氧化物采用柠檬酸作为形貌控制剂,得到的样品呈现空心球结构,球表面光滑,直径约3 μm。高分辨透射电镜表征表明,棒状Ce0.8Zr0.2O2-δ优先暴露的是(111)和(220)晶面,且对应的晶面间距分别为0.31 nm 和0.19 nm,对于CO 氧化成CO2过程中,(220)晶面表现出优越的催化活性[18];而球状样品只观察到稳定的(111)晶面。Raman 光谱分析表明,棒状和球状Ce0.8Zr0.2O2-δ的氧空位浓度分别为0.0138和0.0121,优先暴露活性(220)晶面的样品具有更高的氧缺位浓度,这样可提高氧的迁移率,使得复合氧化物中的晶格氧可以更有效地参与CO氧化反应,从而提高催化活性。
Wang 等[19]通过一锅水热法直接合成CexZr1-xO2(x=0, 0.1,0.2,0.3,0.4, 0.5, 0.6, 0.7, 0.8, 0.9,1)。研究结果表明,CeO2具有最大的比表面积154 m2/g,其次为Ce0.9Zr0.1O2达到143 m2/g,最小的为ZrO2(24 m2/g)。在不搅拌条件下,在150℃水热条件下能合成组分均一的Ce0.3Zr0.7O2,但在同样条件下Ce0.7Zr0.3O2出现了分相。这可能是由于ZrO2或ZrO(OH)2作为形核中心,富Ce 组分在富Zr 周边聚集,阻碍了反应的均匀进行。而且,合成的Ce0.5Zr0.5O2在1000℃范围内具有良好的热稳定性,在还原条件下,高于1100℃时,晶相由准立方相转变为阳离子有序的烧绿石相,这种离子有序排列可显著提高铈锆固溶体的氧储放性能;在氧化条件下,高于1200℃时,晶相由准立方相转变为三斜相。
2.4 其它制备方法
铈锆复合氧化物的制备方法还有高能球磨法、固相合成法、微乳液法、反向微乳液法等。固相合成法与高能球磨法都具有能耗大、效率低、成分不均匀和容易混入杂质等缺点。微乳液法是透明的油包水或者水包油形成的单分散体系,通常是由油(通常为碳氢化合物)和水(或电解质水溶液)在表面活性剂和助表面活性剂(通常为醇类)的作用下形成具有特定性质的稳定体系,Zhao 等[20]将CTAB、丁正醇和环己烷混匀搅拌直至透明形成油相,再加入铈锆混合液,合成了Ce0.67Zr0.33O2,其储氧量约650 μmol/g,经1100℃老化4h 后,其储氧量仅128.4 μmol/g,热稳定差。
3 CeO2-ZrO2 复合氧化物的掺杂改性
改善铈锆基复合氧化物的储放氧性能和热稳定性是提高三效催化剂性能的关键手段之一,除优化制备条件外,通常采取在铈锆固溶体中掺杂其它组分的方法,使其获得更优的储放氧性能和热稳定性。有研究表明,采用离子掺杂的方式掺入2.5%~5.0%(摩尔分数)的三价金属离子,可以显著改善铈锆基复合氧化物的储氧能力,且掺杂离子的半径越接近CexZr1-xO2固溶体的临界半径,越有利于提高其低温还原性能[21]。铈锆复合氧化物掺杂主要有稀土元素、碱土金属以及过渡金属。
3.1 稀土元素改性
稀土元素Y、La、Pr、Nd、Tb、Dy 等掺杂能有效提高铈锆固溶体的热稳定性、储放氧能力(Oxygen Storage Capacity, OSC)及氧化还原性,改性效果取决于氧化物结构和稀土元素半径。
从理论上讲,离子半径接近铈锆临界半径的Y3+(0.1015 nm)易进入铈锆固溶体晶格且会有利于提高铈锆氧化还原能力。Andriopoulou C 等[22]采用溶胶凝胶法制备一系列钇掺杂的铈锆复合氧化物Ce0.33YxZr0.67-xO2(x=0,1%,3%,5%),系统研究了钇掺杂后铈锆复合氧化物储放氧性能的变化规律及其影响因素。样品XRD 图谱研究表明,钇能够进入复合氧化物晶格,与Ce0.33Zr0.67O2体系形成均匀固溶;与新鲜样相比,老化样的Ce0.33Zr0.67O2几个主要衍射峰(28°~30°、47°~50°、55°~60°)的峰型对称性相对较差,表明样品可能发生了分相;但随着钇掺杂量的增大,样品的衍射峰对称性逐渐提高,这表明,钇元素的掺杂能够抑制分相形成,提高体系的结构热稳定性。通过分析样品表面元素分布发现,随着钇掺杂量的增加,老化样品中表面钇含量成比例增加,与此同时,锆含量逐渐降低,可认为在材料表面Y3+主要取代Zr4+。为保证表面电荷平衡,Y3+的取代必然使得表面Ce4+的含量增多。通过分析表面吸附氧含量发现,随着钇掺杂量的增加,晶格氧的比例逐渐上升而表面吸附氧的比例迅速减少,表明钇的加入削弱了样品表面吸附能力,并且抑制了铈的可逆氧化还原反应。
Wang 等[23]研究了添加不同含量的Nd 对Ce0.2Zr0.8O2性能的影响,发现形成了比表面积更大的Ce-Zr-Nd 三元固溶体,氧化还原性能和储氧性能也相应提高,且5%的Nd 添加量具有较优异的性能,其比表面积达到127.1 m2/g,同时具有良好的热稳定性能;Guo 等[24]发现当铈锆比一定时,掺杂不同含量的Nd 对Ce-Zr-Nd 结构、性能有重大的影响,Ce0.35Zr0.50Nd0.10O1.85具有最多的氧空位和更高的储氧能力,随着Nd 含量的增加,氧空位减少,储氧能力下降。同时有研究表明,添加Nd 能显著降低NOx还原和CO 氧化温度,分别从278℃和280℃降低至229℃和235℃[25]。
Wang 等[26,27]研究了不同稀土元素(La、Nd、Pr、Sm、Y) 掺 杂 对Ce0.2Zr0.8O2性 能 的 影响,结果表明,La、Nd、Pr 的改性效果更明显,不仅提高了其热稳定性及储氧性能,而且改善了Ce0.2Zr0.8O2的操作窗口及起燃温度,Sm 和Y 降低了其催化活性。
Dulgheru 等[28]研究了La、Nd、和Pr 稀土元素掺杂对Ce0.3Re0.2Zr0.5O2的影响,La、Pr 掺杂提高了NO/O2还原低温活性,Nd 掺杂对其影响较小;Ce0.3La0.2Zr0.5O2活性最高,将起燃温度降至约200℃,这是因为La 在CeO2晶格中提高了结构稳定性。有研究表明[29],掺杂Tb 会使CeO2-ZrO2固溶体更容易被还原,从而使其具有更好的储氧性能,并且与未掺杂的CeO2-ZrO2相比,具有更高的比表面积和更好的热稳定性。
3.2 碱土元素改性
碱土元素均能与CeO2-ZrO2复合氧化物形成三元固溶体,但固溶度随掺杂离子半径变化差异较大。Mg2+、Ca2+、Sr2+和Ba2+的离子半径分别为0.066 nm、0.112 nm、0.125 nm 和0.142 nm,Ca2+和Sr2+具有相对适宜的离子半径,其固溶度分别可达23%和8%,在面心立方结构的晶体中产生氧空位,提高体相氧的迁移性能,改善铈锆固溶体的热稳定性。而Mg2+半径较小,Ba2+半径较大,很难取代阳离子进入CexZr1-xO2,固溶度有限。
SrO 的掺杂可保持铈锆固溶体的萤石立方结构,对热稳定性有所改善,且表面剩余的Sr 形成了SrZrO3,抑制了复合氧化物的烧结和老化过程中相的分离。Fan 等[30]以Sr 掺杂和负载两种不同方式改性CeO2-ZrO2,系统研究了Sr 改性对固溶体的组织结构、热稳定性及储氧性能的影响。研究表明,掺杂引入的Sr 在CeO2-ZrO2晶格中均匀分布,而负载样中的Sr 主要分布在晶界上。Sr 的引入可以明显阻止水热老化条件下CeO2-ZrO2载体的烧结和分相,提高了热稳定性及储氧性能,且负载样性能优于掺杂样。这主要是由于不同的引入方式导致Sr 与CeO2-ZrO2载体的相互作用方式不同。掺杂样活性氧主要来源于晶格畸变、电价平衡和尺寸效应,而负载样的活性氧主要源于SrZrO3/CeO2-ZrO2界面,如图2 所示。

图2 Sr 改性CeO2-ZrO2 复合氧化物微观结构示意图[31]Fig.2 Schematic diagram of microstructure of Sr modified CeO2-ZrO2 composite oxide
An 等[31]对Ce0.67Zr0.33O2掺杂Ca 和Mg 进行了研究。结果表明,由于电荷补偿和半径的影响,在固溶体中产生了较多的氧空位和晶格缺陷,且掺杂抑制了固溶体的相分离,提高了热稳定性和储氧能力。但经氧化还原处理后,Ca 和Mg 的掺杂效果不同,由于Ca2+半径适中,产生了更多的氧空穴,使氧离子在晶格中更容易扩散,提高了Ce0.67Zr0.33O2的储氧能力;而MgO 在CeO2中可溶性小,氧化还原处理后Mg-Ce-Zr-O 体系的缺陷结构被破坏,使得Ce0.67Zr0.33O2的储氧性能明显降低。
Ba 能使Pd2+具有高电子密度,从而使Pd2+具有类似Rh0的电子层结构(Kr[4d85s1]);其次在贫燃条件下,NOx能被BaO 吸收并形成Ba(NO)2或Ba(NO)3,储存的NOx在富燃条件下被CO 和HC 还原为N2。Lin 等[32]采用四种不同的方法(共沉淀法、氧化沉淀法、柠檬酸溶胶凝胶法、反向乳液法)合成Ba 掺杂Pd/CeO2–ZrO2催化剂,并研究了其对CO、HC 和NOx催化效果。研究结果表明,共沉淀法得到的催化剂具有最好的氧化还原性能,而氧化沉淀法制备的样品经老化后具有最好的热稳定性和有CO、HC 和NOx转化率。Yang 等[33]系统研究了不同含量的BaO(0,3%,5%,9%)掺杂对Pd/CeO2–ZrO2催化性能的影响,结果表明,掺杂的Ba2+进入了CeO2晶格中,形成了均一的Ce-Zr-Ba 三元固溶体,提高了结构的热稳定性和NOx存储能力,但Ba 的引入降低了HC 反应物在催化剂表面的吸附,Ba 高电子密度也加速了NO 的分解和促进了中间产物(NCO 和CN)的生成。因此,Ba 的掺杂改性提高了HC 和NOx的转化率,但由于氧空位的减少从而抑制了CO 低温氧化。
3.3 过渡元素改性
过渡金属具有未充满电子的价层轨道,该区域很多元素的电子构型中都有单电子,比较容易失去,因此这些金属都有可变价态。过渡金属Cu、Mn、Fe、Ni 、Co 等独特的电子构型决定了其良好的低温还原性能。适量过渡金属掺杂到铈锆固溶体中可形成三组分固溶体氧化物,过渡金属与载体以及过渡金属与贵金属间的相互作用提高了铈锆复合氧化物的储氧性能,并且具有良好的低温氧化还原性能,降低了催化剂的起燃温度[34]。
汪等[35]采用均相共沉淀法制备了铈锆复合氧化物,并用等体积浸渍法制备了其负载的Pd/CexZr1-xO2,研究了Ni、Cu、Mn 等过渡金属掺杂对催化剂物化性能的影响。掺杂Ni 后样品出现NiO衍射峰,说明Ni在载体上发生聚集,分散性差,而Cu 和Mn 改性后物相结构没有发生变化;相对于Pd/CZ 催化剂,添加过渡金属的各催化剂比表面积均减小,其中掺杂Ni 的催化剂的比表面积下降最明显;通过H2-TPR 表征和测试CO、HC 转化率及NO2生成率,发现,过渡金属掺杂有利于提高催化剂的催化氧化性能,其中,Cu 和Mn 的改善作用最为明显,Ni 掺杂效果不大。
Jia 等[36]研究了Mn0.1Ce0.9O2和Mn0.1Ce0.6Zr0.3O2的氧化还原性质,结果表明,这些复合氧化物都具有类似CeO2的萤石立方结构,表面都存在Mn2+/Mn3+氧化还原电子对,并且Mn-O 和Ce-O 间的协同作用促进了铈锆基材料的氧化还原性能。Wang 等[37]通过溶胶凝胶法合成Co0.1Ce0.6Zr0.3Ox,并通过浸渍法负载了0.5%Pd,结果表明,Co 进入到铈锆复合氧化物的晶格中,由于半径效应和电荷效应,提高了氧空位和晶格缺陷,H2-TPR 和动态储氧量测试表明,Co 掺杂能提高储氧量。Li 等[38]制备了掺杂不同过渡金属(Co、Fe、Ni、Mn、Cr)的铈锆复合氧化物和单钯三效催化剂。结果表明,掺Fe 和Co 的催化剂表现出了较优的催化活性,降低了起燃温度和完全转化温度。这是因为Fe 和Co 的掺杂提高了铈锆氧化物的表面原子比例,部分Ce4+变成Ce3+以保持电荷平衡,可以促进Ce4+还原生成Ce3+和氧空缺的形成,提高了催化剂的动态氧存储/释放能力。Ni 的掺杂也提高了催化性能,尤其是CO、NO 和NO2的转化;Mn 的掺杂仅促进了CO 的转化;Cr 的掺杂降低了催化剂的活性。对于Mn 和Cr 掺杂的催化剂,其表面Ce/Zr 原子比明显低于不掺杂的催化剂,即Ce 原子在表层被Cr 或Mn 取代。而且,表层Ce3+浓度也低于未掺杂的催化剂,表明Cr 和Mn 的掺杂会抑制Ce4+转化为Ce3+,降低了铈锆氧化物的储氧能力。
4 结论与展望
铈锆复合氧化物的制备方法对制备高性能的材料至关重要,目前有各种方法制备高性能的CexZr1-xO2储氧材料,各制备方法均有优、缺点。溶胶-凝胶法能在温和的条件下实现铈分子和锆分子的分散,还能明显提高铈锆的均匀性,但该方法成本高、产能低、有机溶剂对人体有一定的危害性。水热法能根据需要设计出目标样品形貌,得到的样品纯度高、分散性好、晶粒大小可控,但该方法成本高,合成条件苛刻,其反应物浓度、温度、酸碱度、升温速率等均能影响产物的性能。共沉淀法制备成本低、工艺简单,得到的铈锆复合氧化物粒度均匀,是目前主要制备铈锆复合物的方法。铈锆复合氧化物储氧材料经掺杂后能在一定程度上提高热稳定性、储氧性能及催化性能,但是仍存在着一些不足,如易发生团聚而降低比表面积、温度高于1000℃时发生烧结而降低性能、高温下铈锆固溶体易分离产生Ce 四方相和Zr 四方相而降低氧存储性能等。
目前对CexZr1-xO2储氧材料的研究取得了一定成果,但在CexZr1-xO2结构与性能之间的关系、如何有效提高其储放氧性能和热稳定性等方面还有待深入探索。CexZr1-xO2储氧材料热稳定性高、储放氧能力强、起燃速度快,是汽车尾气净化催化剂的关键材料,促进了新一代耐高温三效催化剂的产生,随着排放法规日益严格,提高其热稳定性及氧化还原性能将是未来研究的热点。
