中空球形碳酸锰合成及热分解制备MnO x研究①
2021-09-15黄春荣邵学财穆远慧刘丰源兰苑培
邹 飞,黄春荣,蹇 攀,邵学财,穆远慧,刘丰源,2,兰苑培,2
(1.贵州大学 材料与冶金学院,贵州 贵阳550025;2.贵州省冶金工程与过程节能重点实验室,贵州 贵阳550025)
锰具有丰富的化合价态[1],常见氧化物有MnO、MnO2、Mn2O3、Mn3O4、Mn5O8[2],其氧化物广泛应用于冶金[3]、电化学[4]、化工[5]、催化[6]等领域。
MnCO3的制备方法有反胶束法[7]、液相沉淀法[8]、微乳液法[9]、均匀沉淀法[10]、水热法[11]等。 目前制备出的MnCO3多为球形、类球形或者其他形貌[12-15],而中空球形MnCO3的制备还鲜有报道。
MnCO3分解产物受温度[16]和气氛[17]的影响,目前对其热分解研究主要集中在空气气氛中,氢气或惰性气体中的热分解特性和物相转变行为仍需进一步证实和完善。据文献[18-19]报道,MnCO3热分解前后微观形貌差异较小,有望通过调控MnCO3形貌并采用适宜的热分解条件获得不同形貌的MnOx材料。因此,本文采用水热法调控MnCO3形貌,制备具有中空结构的MnCO3微球,并研究其在空气、氩气、氢气气氛中的热分解行为。
1 实验材料与方法
1.1 实验方案
实验原料MnC4H6O4·4H2O(99.0%)、NH4HCO3(99.995%)均购置于阿拉丁。称取一定量MnC4H6O4·4H2O溶于20 mL蒸馏水中,另将1 mmol的NH4HCO3溶入20 mL蒸馏水中,在500 r/min的转速下,将含锰溶液缓慢滴加到碳酸氢铵溶液中,持续搅拌30 min后转入100 mL聚四氟乙烯反应釜中,加入40 mL蒸馏水后进行加热,具体实验参数见表1。反应一定时间后,经乙醇和蒸馏水反复洗涤过滤,将滤饼放置于真空干燥箱中干燥24 h,得到灰白色MnCO3粉末。
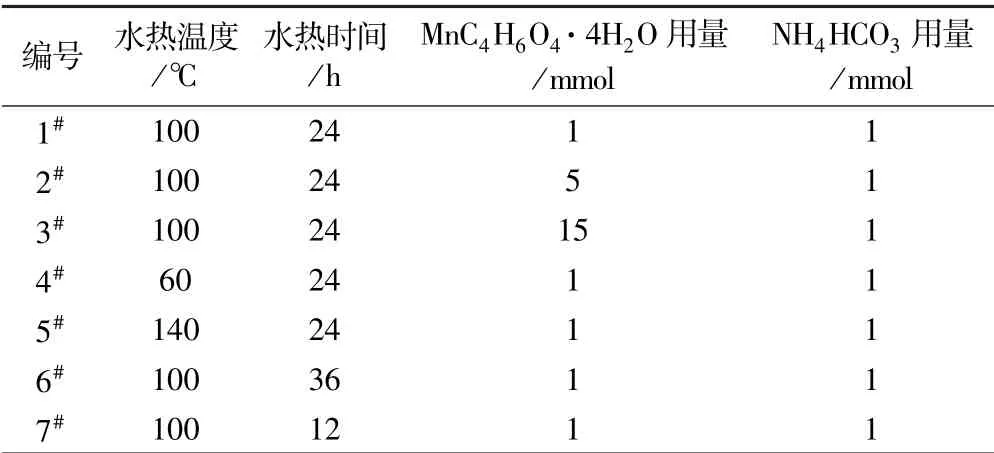
表1 制备MnCO3实验方案
分别在空气、氩气、氢气气氛中研究MnCO3热分解行为。称取0.3 g MnCO3粉末置于刚玉舟中,空气气氛下焙烧时,样品直接放置于敞开管式炉;氩气(99.999%)气氛和氢气(99.999%)气氛焙烧时,先对炉管反复抽真空并吹氩除氧。焙烧时气体流量200 mL/min、焙烧时间2 h。
1.2 表征方法
使用XRD(Rigaku D/Max-2200V X-ray diffractometer)进行物相分析;采用SEM(德国蔡司ΣIGMA-X-Max20)和TEM(Tennai G2 F20)对样品进行形貌表征;采用TG(METTLER TOLEDO)分析产物的热分解行为,测试温度25~1 000℃,气体流量50 mL/min,升温速率10℃/min,氢气、氩气测试时反复抽真空并吹氩以置换除氧。
2 结果与讨论
2.1 MnCO3物相及形貌
图1为不同条件下制备所得MnCO3样品XRD图谱。从图1可以看出,不同条件下制得的MnCO3样品衍射图谱特征峰均相同,衍射峰与标准卡片PDF#86-0172相吻合,无其他杂峰,表明各条件下均能得到MnCO3。另外,样品衍射峰尖锐,表明具有较好的结晶度。
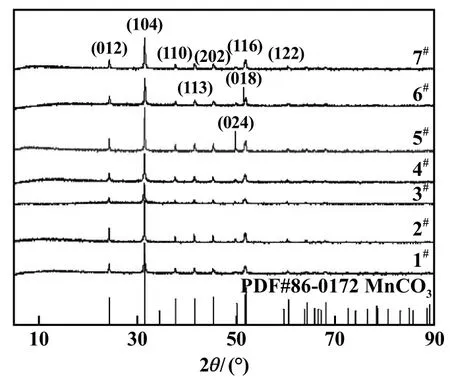
图1 MnCO3样品XRD图谱
不同水热条件下制备所得MnCO3样品微观形貌如图2所示。由图2发现,不同醋酸锰添加量、水热时间以及水热温度条件下所制备的MnCO3微观形貌差异较大。醋酸锰添加量1 mmol时,所得颗粒为中空球形,球面光滑;醋酸锰添加量增大到5 mmol时,所得颗粒形貌严重不规则,表面粗糙,团聚严重;当醋酸锰添加量继续增大至15 mmol时,颗粒均匀,分散性较好,但颗粒为不规则球形。由图2(a)中放大图可观察到,微球由大量多面体晶粒堆积而成。反应时间12 h时,微球颗粒已经成型,颗粒均匀,分散性较好,形貌完整;时间延长至24 h,微球粒径增大,且颗粒间相互黏结在一起;时间延长到36 h,微球颗粒粒径减小,但其团聚现象严重。60℃和140℃下得到的微球分散性良好,粒径也较为均匀,其中60℃下小颗粒数量较多,呈不规则立方体,表面由纳米晶体组成。可见,MnCO3颗粒的形成经历了晶核形成、细小晶粒团聚和长大,以及在表面张力作用下通过自组装最终形成圆球微粒。在图2(a)、(b)中均可发现明显的中空球形结构。从图2(g)可以看出,在该实验条件下制备的MnCO3颗粒分散性良好,且球形结构较为完整,球形颗粒表面光滑,粒径分布均匀。

图2 不同水热条件下制备的MnCO3样品SEM图
7#MnCO3样品TEM图像如图3所示。从图3(a)可以看出,MnCO3具有较为规整的球形,直径约为2.3μm,且表面有纳米结构凸起;由图3(b)右下角可以看出,该微球具有中空球形结构,与SEM结果一致。综合不同条件下MnCO3样品XRD、SEM和TEM结果,当醋酸锰添加量1 mmol、反应时间12 h、反应温度100℃时,即可获得形貌较好的中空球形MnCO3。由此,以7#条件制备MnCO3样品并进行后续研究。

图3 MnCO3样品TEM图
2.2 MnCO3的热分解行为
不同气氛条件下MnCO3样品TG-DSC曲线如图4所示。
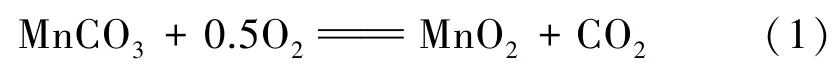
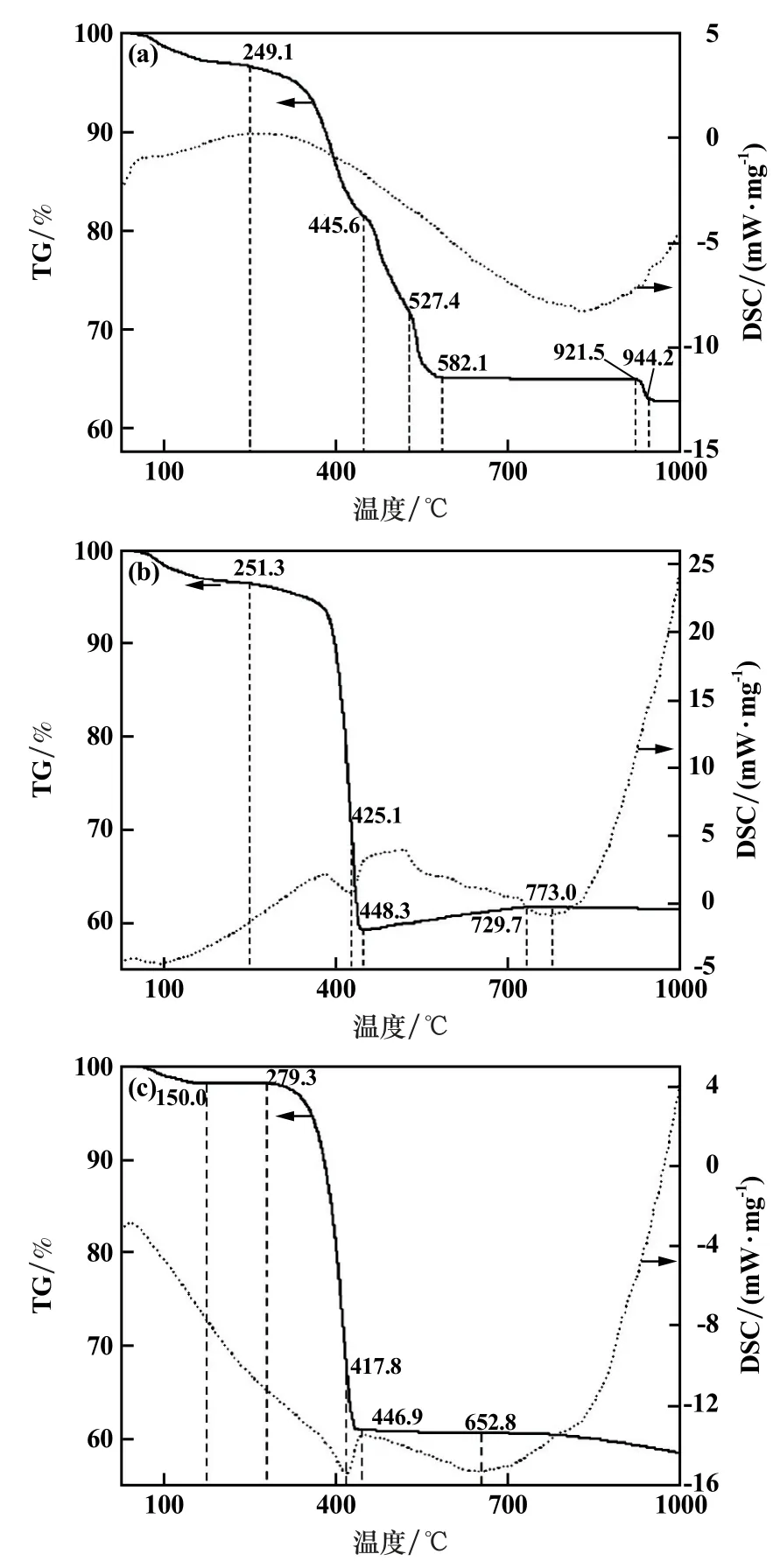
图4 MnCO3在不同气氛条件下的TG-DSC曲线
由图4(a)可知,在空气中,249.1℃之前的质量下降对应吸附水和结晶水的脱除;249.1℃后,TG曲线下降明显,此时MnCO3开始分解:445.6℃时TG曲线的变化为生成的MnO2转变成Mn2O3和未分解的MnCO3直接分解为Mn2O3共同作用的结果;527.4℃时,MnO2完全转变成Mn2O3,余下的MnCO3继续分解;582.1~921.5℃时,质量不再发生变化,表明MnCO3分解结束,此时总失重率为34.9%,与生成Mn2O3(式(2))的理论失重率(34.8%)吻合;921.5~944.2℃曲线的质量变化为Mn2O3分解生成Mn3O4。
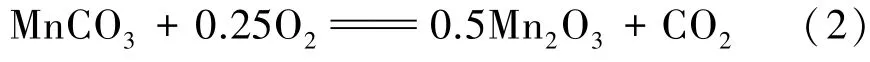
图4(b)显示,MnCO3在氩气中分解时,251.3℃前的失重为结晶水和吸附水的脱除;251.3℃时,MnCO3开始分解(式(3)),448.3℃时分解完毕,此时失重率为40.5%。
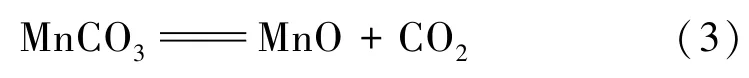
有报道称MnCO3在缺氧分解时只生成MnO[20],但MnO在300℃以上时容易与分解产生并滞留在周围的CO2反应生成Mn3O4:
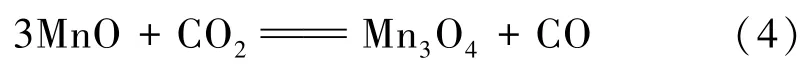
因此,在高于448.3℃温度区间热重曲线缓慢升高,即为MnO被CO2氧化为Mn3O4。
由图4(c)可知,在氢气气氛中,150℃前的失重为样品结晶水和表面水的脱除;150~279.3℃之间曲线平缓没有变化,279.3℃后曲线继续下降,对应MnCO3开始分解:
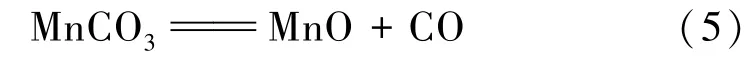
其理论失重率为38.3%,446.9℃时MnCO3分解完毕,总失重率为39.0%,说明最终产物为MnO。
对比3组TG曲线可以发现,MnCO3在空气、氩气、氢气气氛中分解为低价氧化锰时,相对应地起始分解温度升高、分解终点温度降低、分解区间变窄。
基于MnCO3的热分解研究,在400~800℃、不同气氛下对制备的MnCO3进行热分解实验。图5为不同气氛条件下焙烧产物的XRD图谱。
由图5(a)可知,400℃时还存在MnCO3衍射峰,470℃时MnCO3衍射峰消失,主要物相为MnO2,并开始出现Mn2O3衍射峰;540℃时MnO2峰消失;800℃时产物为Mn2O3,与TG-DSC分析结果一致。
由图5(b)可知,400℃时,已经开始出现Mn3O4特征峰,但仍检出MnCO3衍射峰;450℃时,MnCO3特征峰消失,800℃时衍射峰未发生改变。
由图5(c)可知,400℃的产物为MnO,并出现了Mn3O4特征峰;随着温度升高,Mn3O4相消失,温度达到670℃后为MnO。
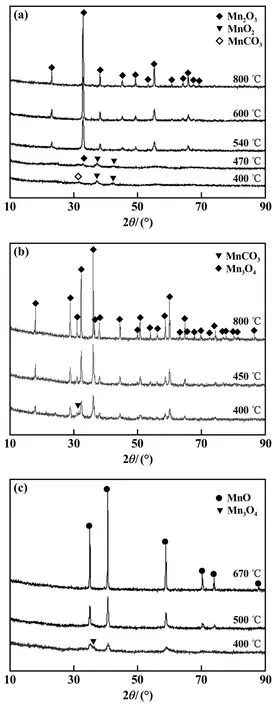
图5 不同气氛、温度条件下MnCO3焙烧产物的XRD图
综合XRD和TG-DSC分析结果可知,MnCO3在空气中分解时,约250℃时开始分解,温度低于445℃时产物为MnO2,温度升高到540℃时,MnO2进一步转变为Mn2O3,当温度高于921℃时,Mn2O3分解为Mn3O4。氩气气氛中,250℃附近MnCO3开始分解为MnO,分解的MnO与CO2反应生成Mn3O4;450℃时,MnCO3分解结束,产物为Mn3O4,当温度上升至800℃时,产物保持不变。氢气条件下,约280℃时MnCO3开始分解,分解产物为MnO,低温条件下少量MnO亦可与CO2反应生成Mn3O4,500℃以后得到纯相MnO。
2.3 MnO x形貌特征
焙烧获得的MnOx微观形貌如图6所示。对比图2与图6可以发现,焙烧前后颗粒微观形貌基本保持不变,图6(f)亦可发现焙烧后仍具备中空结构。焙烧前后表面形貌变化明显,由原来光滑的晶粒结构变为疏松多孔或具有沟壑的凹凸起伏结构,这是由分解时产生的气体脱离颗粒时形成的,其有利于比表面积增加。分析发现不同气氛的焙烧产物表面结构有一定差异,其中空气中焙烧后表面有明显孔隙结构,而氢气/氩气气氛下焙烧后表面出现密集颗粒状的突起。

图6 不同气氛、不同温度下MnCO3焙烧产物的SEM图
焙烧后MnOx结构基本保持不变,且表面特性改善,有利于MnOx后续的功能化应用。调节焙烧条件可获得不同价态、成分的MnOx产物或MnOx-MnCO3复合材料,提供了更多的后续应用选择。因此,通过改变水热条件可调控MnCO3形貌,通过选择焙烧工艺可获得具有不同形貌、价态、成分结构的锰系复合材料,为调控、提升锰系材料性能提供了新思路和方法。
3 结 论
通过调控水热反应时间、温度和前驱体添加量,制备了具有不同形貌和表面特征的MnCO3,其中包括中空球形结构MnCO3。热分解研究发现,中空球形MnCO3在室温至1 000℃的热分解产物变化分别为:空气条件下,MnCO3→MnO2→Mn2O3→Mn3O4;氩气条件下,MnCO3→MnO→Mn3O4,其中MnO将被分解产生的CO2所氧化;氢气条件下,MnCO3→MnO/Mn3O4→MnO,低温区少量MnO将被CO2氧化为Mn3O4。不同气氛条件下焙烧后获得的MnOx基本保持MnCO3的形貌特征,且表面结构明显改善,利于后续MnOx的功能化应用。调控MnCO3形貌及焙烧条件,可作为不同形貌、价态、成分锰氧化物及复合材料制备的新方法。
