贻贝壳在不同方法下合成羟基磷灰石多孔微球的性能研究
2021-09-14李超群顾忠旗周丽萍娄永江
李超群 ,顾忠旗 ,黄 继 ,石 娟 ,周丽萍 ,王 晴 ,娄永江*
(1.宁波大学 食品与药学学院,浙江 宁波 315832;2.嵊泗县海洋科技研究所,浙江 舟山 202450)
羟基磷灰石(Hydroxyapatite,HA)是自然界中天然存在的矿物质,广泛存在于脊椎动物的牙齿和骨骼中[1-2].作为一种典型的生物材料,其具有良好的生物相容性、生物活性和离子交换性[3].目前HA 主要应用于药物控释[4]、基因传递[5-6]、组织工程[7]、骨组织修复[8]以及其他生物医学领域[1].张月等[9]阐述了纳米HA 在口腔骨缺损中的临床应用.Tank 等[10]成功地用钴掺杂的纳米HA 进行抗菌和溶血研究.同时,HA 具有很强的吸附作用,可以用来吸附重金属和其他污染物,也可以用来制备复合物、杀菌剂和催化剂等[3,11-16].Singh 等[17]研究了钙磷盐在微波和水热及有无表面活性剂条件下合成HA 纳米棒.Aggarwal 等[18]以钙磷盐为原料,用水热法合成HA 介孔颗粒.HA 具有介孔特性,使其具备较强的吸附和载体作用,因此更具有合成HA 类复合材料的优势.传统制备HA 采用硝酸钙和无机磷酸盐合成.但是近年来无机钙盐和磷酸盐的矿物原料受限,而以贝壳为原料制备纳米带状HA、多孔HA 具备低成本、低污染以及富含微量元素等优势[19].且有研究表明[20-21],生物来源的HA 相较于化学合成的HA 具有更佳的空间网状结构和相互交通.
近几年来,贝类加工的副产物产生的废弃贝壳每年多达数10 万t[3],除以贝壳为原料制备成各种食药级钙剂外,利用贝壳制备HA 鲜有报道[22].利用废弃贝壳开发生物材料可以解决资源缺乏问题,提高副产物的附加值,经济效益巨大[20].此外,球形多孔HA 相比于其他形状,具有比表面积大、更多的药物和金属负载量、良好的力学性能和流变性能,更有利于合成具有特殊功能的材料[23].但是对于植物来源或者蛋壳类,因其主要成分为CaCO3,因而大多采用高温分解CaCO3后与磷酸盐前驱体反应制备HA,这种方法存在产物的形状和尺寸难以控制的问题[21].
本文选用舟山嵊泗的贻贝壳作为CaCO3原料,采用水热法、沉淀法、十六烷基三甲基溴化铵(CTAB)模板剂法以及反相微乳液法制备HA,并对合成的HA 进行结构表征,开展了贝壳合成球形、多孔HA 的技术研究,且选用银离子验证贻贝壳HA 的吸附作用.研究表明:该方案可行,并有助于解决废弃贝壳环境污染问题;同时,对实验室及工业生产HA 上具有减少成本、提高HA 药物和重金属吸附量以及合成功能性材料等作用.
1 材料与方法
1.1 试剂与仪器
HNO3、HCl、NaOH、Na2CO3为分析纯,购于阿拉丁试剂有限公司;贻贝壳取自舟山市嵊泗枸杞贻贝养殖区;(NH4)2HPO4、NH4H2PO4为分析纯,购于上海麦克林生化科技有限公司;Na2HPO4·12H2O、无水乙醇、曲拉通X-100(Triton X-100)、吐温80(Tween 80)为分析纯,购于国药集团化学试剂有限公司;十六烷基三甲基溴化铵(CTAB)为分析纯,购于北京索莱宝科技有限公司.
JE-OLJSM6700 型X 射线能谱(EDS)和扫描电子显微镜(SEM),产自日本电子株式会社;D8 Advance 型X 射线粉末衍射仪(XRD),产自德国布鲁克公司;Nicolet 6700 智能型傅里叶红外光谱(FTIR),产自美国赛默飞世尔;ASAP20202 HD88全自动比表面积及微孔孔隙分析仪(BET),产自美国麦克仪器公司;SPECTRO ARCOS 电感耦合等离子体发射光谱(ICP-OES),产自德国斯派克分析仪器公司.
1.2 方法
1.2.1 碳酸钙的制备
贝壳洗涤烘干后,取25 g 研磨过30 目的贝壳粉,加入500 mL 1 mol·L-1的HCl 溶液,反应48 h,将得到的滤液用1 mol·L-1的NaOH 溶液调节pH 至7,定容至1 000 mL 容量瓶中;取100 mL 该溶液,快速倒入100 mL 0.25 mol·L-1的Na2CO3溶液中,搅拌2 h,分别用无水乙醇和纯水洗涤、过滤,烘干制得贝壳CaCO3.然后用EDS 进行元素分析.
1.2.2 多孔HA 的制备
(1)水热法(样品a):取2.50 g CaCO3、0.86 g(NH4)2HPO4和0.99 g NH4H2PO4(钙磷摩尔比1.67),放入聚四氟乙烯内衬中,加30 mL 纯水,调pH 至10,密封后置140 ℃干燥箱控温24 h,反应结束可见上层液体澄清透明,离心得沉淀物分别用乙醇和纯水各洗涤3 次,约60 ℃干燥制得样品[16].
(2)沉淀法(样品b):在30 mL 纯水中加入1 g CaCO3、2 g Na2HPO4·12H2O,磁力搅拌直到产生白色悬浊混合溶液,调pH 至11,超声30 min,密封后在50 ℃下反应80 h,离心得沉淀物,分别用乙醇和纯水各洗涤3 次,约60 ℃干燥制得样品.
(3)CTAB 模板剂法(样品c):取CTAB 0.25 g,加入20 mL 纯水搅拌至溶液澄清,加入Na2HPO4·12H2O 0.79 g,搅拌30 min 至溶液澄清,调pH 至10,标记为溶液1.将2.36 g CaCO3溶于10 mL 水,调pH 至11,标记为溶液2.将溶液2 滴加到溶液1中,搅拌24 h,离心得沉淀物分别用乙醇和纯水各洗涤3 次,约60 ℃干燥6 h,接着550 ℃煅烧6 h 制得样品.
(4)反相微乳液法(样品d):以钙磷质量比为5:3配置CaCO3溶液和Na2HPO4·12H2O溶液.将Triton X-100 和Tween 80 溶于环己烷中,加入体积比为5:4 的正己醇和正丁醇,然后滴加CaCO3悬浊液,搅拌中加入等体积数Na2HPO4·12H2O 溶液,调pH至11,搅拌10 min,密封沉淀24 h,无水乙醇破乳,离心得沉淀物分别用乙醇和纯水各洗涤3 次,约80 ℃干燥6 h,接着550 ℃煅烧6 h 制得样品.
1.3 吸附银离子实验
4 种样品分别取4 g 加入100 mL 水,超声震散,再加入100 mL 2 g·L-1硝酸银,常温反应7 h,过滤,去离子水洗涤,60 ℃烘干,研磨过300 目筛,得到纳米级载银羟基磷灰石(AgHAp).ICP-OES 表征测试4 种产物中银离子的吸附含量.
1.4 表征方法
SEM 和EDS:粉末样品涂在样品台上,喷金后分析.
XRD:标识X 射线、Cu Kα 辐射,波长0.154 06 nm,电压40 kV,电流40 mA,扫描范围5°~90°,每步扫描时间0.2 s,温度20 ℃,相对湿度50%.
FTIR:KBr 压片,扫描范围400~4 000 cm-1,扫描次数32 次·min-1.
BET:样品预热至100 ℃后,置入氮气气氛中12 h,BET 比表面积在相对压力0.05~0.20 之间计算,样品介孔分布由等温曲线脱附分支运用孔径分布测试(BJH)方法计算,总孔容在相对压力为0.974时得到.
ICP-OES:将制得的样品各取0.5 g,根据国标法溶解于100 mL 硝酸(V硝酸:V水=5:95)中,溶解后取1 mL 定容至250 mL,之后利用ICP-OES 测试溶液中元素的浓度[19].
1.5 数据处理
采用Origin 9.0 软件进行数据分析和处理.
2 结果与讨论
2.1 碳酸钙的EDS 表征
图 1 为贝壳碳酸钙的EDS 图像,从图1 可知,贻贝壳制备的CaCO3为方解石型,形状为球形和少量立方体型,主要组成元素为O、C 和Ca,含有微量的Na.采用舟山贻贝碳酸钙水热法制备HA,反应结束后上层溶液澄清透明.王润南等[16]选择连云港海滩的贝壳粉采用水热法制备HA,反应后上层溶液为浅黄色,表明贻贝碳酸钙中含有微量或没有有机质,纯度较好.
2.2 4 种方法制得产物的表征
2.2.1 SEM 表征观察形貌
图 2 为不同方法制得的HA 样品的SEM 图谱,其中水热法制得HA 为球状.4 种样品表面富集针状纳米粒子,详见表1.

图2 4 种方法制得样品的SEM 图谱
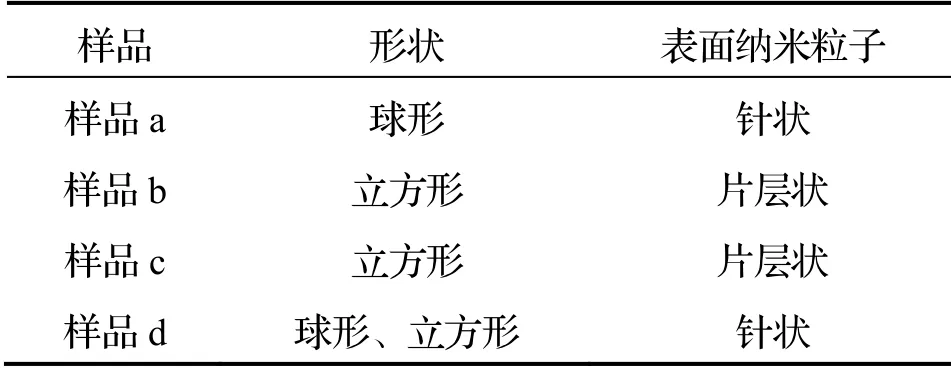
表1 4 种样品SEM 表征结果
2.2.2 XRD 表征分析产物结构
图 3 为4 种方法制得的样品的XRD 图谱.从图3 可知,样品a 有明显的HA 特征峰且无杂峰,表明贝壳CaCO3已经转化为HA;此外,HA 特征峰强度大、峰线窄且非常尖锐,说明产物具有良好的结晶度[3],这与文献[24]得到的结果相似.样品b 同样含有HA 的特征峰,但有杂峰,文献[25]中CaCO3的XRD 图谱可以佐证样品b 含有CaCO3杂峰.样品c也有明显的HA 特征峰和杂质峰,参考文献[1]中CaCO3/HA颗粒的XRD 图谱,可以推测样品c有未转化的CaCO3,且转化率低;根据文献[26-27]中CaCO3的XRD 图谱,可以判断样品c 为方解石型CaCO3/HA 复合材料.样品d 与样本品c 基本一致,均为CaCO3/HA 复合物.对照文献[19]中CaCO3/HA 复合生物材料的XRD 图谱可知,用反相微乳液法制HA 的转化度不高,CaCO3残留量大.

图3 4 种方法制得样品的XRD 图谱
2.2.3 FTIR 表征进行定性分析
图 4 为4 种方法制得样品的FTIR 图谱.从图4 可知,样品a 在波数3 450.62 cm-1附近的宽吸收带对应为H2O(3 400~3 500 cm-1)中O-H 的拉伸模式[3,28-29].在波数为1 039.50、603.20、565.96 cm-1附近检测到PO43-基团的伸缩振动峰,表明样品中含有HA,这与XRD 分析结果一致[3,19,28-29].样品b在波数3 446.40 cm-1处的吸收峰为H2O 的特征峰.在1 038.44、603.89、567.06 cm-1处是PO43-官能团的特征峰[3,30].在1 420.66、874.53、711.98 cm-1处为CaCO3中CO32-的特征吸收峰[22].出现这些峰的原因可能是实验过程中吸收了空气中的CO2,使磷酸盐被碳酸盐替换;抑或CaCO3未反应完全[31].样品c 在波数为3 571.92 cm-1处的吸收峰对应HA 中-OH 产生的伸缩振动峰[32].在3 469.74 cm-1处的吸收峰为H2O 中O-H 的特征峰.而在1 046.66、602.61、570.66 cm-1处的吸收峰是HA中PO43-的特征峰[29,32-33].在1 419.98、1 091.07、874.78、711.94 cm-1处为CaCO3红外光谱吸收峰.根据文献[22]的研究结果判断为方解石CaCO3,这与XRD判断一致.样品d在波数3467.75cm-1处的吸收峰为H2O 的 O-H 特征峰.1 047.72、1 091.53、962.35 cm-1处的吸收峰为P-O 的伸缩振动峰[31],在603.23、570.38 cm-1处为O-P-O 的弯曲振动峰[34].参考文献[22]研究结果,在1 421.01、874.60、847.56、712.05 cm-1处出现明显的CaCO3的CO32-特征峰.CaCO3的振动吸收峰强度大,即大部分CaCO3未转化成HA[28],这与XRD 的分析结果一致.
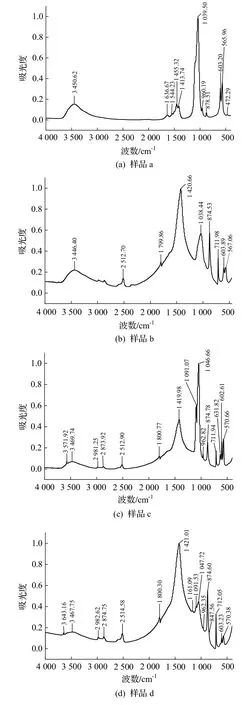
图4 4 种方法制得样品的FTIR 图谱
2.2.4 BET 表征产物介孔结构
图 5 和图6 为4 种方法制得样品的BET 图谱.

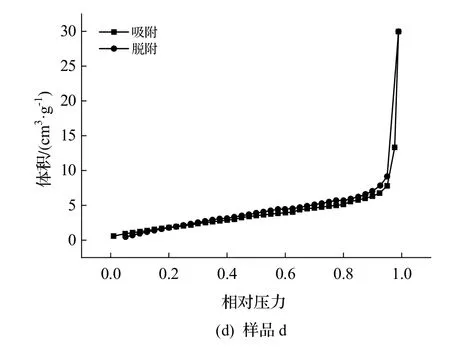
图5 4 种方法制得样品的氮气吸附-脱附等温曲线


图6 4 种方法制得样品的孔径分布
从图5 和图6 可知,4 种样品均出现明显的回滞环,吸附-脱附等温曲线属于Ⅳ型等温线[35].在接近饱和蒸气压P0时出现急剧上升,这是介孔结构的特征[1].
4 种样品的BET 表征数据见表2.从表2 可知,4 种样品的比表面积大小为:样品a>样品c>样品b>样品d;孔体积大小为:样品a>样品c>样品d>样品b;孔径大小为:样品b>样品a>样品c>样品d;平均孔径大小为:样品a>样品c>样品d>样品b.综上表明:样品a 的介孔结构和比表面积较好,更有利于吸附重金属、有机物以及药物等.
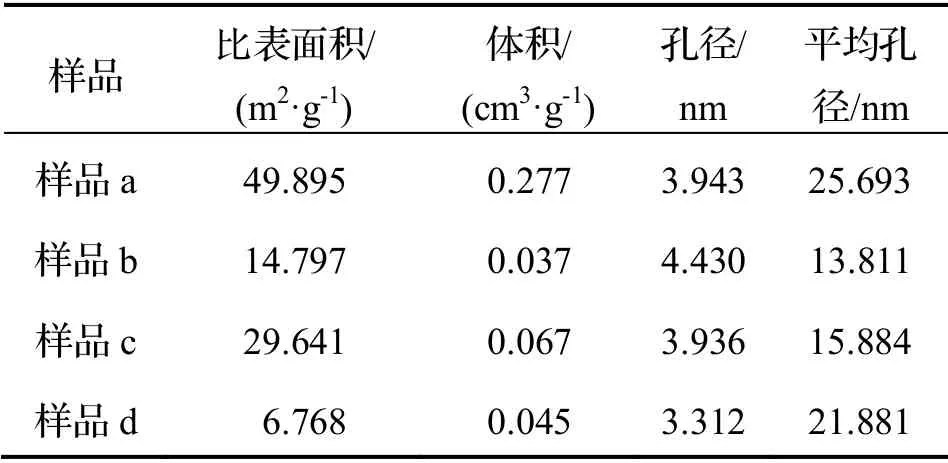
表2 4 种方法制得样品的BET 表征数据
2.2.5 ICP 表征测定元素含量
通过表3 数据计算可知,样品a 中的钙磷比为1.84.XRD 和FTIR 表征结果表明:样本a 全部为HA,推测样品a 的HA 为缺磷型羟基磷灰石[36].样品b 的钙磷比为9.62,样品c 的钙磷比为5.81,样品d 的钙磷比为5.70,假设这3 种样品中的羟基磷灰石为普通型,钙磷比为1.67,3 种样品中CaCO3转化为HA 的程度由大到小依次为:样品d>样品c>样品b.
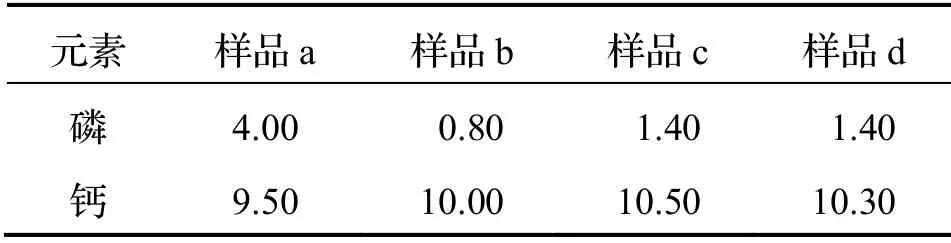
表3 4 种样品中钙磷元素含量 mg·L-1
通过ICP-OES 表征测得样品a、样品b、样品c 和样品d 在相同条件下吸附的银含量的质量分数分别为3.62%、3.24%、1.00%和0.93%.计算可知:样品a 的吸附率为75.10%,样品b 的吸附率为66.95%,样品c 的吸附率为20.20%,样品d 的吸附率为18.75%.吸附力从大到小排序为:样品a>样品b>样品c>样品d,样品a 的吸附率最大,即羟基磷灰石比CaCO3/HA 复合材料的负载量多.在加入钙磷比1.67 且采用水热法制备HA 的条件下,贻贝壳AgHAp 粉体的银含量略优于陈华军等[37]用钙磷盐制备的AgHAp 粉体的银含量,验证了有关生物来源的HA 较化学合成HA 具有相互交通的空间网状结构的结论[20].
3 结论
(1)舟山市贻贝壳中的 CaCO3为方解石型,EDS 分析得出其安全性良好,无有害金属,确定贝壳制备HA 方案安全可行.
(2)以贻贝壳为钙源时用水热法易合成出HA多孔微球,反应完全;用沉淀法、CTAB 模板剂法和反相微乳液法易合成出方解石型CaCO3/HA复合材料.
(3)HA 多孔微球比方解石型CaCO3/HA 复合材料的比表面积和孔径结构更优异,有利于合成更多特殊功能的复合材料.
(4)水热法制备的贻贝壳HA 载银的质量分数为3.62%,吸附率达75.10%,吸附作用略优于化学合成HA,且成本低,可实现贻贝壳的高值化利用.
