丹皮酚对格氏沙雷菌群体感应现象及生物被膜形成的影响
2021-09-09刘景云李婷婷王当丰杨亚茹励建荣王明丽周小敏郭晓华
刘景云,李婷婷,王当丰,杨亚茹,励建荣*,谢 晶,王明丽,周小敏,郭晓华
(1 渤海大学食品科学与工程学院 生鲜农产品贮藏加工及安全控制技术国家地方联合工程研究中心 辽宁锦州 121013 2大连民族大学生命科学学院 辽宁大连 116600 3 江南大学食品学院 江苏无锡 214122 4 上海海洋大学食品学院 上海 201306 5 蓬莱京鲁渔业有限公司 山东烟台 265600 6 浙江兴业集团有限公司 浙江舟山 316120 7 山东美佳集团有限公司 山东日照 276800)
格氏沙雷菌(Serratia grimessi,SG-05),肠杆菌科沙雷菌属,革兰阴性菌,是一种常见的食源性病原菌。SG-05 广泛分布于水、土壤和动植物中,能分泌蛋白酶、核酸酶等胞外物质,造成水产品等高蛋白食品的腐败变质。从淡水鱼类和海水鱼类的腐败微生物中均能分离到沙雷氏菌[1]。如Christensen 等[2]从腐败牛奶中分离出变形斑沙雷氏菌,并证明该菌能够分泌N-酰基高丝氨酸内酯类(N-Acyl-homoserine lactone,AHLs)信号分子。
群体感应(Quorum sensing,QS)是细菌内或细菌间进行信息交流的通讯机制,细菌通过自身合成并释放到胞外的信号分子或者与之共存的细菌产生的信号分子感知周围环境变化,同时启动相关基因的表达调节细菌群体行为[3-5]。如生物被膜的形成、毒力因子的表达。Liu 等[6]发现液化沙雷氏菌QS 相关基因编码的内酯酶能降解自身合成的AHLs 信号分子,进而影响液化沙雷氏菌的黏附和生物被膜的形成。Srinivasan 等[7]研究了蒌叶提取物植醇对黏质沙雷氏菌群体感应AHLs 介导的毒力因子和生物被膜的抑制作用,发现黏质沙雷氏菌的毒力因子表达和生物被膜形成均受到QS 系统的调控,且植醇能有效干扰QS 系统,进而调控毒力因子的表达。
群体感应抑制剂(Quorum sensing inhibitors,QSIs),是一种通过干扰或者抑制QS 现象阻碍细菌信息交流,且不对细菌正常生长产生影响的物质[8]。相比于传统的食品保鲜剂,QSIs 不会杀死病原菌,而是通过QS 系统干扰病原菌生物被膜的形成和致腐基因的表达,最终影响细菌间的生物行为。筛选QSIs 作为食品保鲜剂是控制食品腐败的有效策略之一。孙晓佳[9]通过富马酸钠抑制了水产品优势腐败菌荧光假单胞菌的QS 现象,为控制水产品腐败过程提供了新思路。中草药是筛选QSIs的重要宝库,目前部分中草药粗提物被证明有抑制QS 系统的能力[10-11]。中草药成分复杂,何种有效成分能发挥抑制QS 现象的作用,研究者尚未给出明确的解释。丹皮酚,又称牡丹酚,是一种从牡丹的干燥根皮提取的活性成分。药理研究表明丹皮酚有抗菌、镇痛、抗氧化、抗心律失常和心脑血管保护作用[12-13]。吴晓慧等[14]发现经磺化的丹皮酚对苹果斑枯病菌和玉米纹枯病菌均有显著地抑制作用。李学鹏等[15]发现丹皮提取物和茶多酚联用对冷藏大菱鲆鱼肉的腐败过程有减缓作用,使鱼肉品质得到保持。然而,丹皮提取物成分多样,不能确定发挥抑制作用的单一化合物,这增加了后期研究其抑制机制的难度。
本文以丹皮酚(丹皮提取物的主要成分)为研究对象,研究了丹皮酚对格氏沙雷菌QS 和生物被膜形成的抑制作用,以期增加丹皮酚的实际利用价值,同时也为中草药来源的活性物质作为水产品保鲜剂提供理论支持。
1 材料与方法
1.1 菌种与试剂
格氏沙雷菌,分离自腐败大菱鲆。生物报告菌株紫色杆菌 (Chromobacterium violaceum 026,CV026),该菌株携带有硫酸卡那霉素抗性,本身不会产生AHLs 信号分子,能够感知环境中的AHLs,产生紫色菌素,显现紫色反应。检测AHLs信号分子类型为C4-HSL~C8-HSL。以上2 种菌株均保藏于渤海大学水产品贮藏加工研究所。
丹皮酚(纯度99%)、脱脂奶粉,上海源叶生物科技股份有限公司;LB 肉汤、LB 营养琼脂、琼脂粉、蛋白胨、胰蛋白胨,北京索莱宝科技有限公司;硫酸卡那霉素、结晶紫、冰乙酸、氯化钠、十二烷基磺酸钠(Sodium dodecyl sulfate,SDS),上海阿拉丁生化科技有限公司;AHLs 信号分子标准品(C4-HSL,C6-HSL,C8-HSL,C10-HSL,C12-HSL,C14-HSL),美国Sigma 公司;正丁醇、浓硫酸、苯酚,上海迈瑞尔化学技术有限公司;D(+)-葡萄糖,上海麦克林生化科技有限公司;载玻片、盖玻片 江苏飞舟玻塑有限公司;锌片,上海迈砷化工有限公司;硫酸肼,生工生物工程(上海)股份有限公司。
1.2 仪器与设备
W-CJ-2FD 超净工作台,苏州安泰空气技术有限公司;MS105UD 电子分析天平,瑞士梅特勒-托利仪器有限公司;立式压力蒸汽灭菌锅,上海申安医疗器械厂;imark 酶标仪,美国BIO-RAD 公司;LRH 系列生化培养箱,上海一恒科技有限公司;Biofuge Stratos 冷冻高速离心机,美国Thermo Fisher 公司;Nikon80i 显微镜,日本尼康公司;SS-4800 场发射扫描电子显微镜,日本日立公司;Czone 系列抑菌圈测定及菌落计数仪,杭州迅数科技有限公司。
1.3 方法
1.3.1 最小抑菌浓度确定及QSIs 检测 参照刘胜帅等[16]的方法略加修改。通过牛津杯打孔法测定丹皮酚对SG-05 的最小抑菌浓度。将菌种CV026 和SG-05 过夜活化,28 ℃、160 r/min 培养至OD600nm为1 左右。分别以1∶100 的接种比接种于LB 营养琼脂中,待LB 营养琼脂凝固后用牛津杯打孔,将预先配制好的不同质量浓度丹皮酚(1,2,4,6,8 mg/mL)加入孔中,添加去离子水作为空白对照。平板置于28 ℃生化培养箱中静置培养48 h,肉眼观察抑菌圈情况,并记录抑菌圈直径大小。
将CV026 过夜活化至OD600nm为1 左右,以1∶100 的比例接种于LB 营养琼脂中混匀后倒板,待其凝固后牛津杯打孔。将预先配制的丹皮酚(500,250,125,62.5 μg/mL)加入孔中,以去离子水作为空白对照,以20 μg/mL C6-HSL 为阳性对照组。平板置于28 ℃生化培养箱中静置培养48 h,肉眼观察抑制紫色菌素情况。
1.3.2 紫色菌素产量测定 参照Ganesh 等[17]的方法略加修改。将CV026 过夜活化,以1∶100 的比例接种于10 mL LB 肉汤中,添加丹皮酚使其终质量浓度分别为500,250,125,62.5 μg/mL。以去离子水为空白对照,C6-HSL 信号分子 (终质量浓度为20 μg/mL)为阳性对照,28 ℃、160 r/min 摇床培养48 h。
取300 μL 培养后的菌液于1.5 mL 离心管,室温下加入150 μL 10% SDS 裂解15 s,裂解后加入600 μL 正丁醇提取紫色菌素5 s。最后于8 000 r/min 离心5 min,并在波长595 nm 下测定上清液吸光度。
1.3.3 丹皮酚对SG-05 信号分子产量的影响参考梅永超等[18]的方法进行AHLs 粗提液制备。将SG-05 过夜活化至OD600nm为1 左右,以1∶100 比例接种于10 mL LB 肉汤中,添加丹皮酚使其终质量浓度分别为500,250,125,62.5 μg/mL,以去离子水作为空白对照,20 μg/mL 的C6-HSL 信号分子为阳性对照,28 ℃、160 r/min 振荡培养48 h。以转速10 000 r/min 离心15 min,将上清液取出,加入等体积经过冰乙酸酸化的乙酸乙酯提取2 次,向提取液中加入适量的无水硫酸钠。旋转蒸发去除乙酸乙酯,取1 mL 甲醇溶解残留物,-20 ℃保存待用。
LB 营养琼脂中以1∶100 比例接种过夜活化的CV026,倒平板,待琼脂凝固后用预先灭菌好的牛津杯打孔。分别取200 μL 上述保存的AHLs 粗提液打入孔中,28 ℃生化培养箱静置培养48 h,观察并测定紫色菌素直径大小。
制备以甲醇为溶剂的6 种AHLs 标准品的混合溶液,利用GC-MS 检测各类信号分子标准品的保留时间,同时测定上述AHLs 粗提液中的信号分子类型与产量。测定参数参考冯杰[19]的方法。
1.3.4 丹皮酚对SG-05 胞外蛋白酶活性的影响将过夜活化的SG-05(OD600nm为1 左右)以1∶100比例分别接种于含有丹皮酚(500,250,125,62.5,0 μg/mL),和C6-HSL(终质量浓度20 μg/mL)的肉汤中,28 ℃、160 r/min 振荡培养12 h。用无菌滤器将各菌液过滤,取滤液待用。
参照Sacherer 等[20]的培养基配方,配制牛奶琼脂固体培养基,使用牛津杯打孔,向孔中加入200 μL 滤液。平板置于生化培养箱中,培养条件为28 ℃、24 h。以平板中透明圈直径来反映胞外蛋白酶的产量。
1.3.5 丹皮酚对SG-05 群集的影响 参照Li等[21]的方法,配制群集培养基。配方为:0.5% D-(+)葡萄糖、1%蛋白胨、0.5%琼脂粉、0.5%氯化钠。将5 μL 过夜活化的SG-05 (OD600nm为1 左右)打在含有不同丹皮酚质量浓度的群集培养基上,待其风干后置于生化培养箱中在28 ℃培养48 h 后,测量运动直径,并且以添加去离子水和C6-HSL 为空白和阳性对照。
1.3.6 丹皮酚对格氏沙雷菌SG-05 胞外多糖的影响 参考Kalpana 等[22]的方法。将盖玻片为载体的生物被膜培养后(处理条件与1.3.7.2 节相同),取出盖玻片用500 μL 0.9% NaCl 冲洗,加入等体积的5%的苯酚,培养5 min 后,再加入5 倍体积的含有0.2%硫酸肼的浓硫酸溶液,黑暗中反应1 h 后,10 000 r/min 离心10 min,上清液在波长490 nm 处测定吸光度。
1.3.7 丹皮酚对SG-05 生物被膜的影响
1.3.7.1 丹皮酚对SG-05 生物被膜形成量的影响
参考付娇娇等[23]和Lipsy 等[24]的方法并稍加修改。
将过夜活化的SG-05(OD600nm为1 左右)以1∶100 的比例接种于LB 肉汤,加入终质量浓度为500,250,125,62.5 μg/mL 的丹皮酚,以去离子水为空白,C6-HSL 信号分子作阳性对照。取1 mL 培养后的菌液分装于无菌离心管中,在28 ℃下静置培养48 h。取培养液测定波长595 nm 下的菌液密度后,弃去离心管中的培养液,用无菌水清洗,风干30 min 后添加1 mL 0.2%结晶紫染色20 min。弃染液,用无菌水冲洗3~5 次,直至冲洗的无菌水干净透明,而后利用33%冰乙酸将固着在管壁的染色液溶解后,使用酶标仪测定溶解液在波长595 nm 下的吸光度,并通过公式计算生物被膜的相对形成量。计算公式[18]如下:

式中,OD595nm处理组——丹皮酚处理后测得的结晶紫溶解液的OD595nm值;OD595nm空白对照组——添加去离子水后测得的结晶紫溶解液OD595nm值。
1.3.7.2 丹皮酚对SG-05 生物被膜形态的影响
参考严羽萍等[25]的方法并稍加修改。
1)光学显微镜分析 使用前,将载玻片置于无水乙醇和去离子水中先、后超声30 min,干燥灭菌后备用。无菌培养皿中加入10 mL 含有不同质量浓度丹皮酚 (500,250,125,62.5 μg/mL)的LB肉汤,并以1∶100 比例接种SG-05,混合均匀后静置于28 ℃生化培养箱72 h。以去离子水和C6-HSL 信号分子为空白和阳性对照。
2)扫描电子显微镜分析 将锌片用抛光机除去表面的氧化层,而后剪切成10 mm×10 mm 大小的正方形,置于无水乙醇和去离子水中先、后超声30 min,烘干后灭菌备用[18]。后续操作与光学显微镜相同。培养后将锌片取出,用无菌水冲洗3~5次后置于4 ℃预冷的2.5%戊二醛溶液中浸泡4 h,而后用50%,70%,80%,90%乙醇进行梯度洗脱,100%无水乙醇脱水2 次,乙酸异戊酯置换2次。干燥后喷金处理进行扫描电子显微镜的观察[26]。
2 结果与分析
2.1 最小抑菌浓度的确定及QSIs 检测结果
通过牛津杯打孔法确定丹皮酚对CV026 和SG-05 的最小抑菌浓度。当丹皮酚质量浓度为1~8 mg/mL 时,丹皮酚对CV026 和SG-05 的最小抑菌浓度分别是1 mg/mL 和2 mg/mL。综合考虑,选取亚抑菌浓度为0.5 mg/mL。试验中选取丹皮酚质量浓度为500,250,125,62.5 μg/mL 进行后期试验。从图1可以看出添加丹皮酚的孔周围有不透明的抑紫圈出现,初步表明丹皮酚没有抑制CV026 正常生长,但具有抑制CV026 产生紫色菌素的能力,说明了丹皮酚能干扰生物报告菌株CV026 的QS 系统,进而影响紫色菌素的产量。

图1 丹皮酚对CV026 产紫色菌素的抑制性Fig.1 Inhibition effect of paeonol against the secretion of violacein from CV026
2.2 紫色菌素产量测定结果
如图2所示,当生物传感器CV026 处于亚抑菌浓度下时,紫色菌素的产量因丹皮酚质量浓度的增加而明显下降,而CV026 的菌液密度几乎不受影响。与空白对照组(去离子水)相比,丹皮酚质量浓度为500 μg/mL 时,紫色菌素的产量下降近57.95%。结果表明,亚抑菌浓度下,丹皮酚能在不影响CV026 正常生长的前提下,通过干扰CV026的QS 系统进而抑制CV026 产生紫色菌素的能力。这充分表明了作为中草药来源的丹皮酚提取物的主要成分丹皮酚对抑制CV026 产生紫色菌素有良好的效果。同样,Odilon[27]研究发现经100 μg/mL 的五倍子和黄连处理的CV026,其紫色杆菌素产量分别下降了50.44%和34.50%。
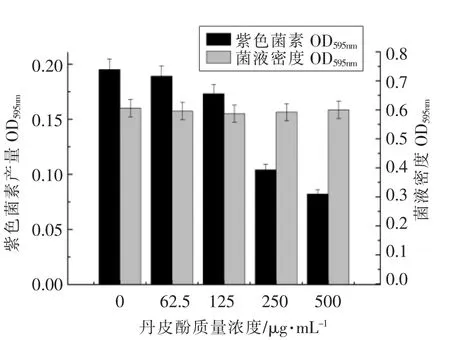
图2 不同质量浓度丹皮酚对CV026 产紫色菌素和菌液密度的影响Fig.2 Effects of different mass concentration paeonol on the production of violacein and bacterial density of CV026 strain
2.3 丹皮酚对SG-05 信号分子产量的影响
在外源短链AHLs 类信号分子存在的前提下,紫色杆菌CV026 产生紫色圈的直径大小能间接地衡量SG-05 AHLs 的产量。如图3a所示,经丹皮酚处理后,紫色圈直径下降。随着丹皮酚质量浓度的增加,紫色圈直径呈下降趋势。图3b 表示不同质量浓度丹皮酚处理后紫色圈的直径大小。由图可知,经500 μg/mL 丹皮酚处理的紫色圈直径抑制率为17.43%。当添加外源信号分子C6-HSL 后紫色圈直径增加,这间接表明丹皮酚能干扰紫色杆菌CV026 的QS 系统,最终影响紫色菌素的产量。

图3 丹皮酚对SG-05 分泌AHLs 的影响Fig.3 Effects of paeonol on the secretion of AHLs in SG-05
6 种AHLs 标准品的出峰时间和顺序如图4所示,信号分子混合标准品分离效果明显。C4-HSL,C6-HSL,C8-HSL,C10-HSL,C12-HSL,C14-HSL,分别在保留时间4.408,6.254,8.305,10.685,13.374,16.882 min 出现特征峰。混合标准品的出峰时间与孙晓佳等[5]的结果一致。由图5可知,菌株SG-05 的乙酸乙酯提取物经GC-MS 分析可在C6-HSL 和C10-HSL 处出现特征峰,表明两者为SG-05 产生的主要信号分子。李婷婷等[28]发现格氏沙雷菌能诱导根癌农杆菌(Agrobacterium tumefaciens)A136 水解5-溴-4-氯-3-吲哚基-β-D-半乳糖苷(X-gal)产生蓝色。这与GC-MS 分析SG-05 能产生长链信号分子C10-HSL 的结果一致。图6所示为GC-MS 分析得到的C6-HSL 和C10-HSL 2 种主要信号分子经不同质量浓度丹皮酚处理后的含量变化。经丹皮酚处理后,信号分子峰面积下降。该结果与本试验中紫色菌素抑制试验的结果相一致,进一步表明丹皮酚能有效地降低SG-05 分泌信号分子的能力,推测这可能是丹皮酚能作为QSIs 降低信号分子的活性,进而影响信号分子的产量。Ding 等[29]通过分子模拟和GCMS 分析发现苯甲醇能抑制荧光假单胞菌P07 信号分子产量。

图4 GC-MS 测定AHLs 混合标准品Fig.4 The mixture of different AHLs standards detected by GC-MS

图5 GC-MS 测定SG-05 的信号分子种类及含量Fig.5 Types and contents of AHLs in SG-05 detected by GC-MS
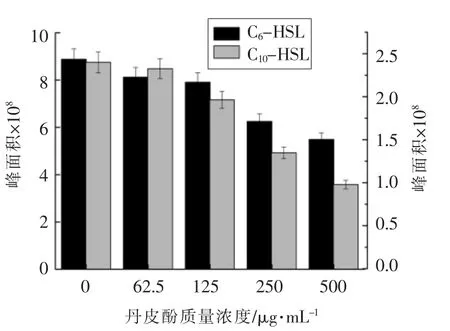
图6 丹皮酚对SG-05 分泌AHLs 的影响Fig.6 Effects of paeonol on the secretion of AHLs in SG-05
2.4 丹皮酚对SG-05 胞外蛋白酶活性的影响
胞外蛋白酶能快速分解鱼类蛋白质导致鱼类腐败变质,因而胞外蛋白酶是检验水产品新鲜度的重要指标。Abinaya 等[30]研究发现从拟南芥分离到的3,5,7-三羟基黄酮具有干扰铜绿假单胞菌产生胞外蛋白酶的能力。Zhou 等[31]研究表明黏质沙雷氏菌胞外蛋白酶的分泌量受到AHLs 介导的QS 系统的调控。本试验通过SG-05 在牛奶琼脂平板上产生透明圈直径的大小作为检验其产生胞外蛋白酶能力的标准,结果如图7所示。由图可知,相比空白对照组,添加丹皮酚能显著降低蛋白酶水解圈直径的大小,且丹皮酚质量浓度和蛋白酶水解圈直径的大小呈负相关。并且,当向培养基中补充外源信号分子C6-HSL 时,蛋白酶的水解透明圈直径明显增大,表明SG-05 分泌蛋白酶的能力能够受到QS 系统的调控,上述试验结果表明丹皮酚处理能干扰该系统进而抑制蛋白酶水解圈直径的大小。

图7 丹皮酚对SG-05 胞外蛋白酶的影响Fig.7 Effects of paeonol on extracellular protease activity of Serratia grimessi
2.5 丹皮酚对SG-05 群集现象的影响

图8 丹皮酚对SG-05 群集运动的影响Fig.8 Effect of paeonol on swarming motility of Serratia grimessi
鞭毛介导的群集运动能力能调节SG-05 和接触面(如食品机械表面)的附着能力,且通过形成生物被膜促进食品污染。因此,本文研究了丹皮酚对SG-05 群集能力的影响。表1所示为不同质量浓度丹皮酚处理SG-05 迁移直径的大小和群集能力的抑制率。经500 μg/mL 丹皮酚处理后,SG-05的迁移能力被显著抑制,其抑制率高达50.94%。这表明丹皮酚干扰了SG-05 鞭毛介导的迁移能力。与添加去离子水相比,添加终质量浓度为20 μg/mL C6-HSL 后,SG-05 群集的直径有所增加,这表明外源信号分子C6-HSL 能促进格氏沙雷菌的群集能力,进一步表明SG-05 鞭毛介导的群集能力可能受到AHLs 介导的QS 系统调控。Asif等[32]研究异腈官能团修饰的酪氨酸对铜绿假单胞菌QS 系统和群集能力的影响,发现添加外源的、经异腈功能修饰的酪氨酸后,铜绿假单胞菌能通过增强鼠李糖脂的产量或通过QS 系统间接增强铜绿假单胞菌的群集能力,与本文研究结果具有一致性。
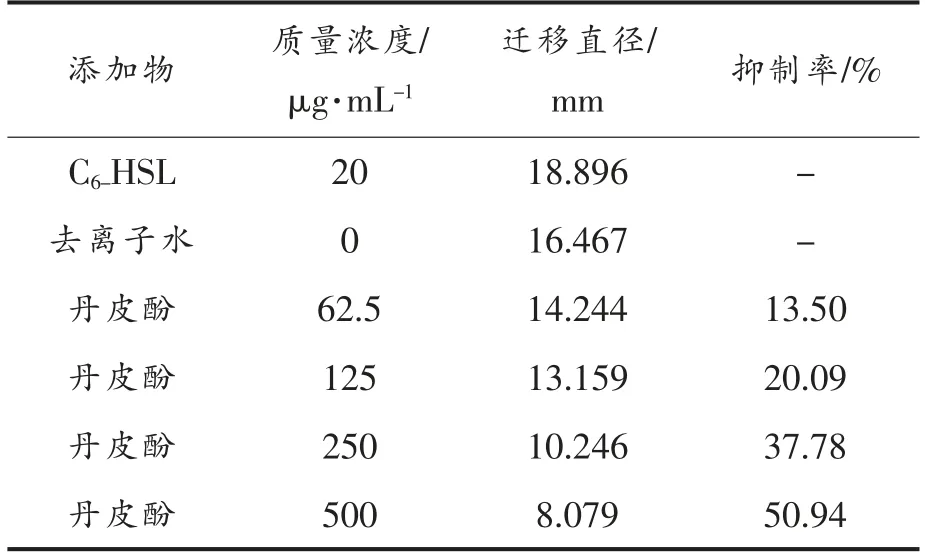
表1 丹皮酚对SG-05 群集运动直径的影响Table 1 Effect of paeonol on swarming motility diameters of Serratia grimessi
2.6 丹皮酚对SG-05 胞外多糖的影响
SG-05 自身能够分泌包括蛋白质、核酸、多糖等胞外多聚物,而这种胞外多聚物的聚集有利于其生物被膜在初级阶段的形成及黏附。研究表明,胞外多糖是细菌生物被膜的重要成分,在保持其内聚力、获取营养和阻止抗生素进入细胞等方面发挥重要的作用[33]。Zhou 等[31]发现大麦芽碱能干扰黏质沙雷氏菌的QS 系统,进而影响黏质沙雷氏菌胞外多糖的形成。表2所示为丹皮酚对SG-05胞外多糖的影响。由表可知,丹皮酚对SG-05 胞外多糖的产生具有质量浓度依赖性抑制作用。经500 μg/mL 丹皮酚处理时,SG-05 胞外多糖的抑制率高达44.35%。该结果与本试验中丹皮酚对SG-05 生物被膜形成量的抑制结果一致,进一步证实了胞外多糖在生物被膜形成中的重要作用。

表2 丹皮酚对SG-05 胞外多糖的影响Table 2 Effect of paeonol on exopolysaccharides in Serratia grimessi
2.7 丹皮酚对SG-05 生物被膜的影响
2.7.1 丹皮酚对SG-05 生物被膜形成量的影响生物被膜是由相关微生物细胞组成的复杂结构。一般情况下,生物膜具有三维结构,拥有充足的通道和孔隙,以此实现细胞间的相互作用和生物群落状态的维持[34]。生物被膜的形成是一个高度自发的过程,在此过程中细菌生长和消亡交替是进行的,并且随着生存环境的变化发生动态变化,一般将其分为5 个阶段:定殖阶段、可逆吸附阶段、不可逆吸附阶段、生物膜形成阶段、脱落阶段。Singh 等[35]研究了QS 系统和生物被膜间的关系,发现从微生物代谢物中提取获得的某些物质可以干扰QS 系统,进一步影响细菌生物被膜形成能力。因此,本文基于QS 机制,通过丹皮酚作用抑制SG-05 生物被膜的形成。
酶标法被广泛应用于测定微生物生物被膜的相对形成率,其吸光值的相对下降量可反应丹皮酚对SG-05 生物被膜形成率的抑制程度。如图9所示,在亚抑菌浓度下,随着丹皮酚质量浓度的升高,SG-05 生物被膜相对形成率呈下降趋势,与此同时,菌液密度几乎呈现平稳状态,表明亚抑菌浓度下格氏沙雷菌的正常生长几乎不受影响。与空白对照组(生物被膜相对形成率为100%)相比,经500 μg/mL 丹皮酚处理后样品的生物被膜相对形成率仅为48.89%,而添加信号分子C6-HSL 时,其生物被膜相对形成率高达113.74%,表明丹皮酚可能通过干扰AHLs 介导的QS 系统调控SG-05 生物被膜的形成,这与李学鹏等[36]的研究结果基本一致。

图9 丹皮酚对SG-05 生物被膜相对生成率的影响Fig.9 Effects of paeonol on biofilm relative formation rate of SG-05
2.7.2 丹皮酚对SG-05 生物被膜形态的影响 通过光学显微镜和电子扫描显微镜研究丹皮酚对SG-05 生物被膜形态的影响,其结果如图10a所示,经过结晶紫染色后的菌体成紫色片状分布,随着信号分子C6-HSL 的添加,紫色成片的膜状物有叠加的效果,即观察到有层次感。相比于空白对照组,丹皮酚处理后,载玻片表面仅有少量菌体聚集,片状膜状物相对减少。随着丹皮酚质量浓度的增加,载体表面膜状物呈浓度依赖性降低,这与Li等[37]研究的香兰素对蜂房哈夫尼亚菌生物被膜形态的影响具有一致性。
由图10b 可知,相比于空白对照组,添加信号分子C6-HSL 后锌片表面形成的生物被膜浓厚且致密,这表明SG-05 生物被膜的形成可能受到AHLs 介导的QS 系统的调控。Thomson 等[38]研究表明QS 机制控制着病原菌毒力因子和生物被膜的表达。丹皮酚处理后,锌片上形成的生物被膜稀疏松散,仅有少量的菌体聚集,这与光学显微镜的分析结果一致。这2 种生物被膜形态分析均表明丹皮酚能抑制SG-05 生物被膜的形成,这可能是丹皮酚影响了细菌菌体的聚集和相连或者使其生物被膜断裂,最终影响生物被膜的形成。

图10 丹皮酚对SG-05 生物被膜影响的光学显微镜图(a)和扫描电子显微镜图(b)Fig.10 Optical microscopic images(a)and scanning electron microscopic images(b)of effects of paeonol on biofilm of Serratia grimessi
3 结论
近年来,以中草药成分作为QSIs 的研究成为干扰或阻碍QS 途径的主要方向之一。文章以紫色杆菌CV026 为报告菌株检测SG-05 群体感应现象,进一步探究了丹皮酚对SG-05 群体感应表型的影响。当500 μg/mL 丹皮酚处理后,紫色圈直径抑制率为17.43%,GC-MS 分析结果也表明丹皮酚能显著降低SG-05 中C6-HSL 和C10-HSL 产量;胞外蛋白酶也受到抑制作用;群集运动性和胞外多糖产生量抑制率分别为50.94%和44.35%。此外,丹皮酚降低了生物被膜相对生成率,破坏了生物被膜结构。综上,丹皮酚作为丹皮主要成分,能通过干扰格氏沙雷菌SG-05 群体感应系统,进而抑制其腐败表型。
