多发性骨髓瘤合并肾透明细胞癌一例
2021-09-05王天钰杨敏
王天钰,杨敏
遵义医科大学附属医院血液内科,贵州 遵义563003
多发性骨髓瘤(multiple myeloma,MM)是一种单克隆浆细胞来源的恶性肿瘤[1],相关医学统计资料显示,其发病率达3/10万,约占血液系统肿瘤的10%[2],其最常见的并发症之一为肾脏损害,约一半的患者在多发性骨髓瘤首发时就会表现出肾脏的受累[3]。肾细胞癌(renal cellcarcinoma)亦被简称为肾癌,占成人恶性肿瘤的2%~3%,其中90%为透明细胞癌,我国肾癌的发病率逐年上升[4]。既往已有文献报道过多发性骨髓瘤合并肾癌的病例,一方面,多发性骨髓瘤患者免疫系统受损,易导致肾癌的发生;另一方面,多发性骨髓瘤患者应用烷化剂化疗,烷化剂的用量与肾癌的发生也有联系[5-6],但这种病例并不常见。本文回顾性分析了1例多发性骨髓瘤继发肾癌患者的临床资料,同时结合文献进行讨论,现报道如下:
1 病例简介
患者女性,55岁,2019年7月因体检发现肾功能异常就诊于我院,行骨髓象检查示(图1):幼稚浆细胞11.5%,成熟浆细胞1.0%,形态学特征与多发性骨髓瘤相符。血清蛋白电泳(图2):白蛋白,40.50;α1球蛋白,4.70;α2球蛋白,6.00;β球蛋白,3.00;β球蛋白2,1.50;γ球蛋白,44.30;β2微球蛋白,2 098 5.00 ng/mL;免疫球蛋白:免疫球蛋白G,63.00 g/L;免疫球蛋白A,0.09 g/L;免疫球蛋白M,0.45 g/L;补体C3,0.58 g/L;免疫球蛋白E,9.51 IU/mL;补体C4,0.036 g/L。血清游离lambda轻链6 700 mg/L,血尿游离kappa轻链183 mg/L,血尿游离lambda轻链10 250 mg/L;血清免疫固定电泳:SP(+),IgG(+),λ(+),结合各项检验结果,明确诊断为多发性骨髓瘤,并开始规律予以BD方案1个疗程、BLD方案6个疗程、LD方案1个疗程化疗,经治疗患者肾功能得到改善,但多发性骨髓瘤相关指标无明显好转。于2020年3月返院化疗时行腹部彩超发现左肾占位,在回顾了患者发病以来的所有影像学资料后,笔者确定这是新的病灶,进一步完善了双肾CT平扫+增强示(图3):左肾Ca,透明细胞型;约40 mm×45 mm。左肾包块穿刺病理诊断(图4):考虑左肾透明细胞癌。免疫组化:(左肾)透明细胞癌(Fuhrman I级),免疫组化结果示:Vimentin(+);CA9(+);P504s(+);RCC(-);CK7(-);CD117(-);TFE3(-)。该患者多发性骨髓瘤和肾透明细胞癌均已诊断明确,由于患者行手术治疗风险大,暂不适宜行肾脏肿块切除术,故继续予以BLD方案、伊沙佐米、沙利度胺联合脂质体多柔比星化疗。目前患者病情趋于稳定,肾脏占位未见明显增大,定期规律化疗中。
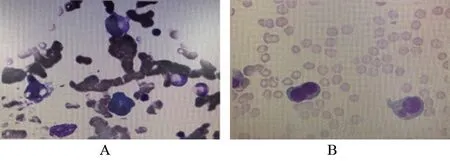
图1 骨髓象示形态学与多发性骨髓瘤相符(×1 000)
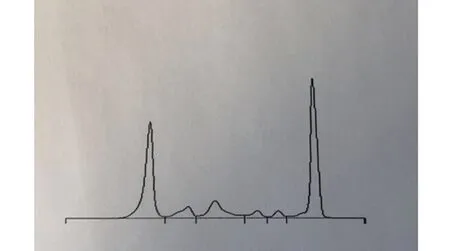
图2 血清蛋白电泳
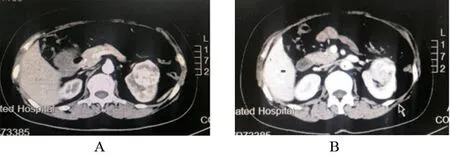
图3 腹部增强CT,考虑肾癌

图4 左肾包块穿刺病理结果示,透明细胞癌(Fuhrman I级)
2 讨论
多发性骨髓瘤是世界上第二大常见的血液恶性肿瘤,特征为免疫球蛋白水平升高,临床上常以肾功能损害或骨痛为首发表现,治疗上常采用化疗、造血干细胞移植或分子靶向治疗。肾透明细胞癌(renal clear cell cancer,RCCC)是肾恶性肿瘤中最常见的类型,占肾癌的70%~80%,治疗上常采用手术治疗。在本例病例中,患者最先是以肾功能异常就诊,行骨髓涂片提示原幼浆细胞占比高,浆细胞系增生,左肾包块穿刺病理结果示符合肾透明细胞癌表现,该患者多发性骨髓瘤合并肾透明细细胞癌诊断明确。尽管多发性骨髓瘤合并肾透明细胞癌并不常见,但这两种恶性肿瘤的发病率高于预期。OJHA等[7]认为,这两种疾病的关联是双向性的,他们收集了1973—2006年波士顿Dana-Farber癌症研究所中多发性骨髓瘤和肾癌患者的病例资料,其中,34 156例多发性骨髓瘤患者中有69例继发了肾细胞癌,该研究表明,多发性骨髓瘤患者继发肾细胞癌的可能性是其他人群的1.51倍。CHOUEIRI等[8]回顾了美国俄亥俄州克利夫兰诊所1990—2005年提供的两个关于多发性骨髓瘤和肾癌患者们的综合数据库,进行分析后得出结论,在同一患者中,多发性骨髓瘤合并肾癌的发生率高于预期。BHANDARI等[9]也在600例浆细胞发育不良患者的机构数据库中发现有6例患者继发了肾细胞癌。另外,KURTZ等[10]进行相关病例分析研究后得出结论,肾癌合并多发性骨髓瘤的发病率达2.3%。这些只是过去几十年里关于这两种恶性肿瘤共存的其中一部分案例,从这些数据可以看出,多发性骨髓瘤和肾癌间确实存在着某种联系,这为本例病例提供了流行病学史支持,也从流行病学史的基础上证明了本例多发性骨髓瘤合并肾癌的病例并非偶然。
但是,到目前为止,其发病原因尚不明确,有人认为第一种肿瘤的治疗如化疗等可能会造成机体免疫系统损伤,甚至导致染色体的畸变,这可能是第二肿瘤发生的原因之一;也有人认为第二肿瘤的发生可能与家族遗传影响、生物环境等因素有关[11]。本病例于10+年前诊断为梅尼埃病,该病的发病机制与免疫反应学说、染色体异常学说、机体功能紊乱学说均密切相关。另外,该患者在发现肾脏占位前已进行过多个疗程的化疗,可能导致机体免疫系统遭到损伤,甚至发生了染色体的畸变,进而增加了第二肿瘤的发生机率。流行病学研究发现,高体重指数及吸烟易诱发多种肿瘤,包括多发性骨髓瘤、肾癌及胃癌的单独或者同时发生[12]。除了发病因素的高度相似外,细胞因子学说也在被广泛的提及,在多发性骨髓瘤与肾癌常见的病理生理学机制中,白细胞介素-6(IL-6)的分泌均能对其肿瘤细胞的生长及增殖发挥作用,一种恶性肿瘤会分泌像IL-6或TNF-α这样的肿瘤刺激激素,这可能会增加第二种恶性肿瘤的风险。SAKAI等[13]曾报道过多发性骨髓瘤合并肾癌患者手术切除肾脏占位后,多发性骨髓瘤的相关指标得到明显改善,且其IL-6水平明显降低。OZTURK等[14]还指出了IL-6在这种共存病例中的重要性,他们还提供了一些多发性骨髓瘤和肾细胞癌共存的案例,在这些案例中,患者IL-6水平明显升高。另一个可能学说为NF-κB信号通路学说,肾癌的特点之一是其肿瘤细胞拥有丰富的血管,大量研究表明,其生长、进展及转移主要依赖新生血管生成及NF-κB的激活[15],高度活跃的NF-κB与肾癌的进展密切相关[16]。笔者未来或许可以将NF-κB激活途径的关键环节作为RCCC新的治疗靶点,因为RCCC细胞对蛋白酶抑制剂的敏感性可以通过降低NF-κB的活性得到提高。化疗药物在骨髓瘤细胞中也是通过抑制血管内皮生长因子的表达发挥作用,从而抑制骨髓瘤细胞的生长及其血管的形成,扰乱骨髓瘤细胞内的微环境,进而诱导骨髓瘤细胞的凋亡,同时也能抑制转录因子NF-κB的活性,抑制细胞增殖、阻滞细胞周期、促进细胞凋亡[17]。换言之,肾癌和多发性骨髓瘤均能通过NF-κB信号通路激活其肿瘤细胞,而化疗药物反过来也能通过NF-κB信号通路抑制其肿瘤细胞的增殖,故针对肾癌合并多发性骨髓瘤的患者,选择能阻碍NF-κB信号通路的化疗药物能有效的抑制两种肿瘤的发生与发展。
通过本报道及文献复习,所有临床医生都应该注意到,这两种恶性肿瘤是可以共存的,且这两种恶性肿瘤的发生率超出了预期,第一肿瘤后的化疗相关、环境、遗传或免疫介导等因素都可以解释这一关联。尽管其作用机制需要进一步深入研究,但在今后的诊断或随访时,应注意这两种疾病组合的可能性,应该进行更加系统、全面的检查,提高对同一患者患两种肿瘤的警惕性。
