干蟾皮炮制前后两种毒性成分的含量比较*
2021-09-04傅兴圣
周 谧,朱 琳,傅兴圣
1 南通市食品药品监督检验中心,南通 226006;2 三明市尤溪县中医医院,福建三明365000
干蟾皮为蟾蜍科动物中华大蟾蜍Bufo bufo gargarizans Cantor 的干燥皮[1]。干蟾皮辛、凉,有毒,具有清热解毒、利水消胀之功效,临床用于治疗小儿疳积、咽喉肿痛、肿瘤;外治痈肿疔疮。干蟾皮的化学成分较复杂,主要含有蟾蜍毒素,为多种强心甾体化合物的总称,在干燥加工过程中分解为蟾毒配基类成分,主要包括华蟾酥毒基、脂蟾毒配基、蟾毒灵、日蟾毒它灵等,具有一定的毒性[2]。临床大多使用其炮制品,以砂炒为主,炮制后毒性降低,但缺乏炮制降毒机理的研究支持。前期曾采用高效液相色谱法对干蟾皮和炒干蟾皮中的华蟾酥毒基、脂蟾毒配基、蟾毒灵、日蟾毒它灵、沙蟾毒精等5 种毒性成分进行测定,其中华蟾酥毒基、脂蟾毒配基这两种成分含量较高,分离效果较好;而蟾毒灵、日蟾毒它灵、沙蟾毒精这3 种成分在炒干蟾皮中的含量极低,难以进行比较。本文采用高效液相色谱法对华蟾酥毒基、脂蟾毒配基这两种主要毒性成分进行含量测定[3,4],比较干蟾皮炮制前后两种成分含量的变化,同时综合分析炮制后毒性降低的机理。
1 仪器与药品、试剂
Ulimate 3000 型双三元高效液相色谱仪(美国Thermo Fisher Scientific 公司);CP225D 电子分析天平(德国Sartorius 公司)。
脂蟾毒配基对照品(批号:110718-201108)、华蟾酥毒基对照品(批号:110803-200605)均为中国药品生物制品检定所提供;蟾毒灵(批号:CAS#465-21-4 W05D6Z7090)为上海倍卓科技公司提供;甲醇、乙腈为色谱纯,其余试剂为分析纯;水为纯化水。
本实验共收集了10 批生品(产地:S1、S2、S8 为南通如东,实地收集:S3~S7、S9、S10 为安徽亳州药材市场)和8 批炮制品(产地:C1、C2、C8 为安徽亳州药材市场,C3 为南通如东,实地收集:C4、C7 为南通市精华制药,C5 为南通市三越中药饮片公司,C6为江苏华康中药饮片公司),经由南通市食品药品监督检验中心龚旭东主任中药师鉴定确认。
2 方法与结果
2.1 样品的炮制
干蟾皮饮片(生品):取原药材,除去杂质及灰屑,切去头爪,切成小块或片,洗净,干燥。制干蟾皮饮片(砂炒):取砂子置锅内,用武火炒热后加入净干蟾皮块,拌炒至焦黄发泡时,取出,筛去砂子,放凉[5]。饮片见图1。

图1 干蟾皮样品图
2.2 色谱条件
色谱柱:DIKMA C18(4.6×250 mm,5 μm);流动相:乙腈-0.5%磷酸二氢钾(50∶50)(用磷酸调节pH值3.2);柱温:30 ℃;检测波长:296 nm;流速:1.0 mL·min-1;进样量:20 μL。
2.3 溶液的制备
2.3.1 对照品溶液精密称取华蟾酥毒基、脂蟾毒配基对照品各10 mg,分别置于100 mL 量瓶中,用甲醇溶解并稀释至刻度,摇匀,作为对照品贮备液。分别精密吸取贮备液各5 mL,置同一50 mL 量瓶中,加甲醇稀释至刻度,摇匀,滤过,取续滤液,即得。
2.3.2 供试品溶液取干蟾皮粉末(粗粉)约1.5 g,精密称定,置具塞锥形瓶中,精密加入甲醇50 mL,称定重量,超声振荡处理(功率500 W,频率40 kHz)30 min,放冷,再称定重量,用甲醇补足减失的重量,摇匀,滤过,取续滤液,即得。
2.3.3 空白溶液取甲醇作为空白溶液,按“2.2”项下色谱条件进行测定,结果显示,空白溶液在与华蟾酥毒基、脂蟾毒配基对照品色谱峰保留时间处无色谱峰,表明空白溶剂对测定没有干扰。
2.4 方法学验证
2.4.1 系统适用性要求理论板数按华蟾酥毒基峰计算应不低于10000,相邻色谱峰之间分离度均符合要求。见图2。

图2 高效液相色谱图
2.4.2 线性关系制备分别精密吸取“2.3.1”对照品溶液适量,配制成华蟾酥毒基浓度分别为1.02、2.04、5.09、10.18、25.44、50.88 μg·mL-1,脂蟾毒配基浓度分别为0.97、1.94、4.85、9.71、24.27、48.54 μg·mL-1的系列混合对照品溶液,分别进样20 μL,记录峰面积,以浓度(μg·mL-1)为横坐标X,以峰面积(mAu)为纵坐标Y,绘制标准曲线。华蟾酥毒基回归方程为Y=11.203X+0.022,r=0.9999;脂蟾毒配基回归方程为Y=10.895X-0.151 5,r=0.999 9。结果表明,华蟾酥毒基对照品浓度在1.02~50.88 μg·mL-1、脂蟾毒配基对照品浓度在0.97~48.54 μg·mL-1呈现良好的线性关系。
2.4.3 进样精密度试验取一定浓度的对照品溶液20 μL,连续进样6 次,记录峰面积。结果华蟾酥毒基峰和脂蟾毒配基的峰面积RSD 分别为0.21%、0.42%。
2.4.4 稳定性试验取同一份干蟾皮供试品溶液(S2),分别于0、1、2、4、6、12、24、36、48 h 进样20 μL,华蟾酥毒基和脂蟾毒配基峰面积的RSD 分别为0.42%和0.67%,表明供试品溶液在48 h 内稳定。
2.4.5 专属性考察在“2.2”项色谱条件下,华蟾酥毒基、脂蟾毒配基均峰形良好,无杂质干扰,保留时间分别为12.6 min、13.5 min。
2.4.6 重复性试验取同一批干蟾皮供试品(S8)1.5 g,共6 份,分别精密称定,依法制备供试品溶液,按“2.2”项下色谱条件测定。结果华蟾酥毒基含量的RSD 为1.45%,脂蟾毒配基含量的RSD 为2.34%。
2.4.7 加样回收率试验精密称取已知含量的干蟾皮样品(S2)0.75 g,共9 份,按低、中、高浓度(每个浓度3 份,低、中、高浓度分别为0.8∶1、1∶1、1∶1.2)分别加入三个浓度的混合对照品溶液,按“2.3”项下的方法制备供试品溶液,按“2.2”项下色谱条件进样测定,计算加样回收率,结果见表1。注:华蟾酥毒基平均回收率:99.49%,RSD 2.64%;脂蟾毒配基平均回收率:97.30%;RSD 1.85%

表1 华蟾酥毒基和脂蟾毒配基加样回收率试验结果(n=9)
2.4.8 耐用性试验选择不同厂家色谱柱(DIKMA C18,250mm×4.6mm,5μm;Waters C18,250mm×4.6mm,5 μm 和Merck C18,150 mm×4.6 mm,5 μm)及不同型号的高效液相色谱仪(戴安Ulimate3000 双三元;岛津LC-20A 和安捷伦1200)测定各供试品,结果显示,不同厂家色谱柱和不同型号的仪器均能对样品进行较好分离,适用性良好。
2.5 样品测定
分别取不同产地的10 批生品(S1~S10)和8 批炮制品(C1~C8),按“2.3”项下的方法制备供试品溶液,进样高效液相色谱仪,测定华蟾酥毒基和脂蟾毒配基的色谱峰面积,用线性关系计算含量,以干燥品计,结果见表2。
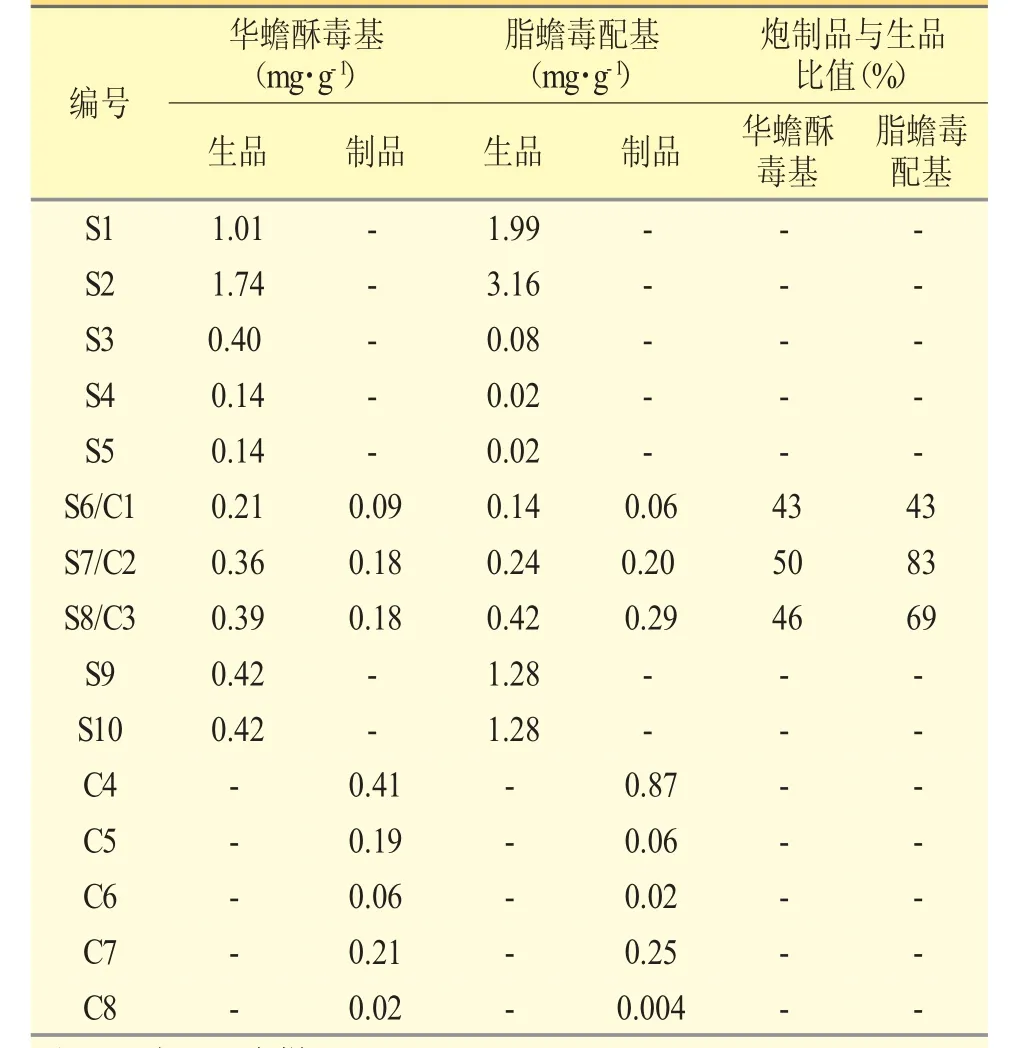
表2 干蟾皮样品来源及含量测定结果
3 讨论
在10 批干蟾皮生品和8 批干蟾皮炮制品中,2种成分的含量差异较大,表明干蟾皮的质量参差不齐;干蟾皮药材S1、S2 为产地采集,2 项指标均高于市场收集批次,差异明显;制干蟾皮饮片C4、C7 为南通市精华制药生产,2 项指标均高于其他收集批次,差异明显。在干蟾皮生品中,华蟾酥毒基的含量为0.14~1.74 mg·g-1,均值为0.53 mg·g-1;脂蟾毒配基的含量为0.02~3.16 mg·g-1,均值为0.75 mg·g-1;制蟾皮中华蟾酥毒基的含量为0.02~0.41 mg·g-1,均值为0.17 mg·g-1;脂蟾毒配基的含量为0.004~0.87 mg·g-1,均值为0.22 mg·g-1。检测表明,在炮制品中,2 种毒性成分的含量低于生品。此外,有3 批生品(S6、S7、S8)委托南通市三越中药饮片公司炮制,生品与相应炮制品测定结果显示,2 种毒性成分经过炒制均呈不同程度的降低,华蟾酥毒基平均下降46%,下降程度在批间相差不大;脂蟾毒配基平均下降65%,下降程度在批间相差很大。逻辑性的表明,炒制后毒性降低。
干蟾皮药材有着较好的疗效,但也存在一定的毒性作用,通过炮制,则可降低其毒性,保证使用后既达到应有的疗效,又不致产生不良反应。华蟾酥毒基和脂蟾毒配基既是毒性成分,也是药效成分。通过对炮制前后干蟾皮中的这2 种毒性成分的比较研究,炮制后其含量有不同程度的降低,与干蟾皮炮制减毒的目的相符。干蟾皮炮制减毒的机理之一是通过砂炒加热,使毒性成分含量下降。本实验首次开展的干蟾皮炮制减毒机理研究,为干蟾皮安全有效、稳定可控应用提供理论基础。
