3D可视化技术辅助腹腔镜下巨大肾上腺肿瘤切除术的临床研究*
2021-09-01刘建宋擎添张波甘宇李冰晟陈志何垚
刘建,宋擎添,张波,甘宇,李冰晟,陈志,何垚
(1.华中科技大学协和深圳医院泌尿外科,广东深圳518052;2.中南大学湘雅医院泌尿外科,湖南长沙410008)
腹腔镜下肾上腺肿瘤切除术是肿瘤直径≤6 cm肾上腺肿瘤治疗的金标准。然而,国内外对于较大的肾上腺肿瘤,特别是肿瘤直径>6 cm 的巨大肾上腺肿瘤,是行腹腔镜下肾上腺肿瘤切除术,还是行开腹手术具有一定争议[1]。若行腹腔镜手术,手术具体应该选择哪种入路,这一点上还未达成共识[1]。
3D 可视化技术是近年来才出现的新技术。该技术利用术前的影像学图像合成3D 影像数据,帮助医生直观地了解肿瘤的大小、形态及位置、与邻近器官及大血管的关系,有助于术前制定最优的手术计划。虽然国内外有少量文献报道3D 可视化技术在腹腔镜下肾上腺肿瘤切除术中的应用[4-7],但是这些文献报道的肾上腺肿瘤相对较小,且几乎没有文献报道3D 可视化技术辅助腹腔镜在肿瘤直径>6 cm 的巨大肾上腺肿瘤切除术中的作用,而对3D 可视化技术对不同手术入路影响的报道更是完全缺失。
1 资料与方法
1.1 一般资料
回顾性分析2018年7月—2021年3月在中南大学湘雅医院行腹腔镜下巨大肾上腺肿瘤切除术的54 例患者的临床资料,根据其术前是否行3D 可视化技术重建分为3D 可视化组(31 例)和CT 组(23 例)。纳入标准:术前完善泌尿系B 超、CT 等检查,确诊为肾上腺肿瘤,且影像学显示肿瘤直径>6 cm。排除标准:肿瘤直径≤6 cm、双侧肾上腺肿瘤、恶性肿瘤病史、手术禁忌证、肾上腺与肾脏手术史。
3D 可视化组嗜铬细胞瘤16 例,皮质腺瘤3 例,髓质脂肪瘤3 例,肾上腺囊肿3 例,节细胞神经瘤2 例,皮质腺癌2 例,神经鞘瘤1 例,淋巴瘤1 例。其中21 例患者行经后腹腔途径入路腹腔镜下巨大肾上腺肿瘤切除术,另外10 例患者行经腹腔途径入路。CT 组嗜铬细胞瘤13 例,髓质脂肪瘤4 例,皮质腺瘤2 例,节细胞神经瘤2 例,神经鞘瘤1 例,肾上腺囊肿1 例。其中18 例患者行经后腹腔途径入路腹腔镜下巨大肾上腺肿瘤切除术,另外5 例患者行经腹腔途径入路进行手术。两组患者性别、年龄、BMI、患侧、手术入路、肿瘤直径比较,差异无统计学意义(P>0.05),具有可比性。见表1。
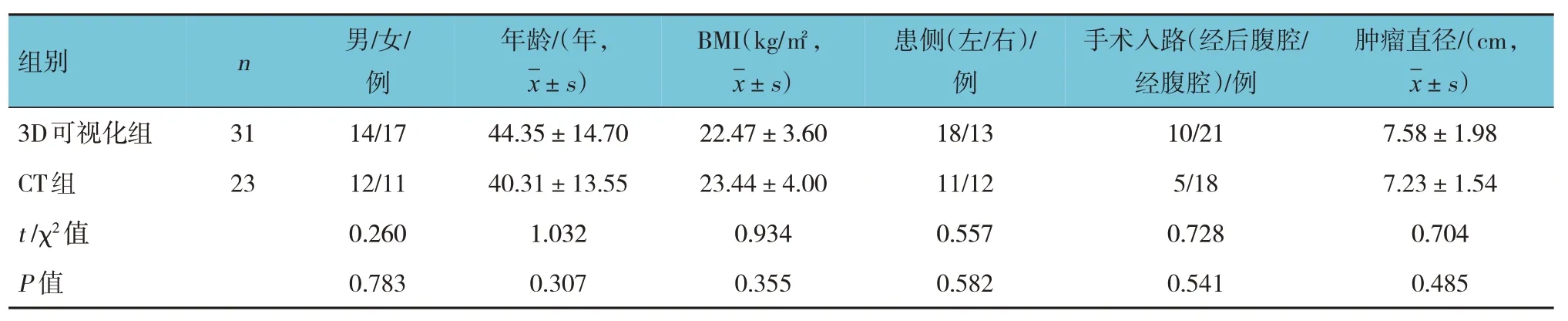
表1 两组患者一般资料比较
1.2 CT扫描和3D重建
3D 可视化组与CT 组患者术前均行增强CT 扫描(包括动脉期、实质期和排泄期)。将3D 可视化组患者的CT 图像数据输入医学3D 成像系统(深圳市旭东数字医学影像技术有限公司)建立3D 可视化模型,并使用E3D3D 数字云平台观看。该3D 可视化模型使用不同的颜色来区分各种结构如肿瘤、肾上腺、肿瘤周围重要器官及各大血管走行等。术者可以通过旋转、放大、删除和透明化来获得更好的视觉效果。见图1。
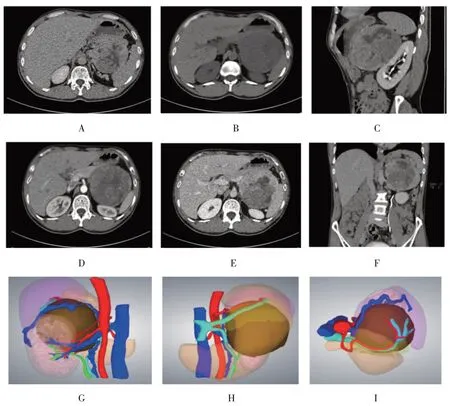
图1 巨大肾上腺肿瘤的CT和3D可视化技术图像
1.3 手术方法
1.3.1 经后腹腔行腹腔镜下肾上腺肿瘤切除术麻醉生效后,患者患侧卧位,升高腰桥,摆折刀位。于腋后线12 肋缘下、腋中线髂棘上2 cm 及腋前线肋缘下留置套管针,手扩法加球囊扩张器建立后腹腔,气腹建立后维持压力14 mmHg。置入腹腔镜监视器及操作器械。游离腹膜后脂肪,进一步扩大腹膜后间隙。纵行打开肾周筋膜,游离肾周脂肪,显露并游离患侧肾上极。术中根据3D 可视化模型明确术中解剖结构,精准找到肾上腺肿瘤,进一步游离并离断肿瘤,将肿瘤置入标本袋并取出,检查肿瘤完整。仔细检查创面,及时创面止血。
1.3.2 经腹腔行腹腔镜下肾上腺肿瘤切除术麻醉生效后,取健侧斜卧位,背部与床位面呈45°角,患侧腰背部略垫高。脐部健侧弧形切口切开皮肤及皮下组织,建立人工气腹。置入10 mm 套管针及30°腹腔镜。检查无明显器官损伤,再分别于左侧麦氏点、锁骨中线脐部水平线交叉点及交叉点上5 cm处置入套管针。进入腹腔找到患侧结肠,沿患侧结肠旁沟打开腹膜,向内侧适当游离结肠,使结肠自然下垂并导向内侧,缓慢游离患侧肾脏周围组织与器官,显露患侧肾周脂肪。继续游离患侧肾上极,根据3D 可视化模型明确术中解剖结构的位置,仔细将其与患侧肾脏游离后进一步游离并离断肿瘤,将肿瘤置入标本袋并取出,检查肿瘤完整。仔细检查创面,及时止血。
1.4 统计学方法
数据分析采用SPSS 26.0 统计软件。计量资料以均数±标准差(±s)表示,比较用t检验;计数资料以构成比表示,比较用χ2检验。P<0.05 为差异有统计学意义。
2 结果
2.1 两组患者术中及术后情况
两组患者均顺利完成手术,无中转开腹手术。无明显围手术期并发症,术后随访1~33 个月,中位随访时间15 个月,随访期间无明显术后并发症。两组患者的肿瘤直径、术中出血量比较,经t检验,差异无统计学意义(P>0.05)。两组患者的术后住院时间和手术时间比较,差异有统计学意义(P<0.05),3D 可视化组短于CT 组。见表2。
表2 两组患者术中及术后恢复情况比较 (±s)
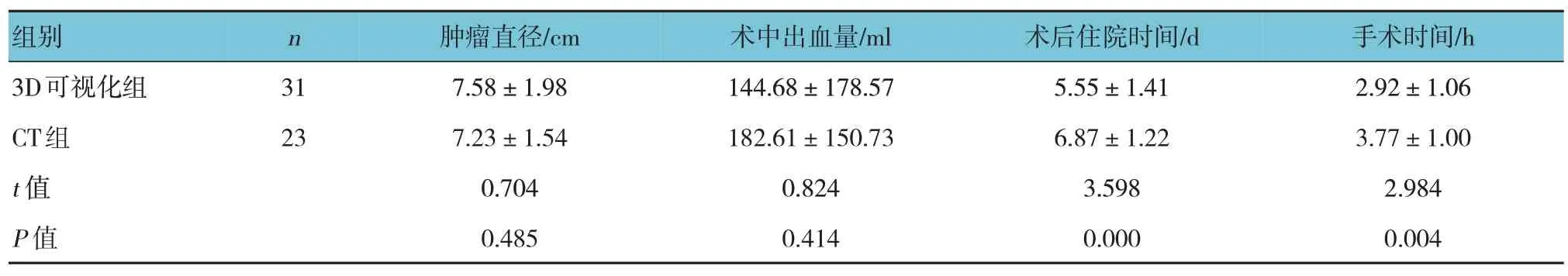
表2 两组患者术中及术后恢复情况比较 (±s)
组别n 肿瘤直径/cm 术中出血量/ml 术后住院时间/d 手术时间/h 3D可视化组31 23 CT组t 值P 值7.58±1.98 7.23±1.54 0.704 0.485 144.68±178.57 182.61±150.73 0.824 0.414 5.55±1.41 6.87±1.22 3.598 0.000 2.92±1.06 3.77±1.00 2.984 0.004
2.2 两组经后腹腔途径入路患者术中及术后恢复情况
两组患者的肿瘤直径比较,经t检验,差异无统计学意义(P>0.05)。两组患者的术中出血量、术后住院时间和手术时间比较,差异有统计学意义(P<0.05),3D 可视化组优于CT 组。见表3。
表3 两组经后腹腔途径入路患者术中及术后恢复情况比较 (±s)
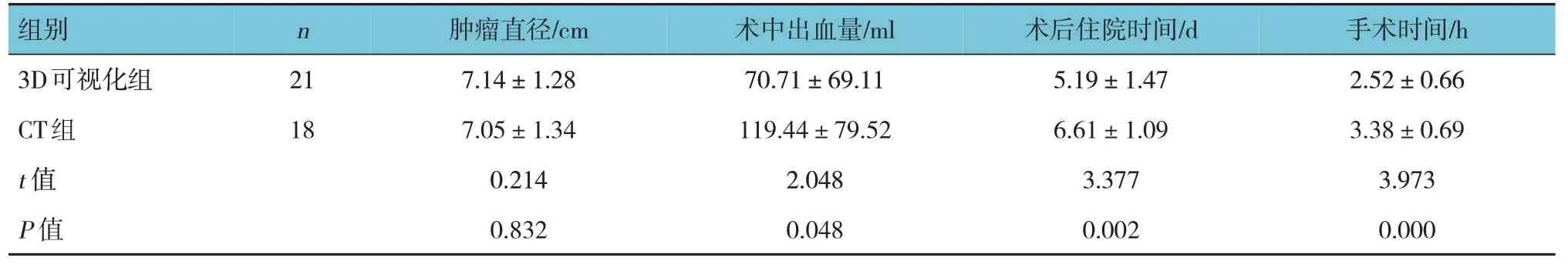
表3 两组经后腹腔途径入路患者术中及术后恢复情况比较 (±s)
组别n 肿瘤直径/cm 术中出血量/ml 术后住院时间/d 手术时间/h 3D可视化组CT组t 值P 值21 18 7.14±1.28 7.05±1.34 0.214 0.832 70.71±69.11 119.44±79.52 2.048 0.048 5.19±1.47 6.61±1.09 3.377 0.002 2.52±0.66 3.38±0.69 3.973 0.000
2.3 两组经腹腔途径入路患者术中及术后恢复情况
两组患者的肿瘤直径、术中出血量比较,经t检验,差异无统计学意义(P>0.05)。两组患者的术后住院时间和手术时间比较,差异有统计学意义(P<0.05),3D 可视化组短于CT 组。见表4。
表4 两组经腹腔途径入路患者术中及术后恢复情况比较 (±s)
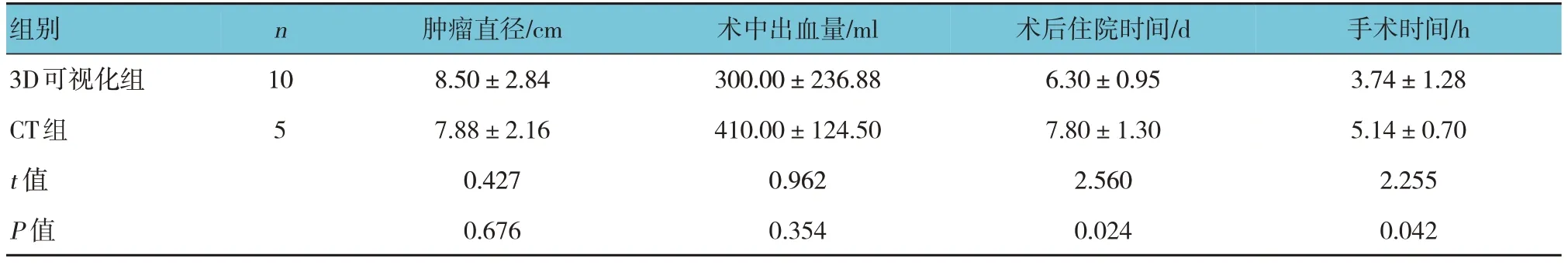
表4 两组经腹腔途径入路患者术中及术后恢复情况比较 (±s)
组别n 肿瘤直径/cm 术中出血量/ml 术后住院时间/d 手术时间/h 3D可视化组CT组t 值P 值10 5 8.50±2.84 7.88±2.16 0.427 0.676 300.00±236.88 410.00±124.50 0.962 0.354 6.30±0.95 7.80±1.30 2.560 0.024 3.74±1.28 5.14±0.70 2.255 0.042
3 讨论
随着影像诊断技术的不断发展与普及,肾上腺肿瘤的检出率逐年升高,临床上发现的巨大肾上腺肿瘤也越来越多[8]。对巨大肾上腺肿瘤,腹腔镜手术主要为经腹腔途径与经后腹腔途径两种手术入路[9]。两种入路各有其优缺点,其中经后腹腔入路的优点包括入路直接,可以较快地游离到肾上腺,减少内脏器官的游离,解剖结构熟悉,术后疼痛轻等[10];其劣势为后腹腔空间狭小[11],过于巨大的肾上腺肿瘤会占满整个视野,导致其游离困难。而经腹腔途径入路的优点包括空间较大,便于处理相对较大的瘤体,必要时易于改为开腹手术,而缺点为术后肠道功能恢复较慢,术后腹壁切口可能形成切口疝等。
3D 可视化技术是一种能帮助外科医生在术前轻松获取大量信息的技术。过去外科医生通常依靠影像学检查,如CT 在脑中自行构建术中的解剖情况,从而计划手术过程。然而,对于巨大肾上腺肿瘤患者,由于手术部位解剖结构复杂,二维图像一般不足以成功传达结构细节。而3D 可视化技术可以直观地显示肿瘤的大小、位置、形态、血管走行及与周围邻近器官的毗邻关系,实现个性化的术前计划[12-13]。很多肾上腺肿瘤具有内分泌功能,因此术中分离肾上腺区部位需要更加轻柔准确。例如嗜铬细胞瘤作为临床上非常常见的肾上腺区巨大占位[14-15],一旦受到刺激很容易在术中释放大量的儿茶酚胺[16-17],引发血压剧烈波动。因此需要外科医生熟知解剖结构,精细操作,精准定位[18-19]。而帮助外科医生熟知解剖结构,精准定位正是3D 可视化最有价值的地方。
根据回顾性分析结果发现,3D 可视化技术在缩短术后住院时间和手术时间方面起到了积极作用。不论是在经腹腔途径还是后腹腔途径,3D 可视化技术都表现出了其在手术治疗中的作用。3D可视化技术辅助经后腹腔的巨大肾上腺肿瘤切除术能更好地缩短术后住院时间和手术时间,减少术中出血量。这可能是因为经后腹腔途径空间较小,常规CT 下医生只能了解肿瘤周边组织器官的大概位置,需要在巨大肾上腺肿瘤的干扰下完成游离并离断肿瘤供应血管,而3D 可视化技术能帮助医生迅速定位肿瘤位置及周围组织器官情况,做到精准处理[20]。相比之下,经腹腔的巨大肾上腺肿瘤切除术由于空间相对充足,巨大肾上腺肿瘤不会占据过多视野,镜下解剖结构展示相对清楚,所以3D 可视化辅助可能对经后腹腔途径的巨大肾上腺肿瘤切除术效果更好。
国外有学者对3D 可视化技术在胰腺手术上的作用进行了研究,结果表明在诊断方面,3D 可视化技术并不能提高诊断的准确性,但通过运用3D可视化技术,外科医生能在确定肿瘤分期和理解制定手术计划的方面明显获益[21-22]。卓翔等[23]的研究发现,使用3D 可视化技术辅助腹腔镜下肝切除术能够减少术中出血量,缩短手术时间,加速术后恢复。有学者运用3D 可视化技术辅助腹腔镜下肾部分切术处理复杂肾肿瘤,结果表明相对于直接行腹腔镜下肾部分切术,3D 可视化技术的运用可以在术中保留更多的肾实质,且缩短肾动脉阻断时间[24-25]。
对3D 可视化技术辅助腹腔镜下巨大肾上腺肿瘤切除术,笔者的经验是根据3D 可视化技术提供的肿瘤大小及与周围脏器血管的关系,于术前初步制定手术入路及解剖游离方案。当肿瘤<10 cm则多选择经后腹腔途径入路,对于位置较高的肿瘤,特别是右侧肾上腺肿瘤,该入路可较快地找到肿瘤且不需要游离解剖部分腹腔脏器,如肝脏、结肠、十二指肠等。根据3D 可视化技术提供的肿瘤血管供应情况,能精准地游离并结扎肾上腺中央静脉等肿瘤重要血管,并可以较快地将肿瘤完整切除。而当肿瘤>10 cm 或肿瘤与腔静脉、肠系膜上动脉、胰腺、胃、肠道等腹腔器官关系密切时,最好选择经腹腔途径入路。该入路可以提供更大的空间,便于暴露肿瘤,且根据3D 可视化技术提供的肿瘤与周围脏器血管的关系,进行肿瘤与周围脏器的精细游离操作,并对肿瘤血管进行精准结扎、离、断。
本研究存在一定的局限性。病例数较少,特别是行经腹腔途径的巨大肾上腺肿瘤切除术患者数较少。同时未对肿瘤类型进行细分,如功能性肿瘤与非功能肿瘤。随着3D 可视化技术在临床上的进一步开展及运用,可以行多中心前瞻性对比研究进一步评估其应用价值。
综上所述,本研究初步得出3D 可视化技术辅助腹腔镜下巨大肾上腺肿瘤切除术能缩短术后住院时间和手术时间的结论,且经后腹腔途径较经腹腔途径能更好地发挥3D 可视化技术优势。
