无花果叶生物炭对小麦种子萌发与幼苗生长的影响
2021-08-26朱海云张保华
朱海云,张保华
(1.宁夏工商职业技术学院能源化工学院,宁夏银川 750021;2.青岛农业大学新农药创制研究所,山东青岛 266109)
生物炭是指生物质在无氧或缺氧的条件下经过高温热解碳化去除挥发性油和汽后得到具有多孔结构、较高pH 值、强阳离子交换量和较大比表面积的一类稳定、高度芳香化、富含碳素的固态物质[1-2]。由于生物炭的独特结构特征和理化性质,目前在水环境治理[3-4]、土壤修复改良[5]、水土保持[6]、农作物病害控制[7-8]及农业环境[9]等方面得到了广泛应用。
已有研究表明,不同来源生物质及制备条件得到的生物炭具有不同的形貌结构和表面特性[10]。杨放等[11]研究发现,不同热解材料在相同制备温度下得到的生物炭营养元素也有差异。张春燕等[12]以向日葵秸秆、橘皮、泡桐壳、稻壳等不同废弃植物类物质制备生物炭,并对其性能进行对比分析,结果发现,不同植物类生物炭具有不同的成炭率、孔隙率和吸附性能。生物炭作为一种重要的土壤肥力改良剂,在农业领域备受关注,但是由于不同来源的生物炭组成、性能存在差异,造成对作物生长的不同影响,如SPOKAS 等[13]研究发现,生物炭施用到土壤中可以促进植物生长,但另有研究发现,其对植物有一定的生长抑制作用[14],而李阳等[15]研究发现,生物炭对小麦根、芽的生长表现出低剂量促进、高剂量抑制的现象。
无花果(Ficus caricaL.)属于桑科榕属多年生亚热带落叶灌木或小乔木果树[16],是一种营养价值高,且具有一定药效和功能的新型水果[17],也是人类最早栽培的经济树种之一。在我国无花果有2 000 多年的栽培历史[18],据2016年统计结果可知,全国无花果种植面积为5 000 hm2,山东省约占50%,威海市种植面积最大,约有2 000 hm2[19]。随着无花果种植技术的不断提高,其种植面积日益扩大。无花果采摘后,会有大量的叶片无法处理,如何变废为宝,实现资源利用,成为种植户、研究人员和政府关注的问题。如果能利用无花果叶作为生物炭制备原料的来源,则可以减轻因堆积或焚烧废弃物造成的环境污染,同时有利于生物炭在农业种植的循环应用。
本研究基于无花果叶片的资源利用,选择无花果叶作为研究对象,采取不同的热解温度制备生物炭,并以小麦为供试作物进一步探索不同热解温度制备的生物炭及其不同用量对小麦种子萌发、幼苗生长及幼苗抗氧化酶活性的影响,旨在明确无花果叶生物炭对小麦种子萌发及生长的影响,从而为无花果叶生物炭在农业种植及生产中的进一步应用提供参考。
1 材料和方法
1.1 材料与仪器
材料:供试小麦品种为鲁麦15 号,无花果叶采自田间种植园。仪器:Varian640-IR 红外光谱仪(青岛圣中仪器有限公司),JSM-7500F 型扫描电子显微镜(日本电子株式会社),鼓风干燥箱(山东省龙口市先科仪器有限公司)。
1.2 试验方法
1.2.1 生物炭的制备 取无花果叶洗净、烘干,粉碎过筛,将过2 mm 筛后的细粉放置在不锈钢盘子中,并置于鼓风干燥箱中80 ℃干燥4 h。然后将其分装入坩埚,压实、密封,放入马弗炉,真空状态下以10 ℃/min 分别升至碳化温度400、500、600 ℃,灼烧6 h。将制得的生物炭装入干燥密封袋保存待用。
1.2.2 生物炭理化性质 生物炭的pH 值按照生物炭与去离子水为1∶10(固液质量体积比)混合振荡均匀后静置30 min,用pH 计测定;生物炭产率通过碳化处理前后物料质量差进行计算[20];灰分按照参考文献[21]的方法测定。
1.2.3 生物炭的性能表征 采用扫描电子显微镜SEM 观察不同碳化温度制备的无花果叶生物炭的形貌结构。
1.2.4 无花果叶生物炭浸提液制备 分别取0.2、0.6、1.0、2.0 g 的无花果叶生物炭加入100 mL 的去离子水,超声浸提1 h 后抽滤,得到2、6、10、20 g/L浓度的无花果叶生物炭浸提液备用。
1.2.5 小麦发芽与生长试验 选取籽粒饱满的小麦种子,用1%次氯酸钠溶液消毒处理,用自来水冲洗数次,再用纯净水反复冲洗,浸种催芽4 h 备用。将40 粒种子均匀摆放在铺有3 层纱布的9 cm 培养皿中,每天分别加入不同浓度无花果叶生物炭浸提液2 mL,以清水作为对照(CK),每个处理4 次重复。将培养皿置于人工气候箱中[温度(25.0±0.5 ℃;湿度85%;光照12 h,黑暗12 h)]培养。每天统计各处理组发芽种子数;总萌发时间7 d,萌发结束后统计各处理种子根长、芽长。
1.2.6 测量指标及方法 不同无花果叶生物炭处理的小麦幼苗在3 d 时观察发芽(GR)情况,培养7 d时测定根长、芽长、根冠比(地下部分干重与地上部分干重之比)。小麦幼苗生理指标主要测定植株的超氧化物歧化酶(SOD)、过氧化物酶(POD)含量。具体方法参照参考文献[22]。
1.3 数据处理
利用Microsoft Excel 2007 软件对数据进行处理和作图。
2 结果与分析
2.1 无花果叶生物炭特性
由表1 可知,随着碳化温度由400 ℃升高至600 ℃,制备的生物炭产率逐渐减少,从36.21%减少至31.59%,降低4.62 个百分点;pH 值由9.9 增大至11.4,增加1.5;灰分则呈增加的趋势。总体来看,产率、pH 值、灰分3 个指标,处理温度600 ℃与400 ℃差异达显著水平(P<0.05)。pH 值升高的原因可能是生物炭中与有机物结合或络合的矿质元素在裂解过程中逐渐向氧化态和碳酸盐形态转变,而且随着碳化温度升高,转变率升高,从而使生物炭的水溶液呈碱性[23]。
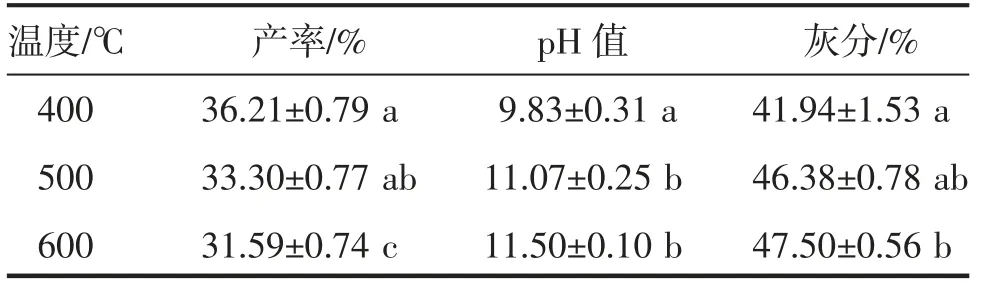
表1 不同温度制备的无花果叶生物炭理化性质
2.2 无花果叶生物炭SEM 分析
不同碳化温度制备生物炭的物理结构及性能也会有所差异[24]。由图1 可知,随着碳化温度由400 ℃升高至600 ℃,制备的生物炭微孔数量增加,多孔结构逐渐凸现,从而提高了生物炭的比表面积和吸附性能,这有利于对化学物质或细菌的吸附和固定[20,25]。

图1 不同处理温度制备无花果叶生物炭的SEM 图
2.3 无花果叶生物炭对小麦生长的影响
由图2 可知,无花果叶生物炭对小麦的萌发均有影响,在浓度为2 g/L 时,3 种生物炭处理的小麦发芽率均高于90%,与对照差异不显著(P>0.05)。随着生物炭浓度的增大,对小麦发芽率的抑制增强,500 ℃和600 ℃处理的生物炭对小麦发芽率的抑制更为明显,600 ℃处理的生物炭在使用浓度为20 g/L时发芽率最低(55%),与对照差异显著(P<0.05)。无花果叶生物炭对小麦的根长促进率和芽长促进率表现出不同的结果,500 ℃和600 ℃处理的生物炭对根长促进率总体要高于400 ℃处理的生物炭,且500 ℃处理的生物炭,根长促进率明显高于其他两种处理,同时,3 种生物炭随着处理浓度的增大根长促进率均呈现先升高后降低的趋势,在生物炭浓度为6 g/L 时,500 ℃处理的生物炭小麦根长促进率最高,达到213.93%。3 种生物炭的芽长促进率也表现出随生物炭浓度的增加而呈现先升高再降低的规律,但600 ℃处理的生物炭芽长促进率在6~20 g/L浓度下要高于其他两种处理,6 g/L 时芽长促进率最高,为52.39%,与400 ℃处理的生物炭差异显著(P<0.05)。不同无花果叶生物炭处理对小麦根冠比的影响表现为低浓度大于高浓度处理,且生物炭处理浓度为2 g/L 时,400 ℃和500 ℃处理的生物炭根冠比分别为0.60 和0.57,与对照相比差异显著(P>0.05)。随着生物炭浓度增大,根冠比逐渐减小,在生物炭浓度为20 g/L 时达到最小值,分别为0.34、0.46、0.41,均低于对照。
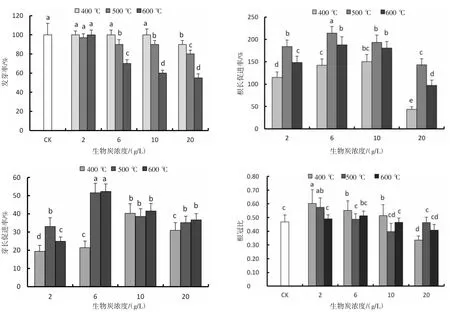
图2 无花果叶生物炭对小麦发芽率、根和芽生长及根冠比的影响
2.4 无花果叶生物炭对小麦幼苗SOD、POD 活性的影响
由图3 可知,400 ℃和500 ℃处理的生物炭随着浓度的提高,小麦幼苗SOD 活性呈现先升高后降低的趋势,400 ℃处理的生物炭在浓度为10 g/L 时小麦幼苗SOD 活性为最大值,为254.36 U/mg,500 ℃处理的生物炭在浓度为6 g/L 时,小麦幼苗SOD 活性达最大值,为231.09 U/mg;600 ℃处理的生物炭对小麦幼苗SOD 活性的影响虽然是随着浓度的增大而呈现先升高后降低的趋势,但降低趋势不明显。400 ℃处理的生物炭对小麦幼苗SOD 活性的影响低于500 ℃和600 ℃处理的生物炭。3 种生物炭对小麦幼苗POD 活性的影响,随着生物炭浓度的增加,400 ℃处理的生物炭小麦幼苗POD 活性先升高后降低,最大值为浓度6 g/L 时,POD 活性为159.60 U/mg,而其他两种生物炭均表现出先升高再降低的变化趋势,尤其是500 ℃处理的生物炭在浓度为2 g/L 时,POD 活性最高达到207.60 U/mg,其后随着生物炭浓度的增加逐渐降低。3 种生物炭在浓度为2 g/L 时,小麦幼苗POD活性与对照差异显著(P<0.05),但其他浓度生物炭,除400 ℃处理的生物炭与对照差异显著(P<0.05),其他均与对照差异不显著(P>0.05)。

图3 无花果叶生物炭浓度对小麦幼苗SOD、POD 活性的影响
3 结论与讨论
碳化温度对生物炭的理化性质有决定作用。本研究通过采取不同的炭化温度制备了无花果叶生物炭,发现随着碳化温度的升高,制备的生物炭多孔结构逐渐丰富,pH 值和灰分随着温度升高而增加,而产率逐渐降低,从400 ℃至600 ℃处理生物炭,产率从36.21%下降至31.59%,pH 值从9.83 升高到11.05,灰分从41.94%增加到47.50%。有研究表明,随着温度的升高,生物质热能反应剧烈,质量损失较多,导致生物炭产率降低[26],而灰分增加,同时灰分中的金属弱酸盐又导致pH 值升高到碱性[23],与本研究结果一致。
本研究发现,无花果叶生物炭对小麦的发芽率影响较大,而且碳化温度越高制备的生物炭影响越显著,在生物炭浓度为20 g/L 时,3 种生物炭与对照差异显著(P<0.05),600 ℃处理的生物炭小麦发芽率仅为55%,远低于对照的发芽率100%,其原因可能是不同温度制备生物炭的pH 值对小麦发芽率的影响不同,而生物炭浓度增大,其培养液的pH 值也会增大,从而影响了小麦的发芽率;也有研究认为是由于生物炭中的重金属等污染物对小麦的发芽和幼苗生长造成影响[27]。随着生物炭浓度的增大,对小麦幼苗根和芽的促进生长作用呈先升高后降低的趋势,400 ℃处理的生物炭根长促进率和芽长促进率整体小于其他两种生物炭,在浓度为20 g/L 时,根长促进率仅为42.12%。研究也发现,根冠比随着浓度的增大而减小,且在20 g/L 时根冠比与对照差异显著(P<0.05),400 ℃处理的生物炭根冠比仅为0.32。之所以出现这种结果,是由于生物炭中的N、P、K 等营养物质的量随着生物炭浓度的增大也会增大,而在低浓度条件下,此类营养物质对根的促进作用高于对芽的促进作用[27],但生物炭高浓度条件下,由于pH 值的增大和有毒污染物的增加,会影响根的生长,从而表现出根长促进率、芽长促进率及根冠比减少的结果[22]。
SOD 活性和POD 活性可以清除植物生长过程中产生的O2-和H2O2等自由基,从而维持植物细胞的自由基处于较低水平,避免活性氧对细胞膜脂的伤害作用[28],这类抗氧化酶可灵敏反映植物对氧化胁迫的响应幅度,从而可以从生化方面评价生物炭对植物生长的影响效应[29]。通过测定小麦幼苗的SOD、POD 活性,发现SOD 活性随着生物炭浓度的增大呈先升高后降低的趋势,而且均与对照差异显著(P<0.05),600 ℃处理的生物炭在浓度为10 g/L时小麦幼苗SOD 活性是对照的2.15 倍;而对POD活性的影响,3 种生物炭的影响规律不尽相同,但在2 g/L 浓度下小麦幼苗POD 活性显著大于对照(P<0.05),随着浓度的增大POD 活性降低,在浓度为20 g/L 时与对照差异不显著(P>0.05)。这种结果的出现可能是由于生物炭低浓度条件下,污染物含量相对较低,从而增强抗氧化酶编码基因的表达,提高了SOD 和POD 的活性,当生物炭浓度增大时,污染物的累积会降低酶活性[30]。
综上研究表明,无花果叶生物炭的不同碳化温度会对小麦萌发和生长有影响,浓度为2~10 g/L 时对小麦的生长有促进作用,20 g/L 时有抑制作用,而生物炭的适宜浓度则有利于小麦根系和茎的生长。因此,在生物炭应用中,不但要考虑制备条件对生物炭性能的影响,还要注意生物炭浓度的不同对作物的生长会产生的促进或抑制作用,有的还会对作物产生毒性,需要通过大量试验确定合适的生物炭及其浓度。
