多西他赛联合卡铂治疗转移性去势抵抗性前列腺癌的临床疗效
2021-08-24白杲琛何志嵩
白杲琛,宋 毅,金 杰,虞 巍,何志嵩
(北京大学第一医院泌尿外科,北京大学泌尿外科研究所,国家泌尿、男性生殖系肿瘤研究中心, 北京 100034)
前列腺癌是男性生殖泌尿系统最常见的恶性肿瘤,发病率在美国高居首位[1]。我国前列腺癌的发病率虽然低于欧美国家,但随着生活方式的改变及检出率的提高,我国前列腺癌的发病率已呈上升趋势[2]。前列腺癌容易发生转移,演变为转移性激素敏感性前列腺癌(metastatic hormone-sensitive prostate cancer, mHSPC),内分泌治疗可以降低体内的雄激素水平,从而控制肿瘤生长,是治疗mHSPC的主要方法,但随着疾病进一步进展,绝大多数患者对内分泌治疗的敏感性变差,从而转变为转移性去势抵抗性前列腺癌(metastatic castration-resistant prostate cancer, mCPRC)。目前,多种药物已经成为mCRPC的一线治疗方案,其中紫杉醇类药物和阿比特龙、恩扎卢胺等新型内分泌药物最先成为治疗mCRPC的重要手段,能够在一定程度上改善患者的生存质量,延长患者的生存期[3],其中多西他赛可以为mCRPC患者带来明确的生存获益,被广泛用于这些患者的一线或二线治疗中[4]。多数患者在进行多周期的多西他赛治疗后容易出现耐药性,肿瘤负荷过大也会对多西他赛的疗效带来不利影响,因此,其他化疗药物越来越多地被应用到临床中。铂类作为一类常用的化疗药物,虽然对于前列腺癌的作用机制仍未明确,但在单药或联合治疗多项临床研究中表现出了一定的疗效和潜力[5-6],可用于肿瘤高负荷或多西他赛抵抗的mCRPC[7]。本项研究的15例mCRPC患者为肿瘤高负荷、预计多西他赛单药治疗效果不佳、或接受了多西他赛治疗后出现了抵抗。我们采用多西他赛联合卡铂治疗,并观察近期疗效及不良反应,以评估该方案的有效性和安全性。
1 资料与方法
1.1 研究对象
回顾性分析北京大学第一医院2017年5月至2019年7月收治的接受多西他赛联合卡铂治疗的mCRPC患者,均为组织学证实的前列腺腺癌,无导管腺癌或小细胞癌等特殊病理类型;影像学证据证实为全身转移性疾病;在维持去势治疗后血清睾酮水平<500 ng/L,临床上符合mCPRC的诊断标准;美国东部肿瘤协作组(eastern cooperative oncology group, ECOG)体能评分≤2分;无重要脏器功能障碍及严重神经系统病变;既往未接受过铂类化疗。满足以下条件的mCRPC患者被定义为肿瘤高负荷并接受多西他赛联合卡铂的一线治疗:存在内脏转移和/或4个以上骨转移,且至少有一个骨转移位于脊柱和骨盆外。满足以下条件的mCRPC患者被定义为多西他赛抵抗并接受多西他赛联合卡铂的二线及以上治疗:在多西他赛治疗期间或治疗后45 d内连续两次PSA较最低水平升高25%以上且≥2 mg/L,和/或出现实体瘤疗效评价标准(response evaluation criteria in solid tumors, RECIST)1.1 版定义的可测量软组织病灶进展,和/或至少出现2个新发的骨转移病灶。所有患者均签署知情同意书。
1.2 方法
所有患者均进行多西他赛联合卡铂的化疗方案,同时行基础雄激素阻断治疗(androgen deprivation therapy, ADT),每个周期为28 d。每周期开始前行血常规、肝肾功能、出凝血功能及PSA检测,化疗过程中低盐饮食。每周期第1天多西他赛静脉滴注,按照75 mg/m2计算剂量,1 h输完;第2天卡铂静脉滴注,按照Calvert公式计算剂量,即卡铂剂量(mg)=血药浓度-时间曲面下面积×[肌酐清除率(mL/min)+25],血药浓度-时间曲线下面积一般取5 mg/(mL·min), 1~2 h输完。化疗前1天晚10点、化疗前3 h和1 h均口服地塞米松,每次 7.5 mg。所有患者在治疗期间均未使用骨保护剂,治疗过程中规律行血常规及不良反应监测,当出现疾病进展、不可耐受的不良反应或患者不愿意继续治疗时,该治疗方案将中止。
1.3 疗效评价
所有患者完成安全性评价,并对至少完成4个化疗周期的患者进行疗效评价,(1)前列腺特异性抗原(prostate-specific antigen, PSA)评价标准:PSA下降幅度>50%评价为有效,PSA下降幅度在0%~50%之间评价为稳定,PSA下降幅度<0%评价为进展;(2)可测量转移灶评价标准:按照RECIST 1.1 版进行评价,分为完全缓解、部分缓解、疾病稳定和疾病进展;(3)按照疼痛数字评分法(numerical rating scales, NRS)评价疼痛缓解情况;(4)按照常见不良反应事件评价标准(common terminology criteria for adverse events, CTCAE)4.0版对治疗过程中出现的不良反应进行分级。
2 结果
2.1 临床特征和治疗周期
如表1所示,共有15例mCRPC患者接受多西他赛联合卡铂治疗,中位年龄70岁(43~77岁)。4例因肿瘤负荷过大接受多西他赛联合卡铂的一线治疗,7例因多西他赛抵抗接受多西他赛联合卡铂的二线治疗,4例因多西他赛和阿比特龙抵抗接受多西他赛联合卡铂的三线治疗。
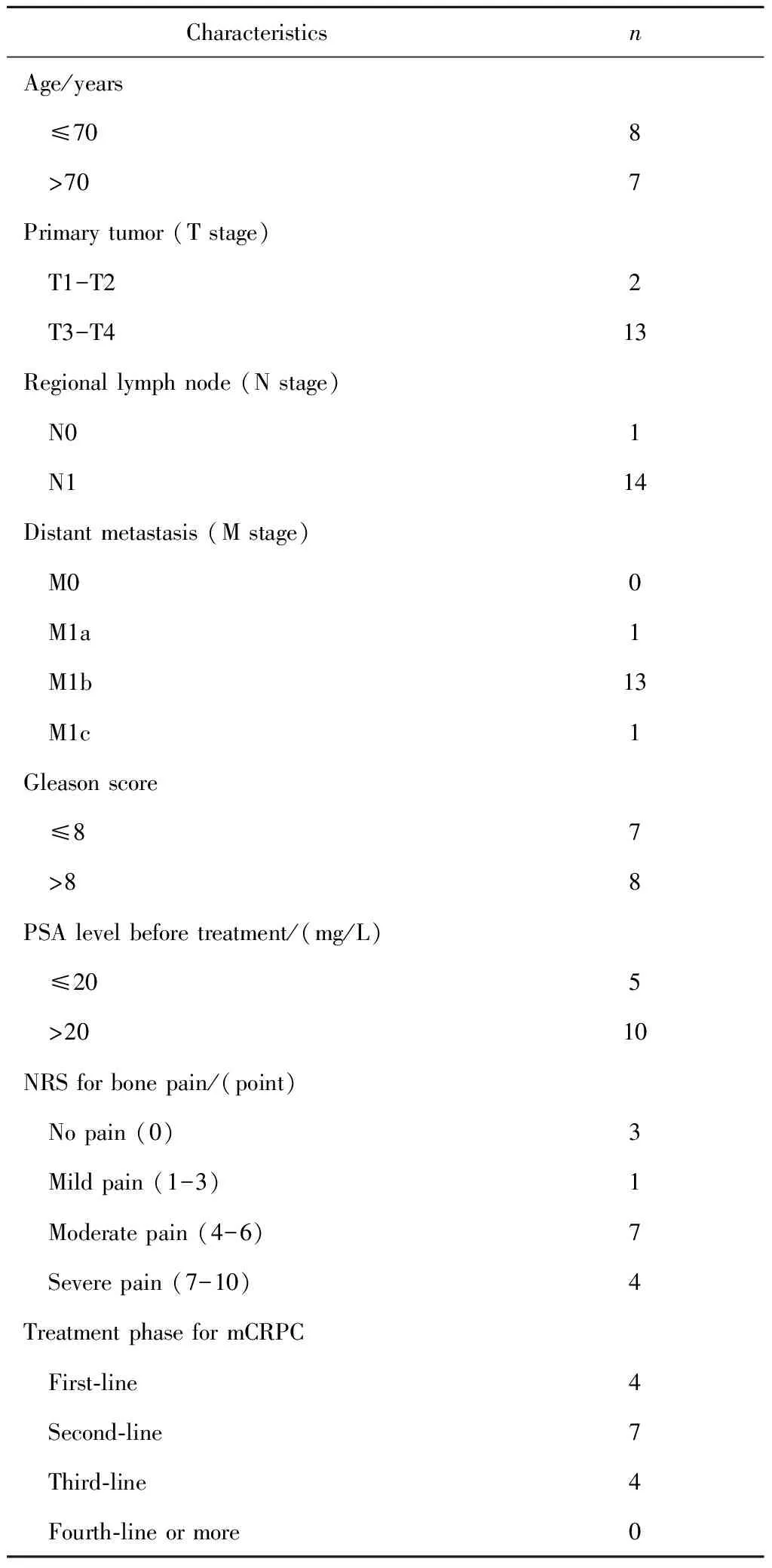
表1 15例mCRPC患者的临床特征Table 1 Clinical characteristics of 15 patients with mCRPC
15例患者中,2例因化疗相关的3级贫血或4级重症感染只接受了1个周期的化疗,1例在接受1个周期化疗后因不愿继续治疗而中止,其余12例患者接受了4~10周期的化疗,平均6.3个周期,中位周期为5.5周期。
2.2 近期疗效评价
图1显示了至少完成4周期化疗的12例患者的PSA变化情况,12例患者中,化疗4周期后PSA下降幅度>50%的为8例,总体有效率为66.7%;PSA下降幅度在0%~50%(疾病稳定)的为1例,PSA下降幅度<0%(疾病进展)的为3例,分别占总例数的8.3%和25.0%,其中多西他赛联合卡铂作为一线、二线和三线治疗的有效率分别为100.0%(4/4)、40.0%(2/5)和66.7%(2/3)。9例伴有骨痛的患者,NRS平均分从4.7分下降至2.4分,有4例骨痛明显缓解,癌痛缓解率为44.4%;在具有可测量转移病灶的4例患者中,达到部分缓解2例,疾病稳定1例,疾病进展1例(表2)。
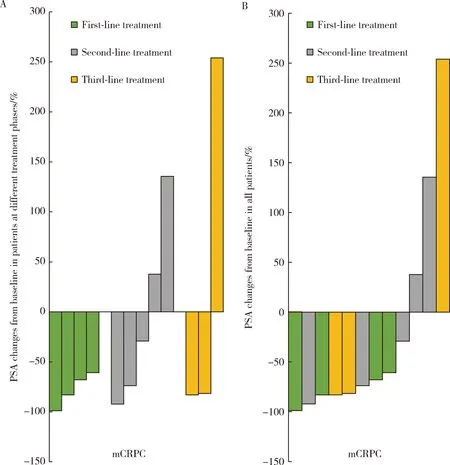
A, PSA changes from baseline after 4 cycles of chemotherapy in patients at different treatment phases; B, PSA changes from baseline after 4 cycles of chemotherapy in all patients. PSA, prostate-specific antigen; mCRPC, metastatic castration-resistant prostate cancer.图1 12例至少接受4周期化疗的mCRPC患者的PSA变化Figure 1 PSA changes in 12 patients with mCRPC who completed at least 4 cycles of chemotherapy

表2 12例至少接受4个周期化疗的mCRPC患者的近期疗效Table 2 Short-term outcomes in 12 patients with mCRPC who completed at least 4 cycles of chemotherapy
2.3 不良反应
15例接受多西他赛联合卡铂化疗的mCRPC患者中,最常见的化疗相关的不良反应为白细胞减少(6例,40%)和贫血(6例,40%),其中2例因化疗相关的严重贫血或重症感染中止化疗,其他较为常见的不良反应有恶心/呕吐、乏力、神经障碍等,但多数患者不良反应较为轻微,通过治疗后均可继续化疗(表3)。

表3 15例mCRPC患者的治疗相关不良反应的发生情况 [n(%)]Table 3 Occurrence of treatment-related adverse reactions in 15 patients with mCRPC [n (%)]
3 讨论
在过去的几十年里,化疗在mCRPC的治疗中的作用越来越大。米托蒽醌是第一个在mCRPC中显示出临床活性的药物,被应用于前列腺癌的去势抵抗阶段[8-9]。2004年,TAX327 Ⅲ期和SWOG99-16 Ⅲ期临床实验均证明了多西他赛联合泼尼松治疗mCRPC比米托蒽醌更有利于生存[10-11],奠定了多西他赛在mCRPC一线治疗中的重要地位,而近期的CHAARTED和STAMPEDE临床实验又证实了多西他赛对于激素敏感的晚期前列腺癌、特别是肿瘤高负荷患者的有效性[12-13],已被批准用于mHSPC的治疗中。
铂类属于细胞周期非特异性药物,它通过与细胞DNA形成共价化合物导致DNA损伤,发挥抗肿瘤活性。越来越多的研究表明,铂类对晚期前列腺癌有活性,在单药或联合治疗中有积极的作用[14]。目前,在晚期前列腺癌的治疗中最常见的铂类药物是卡铂、顺铂和奥沙利铂。在既往铂类药物治疗mCRPC的研究中,卡铂与紫杉醇类药物的联合应用最为广泛,可以提高PSA反应率,延长无进展生存期和总生存期[15]。另外,顺铂联合蒽环类或异环磷酰胺、奥沙利铂联合培美曲塞或卡培他滨较为常用,这些方案在一些研究中均表现出了一定的有效性[16-19],但研究相对较少。基于既往研究结果,我们选择疗效更为确切的多西他赛联合卡铂的方案,用于肿瘤高负荷或多西他赛抵抗的mCRPC,力求让患者获得更好的治疗效果和生存获益。
Flaig等[20]的一项研究入组了113例采用多西他赛联合卡铂一线治疗的mCRPC患者,其中74例患者在化疗4个周期后疾病无进展,有效率达65.5%。另外,Oh等[21]报道了40例采用雌氮芥、多西他赛及卡铂一线治疗的mCRPC患者,其中23例PSA下降幅度大于50%;具有可测量转移灶的23例患者中,1例完全缓解,10例部分缓解,可见卡铂联合多西他赛在mCRPC的一线治疗中表现出了一定的疗效。本项研究中有4例患者因肿瘤高负荷采用多西他赛联合卡铂作为一线治疗,化疗4周期后PSA下降幅度均超过50%,虽然样本量较少,也从一定程度上证实了其有效性。另外,一些研究认为,铂类化合物对于出现神经内分泌分化的前列腺癌具有更强的抗肿瘤活性[22]。也有一些研究认为,导致DNA缺陷修复的相关基因的胚系或体细胞变异是铂类化合物增敏性的潜在生物标记物,其中以BRCA2基因突变最为重要[23-24]。本项研究未纳入前列腺神经内分泌肿瘤及被证实DNA缺陷修复的相关基因的胚系或体细胞变异的患者,在今后的研究中可行进一步探索。
多西他赛、阿比特龙和恩扎卢胺作为目前最常用的mCRPC治疗药物,被广泛用于一线治疗中。若一线治疗药物出现抵抗导致治疗失败,通常会根据患者的病情及身体情况考虑是否启用二线治疗,其中多西他赛联合卡铂化疗作为二线治疗的疗效被逐渐证实和重视。Ross等[25]报道了一项多西他赛联合卡铂治疗多西他赛抵抗的mCRPC的前瞻性研究,入组的34例患者中,PSA和可测量转移灶出现有效反应的比例分别为18%和14%,中位无进展生存期为3个月,中位总生存期为12.4个月。另一项研究中,Kentepozidis等[26]报道了38例既往使用过多西他赛联合泼尼松化疗的mCRPC患者,均接受了至少2个周期的多西他赛联合卡铂的化疗,其中出现临床或生化有效反应的为10例,疾病稳定的为13例,中位无进展生存期为3.6个月,中位总生存期为9.9个月。上述研究显示,对于既往多西他赛抵抗的患者,多西他赛联合卡铂的化疗方案在PSA反应、临床缓解率、无进展生存期、总生存期等疗效评价中均表现良好。本项研究中,多西他赛联合卡铂作为二线或三线方案治疗多西他赛抵抗的mCRPC患者的有效率分别为40.0%和66.7%,略高于既往国外研究数据[25-26],可在此基础上逐渐扩大样本量,获得国内更具有代表意义的数据及结论。
前列腺癌最易发生骨转移,骨痛是给患者带来痛苦、降低生活质量的重要因素[27]。本项研究中,经过评估和依据个人意愿,伴有骨痛的患者均未行护骨治疗,但接受多西他赛联合卡铂治疗后骨痛缓解率为44.4%,对比既往报道的其他治疗mCRPC的药物(米托蒽醌联合泼尼松缓解率为29%,卡巴他赛缓解率为9%)具有明显优势,能够显著改善患者的生活质量[10,28]。
在既往以卡铂为主要化疗药物的研究中,贫血和血小板减少是最常见的化疗相关的不良反应。在卡铂联合其他药物进行化疗时,高达36%的患者出现3级或4级血液毒性,严重的肾毒性及胃肠道反应并不常见[7]。本研究中接受多西他赛联合卡铂化疗的15例患者中,大部分患者均可耐受不良反应,在接受对症支持治疗后均可继续化疗,3级(2例,13.3%)和4级(1例,6.7%)不良反应发生率也较低。另外,白细胞减少、贫血、血小板减少等与骨髓抑制相关的不良反应较多,仅有的2例3级不良反应均为贫血,其中1例因不能耐受中止化疗,因而我们需要在今后的诊疗中予以重视和预防。总之,该方案对大部分mCRPC患者的安全性良好,但mCRPC患者多为高龄,伴随疾病多,且多数肿瘤高负荷或既往接受过多种治疗,在临床治疗过程中需要加强对此类患者的监测,及时处理不良发应,必要时调整治疗方案。
综上所述,本研究初步验证了多西他赛联合卡铂对于mCRPC有良好的临床疗效,且不良反应可以耐受,值得在临床工作中推广。本研究是国内报道的多西他赛联合卡铂治疗mCRPC的系列病例研究,所得结论具有一定代表性,但是,该方案在国内外文献治疗mCRPC的报道中仅有初步结论,卡铂的起始剂量、维持剂量、剂量调整等尚无国内外指南,对患者的生活质量改善、生存获益及远期安全性值得进一步探索。
