基于绝热氧化实验的不同惰性气体阻燃效果研究
2021-08-23刘贵文
刘贵文
(内蒙古平庄煤业(集团)有限责任公司,内蒙古 赤峰 024076)
煤矿内因火灾是我国矿井五大灾害之一,严重威胁着井下人员安全,制约着我国煤矿安全高效生产[1-3]。煤自燃的实质是煤和氧气发生的氧化反应,因而阻止煤自燃的一个关键技术切入点便是切断氧气与煤体接触的途径[4-6]。惰气灭火是煤矿常用的灭火技术手段,原理为氮气部分地替代氧气进入到煤体裂隙表面,与煤的微观表面进行交换吸附,从而使得煤表面对氧气的吸附量减少,在很大程度上抑制或减缓了遗煤的氧化作用[7]。
在常压常温下氮气和二氧化碳在置换煤体中氧气存在一定的差异性,表现出了不同的惰化性能[8]。由于煤自燃是一个产热和蓄热的角力过程,可分为不同阶段,而不同阶段煤的氧化特征又不同[9-12]。因此,在研究惰性气体阻止煤自燃的能力时,应该考虑惰气注入时煤体的温度,以全面掌握在煤炭不同氧化阶段不同惰气阻燃的差异性。为此,采用绝热氧化装置,以非吸附性He为参考气体,设计不同温度起点(70、110、150℃)的注惰(N2、CO2)阻燃实验;以温度和出口O2体积分数为观测指标,对比研究不同惰气的阻燃效果。
1 实验原理及方法
1.1 煤的绝热氧化实验原理和实验装置
采用绝热氧化法模拟煤的自燃过程,是对一定量的煤样供氧使其自热升温,通过杜瓦瓶、隔热石棉和恒温箱等绝热措施将煤样罐中的煤样氧化产生的微小热量保留,以实现煤样的自加热过程,直至温度升高出现自燃现象[13]。该过程是在实验室的条件下,通过小容量煤样实验,准确表现煤自燃这一过程。
实验装置采用煤炭低温绝热氧化实验装置,主要包括供气系统,抽真空系统,温度和流量控制系统,反应系统、气体采集系统和恒温箱,煤炭低温绝热氧化实验装置如图1。
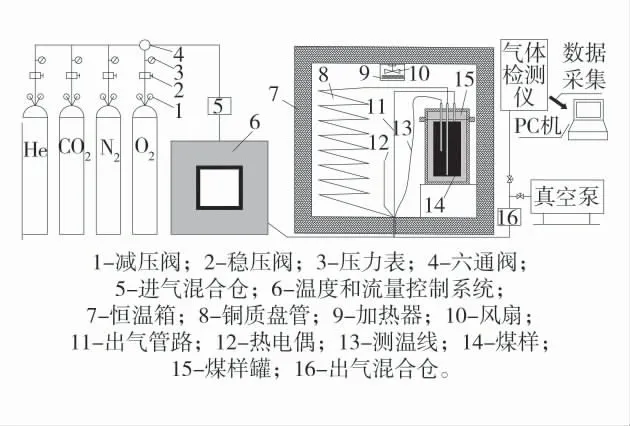
图1 煤炭低温绝热氧化实验装置Fig.1 Experimental device for low-temperature adiabatic oxidation of coal
1)供气系统。主要包括4种高压气体(O2、N2、CO2、He)和气体控制部件,可为煤样罐提供稳定流量的气体。
2)抽真空系统。主要由真空泵和控气阀门构成,该系统工作后能够抽除煤样罐中的O2,以避免煤样在干燥过程中发生氧化。
3)温度和流量控制系统。该系统能够智能追踪煤样罐的温度,保证恒温箱的温度和煤样罐一致,使得进入煤样罐的气流温度等于煤样温度。
4)反应系统。煤样的自热反应发生在煤样罐中。煤样罐内置杜瓦瓶,能够容纳约200 g的煤样;进气口设置在杜瓦瓶底部的中心位置附近,出气口设置在杜瓦瓶顶部,温度传感器设置在杜瓦瓶的中部位置。
5)数据采集系统。系统主要包括O2传感器、温度传感器和PC机,能够实时监测并实现数据的储存与输出。
6)恒温箱。主要由恒温室和铜质盘管构成。在绝热氧化实验过程中,恒温室内温度跟随煤样罐中的温度,并和煤样罐中的温度保持一致,误差在±(0.1~0.2)℃;铜质盘管长约6 m,能够保证进口的气体在恒温室中被预热,从而入煤样罐中后气体温度和煤体温度一致,不会带走煤体的温度。
1.2 实验方法
实验过程中所用的煤样用保鲜膜包裹运至实验室,经破碎筛选粒径为3~5 mm的煤样。采用煤炭低温绝热氧化实验装置进行9组平行实验,实验步骤为:
1)称取制备好的200 g煤样放入煤样罐中,然后将煤样罐装入实验系统中。
2)检查装置气密性后关闭进气口阀门,打开真空泵,进行抽真空。抽真空的时间为2 h。
3)关闭真空泵后,打开高压氮气瓶阀门,在绝热氧化装置上按最大流量(300 mL/min)向煤样罐内通N2,一定时间后煤样罐内不再是负压状态后,打开出气口阀门,并监测O2体积分数。
4)当出气口O2体积分数不为0,继续通N2或者抽真空,待出气口O2体积分数彻底为0时,设置升温程序,对煤样进行升温。升温后,逐步调小N2流量至150 mL/min,对煤样进行105℃条件下干燥15 h。
5)干燥完成后,温度设定为手动模式,使煤样罐温度在40℃下保持20 min;然后将N2换成O2,O2流量设置为60 mL/min,温度设定为自动追踪模式,煤样罐中的煤样开始发生自热反应。
6)煤样罐中的煤体温度升高后,当温度分别达到70、110、150℃,立刻注N2进行阻燃,直至温度降至30℃。
7)重复步骤1)~步骤6),分别进行CO2和He的阻燃实验。
2 实验结果
2.1 煤低温绝热过程的氧化动力学
煤和氧气的反应在微观上是氧气分子和煤中活性基团的反应,会生成各种气体产物、水分和固体产物,该反应被认为是煤中多种物质参与的基元反应[14]。在煤的氧化动力学分析中常常引入Arrhenius公式:
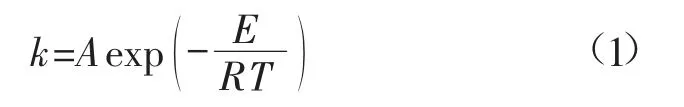
式中:k为反应速率常数,无量纲;A为前指因子,s-1;E为活化能,kJ/mol;R为气体状态常数,8.314 J/(K·mol);T为温度。
根据煤样的升温曲线,大约每隔5℃取数据点1次,绝热氧化实验结果分析如图2。
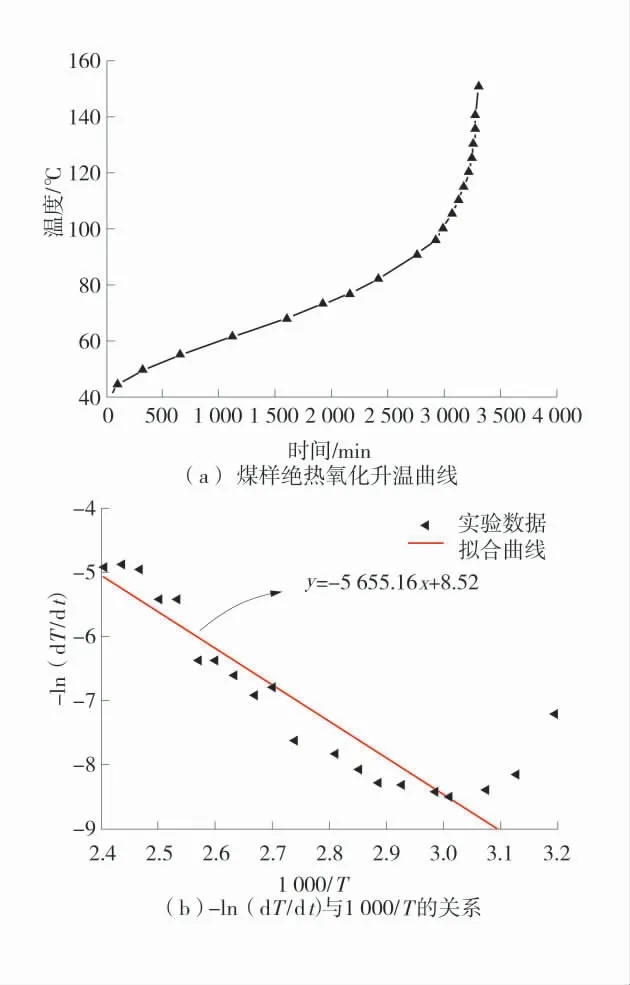
图2 绝热氧化实验结果分析Fig.2 Analysis of the experimental results of adiabatic oxidation
由图2(a)煤样升温曲线可以看出,随着时间的推移,煤温逐渐增高,当温度大约超过100℃后,升温速率加快,大约在6 h左右温度达150℃。以-ln(d T/d t)为纵坐标,以1 000/T为横坐标,得到的Arrhenius图如图2(b),拟合的直线斜率为-5 655.16,相关系数为0.91。于是实验煤样的表观活化能经计算为47 kJ/mol。
在绝热氧化升温过程中,煤氧反应是1个从蓄热到自燃再到燃烧的过程。在蓄热阶段其氧化速度非常缓慢,而到了自燃阶段,氧化速率开始增大,煤开始加速氧化。在这个过程中氧化速率由小变大,这中间存在1个临界温度,当温度超过这个温度,煤氧化速率开始显著加快,煤样加速氧化。然而,煤的绝热氧化的升温速率始终处于动态变化当中,从图2(a)中难以直接找出升温速率变化特征。
为寻求煤样氧化的临界温度,煤的反应速率kcoal可由煤的升温速率来表示[15]。于是在Arrhenius图中,其纵轴可变为煤升温速率的自然对数,得到的煤升温速率和温度倒数的关系如图3。
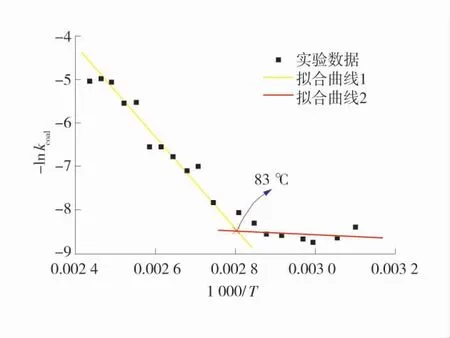
图3 -ln(k coal)与1 000/T的关系Fig.3 The relationship between-ln(k coal)and 1 000/T
在图3中,数据的散点图存在明显的拐点。这里采用线性拟合的方式,研究散点图的拐点。按照直线拟合的方法,得到的煤自燃临界温度为83℃。
2.2 惰气注入后煤样的温度变化
采用绝热氧化升温的方式,在同一实验条件下通入O2使煤氧化升温至70、110、150℃。达到每个温度点后,注入He、N2、CO2,使煤样温度降至30℃。不同惰气阻燃实验的温度变化如图4,其中图4中右侧的图形为注惰后的降温曲线图。由图4可以看出,每组实验的最长时间不超过4 200 min。在升温阶段,不同目标温度的绝热氧化实验的升温曲线存在一定的差异,在降温阶段,随着惰气的注入,煤样罐的温度呈现出先短暂上升后持续下降的趋势,总体上不同温度阶段的惰气阻燃实验的降温曲线不同,而初始的温度越高,在同流量的惰气注入条件下所需的阻燃时间越长。

图4 不同惰气阻燃实验的温度变化Fig.4 Temperature changes of different inert gas flame retardant experiments
2.3 惰气注入后O2体积分数的变化
惰气注入过程中O2体积分数变化如图5。由图5可以看出,无论哪种气体,初始温度为150℃时的O2变化曲线始终在110℃的下方,初始温度为70℃的气变化曲线在最上方。3种初始温度下注惰后O2体积分数变化曲线的位置关系是由煤的氧化速度和煤样罐中O2的余量共同决定的。根据Arrhenius公式可知,温度越高,煤的反应速率越快,在同一时间内煤的耗氧量就越大。在注惰初始阶段,70℃时煤的O2体积分数最高,110℃次之,而150℃的最低。这2种因素的存在决定了3种不同初始温度下O2体积分数随时间变化的曲线的位置关系。
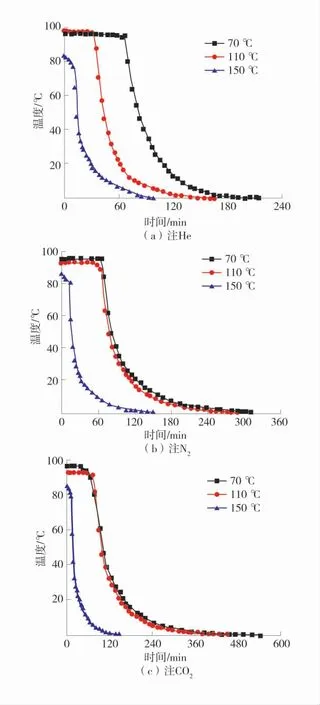
图5 惰气注入过程中O2体积分数变化Fig.5 Changes in O2 concentration during inert gas injection
He、N2、CO2所对应的3条曲线的位置关系是不相同的。其中,He注入后,在O2体积分数近似垂直下降的阶段,3条曲线的位置关系几乎为等间距排列关系。而其他2种气体的3条位置关系较为相似:初始温度为70℃和110℃对应的的曲线几乎重叠,与初始温度为150℃对应的曲线由明显的间距。3种曲线的这种对应关系说明了随着初始温度的升高,出口O2体积分数是由O2消耗量所决定,也就是说N2、CO2置换出煤体中O2的速率低于高温阶段O2被消耗的速率。因此,在高温条件下,需要加大N2或者CO2的流量,一方面以加快稀释煤体孔隙中O2体积分数,置换出吸附态O2;另一方面加大对流换热速率。
3 阻燃效率
惰气在阻燃过程中具有2个特点:一是置换出煤体中的O2,降低O2体积分数;二是利用对流散热降温达到阻燃目的。因此,惰气的阻燃效率为两者效率耦合的结果。因此,定义惰气阻燃的过程中的阻燃效率为:
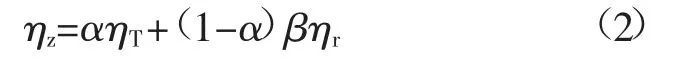
式中:ηz为阻燃效率,%;ηT为降温效率,近似等于平均降温速率归一化后的数值;ηr为相对置换率;%;α为权重系数。
由于惰气的阻燃效果是由单位时间内降温量和O2体积分数下降量决定的,因此,将降温效率的权重系数定义为:

式中:tT为降温总时间,min;tr为氧气置换时间;min。
根据前述实验,权重系数α为:

由于平均降温速率的变化为非线性变化,随初始温度的升高而增大,且具有不可比性,因此,考虑非线性增函数归一化模型(5)将平均降温速率归一至[0,1]区间:
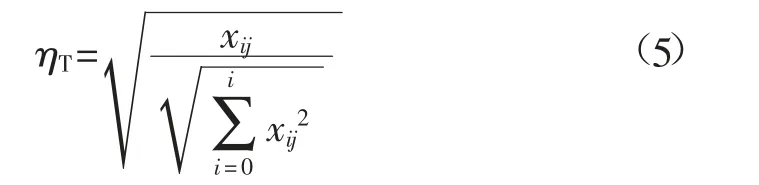
式中:i为气体,为He、N2、CO2;j为不同温度起点,为70、110、150℃;xij为在j这一温度起点下i的平均降温速率,℃/min。
于是,降温效率为:

因此,He、N2、CO2在不同初始温度下的阻燃效率见表1。
由表1可以看以,He的阻燃效率最优,N2次之,而CO2最弱。随着初始温度的升高,He的阻燃效率几乎直线下降,而N2和He由于吸附作用,阻燃效率先升高后下降。该结果表明,惰气在阻燃过程中,由于He为非吸附性气体,它的阻燃效率主要体现在对流散热的能力上。N2和CO2的比热容较小,且大小接近,因此,它们的阻燃效率差异是由竞争吸附能力的不同造成的。
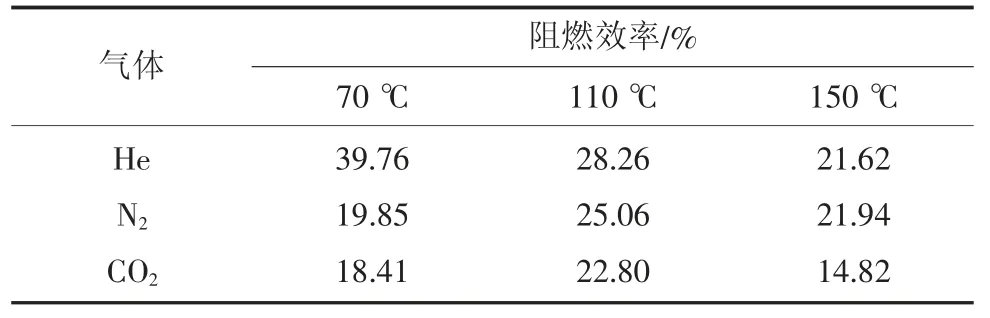
表1 不同惰气的阻燃效率Table 1 Flame retardant efficiency of different inert gases
4 结论
1)实验过程中,煤绝热氧化过程是煤依赖于自身的氧化产热进行升温的,基本不会存在热量的耗散。基于能量守恒,利用Arrhenius公式对煤样进行了氧化动力学分析。通过分析-ln(d T/d t)与1 000/T的拟合曲线,得到煤样的表观活化能为47 kJ/mol;通过分段拟合的方式,煤样绝热氧化升温的临界温度为83℃。
2)通过分析注惰后温度随时间的变化,在不同初始温度条件下注入相同惰性气体后,3条降温曲线不同,初始温度越高,降温至30℃所需的时间越长。在同一初始温度下注入不同惰气后,以时间长度为判断指标,He的阻燃效果最佳,N2次之,CO2最差。通过分析降温速率,以50℃为分界温度,从初始温度降至50℃过程中,N2的降温速率大于CO2的降温速率;从50℃降至30℃过程中,煤体对气体吸附的作用效果明显增强,导致N2和CO2的降温速率变化不一致,且大于CO2的降温速率。通过分析惰气相对置换效率,N2和CO2的置换速率随着温度升高而增大。
3)通过分析出口O2体积分数随时间的变化,无论是哪一种惰性气体,初始温度为150℃时注入惰气后,O2体积分数变化曲线始终在110℃的下方,初始温度为70℃的O2体积分数变化曲线在最上方。出气口O2的变化趋势是由O2的消耗量和O2的置换量决定的。
4)结合惰气在不同初始温度阶段的降温速率和置换效率,得到了不同惰气的阻燃效率。对比不同惰气的阻燃效率,其结果表明,惰气的阻燃效率是由对流交换热和置换煤体中的O2量决定的;由于吸附作用的存在,N2的置换效果优于CO2的置换效果。
