氢化物发生-原子荧光光谱法测定环境水体中痕量锑
2021-08-17刘冰冰张辰凌张永涛
刘冰冰,刘 佳,张辰凌,贾 娜,张永涛
(中国地质科学院水文地质环境地质研究所,自然资源部地下水科学与工程重点实验室,河北正定 050803)
水中锑严重危害人类和其他动植物健康,过量的锑会刺激皮肤、呼吸道和消化道的黏膜,严重可导致肺水肿、肝硬化和胰腺炎等慢性病变[1-3]。研究表明,锑和砷具有致癌性和相似的毒性[4]。我国《生活饮用水卫生标准》(GB 5749—2006)[5]和《食品安全国家标准 饮用天然矿泉水》(GB 8537—2018)[6]中锑的限值皆为0.005 mg/L。锑为《地下水质量标准》(GB/T 14848—2017)[7]新增非常规指标中的毒理学指标,其Ⅰ和Ⅱ类水的限值分别为≤0.000 1 mg/L和≤0.000 5 mg/L。快速准确测定环境水体中痕量锑的含量对人类生命健康具有重要意义。
测定环境水体中锑含量的方法主要为电感耦合等离子体发射光谱法[8-9]、氢化物发生-原子吸收光谱法[10]、电感耦合等离子体质谱法[11-12]、氢化物发生-原子荧光光谱法[13-15]等。电感耦合等离子体发射光谱法和氢化物发生-原子吸收光谱法存在光谱干扰及基体效应等因素,导致其检出限无法满足锑检测需求。电感耦合等离子体质谱法由于仪器价格昂贵,运行成本高,一般不作为首选方法。本试验采用氢化物发生-原子荧光光谱法测定环境水体中痕量锑,操作简便、干扰因素少、检出限低、灵敏度高,可以满足分析测试要求。
1 试验部分
1.1 仪器与试剂
AFS-3100 型氢化物发生-原子荧光光谱仪(北京海光仪器有限公司),锑空心阴极灯。
锑标准贮备溶液1 000 mg/L[GBW(E)081588,中国计量科学研究院];锑标准使用溶液(10.0 μg/L)由锑标准贮备溶液逐级稀释而成;锑标准系列(0、0.20、0.50、1.0、2.0、5.0 μg/L)分别由锑标准使用溶液逐级稀释而成;盐酸、氢氧化钠、硼氢化钾、硫脲和抗坏血酸皆为优级纯。
盐酸溶液(5%):取25 mL浓盐酸,用纯水稀释至500 mL;氢氧化钠(2 g/L):称取氢氧化钠1 g溶于纯水中,稀释至500 mL;硼氢化钾溶液(20 g/L):称取硼氢化钾10.0 g溶于氢氧化钠溶液500 mL中,摇匀,现用现配;硫脲-抗坏血酸溶液:称取12.5 g硫脲加约80 mL纯水,加热溶解,冷却后加入12.5 g 抗坏血酸,稀释至100 mL;钢瓶氩气:纯度不低于99.99%;试验用水为去离子水。
1.2 仪器工作条件
光电倍增管负高压:310 V;锑灯电流:75 mA;载气流量:400 mL/min;屏蔽气流量:900 mL/min;原子化器高度:8~10 mm;原子化器温度:25 ℃;读数时间:10 s;延迟时间:1.0 s;进样体积:0.5 mL。
1.3 试验方法
取水样10.0 mL于10 mL比色管中,向水样中加入1.0 mL硫脲-抗坏血酸溶液和1.0 mL浓盐酸,摇匀,静置30 min。在上述仪器条件下,以硼氢化钾溶液为还原剂、盐酸5%为载流,在氢化物发生-原子荧光光谱仪最佳工作条件下测定其浓度,同时做空白试验。如果样品中锑含量过大,可逐级稀释后测定。
2 结果与讨论
2.1 光电倍增管负高压的选择
在其他工作条件不变的前提下,本试验以1.0 μg/L和3.0 μg/L的锑标准溶液为工作溶液,测定其在不同光电倍增管负高压下的荧光强度,如图1所示,随着仪器光电倍增管负高压的增大,锑标准溶液的荧光强度都逐渐增大。如果荧光强度过低,会导致仪器不稳定,灵敏度低;荧光强度过高,会导致标准曲线漂移,曲线不稳定。因此,选择310 V作为最佳光电倍增管负高压。
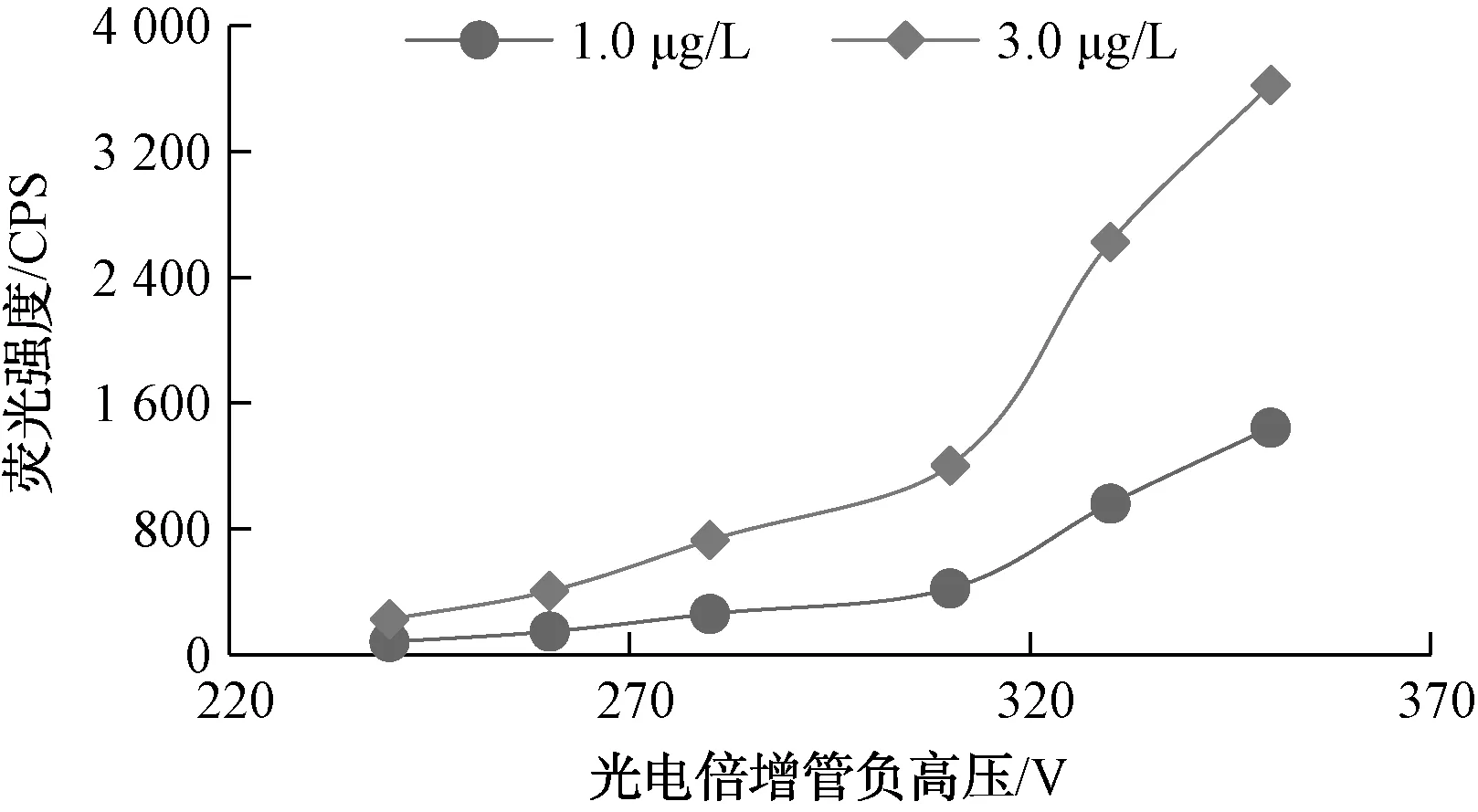
图1 荧光强度随光电倍增管负高压的变化Fig.1 Fluorescence Intensity Changes with Negative High Voltage of Photomultiplier Tube
2.2 灯电流的选择
同样以1.0 μg/L和3.0 μg/L的锑标准溶液为工作溶液,调节灯电流,测定其不同灯电流下的荧光强度,结果如图2所示。随着灯电流逐渐升高,锑标准溶液的荧光强度也逐渐升高。较低的灯电流使荧光强度偏低,方法的准确度也偏低。灯电流升高,荧光强度也随着增大,但是过大的灯电流会导致仪器运行不稳,影响试验结果的精密度。因此,选择75 mA作为试验最佳灯电流。

图2 荧光强度随灯电流的变化Fig.2 Fluorescence Intensity Changes with Lamp Current
2.3 硼氢化钾溶液浓度的选择
还原剂硼氢化钾浓度的选择对方法的准确性和可靠性十分重要。在其他工作条件都不变的前提下,测定不同浓度硼氢化钾溶液对荧光强度的影响,如图3所示。随着硼氢化钾溶液浓度的增加,1.0 μg/L和3.0 μg/L的锑标准溶液的荧光强度都逐渐增大,当其浓度达到15~20 g/L时,荧光强度达到最大后趋于稳定,但是较大浓度的硼氢化钾溶液反应,会产生较多氢气导致仪器不稳定。因此,选择20 g/L作为最佳硼氢化钾溶液浓度。
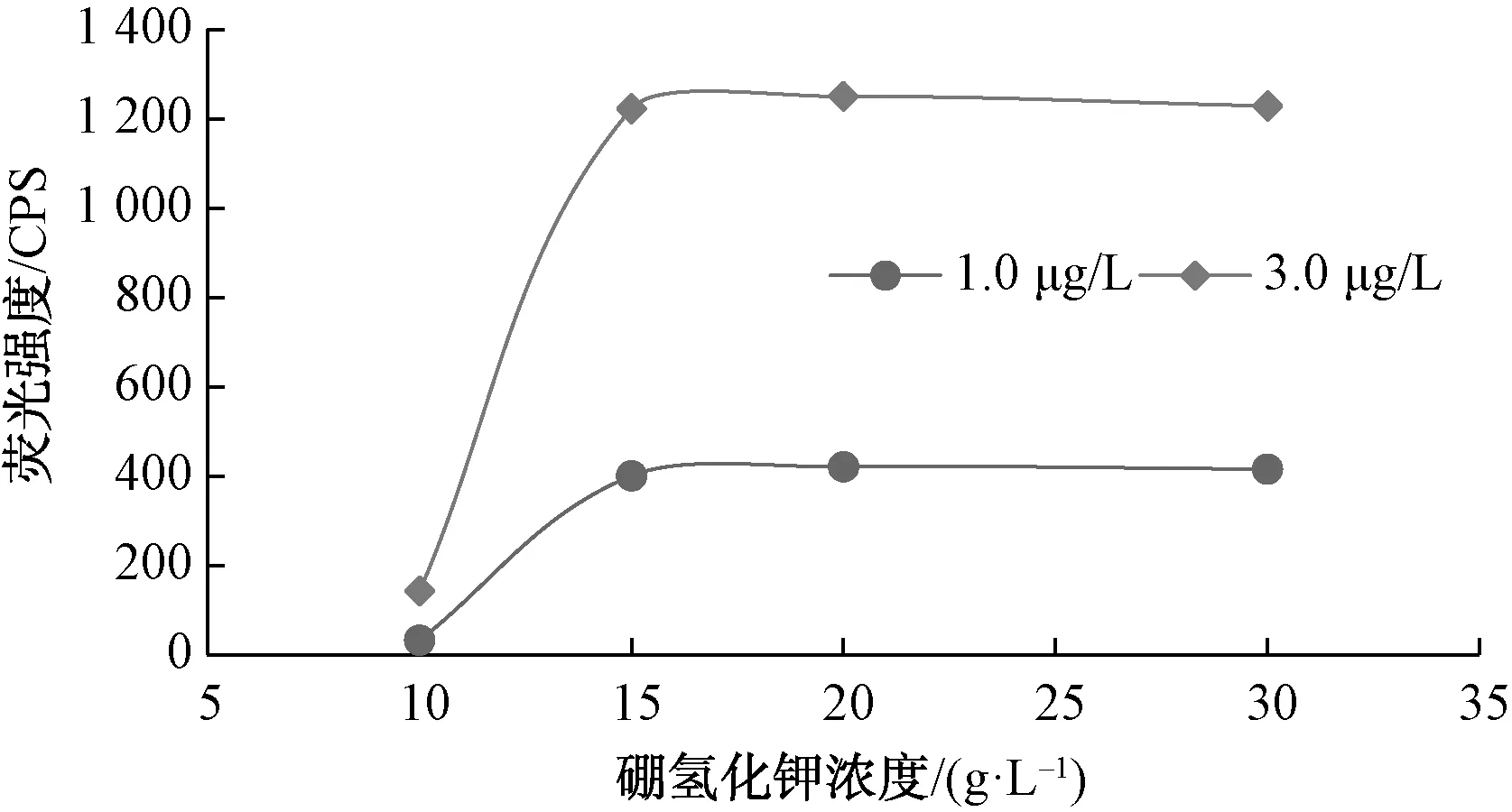
图3 荧光强度随硼氢化钾溶液的变化Fig.3 Fluorescence Intensity Changes with Potassium Borohydride Solution
2.4 载流盐酸浓度的选择
在本试验中,载流盐酸浓度也是一个非常关键的参数。图4为1.0 μg/L和3.0 μg/L锑标准溶液的荧光强度随盐酸浓度的变化情况。随着载流盐酸浓度的增大,锑标准溶液的荧光强度也逐渐增大,盐酸浓度为5%后荧光强度趋于稳定,考虑较大的盐酸浓度会影响仪器的稳定性及仪器管路的使用寿命,因此,选择5%作为最佳盐酸浓度。
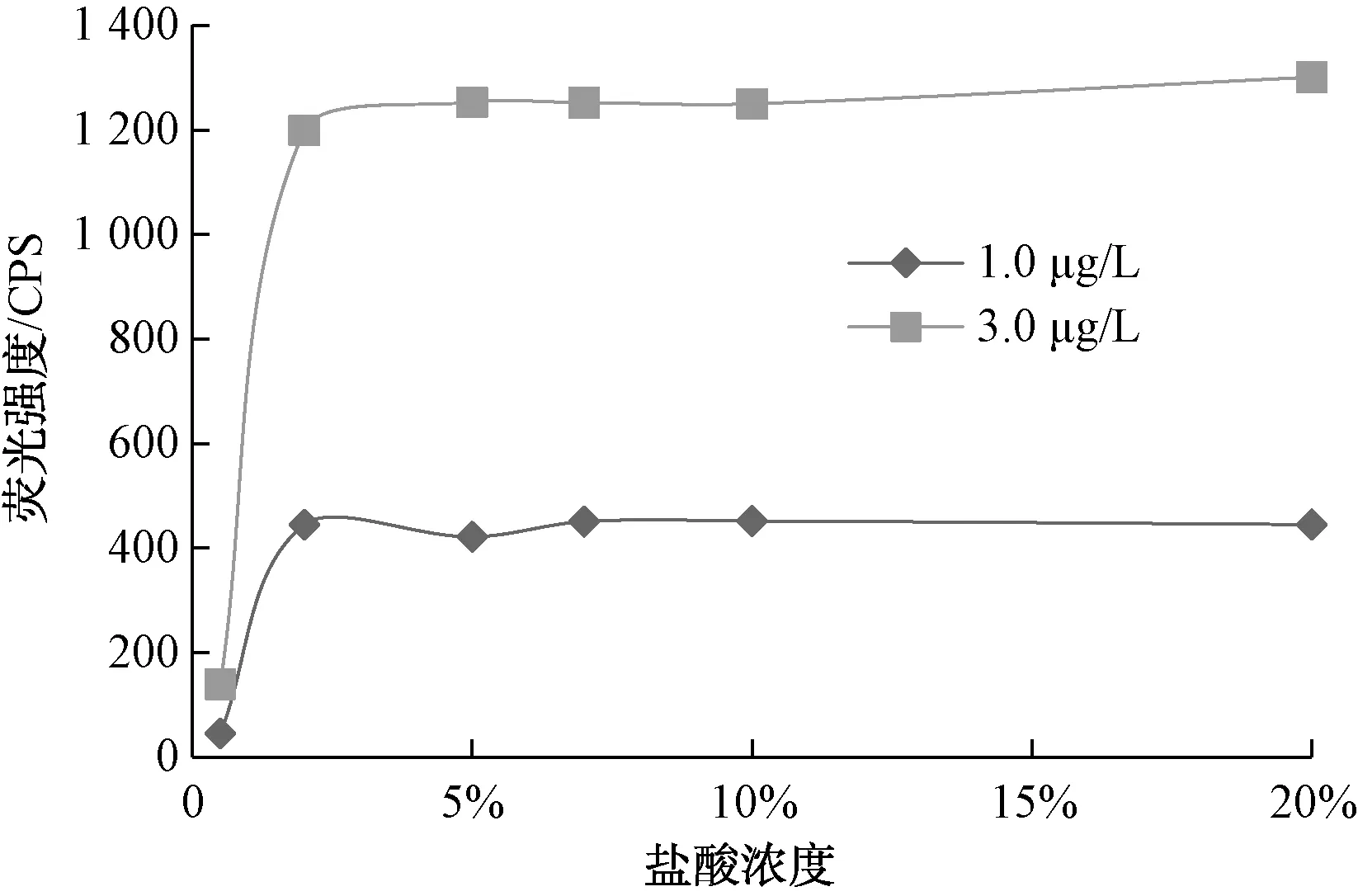
图4 荧光强度随盐酸浓度的变化Fig.4 Fluorescence Intensity Changes with Hydrochloric Acid Concentration
2.5 方法标准曲线、检出限、定量限和线性范围
根据上述方法,配制锑标准系列溶液0、0.20、0.50、1.0、2.0、5.0 μg/L,在原子荧光光谱仪最佳工作条件下,测定各标准系列溶液荧光强度,以荧光强度为纵坐标、浓度为横坐标绘制标准曲线,得到线性方程和相关系数。连续测定12次空白溶液,以其3倍标准偏差作为检出限,以检出限3倍作为定量限,方法的检出限和定量限分别为0.02 μg/L和0.06 μg/L。配制一系列浓度为0、0.06、0.20、0.50、1.0、2.0、5.0、7.0、10.0 μg/L的锑标准溶液,上机测定并绘制标准曲线。当浓度高于5.0 μg/L时,标准曲线开始向下弯曲,出现拐点。本方法以定量限(0.06 μg/L)为最低检测质量浓度,以绘制校准曲线出现拐点(5.0 μg/L)时的分析物浓度为最高检测浓度。因此,本方法的线性范围为0.06~5.0 μg/L,标准曲线、线性方程和相关系数如图5所示。

图5 锑标准溶液工作曲线Fig.5 Standard Solution Curve of Antimony
《地下水质检验方法》(DZ/T 0064—1993)[16]中没有水中锑的检测方法。本方法与依据《食品安全国家标准 饮用天然矿泉水检验方法》(GB 8538—2016)[17]水中锑方法测定出的检出限和定量限以及《地下水质量标准》(GB/T 14848—2017)Ⅰ类水限值的对比如表1所示。GB 8538—2016中水中锑的测定方法包括氢化物发生原子荧光光谱法、氢化物发生原子吸收光谱法及电感耦合等离子质谱法,此3种方法只给出定量限,本方法的定量限低于以上3种方法,可以推测其检出限也低于以上3种方法,且也低于GB/T 14848—2017中Ⅰ类水限值,可以满足测定要求。

表1 本方法检出限和定量限、GB 8538—2016中定量限与GB/T 14848—2017中Ⅰ类水限值的对比Tab.1 Comparison of the Detection Limit and Quantification Limit between this Method and Antimony Determination Method in GB 8538—2016 and Limit of Class Ⅰ Water in GB/T 14848—2017
2.6 精密度和准确度试验
配制浓度分别为0.50、1.0、3.0 μg/L的锑标准溶液,在原子荧光仪光谱仪最佳工作条件下,连续测定12次并计算其相对标准偏差(RSD),结果如表2所示。其相对标准偏差在1.33%~2.45%,说明精密度良好,可以满足环境水体中锑测定要求。分别选取矿化度不同的两个水样进行质量浓度为0.30、1.0、3.0 μg/L的加标回收试验,结果如表3所示,其加标回收率为95.12%~103.5%,相对标准偏差在0.97%~3.12%。

表2 精密度试验Tab.2 Precision Experiment

表3 回收率试验 (n=12)Tab.3 Recovery Experiment (n=12)
3 结论
本试验采用氢化物发生-原子荧光光谱测定环境水体中锑,通过优化仪器工作条件、还原剂硼氢化钾和载流盐酸的浓度,使方法检出限达到0.02 μg/L,定量限为0.06 μg/L。在各类水体标准中,《地下水质量标准》中Ⅰ类水的限值最低,为≤0.000 1 mg/L,即≤0.1 μg/L,本方法检出限低于该限值,完全可以满足各类环境水体中痕量锑的质量要求。同时,该方法的精密度和准确度也满足测定要求,说明本方法适用于各类环境水体中痕量锑的测定。
