淫羊藿饮片标准汤剂制备及质量控制研究*
2021-08-16王亦磊穆庆丽曹雅静
王亦磊 ,穆庆丽 ,曹雅静 ,郭 冬 △
(1. 陕西省榆林市第一医院,陕西 榆林 719000; 2. 陕西省中医药研究院,陕西 西安 710003; 3. 陕西省中医医院,陕西 西安 710003)
淫羊藿 Epimedium brevicornum Maxim. 为小碱科多年生直立草本植物淫羊藿、箭叶淫羊藿、柔毛淫羊藿、巫山淫羊藿或朝鲜淫羊藿的地上部分[1],具有补肾阳、强筋骨、祛风湿功效[2]。药理学研究表明,淫羊藿治疗阳痿、遗精、骨质疏松、手足麻木拘挛疗效较好[3]。淫羊藿含有淫羊藿总黄酮、苷类、多糖类及生物碱等化学成分[4-5],目前已分离得到多种成分,主要为异戊烯基黄酮类成分,主要成分是8-异戊烯基黄酮及其苷类。淫羊藿苷为特征成分,具有抵抗神经元损伤、改善骨代谢、抗氧化、抗炎、抗肿瘤等活性[6-7]。中药饮片标准汤剂是指以中医药理论为指导,选择道地药材,依据现代提取方法,经过加工炮制后成为合格饮片,再经标准化工艺制备成水煎剂[8-10]。严格遵循传统汤剂的煎煮原则及操作流程,以保证质量稳定,工艺统一,以确保用药剂量准确。标准汤剂是衡量中药配方颗粒与临床汤剂是否一致的重要参考指标[11-12]。指纹图谱专属性强,可发现从原药材到中药配方颗粒化学成分的变化,已成为掌握中药配方颗粒质量变化的关键技术[13-17]。本研究中选取产自陕西、甘肃、山西、辽宁、东北的15 批淫羊藿饮片制备标准汤剂,以淫羊藿苷为指标成分,采用高效液相色谱法测定含量,计算出膏率及转移率,并进行指纹图谱研究,为淫羊藿标准汤剂质量标准的制订及配方颗粒的制备提供科学数据。现报道如下。
1 仪器与试药
1.1 仪器
Agilent 1260 型高效液相色谱仪(美国安捷伦公司);KQ-500DE 型数控超声波清洗器(昆山市超声仪器有限公司,功率为 500 W,频率为 40 kHz);BT25S 型天平(精度为十万分之一),BS210S 型电子天平(精度为万分之一),均购自赛多利斯科学仪器(北京)有限公司;ZF-C 型三用紫外分析仪(上海康禾光电仪器有限公司);HH-S4 型电热恒温水浴锅(北京科伟永兴仪器有限公司);EH20B 型电热板(德国 Labtech 公司)。
1.2 试药
淫羊藿苷对照品(批号为120909 -200410,纯度≥98.0%),淫羊藿对照药材(批号为 120918-200809),均购于中国食品药品检定研究院;甲醇、甲酸、乙醚、乙酸、乙酯乙醚、乙醇、丁酮均为分析纯,水为超纯水;淫羊藿药材信息见表1。硅胶G 薄层板、硅胶H 薄层板、硅胶GF254薄层板均购自青岛海洋化工厂。
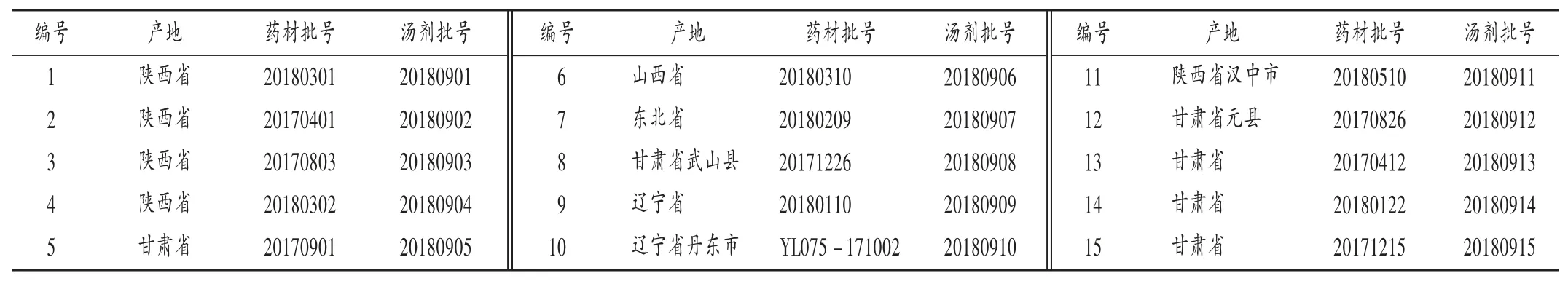
表1 15 批淫羊藿药材信息Tab.1 Information of 15 batches of Epimedium brevicornum
2 方法与结果
2.1 淫羊藿标准汤剂制备
取15 批淫羊藿饮片各100 g,精密称定,加入12 倍量水,浸泡30 min,加热回流提取30 min,趁热过滤(200目筛),分离出煎煮液,药渣再加入12 倍量水,回流提取30 min,趁热过滤(200 目筛),合并滤液,定容至 2 500 mL,备用。剩余部分减压浓缩成质量浓度为0.2 g/mL 的标准汤剂,备用,将标准汤剂冷冻干燥,留样。
2.2 淫羊藿苷含量测定
2.2.1 色谱条件与系统适用性试验
色谱柱:Diamonsil C18柱(250 mm ×4.6 mm,5 μm);流动相:乙腈 - 水(28 ∶72,V / V);流速:0.8 mL / min;检测波长:270 nm;柱温:30 ℃;进样量 10 μL。理论板数按淫羊藿苷峰计不低于1 500。在此色谱条件下的色谱图见图1。

图1 高效液相色谱图1.icariinA. Reference solution B.Test solution C.Negative reference solutionFig.1 HPLC chromatograms
2.2.2 溶液制备
取淫羊藿苷对照品适量,精密称定,加甲醇制成每1 mL 含无水淫羊藿苷1.354 mg 的溶液,即得对照品贮备液。再取对照品贮备液0.8mL,置10mL 容量瓶中,加甲醇稀释至刻度,即得每1 mL 含无水淫羊藿苷108.32 μg的溶液。分别精密量取15 批标准汤剂各10 mL,置25 mL 容量瓶中,加甲醇至刻度,摇匀,0.45 μm 微孔滤膜滤过,即得供试品溶液。按2.2 项下方法,加水制得不含淫羊藿的阴性对照样品,再按供试品溶液制备方法制备不含淫羊藿苷的阴性对照品溶液。
2.2.3 方法学考察
线性关系考察:取淫羊藿苷对照品适量,精密称定,分别加甲醇制成每1 mL 含无水淫羊藿苷2.708,4.333,5.416,27.080,54.160,81.240,108.320,135.400,162.480 μg 的溶液,作为对照品溶液。按 2.1 项下色谱条件进样测定,以对照品质量浓度(X,μg/mL)为横坐标、峰面积(Y)为纵坐标进行线性回归,得淫羊藿苷线性回归方程为 Y =22.438 4 X -13.855 4,R2=0.999 8(n =9)。结果表明,淫羊藿苷质量浓度在 2.708 ~162.480 μg /mL 范围内与峰面积线性关系良好。
精密度试验:取同一批(批号为20180901)样品,依法制备供试品溶液,共6 份,按2.1 项下色谱条件进样10 μL 测定。结果淫羊藿苷峰面积的 RSD 为 2.30%(n =6),表明仪器精密度良好。
稳定性试验:取同一批(批号为20180901)样品,依法制备供试品溶液,按2.1 项下色谱条件分别于0,2,4,8,12,16,24 h 时进样测定峰面积。结果淫羊藿苷峰面积的 RSD 为 3.46% (n = 7),表明供试品溶液在 24 h内稳定。
重复性试验:取同一批(批号为20180901)样品,依法制备供试品溶液,共6 份,按2.1 项下色谱条件进样测定。结果淫羊藿苷峰面积的 RSD 为 5.01%(n =6),表明方法重复性良好。
加样回收试验:取已知含量的样品(批号为20180901),依法制备供试品溶液,取供试品溶液1 mL,共9 份,分别置5 mL 容量瓶中,精密加入淫羊藿苷对照品溶液(质量浓度分别为 108.32,135.40,162.48 μg /mL)1 mL,按2.1 项下色谱条件进样测定,并计算回收率。结果见表2。

表2 淫羊藿苷加样回收试验结果(n =9)Tab.2 Results of the recovery test of icariin(n =9)
2.3 出膏率测定
取定容后的煎液100 mL,置蒸发皿中蒸干,放入烘箱,105 ℃烘干6 h 以上,并记录第1 次浸膏质量;继续烘干1 h,记录第2 次浸膏质量;继续烘干1 h,记录第3 次浸膏质量,取3 次的均值。按出膏率=[干膏质量/饮片质量]×100%计算淫羊藿出膏率。结果15 批淫羊藿 出 膏 率 为 14.80% ~21.80% ,平 均 出 膏 率 为17.14% ,RSD 为 1.71% ( n = 3)。详见表 3。
2.4 转移率测定
按转移率(%)=W/ M×100%计算淫羊藿苷的转移率,其中,W 为汤剂中淫羊藿苷的含量(%),M 为饮片中淫羊藿苷的含量(%)。由表3 可知,15 批淫羊藿标准汤剂中淫羊藿苷含量介于0.26% ~0.64%,转移率介于 51.05% ~60.49% ,平均转移率为 55.30% ,RSD为 3.15% ( n = 15)。
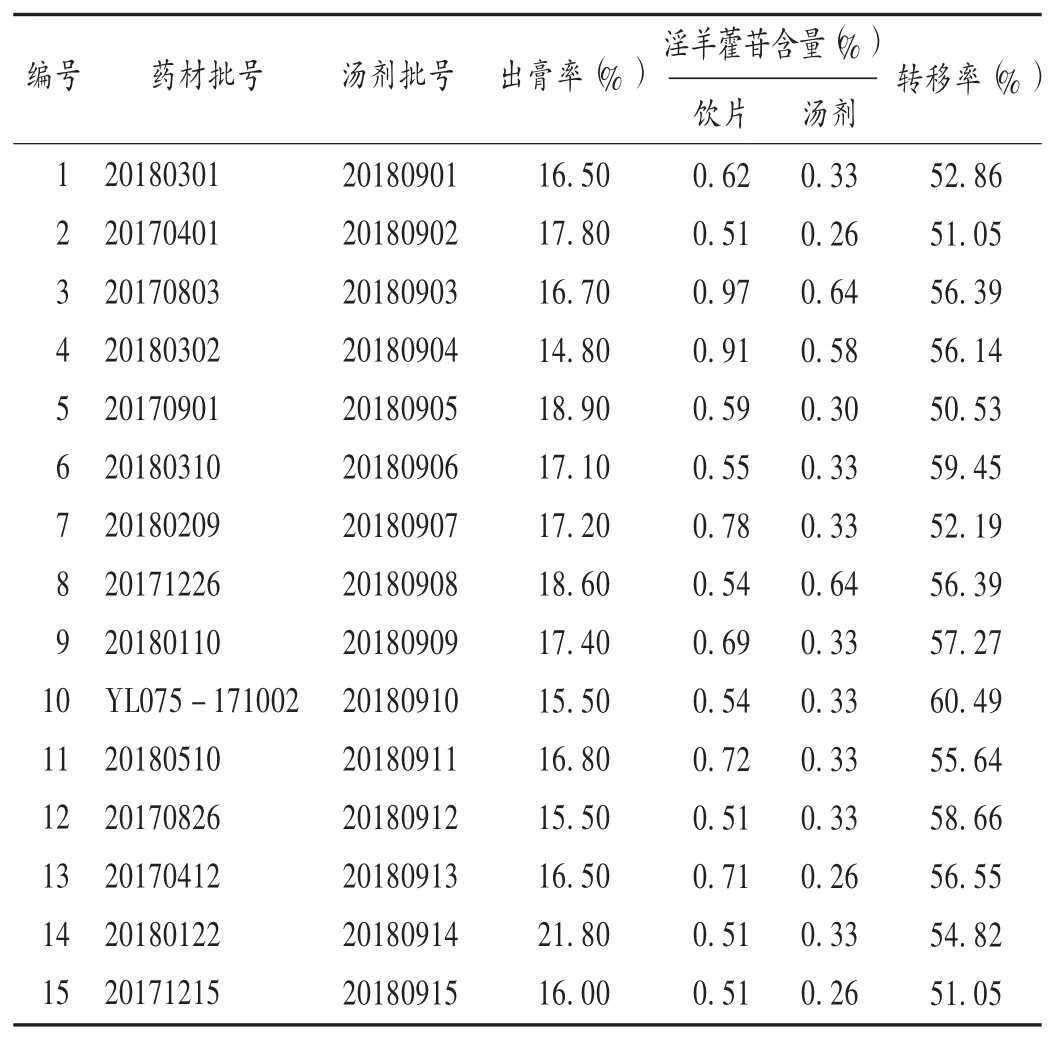
表3 淫羊藿出膏率与淫羊藿苷转移率测定结果Tab.3 Determination results of the extract rate of Epimedium brevicornum and the transfer rate of icariin
2.5 特征指纹图谱分析
指纹图谱的相对性反映中药的化学成分及其量的分布状况,专属性较强,特征较明显,信息量丰富,是一种可同时分析中药多组分、多指标成分的方法[18]。分别吸取15 批供试品溶液各10 μL,按2.1 项下色谱条件进样测定,记录色谱峰,生成的标准汤剂指纹图谱见图2。可见,标定共有峰7 个,通过对照品指认5 个峰,分别为1 号峰,朝藿定 A(Rt = 8.661 min);2 号峰,朝藿定 B(Rt =10.022 min);3 号峰,朝藿定 C(Rt =11.334 min);4 号峰,宝藿苷Ⅰ(Rt = 13.067 min);5 号峰,淫羊藿苷(Rt = 15.607 min)。15 批淫羊藿标准汤剂指纹图谱相似度为 0.95。

图2 淫羊藿标准汤剂指纹图谱1.Epinedin A 2.Epinedin B 3.Epinedin C 4.Pogoside Ⅰ 5.IcariinFig.2 Fingerprint of standard decoction of Epimedium brevicornum
3 讨论
本研究中采集了15 批淫羊藿饮片,其产地为陕西、山西、甘肃、辽宁、东北,基本覆盖淫羊藿的主产区,具有代表性,符合《中药配方颗粒质量控制与标准制定技术要求(征求意见稿)》中关于原料样品的规定。另外,根据2020 年版《中国药典(一部)》相关规定,对15 批淫羊藿饮片进行检查,结果所有饮片均符合要求。试验中采用趁热滤过的方式进行分离,以减少成分的损失,趁热滤过后滤液放置冷水中迅速冷却,抑制成分降解,契合传统汤剂工艺。根据药典规定,含量测定时流动相选用乙腈-水溶液,结果色谱峰峰形较好,目标峰分离度较好。
