高效液相色谱法测定郁李明荟片中芦荟苷的含量
2021-08-11刘梦燕刘露李素凯李冬冬陈笑宇杨锦竹王伟
刘梦燕,刘露,李素凯,李冬冬,陈笑宇,杨锦竹※,王伟
(1.吉林大学,吉林 长春 130012;2.吉林省食品检验所,吉林 长春 130012)
本文中的郁李明荟片保健品是由郁李仁、决明子和芦荟组成的复方片剂,从中医学理论上来讲,郁李仁归脾、大肠小肠经,可下气行滞;决明子入肝肾、大肠经,补肾益气,利水通便;芦荟治肠胃燥热,可健胃下泻,三者同用,具有益气、利水和润肠通便之效。芦荟含有20多种蒽醌类物质[1],其中芦荟苷和芦荟大黄素是泻下通便的主要成分,但用量过大可能会出现毒理安全性问题[2]。周宇红等[3]实验结果表明,芦荟食用安全性取决于其活性物质蒽醌类泻素(芦荟苷)的含量。因此,对保健食品中的芦荟苷进行质量控制十分必要。
目前,芦荟苷的定量检测方法包括紫外分光光度法、高效液相色谱法(HPLC)、质谱法、薄层层析法、硼砂光度法、毛细管区带电泳法及反向离子对色谱法[4-7],HPLC法因其有高适应性、高重复性等优点,与其他色谱相比具有显著优越性,被广泛应用于药品检验、保健食品等领域。但郁李明荟片含中药成分复杂,用已有的HPLC方法进行含量测定分离效果极不理想,为对郁李明荟片中芦荟苷含量进行控制,保证该保健品的有效性和安全性,本试验建立了芦荟苷含量测定的新方法,并进行其方法学研究,结果表明该法准确高效,重现性高,试样处理简单,可作为该品中芦荟苷的质量控制依据。
1 仪器与材料
1.1 仪器设备
Acchrom S3000型高效液相色谱仪;WondaSil C18 Superb(250 mm 4.6 mm,5m)色谱柱;KQ-250DE型数控超声波清洗器;Sartorius BT 25s电子天平。
1.2 试剂与材料
芦荟苷对照品(批号为110787-201206中国药品生物制品检定所);郁李明荟片为实验室自制(郁李仁、芦荟和决明子按5:5:2的比例配比,辅料为玉米淀粉、硬脂酸镁。规格为0.6 g/片,每片含0.48 g芦荟生药。食用方法为每日2次,2片/次);甲醇(色谱纯,赛默飞世尔科技有限公司);磷酸(色谱纯,天津市光复精细化工研究所);水为试验室双蒸水;其余试剂均为分析纯。
2 方法与结果
2.1 色谱条件
色谱填充柱:(WondaSil C18 Superb柱,4.6 mm 250 mm,5m);流动相:甲醇-0.1%磷酸水溶液(37:63);检测波长:355 nm;流速:1 mL/min;柱温:25℃;进样量:20L。
2.2 溶液的制备
2.2.1 对照品溶液的制备 取芦荟苷对照品适量,精密称定,加冰醋酸-甲醇(1:100)制成每1 mL含0.2 mg的溶液,作为对照品溶液。
2.2.2 供试品溶液的制备 取郁李明荟片适量,研成粉末,过五号筛,精密称定0.2 g,置25 mL的量瓶中,加冰醋酸-甲醇(1:100)适量,超声处理(200 w,40 kHz)40 min,取出后过滤,放置至室温,加冰醋酸-甲醇(1:100)溶解并稀释至刻度,摇匀,滤过即得供试品溶液。
2.2.3 不含芦荟的阴性对照溶液的制备 取除芦荟以外的两种药材进行提取干燥,相同方法制粒。将所得颗粒按“2.2.2”所述方法进行处理,得到不含芦荟阴性对照溶液。
2.3 方法学考察
2.3.1 专属性试验 分别取对照品溶液、供试品溶液、不含芦荟阴性对照溶液注入色谱仪,记录色谱图。在芦荟苷对照品色谱相应的位置上,样品呈现保留时间一致的色谱峰,样品中芦荟苷的色谱峰与其他色谱峰分离度良好,且阴性样品溶液在对照品峰位置无干扰峰,说明该方法专属性良好,见图1。
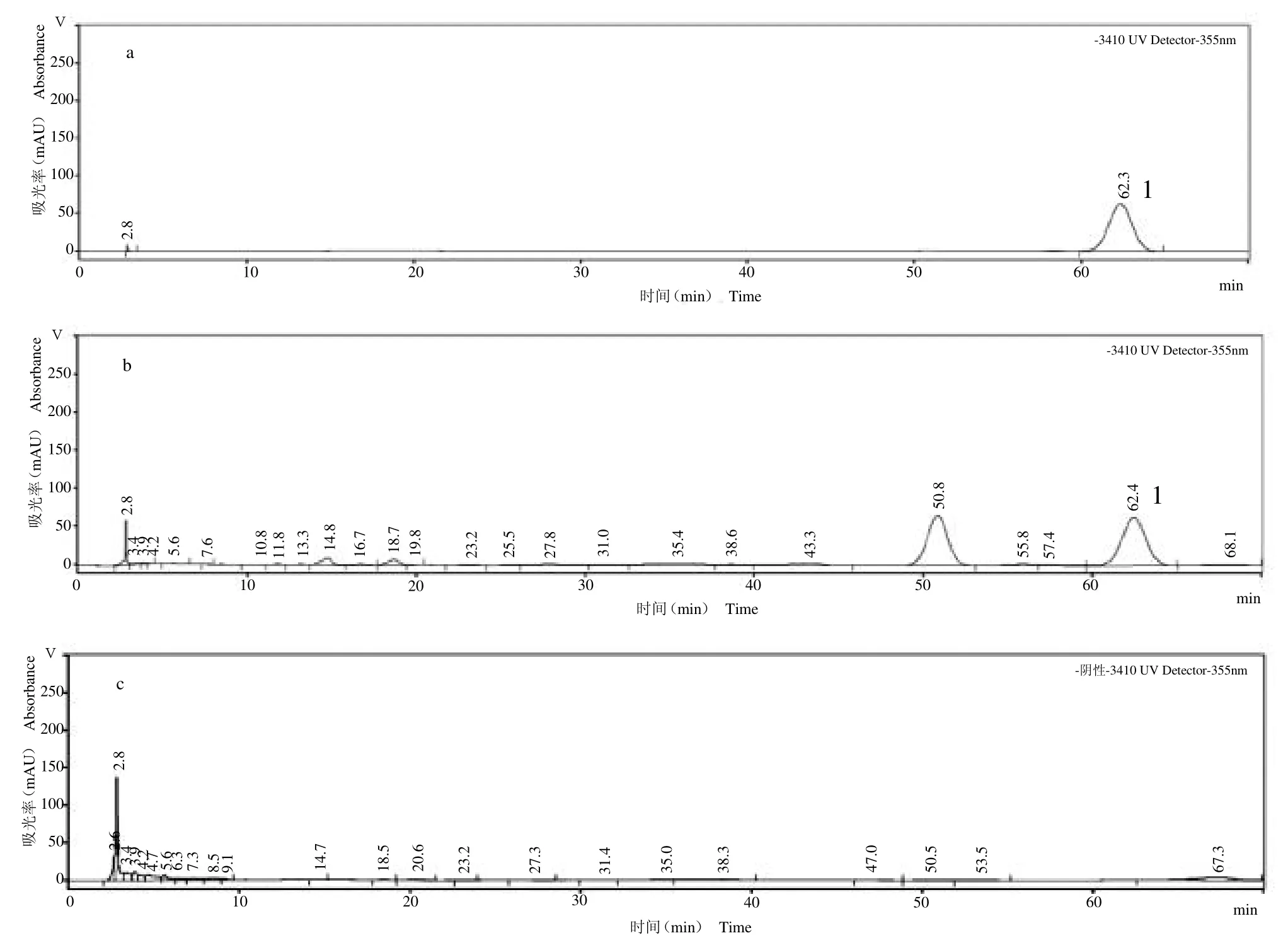
图1 HPLC图谱Fig.1 HPLC chromatograms
2.3.2 线性关系考察 将“2.2.1”项下的对照品溶液用冰醋酸-甲醇(1:100)逐步稀释,得到浓度分别为0.054 4 mg/mL、0.108 8 mg/mL、0.163 2 mg/mL、0.2176 mg/mL、0.272 0 mg/mL和0.326 4 mg/mL的芦荟苷对照品溶液,依次吸取各溶液20L,按照“2.1”项下的色谱条件注入色谱仪,记录峰面积,以芦荟苷对照品浓度为横坐标,峰面积为纵坐标绘制标准曲线,如图2。得到回归直线方程为y=27545x+292.57,R2=0.9995表明芦荟苷在0.054 4~0.326 4 mg/mL范围内线性良好。
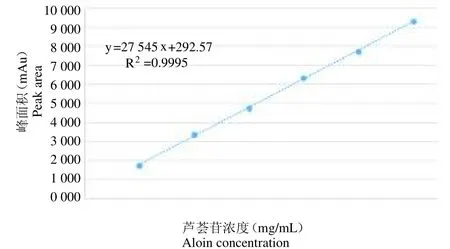
图2 芦荟苷标准曲线Fig.2 The standard curve of aloin
2.3.3 精密度试验 将“2.2.1”项下的对照品溶液,按照时间顺序连续进样6次,每次吸取20L,记录峰面积。求得峰面积的RSD值为0.68%(n=6),表明仪器精密度良好。
2.3.4 重现性试验 按照“2.2.2”项下供试品溶液制备的方法对6份郁李明荟片的样品进行处理,取各溶液20L,注入HPLC仪器中进行测定,计算含量。结果表明,6份郁李明荟片的平行样中所含的芦荟苷含量平均值为21.33 mg/g,RSD为0.63%(n=6),说明该方法的重现性良好。
2.3.5 稳定性试验 精密吸取同一份供试品溶液,按照“2.1”项下的色谱条件在0、2、4、8、12、24 h时进样,测定峰面积,得到RSD为0.40%(n=6),表明供试品溶液在24 h内稳定性良好。
2.3.6 加样回收试验 精密称取6份郁李明荟片的药粉,计算其中芦荟苷含量,再各自加入等量的芦荟苷对照品,按照“2.2.2”项下的供试品溶液制备的方法进行处理,吸取20L进行测定,计算各样品中芦荟苷的实测值,计算平均回收率为97.16%,RSD为1.87%(n=6)(表1),表明该测定方法回收率良好。
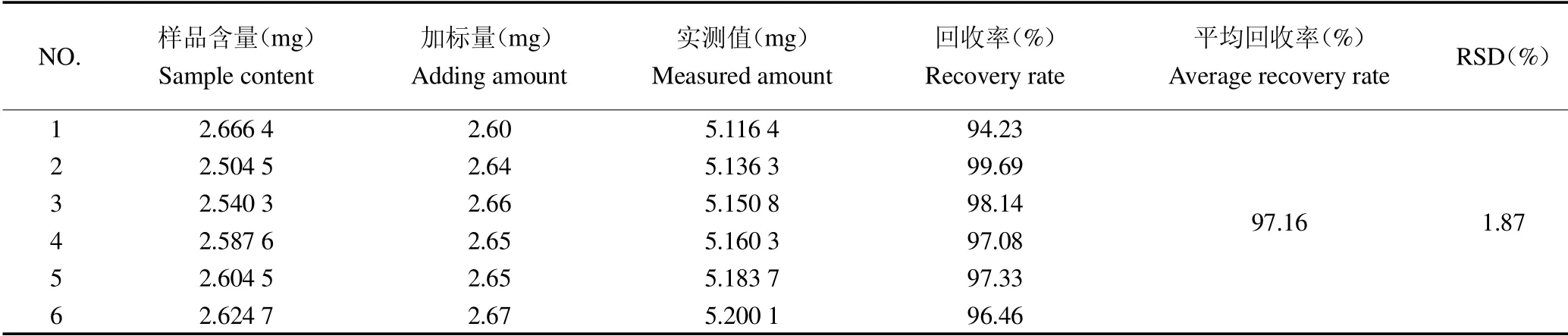
表1 加样回收率试验结果Table 1 The result of the recovery test
2.4 样品含量测定
从3批郁李明荟片中各取3个平行样,按照“2.2.2”项下供试品溶液制备的方法进行处理,分别吸取20L,注入HPLC仪器中进行测定,3个批次平行样平均值分别为21.05 mg/g、21.00 mg/g和21.36 mg/g。3批含量RSD值为0.92%。表明该品芦荟苷含量稳定,均一性良好。
3 讨论
在供试品处理方法的选择上,本试验同时用甲醇超声和冰醋酸-甲醇(1:100)超声处理供试品,在同一色谱条件下连续进样对比发现,冰醋酸-甲醇(1:100)超声处理方法的供试品稳定性较好,这可能与芦荟苷在酸性条件下更稳定有关。另外,供试品超声后对比了文献中过滤和离心(3 000 r,5 min)两种处理方法[8],进液相后发现并无明显差别,故选用相对简便的过滤处理方法。在流动相的选择上,以药典方法乙腈-水(25:75)作为流动相时,供试品和对照品都有拖尾现象且分离度不好。查阅文献,重新选取甲醇-0.1%磷酸水作为流动相[9],经过不断调整,最终确定甲醇-0.1%磷酸水(37:63)为流动相,提高了芦荟苷的分离度,峰形良好。
芦荟中含有多种蒽醌类成分,其中芦荟苷含量较多,是芦荟的代表性成分也是泻下通便的主要功效性成分[10]。本试验采用HPLC法对郁李明荟片中的芦荟苷进行含量测定和方法学研究,建立了芦荟苷含量测定的新方法,结果显示芦荟苷在0.054 4~0.326 4 mg/mL范围内线性良好,回归直线方程为y=27545x+292.57,R2=0.9995;重现性RSD值为0.63%(n=6),重现性良好;平均回收率为97.16%,RSD为1.87%(n=6),表明该方法回收率良好。综上可知该方法稳定可靠,可用于芦荟苷的含量测定和质量控制。
