g-C3N4掺杂锰锌铁氧体复合物的制备及光催化性能研究*
2021-08-04王黎明徐丽慧解明睿
张 潇, 王黎明, 徐丽慧, 沈 勇, 解明睿
(上海工程技术大学 纺织服装学院,上海 201620)
0 引 言
工业废水中的有机物,例如难降解的染料等物质,引发的环境污染已成为世界性问题,因而有效的水处理方法仍然需要研究和完善[1]。在多种传统的化学、物理和生物水净化方法中,包含Fenton反应、光催化、超声波分解及臭氧氧化等在内的高级氧化工艺(AOPs)具有高效、简单、实用的特点,能够无选择性地降解污染物并具备较好的重现性[2]。与此同时,这些方法还存在合成条件相对苛刻、合成路线复杂以及较高的成本等缺点。因此,有必要设计出一种稳定、可重复使用且具有较高经济效益的光化学催化剂。
半导体的光催化剂能够将有机污染物矿化降解,可有效地应对由该类废弃物造成的环境问题。近年来,石墨碳氮化物(g-C3N4)作为可持续的可见光催化剂,因其具有较高的硬度、稳定性以及低成本[3-4],被判定为优秀的光催化材料。然而,g-C3N4有限的非定域导电性、较低的比表面积及较高的光生载流子复合速率,在一定程度上降低其光催化效率[5-6]。g-C3N4材料本身的缺陷可通过共聚、掺杂等改性处理进行改善,如BiOBr/g-C3N4[7]、ZnO/g-C3N4[8]、TiO2/g-C3N4[9]等被设计出,通过提升光生电子/空穴的分离效率,实现对有机污染物的有效降解。
当粉体的纳米材料作为催化剂使用时,通常难以从液相中分离,因此磁性材料的引入能够极大地提升光催化剂的可重复利用率[10]。在对g-C3N4与尖晶石铁氧体(MFe2O4,M是Mn2+、Zn2+等双价阳离子)复合材料的光催化及降解有机污染物应用的研究中[11-13],MnZnFe2O4(MZF)因其独特的催化性能和高电磁性备受关注[14-15]。本文采用自组装方法制备出新型g-C3N4掺杂锰锌铁氧体复合物,g-C3N4/MZF形成p-n异质结构,可有效提高材料的光催化性能,增加光响应范围,使得光生载流子有效分离。
1 实验材料与方法
1.1 主要实验材料和仪器
材料:罗丹明B,三聚氰胺,MnSO4·H2O, ZnSO4·6H2O,FeCl3·6H2O,NH4HCO3,乙醇,甲醇和柠檬酸(分析纯,国药集团化学试剂有限公司)。实验用水为去离子水。
仪器:马弗炉(GR.AF4.5/14型,上海贵尔机械设备有限公司),扫描电子显微镜(S-4800型,日本HITACHI公司),透射电子显微镜(FEI Tecnai G2 F20型,荷兰帕纳科公司),X射线衍射仪(X’pert Powder型,荷兰帕纳科公司),光化学反应仪(BL-GHX-V型,上海比朗仪器制造有限公司),X射线光电子能谱仪(250XI型,美国Thermo公司),PPMS-9仪器(美国Quantum Design公司)UV-2000型紫外透射率分析仪(美国Labsphere公司),紫外-可见分光光度计(UV-3600型,日本岛津公司),FT-IR光谱仪(Spectrum-two型,帕金埃尔默仪器上海有限公司)等表征材料的形貌、元素组成、光学活性和磁性能等。
1.2 实验方法
1.2.1 g-C3N4制备
称取5 g三聚氰胺,以5 ℃/min的速率加热至550 ℃,并于该温度下持续加热4h后,取出经充分研磨获取粉体,待用[13]。
1.2.2 锰锌铁氧体的制备
以3∶2∶5摩尔比将MnSO4·H2O,ZnSO4·7H2O,FeCl3·6H2O配制成混合液,并将其转移至反应釜内,于50 ℃水浴条件下,在30 min内逐滴加入金属离子1.5倍摩尔量的NH4HCO3,再以NaOH 溶液调节pH值至7.4,继续搅拌40min。待反应结束,产物于室温陈化12h,后经抽滤、洗涤及烘干,获得MZF前躯体,再将其置于马弗炉中在1150 ℃下煅烧3h,得到MZF[16-17]。
1.2.3 g-C3N4/锰锌铁氧体复合材料的制备
采用自组装法[11-13],将加入一定量g-C3N4后的甲醇与加入MZF的柠檬酸、水和乙醇混合溶液分别超声分散,再将两悬浮液混合,继续超声30min后,转移至三口烧瓶中持续机械搅拌2h,并于90 ℃下回流3h后停止加热,待冷却至室温后停止搅拌。产物经过滤,去离子水和无水乙醇多次洗涤后,于60 ℃干燥12h,得到g-C3N4/MZF复合材料。与此同时,进一步改变掺杂的质量比,制备g-C3N4/MZF(1:1), g-C3N4/MZF(2:1),g-C3N4/MZF(3∶1)和g-C3N4/MZF(3∶2)复合物。
1.3 测试与表征
1.3.1 X-射线衍射分析(XRD)
本文采用荷兰帕纳科公司生产的X’pertPowder型X射线衍射分析仪,扫描范围20~80°,判断g-C3N4,MZF和g-C3N4/MZF的晶体结构。
1.3.2 傅里叶红外光谱(FT-IR)
通过FT-IR光谱仪(Spectrum-two 型,帕金埃尔默仪器上海有限公司)分析g-C3N4,MZF和g-C3N4/MZF的分子结构和化学组分分析。
1.3.3 扫描电子显微镜(SEM)
通过扫描电子显微镜(S-4800型,日本HITACHI公司),观察MZF的微观形貌。
1.3.4 透射电子显微镜(TEM)
采用透射电子显微镜(FEI Tecnai G2 F20型,荷兰帕纳科公司),观察g-C3N4/MZF复合物的微观形貌。
1.3.5 紫外-可见漫反射光谱分析(DRS)
通过Lambda1050紫外-可见-近红外分光光度计(帕金埃尔默仪器上海有限公司),分析g-C3N4,MZF和g-C3N4/MZF催化剂光吸收性能的测定。
1.3.6 光电子能谱测试(XPS)
采用美国Thermo公司的250XI型X射线光电子能谱仪,测定g-C3N4,MZF和g-C3N4/MZF的元素组成和价带谱结构。
1.3.7 磁滞回线测试(VSM)
通过美国Quantum Design公司的PPMS-9仪器,对MZF和g-C3N4/MZF进行磁滞回线测试,评定材料的矫顽力,剩磁,饱和磁化强度,表征材料的磁性。
1.3.8 光催化活性测试
通过对溶液中罗丹明B的降解程度,评价所制材料的光催化活性,该过程在光反应仪装置(BL-GHX-V型,上海比朗仪器制造有限公司)中进行,以300 W氙灯为光源模拟可见光,并配制10 mg/L的RhB溶液作为指示剂,催化剂用量为0.5g/L。光反应前,通过30 min的暗处理使样品对指示剂达到吸附平衡,光反应开始后,每隔30 min取样,离心取上层清液, 使用紫外可见分光光度计测定其在RhB最大吸收波长554nm处的吸光度,再将所得数值代入公式(1)
η降解率= (Ct/C0)×100%
(1)
计算样品的光催化效率,其中C0、Ct分别为 RhB的光催化初始浓度和t时刻的浓度(mg/L)。为了更加细致地分析降解过程,采用伪一阶模型[13]拟合实验所得数据,结果说明催化剂降解RhB的行为符合一级反应动力学方程,一级速率常数k(min-1)的计算公式(2)如下:
k=ln(Ct/C0)/t
(2)
其中ln(Ct/C0)随光照时间t(min)的变化呈线性关系,表明ln(Ct/C0)光解RhB的过程为一级动力学反应。通过比较各样品的光催化活性判定复合物的最佳掺杂比例,并以此方法进行5次重复试验,评价催化剂的使用稳定性及活性变化。
2 结果与讨论
2.1 材料的晶体结构分析(XRD)
将制备的MZF,g-C3N4/MZF和g-C3N4进行晶体结构(XRD)分析,结果如图1所示。图1显示,在30.5°、35.0°、43.1°、53.5°、57.1°、62.6°处出现MZF的衍射峰,分别与标准卡片(JCPD74-2401)[14]中(220)、(311)、(400)、(422)、(511)和(440)晶面所对应的衍射峰一致。另外,MZF材料的特征峰出现明显的宽化现象,说明其晶粒尺寸较为细小;g-C3N4在13.3°衍射角处出现较弱的衍射峰,与g-C3N4中的(100) 晶面对应,这是g-C3N4的平面3-s-三嗪结构单元形成的特征峰。g-C3N4在2θ为27.6°处出现较强的衍射峰,可以索引为(002)衍射面(JCPDS87-1526)[8],由芳香族结构层间堆叠产生;g-C3N4/MZF复合物中MZF的晶相几乎保持不变,而g-C3N4晶体只观察到(002)面衍射峰,并未观察到(100)面所对应的衍射峰,因此能够推断g-C3N4与MZF 复合后对g-C3N4晶体的周期性结构造成一定的破坏。

图1 MZF, g-C3N4/MZF和g-C3N4的XRD衍射图Fig 1 XRD patterns of MZF, g-C3N4/MZF and g-C3N4
2.2 材料的傅里叶红外光谱分析(FT-IR)
图2为g-C3N4/MZF, MZF和g-C3N4的FT-IR谱图。从图2中可知3 159 cm-1处观测到N-H 键的伸缩振动峰,而位于1 631 cm-1处的吸收峰分别对应O-H键的伸缩振动和弯曲振动。纯净MZF样品在544 cm-1处的吸收峰,对应于中Fe-O[15]带的对称拉伸振动峰,此特征峰是尖晶石型铁氧体结构中所特有的金属氧离子的振动吸收峰。g-C3N4谱线上主要的吸收峰依次位于1236, 1317, 1403和1 539 cm-1,与碳氮六元杂环的典型伸缩振动对应[8],而在806 cm-1处的吸收峰代表着三嗪环结构的弯曲振动。在g-C3N4/MZF复合物吸收图谱中,g-C3N4和 MZF的全部特征吸收峰均可被观测到,由此证明g-C3N4和MZF两相共存于g-C3N4/MZF复合物中,且该结果与XRD 分析中的结论一致。

图2 g-C3N4/MZF, MZF和g-C3N4的FT-IR测试图Fig 2 FT-IR spectra of g-C3N4/MZF, MZF and g-C3N4
2.3 材料的形貌分析(SEM、TEM)
通过SEM(图3)可以观察到典型尖晶石状的MZF微观结构。在TEM(图4a)分析中可清楚的看到g-C3N4具有类石墨烯的层状结构。图4b中,MZF为暗的部分,g-C3N4为亮的部分,二者表现出良好的相互交杂并具有光滑的连接处。通过观察图4c,g-C3N4和MZF异质结的形成被进一步验证,MZF为核被g-C3N4外壳包围。此外,还可以清晰的观测到MZF的(311)面对应的2.56Å (由Scherrer公式计算得到)原子晶格条纹(图4d),g-C3N4的(002)面清晰可见,这与XRD的结果相符合。而在图4e中,g-C3N4/MZF复合材料的EDS光谱也证明了锰、锌、铁、碳、氮和氧的存在。在进行TEM测试之前复合物经过长时间的超声处理,而g-C3N4/MZF的连接界面依旧存在,由此说明了两者的连接为强相互作用,g-C3N4/MZF在结构上形成了异质结,而不是两个分离相的物理混合物,这种紧密耦合有利于电荷在g-C3N4和MZF之间转移,并促进光生电子-空穴对的分离,从而提高光催化性能[18]。

图3 MZF的SEM电镜图Fig 3 SEM pattern of MZF

图4 g-C3N4/MZF(3:2)的TEM图像(a,b,c,d)和TEM-EDs(e)图像Fig 4 TEM images and TEM-EDS image of g-C3N4/MZF(3∶2)
2.4 材料的光电子能谱分析(XPS)
图5为g-C3N4/MZF的X射线光电子能谱,图5(a)中g-C3N4/MZF的全谱测试结果,用C 1s电子结合能(285.2eV)进行校正。各元素所对应的特征峰均已在谱线上标注。图5(b)~图5(g)分别为Mn 2p,Zn 2p,Fe 2p,N 1s,C 1s,O 1s的精细扫描图谱。图5(b)为Mn 2p轨道光谱图,Mn 2p和g-C3N4/MZF中的各元素相比,相对含量较少,因此在全谱和单个元素的轨道光谱中,特征峰并不突出,在650.4和640.0eV结合能处观测到Mn 2p1/2和Mn 2p3/2特征峰,说明Mn元素主要以2+的价态存在。图5(c)可观察到Zn元素2p1/2和2p3/2的对应轨道的电子结合能分别为1043.8和1020.6eV,和Zn2+的化合物的特征峰描述一致。在图5(d)Fe 2p的轨道的光谱图中,Fe 2p1/2和Fe 2p3/2两个主能谱峰的结合能分别是724.4和710.6 eV,在715.1 eV处是Fe3+化合物的卫星峰。图5(e)的N 1s轨道光谱中,在398.1、398.8和400.2 eV处出现N 1s特征衍射峰,分别对应的是C-N-C,N-(C)3和N-H各化学环境中的N元素的特征衍射峰。在C 1s图谱图5(f)中,287.8 eV的特征峰是N-C=N中的C,在284.2 eV观察到的衍射峰是碳氮化合物中C的特征峰。在531.7和529.3 eV结合能处出现的氧峰O1s,如图5(g)所示,分别对应的水分子中-OH的O和MZF中晶格中的O。XPS的图谱表明g-C3N4已成功掺杂到材料中,其结果与XRD分析结果相符。

图5 (a) g-C3N4/MZF(3:2)XPS的全谱图;(b)Mn 2p的XPS光谱图;(c)Zn 2p的XPS光谱图;(d)Fe 2p的XPS光谱图;(e)N 1s的XPS光谱图;(f)C 1s的XPS光谱图和(g)O 1s的XPS光谱图Fig 5 (a) XPS survey of g-C3N4/MZF(3:2); (b) Mn 2p XPS spectra; (c) Zn 2p XPS spectra; (d) Fe 2p XPS spectra; (e) N 1s XPS spectra; (f) C 1s XPS spectra and (g) O 1s XPS spectra
2.5 材料的光催化活性及光催化机理
2.5.1 材料的光催化活性
用对RhB的降解能力对材料g-C3N4,MZF和g-C3N4/MZF进行光催化性能评定。图6a为在黑暗环境中样品对RhB的降解曲线,通过空白及对照实验,发现样品30 min后对RhB达到吸附/解吸平衡,RhB基本未被降解,说明催化剂对RhB仅造成极少的吸附效果。而在g-C3N4/MZF(3:2)/H2O2体系中,出现一定程度的降解,其原因为H2O2分解出少量的·OH。图6b为0.5g/L的不同种催化剂在一定量的电子捕获剂及可见光条件下降解100mLRhB的浓度变化曲线。由图6b可知,MZF催化剂对RhB的降解效果较差,纯g-C3N4则表现出较高的光催化活性,这归因于g-C3N4带隙和独特的电子结构。而g-C3N4/MZF复合物在加入H2O2和可见光照射的条件下对RhB具有明显的降解作用,降解率达到96.0%,这是因为该复合物的有效异质界面异质结有效地提高了材料的光催化活性,降低了光生电子和空穴的复合速率。其中0.5g/L的g-C3N4/MZF(3∶2)/可见光条件下降解效果最好,照射210min后,对RhB的降解率达到96.0%。

图6 (a)不同反应物黑暗中对RhB降解率; (b)各样品在H2O2(0.05mol)/可见光条件下对RhB 降解率; (c)各样品在H2O2(0.05mol)/可见光降解RhB一级动力学拟合; (d)g-C3N4/MZF(3∶2)/可见光不同H2O2浓度对RhB 降解率;(e)g-C3N4/MZF(3∶2)/可见光不同H2O2浓度降解RhB一级动力学拟合Fig 6 (a) The degradation rate of RhB by different reactants in the dark; (b) the degradation rate of RhB in each sample under H2O2 (0.05mol) /vis; (c) the first-order kinetics fitting of RhB degradation of each sample under H2O2 (0.05mol)/vis; (d) the RhB degradation rate of g-C3N4/MZF(3∶2)/vis at different H2O2 concentrations; (e) the first-order kinetics fitting of RhB degradation by g-C3N4/MZF(3∶2)/vis with different H2O2 concentrations
为了更好的观察复合物的降解规律和反应动力学,用实验数据拟合了一阶反应动力学,结果如图6(c)所示。g-C3N4/MZF(3:2)复合物的降解速率将对最高为k=0.01278 min-1。实验还对H2O2作为电子捕获剂的用量进行了讨论,H2O2的浓度为影响复合物降解效率的重要因素[19]。图6(d)为在可见光条件下不同浓度H2O2与0.5g/L的g-C3N4/MZF(3∶2)催化剂降解RhB的降解率曲线。同时结合降解速率变化曲线(图6e),结果表明0.05mol的用量为电子捕获剂的最佳用量。在0.005~0.05 mol/L的H2O2用量范围内,随着捕获剂用量的增加催化剂的降解速率常数明显提高。然而,当H2O2初始浓度进一步增至0.1 mol/L时,降解速率常数出现下降,此现象可解释为过氧化氢的抑制作用,H2O2浓度的增加可促进·OH自由基的清除和随后新的自由基(H2O·)形成。
2.5.2 材料的光催化机理
用紫外可见漫反射光谱研究了样品的光吸收性能[20-21],结果见图7a,MZF样品对光有较强的吸收强度,MZF的掺杂使g-C3N4吸收峰发生明显红移,并对可见光吸增强度,g-C3N4/MZF(3∶2)的最大吸收带为524nm,复合材料提高了光的利用率。同时g-C3N4/MZF的光吸收曲线与纯 g-C3N4的吸光度曲线接近,即在可见光范围(<540nm)内均发生吸收,但其吸收能力强于纯 g-C3N4。计算(ahv)2并与 hv作图,如图7(b)所示,g-C3N4/ MZF的禁带宽度(Eg)为2.73 eV,而g-C3N4和MZF的带隙分别为2.76和0.615 eV,再通过XPS[22]价带谱图(图7(c))得到3种材料的带隙结构(图7(d)),所制复合物具备较大的光吸收范围,较高的可见光利用率及光催化效率。

图7 (a)样品紫外漫反射; (b)(ahv)2对 hv的带隙计算图; (c)XPS价带谱图;(d)带隙结构Fig 7 (a) Diffuse UV-vis DRS spectra; (b) plots of (ahv)2vs.hv; (c) valence band XPS spectra; (d) the band structures of the samples
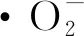

图8 g-C3N4/MZF/H2O2/vis体系降解RhB的机理Fig 8 Mechanism for RhB degradation by g-C3N4/MZF/H2O2/vis system
(3)
(4)
H2O2+e-→·OH+OH-
(5)
h++H2O→·OH+H+
(6)
·OH + RhB→degradation products
(7)
2.6 g-C3N4/MZF的磁性及重复实验的稳定性
g-C3N4/MZF样品经5次重复实验的RhB降解曲线如图9(a)所示,第5次实验中对Rh B的降解率仍可保留在90%以上,有着较好稳定的光催化活性。
图9(b)为样品光催化反应前后的XPS图谱,图中反应前后复合物的特征峰并未消失,说明g-C3N4/MZF在反应过程中仅起催化作用,且有着稳定的化学性质。图9(c)为所制MZF和g-C3N4/MZF(3:2)的磁滞回线谱图,两种样品的饱和磁化强度(Ms)分别为91.1 和43.4 Am2·kg-1,内插图为反应后用磁铁回收复合物图,10s内可将g-C3N4/MZF全部回收。由图9(d)可知材料MZF和g-C3N4/MZF的剩余磁化强度(Mr)分别为0.789 和0.037Am2·kg-1;矫顽力(Hc)分别541.28 A/m和83.58 A/m;制备的产物具有较低的矫顽力(83.58 A/m)。证明复合材料g-C3N4/MZF有着较强的磁性,易磁化且易退磁,便于分离和回收并循环使用[20]。

图9 (a)g-C3N4/MZF(3:2)材料重复实验对RhB降解能力的变化;(b)反应前后样品的XPS谱图; (c)MZF和g-C3N4/MZF(3:2)的磁滞回线谱图(插图为使用外部磁铁进行磁分离后的溶液);(d)剩余磁化强度(Mr)和矫顽力图(Hc)Fig 9 (a) Photocatalytic performance of g-C3N4/MZF(3:2) in repeated experiments; (b) XPS spectra of samples before and after reaction; (c) hysteresis loops for MZF and g-C3N4/MZF(3:2) (the insets show the solution after magnetic separation using an external magnet); (d) remanent magnetization(Mr) and coercivity diagram(Hc)
3 结 论
(1)以g-C3N4和MZF为原料,采用自组装法合成了g-C3N4/MZF复合材料,用XRD、FIRT、XPS、TEM等手段进行表征,g-C3N4和MZF之间形成异质结结构。
(2)在g-C3N4/MZF(3∶2)复合材料中,g-C3N4和MZF的光生电子相互迁移,这一过程可以有效地改善光生电子-空穴对的分离效率,降低其复合的可能性,从而显著地提高光催化活性,并在可见光下照射210 min后,对相同染料达到96.0%降解率。
(3) g-C3N4/MZF复合磁性材料对RhB表现出较高的光催化活性,在实验重复到第5次时,仍保持90%以上光催化降解率,具有稳定的光催化性能和化学性质。且材料具备强磁性,其在降解环境污染物的过程中易于回收以再次使用。
