酪酸梭菌活菌散联合多潘立酮治疗小儿功能性消化不良的疗效及相关作用机制
2021-08-04吴晓燕秦侃王杨张旭中张玄
吴晓燕,秦侃,王杨,张旭中,张玄
(合肥市第一人民医院1.儿科,2.药剂科,安徽 合肥230061;3.安徽医科大学附属医院 儿科,安徽 合肥230032;4.安徽省立医院 儿科,安徽 合肥230002;5.湖北省妇幼保健院儿童保健科,湖北 武汉430070)
功能性消化不良(functional dyspepsia,FD)是儿科常见的消化系统功能紊乱性疾病,患儿常伴有腹胀、恶心、腹痛、早饱、嗳气等临床症状[1-2]。FD 虽为良性疾病,但病程较长,且症状反复发作或持续存在,不利于患儿的健康发育。目前临床尚无特效药物治疗,多以经验性对症治疗为主[3]。多潘立酮属于一种外周多巴胺受体拮抗剂,可加速胃排空,降低胃内压力,减轻胃酸对胃黏膜的损伤,目前广泛用于促进胃及十二指肠蠕动方面治疗中,但长期使用易产生耐药性[4-5]。临床实践发现,胃肠动力药物联合微生物制剂治疗,可加快肠黏膜修复,维持胃肠激素及细胞因子平衡,抑制有害细菌生长[6]。酪酸梭菌活菌散属于革兰阳性厌氧菌制剂之一,用于急慢性腹泻中效果明显,有助于提升胃蛋白酶活性,增强患儿消化功能,但临床关于酪酸梭菌活菌散对FD 患儿是否可产生同样效果的报道较少[7-8]。鉴于此,本研究采取前瞻性随机对照试验,评价酪酸梭菌活菌散联合多潘立酮对FD 患儿疗效、胃动力学、脑肠轴及胃肠激素等的影响,并分析相关作用机制,旨在为临床治疗提供依据。现总结如下。
1 资料与方法
1.1 一般资料
选取2019年3月—2020年7月就诊于合肥市第一人民医院的144 例FD 患儿。根据不同治疗方法将患儿分为对照组和观察组,每组72 例。纳入标准:符合《中国儿童功能性消化不良诊断和治疗共识》[9]中FD 诊断标准;年龄3~16 岁;经内窥镜、B 超等检查未见消化系统器质性病变;入组前4 周未接受微生态制剂、促动力、抗感染等药物治疗;患儿家属知情并签署同意书。排除标准:由胃十二指肠、食管等部位器质性病变而诱发的消化不良;合并先天性心脏病、先天性胃肠畸形、脑性瘫痪、肠道寄生虫病;伴有肝、肾衰竭;内分泌功能严重紊乱、凝血功能障碍、严重贫血、严重免疫系统缺陷;伴有败血症、感染等其他并发疾病。对照组男性35例,女性37 例;年龄3~12 岁,平均(6.03±2.13)岁;病程3~15个月,平均(6.13±2.73)个月;体重13~37 kg,平均(25.03±3.76)kg。观察组男性33例,女性39例;年龄4~12 岁,平均(7.11±2.03)岁;病程4~18 个月,平均(6.73±2.02)个月;体重14~40 kg,平均(26.37±4.05)kg。两组患儿一般资料比较,差异无统计学意义(P>0.05),具有对比性。
1.2 方法
两组患儿给予常规支持治疗,包括调整饮食、建立良好排便习惯、预防及纠正水电解质与酸碱平衡等。在此基础上,对照组接受多潘立酮治疗,即饭前15~30 min 口服多潘立酮多潘立酮混悬液(北京首儿药厂,国药准字H20094232),0.3 mg/(kg·次),3 次/d。观察组采取酪酸梭菌活菌散+多潘立酮(用法、用量均与对照组一致)治疗,饭前15~30 min温水送服酪酸梭菌活菌散(日本米雅利桑制药株式会社,批准文号:SJ20140075),1 g/次,2 次/d。两组均治疗1 周。
1.3 评价指标
①疗效:治疗1 周后,恶心呕吐、腹痛等临床症状全部消失,食欲、食量恢复至正常,胃动力学指标在正常范围内为治愈;临床症状部分缓解,食欲及胃动力学指标恢复明显,食量恢复至正常水平的50%为好转;临床症状、食欲、食量及胃动力学指标均未见好转,或病情加重为无效。总有效=治愈+好转。②胃动力学:治疗前、治疗1 周后使用超声显像仪[型号:CX-970D,绵阳索尼克电子有限责任公司,国食药监械(准)字2008 第3230661 号]测定胃窦收缩幅度、胃窦收缩频率、胃窦运动指数。操作如下:检查前禁饮2~3 h,禁食4~8 h,患儿取坐位,接受空腹B 超,从剑突下行纵行切面可见椭圆形胃窦,其中胃窦容积的计算为胃窦的前后径与1/2 左右径之和。后嘱患儿饮适量温桔子水,6 min后检测患儿胃窦收缩幅度、胃窦收缩频率、胃窦运动指数。③血清相关指标:采集患儿治疗前、治疗1周后采外周静脉血3 ml,以3 000 r/min 离心10 min,通过酶联免疫吸附法(试剂盒购自北京北方生物技术研究所有限公司)测定5-羟色胺(5-HT)、神经肽S受体1(NPSR1)、P 物质(SP)及生长抑素(SST)水平,使用放射免疫计数仪(型号:CN20 型,北京中西远大科技有限公司)测定胃动素(MTL)、促胃泌素(GAS)、瘦素(Leptin)水平,所有操作严格按照说明书执行。④安全性:观察两组患儿用药期间是否出现头晕、嗜睡、胃肠道反应(恶心、呕吐、腹泻、腹痛)等不适症状。
1.4 统计学方法
数据分析采用SPSS 23.0 统计软件。计量资料以均数±标准差(±s)表示,比较用t检验;计数资料以率(%)表示,比较用χ2检验。P<0.05 为差异有统计学意义。
2 结果
2.1 两组患儿疗效比较
两组患儿总有效率比较,差异有统计学意义(χ2=4.516,P=0.034),观察组较对照组高。见表1。

表1 两组患儿疗效比较 [n=72,例(%)]
2.2 两组患儿治疗前后胃动力学指标的变化
两组患儿治疗前后胃动力学指标的差值比较,差异有统计学意义(P<0.05),对照组较观察组高。见表2。
表2 两组患儿治疗前后胃动力学指标的差值比较(n=72,±s)
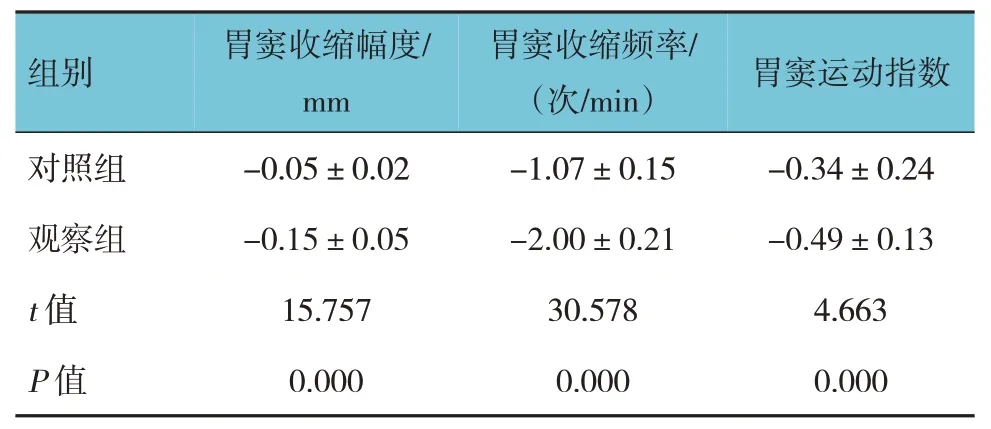
表2 两组患儿治疗前后胃动力学指标的差值比较(n=72,±s)
组别胃窦运动指数胃窦收缩幅度/mm胃窦收缩频率/(次/min)对照组观察组t 值P 值-0.05±0.02-0.15±0.05 15.757 0.000-1.07±0.15-2.00±0.21 30.578 0.000-0.34±0.24-0.49±0.13 4.663 0.000
2.3 两组患儿治疗前后脑肠轴相关因子的变化
两组患儿治疗前后脑肠轴相关因子的差值比较,差异有统计学意义(P<0.05),对照组5-HT、SP 较观察组低,NPSR1 较观察组高。见表3。
表3 两组患儿治疗前后脑肠轴相关因子差值比较(n=72,±s)

表3 两组患儿治疗前后脑肠轴相关因子差值比较(n=72,±s)
组别5-HT/(mg/L)NPSR1/(pg/ml)SP/(pg/ml)对照组观察组t 值P 值21.05±4.26 34.84±5.97 15.955 0.000-18.91±3.16-28.97±4.92 14.598 0.000 10.56±2.02 17.00±2.44 17.251 0.000
2.4 两组患儿治疗前后胃肠激素比较
两组患儿治疗前后胃肠激素比较,差异有统计学意义(P<0.05),对照组MTL、GAS 较观察组高,SST、Leptin 较观察组低。见表4。
表4 两组患儿治疗前后胃肠激素比较(n=72,ng/L,±s)
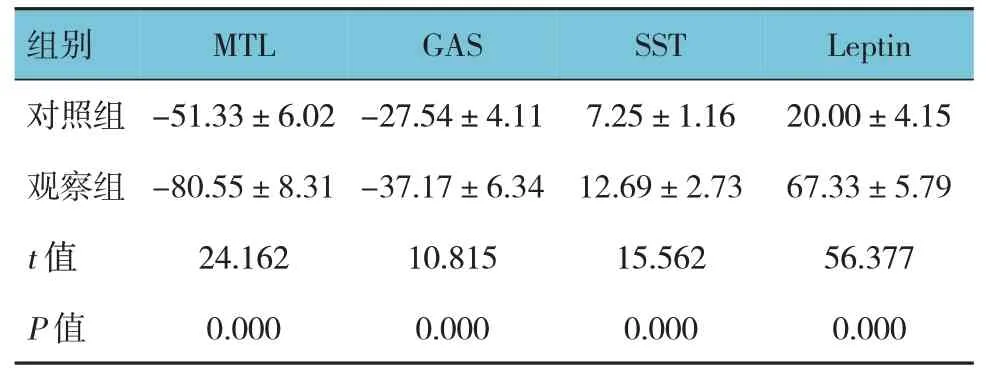
表4 两组患儿治疗前后胃肠激素比较(n=72,ng/L,±s)
组别MTL GAS SST Leptin对照组观察组t 值P 值-51.33±6.02-80.55±8.31 24.162 0.000-27.54±4.11-37.17±6.34 10.815 0.000 7.25±1.16 12.69±2.73 15.562 0.000 20.00±4.15 67.33±5.79 56.377 0.000
2.5 两组患儿不良反应率比较
两组患儿不良反应率比较,差异无统计学意义(χ2=1.719,P=0.326)。见表5。

表5 两组患儿不良反应率比较 [n=72,例(%)]
3 讨论
流行病学研究显示,FD 发病率约占儿科疾病的10%~20%,且近年来呈不断上升趋势[10]。FD 病理、生理机制复杂,迄今为止尚未完全阐明,多认为是由遗传、心理、精神等诸多因素共同作用的结果,而胃酸分泌增多、胃肠动力障碍、内脏高敏感性、幽门螺杆菌等与FD 发病密切相关[11-12]。目前,临床治疗小儿FD 的重点在于消除症状、改善胃动力、预防复发,但尚未形成关于小儿FD 的治疗标准。因此,如何制定一种高效安全的治疗方案是目前临床工作中亟待解决的难题。
本研究结果发现,观察组治疗总有效率较对照组高,治疗前后胃窦收缩幅度、胃窦收缩频率、胃窦运动指数差值较对照组高,与杨丽萍[13]研究结果基本一致,再次表明酪酸梭菌活菌散联合多潘立酮治疗FD 患儿的疗效确切,有助于改善患儿胃动力学参数。分析其原因可能与两种药物的以下几点作用机制相关:①多潘立酮可选择性阻断多巴胺2 受体,恢复食道下端括约肌张力,增强食道蠕动,加速胃排空,减少对胃部刺激,预防胃-食管反流[14];②酪酸梭菌活菌散中富含大量酪酸梭菌,而酪酸梭菌为人体正常肠道的常驻菌,可通过与Toll 样受体相结合,而调节Caja1 间质细胞的活动,刺激肠上皮细胞分泌诸多细胞因子,利于肠道菌群定植,改善肠道动力功能及肠黏膜屏障功能[15];③酪酸梭菌可与肠内有益菌共存,抑制腐败菌生长,消耗肠内氧气,减少胺、吲哚等肠道毒素产生,进而形成有利于双歧杆菌生长的无氧环境;④酪酸梭菌活菌散分泌的低聚糖酶可将食物残渣中的多糖向低聚糖转化,有助于有益菌繁殖及生长,抑制致病菌繁殖,进而恢复肠道菌群失衡;⑤酪酸梭菌活菌散可抑制炎症介质异常表达,减轻或消除肠道炎症,提高肠道免疫耐受力[16-17]。因此,多潘立酮、酪酸梭菌活菌散两种药物联合应用可发挥协同作用,起到减轻胃肠道症状、改善消化功能的作用。
脑-肠-肽是情感认知中枢与肠神经系统、免疫系统、神经内分泌系统相联系的神经-内分泌网络,心理、精神异常及外在刺激可影响神经/胃肠神经通路,降低环形肌收缩力及迷走神经张力,减慢传导速度及胃收缩频率,减弱胃运动,增高内脏敏感性,进而造成胃肠动力障碍[18]。高宏[19]在一项关于FD 与血浆NPSR1 的关系研究中指出,相比健康者,FD 患者血浆中NPSR1 浓度较低,且与FD 发生密切相关。吴晓芳等[20]在一项动物实验中发现,模型组大鼠存在明显脑-肠-肽紊乱,即表现为Ghrelin、MTL、GAS 含量降低,SP、VIP 含量上升,通过调节脑-肠-肽表达,可达到治疗疾病的效果。本研究中观察组治疗前后5-HT、SP、SST、Leptin 差值较对照组高,NPSR1、MTL、GAS 水平较对照组低,可见酪酸梭菌活菌散联合多潘立酮治疗有助于调节FD 患儿脑肠轴因子,改善胃肠激素,保障正常的胃肠运动。原因在于紊乱的微生态作用于脑肠轴,可诱发胃肠激素紊乱及炎症因子释放,增加通透性,造成低度炎症及免疫激活,而酪酸梭菌活菌散作为微生态制剂之一,可产生丁酸及微生物、酶类物质,加快肠黏膜及血脑屏障修复,形成肠道生物学屏障,促进黏膜再生,改善肠道内环境,抑制黏膜受损部位的有害细菌生长,调整肠道菌群平衡,进而维持肠道正常的生理功能、免疫功能[21-22];此外,酪酸梭菌活菌散可降低肿瘤坏死因子-α 的诱导活性,抑制炎症反应及细胞因子诱导的凋亡,进而增强腺体分泌功能,降低胃肠蠕动、内脏的敏感性,调节胃肠激素水平[23]。考虑到联合用药的安全性,本研究在治疗期间密切监测患儿的不良反应,结果发现,观察组不良反应率相比对照组未见明显差异,说明酪酸梭菌活菌散联合多潘立酮治疗FD 的安全性较高,未明显增加不良反应,患儿可耐受。
综上所述,酪酸梭菌活菌散联合多潘立酮治疗FD 患儿的疗效确切,且未明显增加不良反应,其作用机制可能与改善胃动力学、调节脑肠轴因子及胃肠激素水平有关。但本研究仍存在样本量低、观察周期短、病例来源单一等不足,故后期需进一步开展多中心、大样本量的研究。
