基于流式细胞术和基因组Survey的绣球基因组大小及特征分析
2021-08-02陈双双齐香玉冯景王华娣邓衍明
陈双双 齐香玉 冯景 王华娣 邓衍明
摘要:绣球花序饱满、花型多样、花色丰富,是重要的观赏植物。很多绣球品种种植在酸性含铝的土壤中时,花序可由红色变为蓝色、紫色或蓝紫色,使其更受消费者喜爱。但绣球基因组信息缺乏,基因资源开发和分子机制研究相对滞后。利用流式细胞术和基于K-mer分析的基因组Survey技术估测绣球主栽品种“Bailer”(商品名:Endless SummerTM,中文名译为无尽夏)的基因组大小。流式细胞术分析结果表明,以豌豆(Pisum sativum L.)为对照的流式细胞术估测“Bailer”基因组大小为2.17 pg(约2.12 Gb);Illumina HiSeq PE測序产生212.41 Gb的有效数据,K-mer 分析结果显示,修正后的基因组大小为1.96 Gb;根据K-mer分析,该基因组具有明显的杂合峰,杂合度和重复率分别为1.97%、72.80%。此外,经组装,该基因Contigs总数为7 418 139(N50为249 bp),总读长为1.49 Gb,Scaffolds 总数为7 071 975(N50为289 bp),总读长为1.52 Gb,GC含量为38.75%。综上所述,推测绣球“Bailer”基因组大小约为1.96~2.12 Gb,属杂合度较高的复杂基因组。结果可为绣球全基因组测序及相关研究提供了理论依据。
关键词:绣球;基因组大小;流式细胞术;K-mer分析;Survey技术
中图分类号:S685.990.1 文献标志码: A
文章编号:1002-1302(2021)12-0039-06
收稿日期:2020-10-10
基金项目:国家自然科学基金(编号:31901359);江苏省农业科学院探索性颠覆性创新计划[编号:ZX(17)2004];江苏省昆山市科技项目(编号:KN1809)。
作者简介:陈双双(1986—),女,河南安阳人,博士,助理研究员,主要从事观赏植物遗传育种与分子生物学研究。E-mail:chenshuang7876@sina.com。
通信作者:邓衍明,博士,研究员,主要从事花卉遗传育种与分子生物学研究。E-mail:nksdym@163.com。
绣球(Hydrangea macrophylla)别称八仙花,属于虎耳草科绣球属,因其花序色彩艳丽、开花期长、适应性广和抗逆性强而被广泛种植[1]。绣球是观赏植物中的强耐铝(Al)植物,其成熟叶片和萼片可以积累高于3 000 μg/g Al而不呈现任何毒性症状[2]。部分绣球品种花色易变,调节栽培土壤pH值及Al3+含量能使其呈现红色、紫色或蓝色等不同颜色[3]。大量研究表明,萼片中飞燕草素-3-O-葡萄糖苷与Al3+的络合物调控萼片颜色,而颜色的变化取决于萼片中Al3+含量[3-4]。因此,绣球不仅是非常值得开发的观赏植物资源,而且是研究观赏植物蓝色花形成机制的特色材料,在花卉育种领域具有较大的应用价值。
长期以来,对绣球的研究多集中在栽培和育种领域[5-6];近年来,人们开展了绣球分子生物学特性相关研究,如分子标记的开发[7]、花色变化的分子机制[8-10]、铝转运相关基因克隆与功能研究[11-13]等。基因组特征研究是植物基因资源开发和分子机制研究的前提,然而,关于绣球不同品种基因组大小及特征研究的报道尚少,无法为分子生物学研究提供足够的理论基础。早在1957年,绣球体细胞染色体数首次被鉴定为2n=2x=36[14],并在Funamoto等的研究中得到证实[15];此后,Cerbah等也发现,多数绣球种和亚种的染色体数为36,为二倍体(2n=2x=36)[16]。绣球不同品种具有不同大小的基因组,大花绣球[H. macrophylla ssp. macrophylla (Thunb.) Ser.]和粗齿绣球(H. macrophylla ssp. serrata Ser.)的1C值分别为2.15、1.92 pg,相应地GC含量分别高达41.0%、40.6%[16];进一步研究发现,大花绣球二倍体品种的1C值在1.98~2.49 pg之间,但也有研究表明,大花绣球Taube 1C值为(3.75±0.05) pg,而Veitchii为(2.35±0.05) pg[17-19]。这些结果均是基于流式细胞术估测的结果。
流式细胞术和基于K-mer分析的基因组Survey测序是估测基因组大小的常用方法,前者用于评估基因组大小和倍性水平,操作简单,分辨率高,准确性高,后者具有高通量测序、速度快和数据量大等优点[20-21]。本研究采用流式细胞术和基于K-mer分析的基因组Survey测序对大花绣球主栽品种“Bailer”基因组大小进行估测和相互验证,并对测序质量、杂合度、序列重复率等进行评估测定,旨在为绣球全基因组测序提供重要依据,为绣球进化分析、基因挖掘、遗传改良以及结构基因组研究奠定基础。
1 材料与方法
1.1 试验材料
供试材料大花绣球“Bailer”(商品名:Endless SummerTM,中文名译为无尽夏)种植于江苏省农业科学院绣球种质资源圃内,该品种具有新老枝都能开花和花色极易改变等优点,是绣球的主栽品种。豌豆(Pisum sativum L.,2C=9.09 pg)作为对照[22],种子由江苏省农业科学院江苏省农业种质资源保护与利用平台提供。试验于2019年1月至3月在江苏省农业科学院院内进行。
1.2 试验方法
1.2.1 流式细胞分析 采集“Bailer”和豌豆幼嫩新鲜叶片,分别称取3份,每份约1 g,置于盛有细胞裂解液LB01[15 mmol/L Tris,2 mmol/L Na2乙二胺四乙酸(EDTA),0.5 mmol/L 四盐酸精胺,80 mmol/L KCl,20 mmol/L NaCl,0.1% Triton X-100,pH值为7.0~8.0]的培养皿中,并迅速用锋利的刀片将其切碎。将培养皿中的解离液过滤至1.5 mL离心管中,1 000 r/min 离心 5 min 后弃上清,收集细胞沉淀,加入100 μL解离液悬浮。将待测样品“Bailer”与对照样品豌豆细胞悬液等比例混合,加入荧光染料PI(碘化丙啶),于4 ℃冰箱放置15 min后进行上机检测[20]。
使用美国BD公司的流式细胞仪对“Bailer”基因组大小进行评估,变异系数控制在5%以内。每个样品进行3次重复试验。测试数据利用仪器自带软件FACSTM Software 1.0.0.650进行分析,数据统计分析利用SPSS 17.0完成。绣球基因组(核DNA含量)估算方法如下:待测样品核DNA含量=对照样本核DNA含量×[(待测样品G0/G1 峰荧光强度)/(对照样品G0/G1峰荧光强度)][23]。
1.2.2 样品DNA制备与基因组测序 采集“Bailer”幼嫩叶片,立即用液氮速冻后保存于 -80 ℃。使用天根植物基因组DNA提取试剂盒进行DNA提取,Nanodrop 2000分光光度计(德国,eppendorf)和1%琼脂糖凝胶电泳检测DNA浓度及质量。检测合格的DNA样品通过Covaris超声波破碎仪随机打断成长度为350 bp的片段,经末端修复、加A尾、加测序接头、纯化、PCR扩增等步骤完成整个文库制备,构建好的文库通过Illumina Hiseq PE进行测序。获得的原始数据经过滤后利用Vsearch软件(https://github.com/torognes/vsearch)进行评估,包括数据产量、测序错误率、Q20含量、Q30含量、GC含量等。同时,利用Blast工具将部分有效测序数据(clean data)与NCBI核苷酸数据库(NT)进行比对,选取比对结果中的前3个,分析样本是否存在外源污染。
1.2.3 K-mer分析估算基因组大小、杂合度及重复率 采用基于K-mer的分析方法来估计基因组大小和杂合率等,即从一段连续序列中迭代地选取长度为K个碱基的序列,取K=17进行分析。假设K-mer的深度频率服从泊松分布,并且从碱基讀数中获取的所有K-mer都可以遍历整个基因组,则可以计算K-mer频数分布和K-mer深度分布曲线。根据曲线获得K-mer深度估计值,用于估计基因组大小。通过K-mer曲线的分布情况,估计基因组特征,计算杂合峰值与纯合峰值的比值,从而得到杂合率;利用纯合峰1.8倍后的K-mer个数所占的比例来估计重复序列比例[24]。
1.2.4 基因组组装 利用SOAPdenovo(https://github.com/aquaskyline/SOAPdenovo2)对测序数据进行拼接组装,选择K-mer=41组装Contigs和Scaffolds。将读取长度小于100 bp的低质量序列删除,并将过滤后的有效数据组装为Contigs,最后利用reads之间的连接关系和插入片段大小信息,将Contigs组装成Scaffolds[24]。
2 结果与分析
2.1 基于流式细胞术绣球基因组大小分析
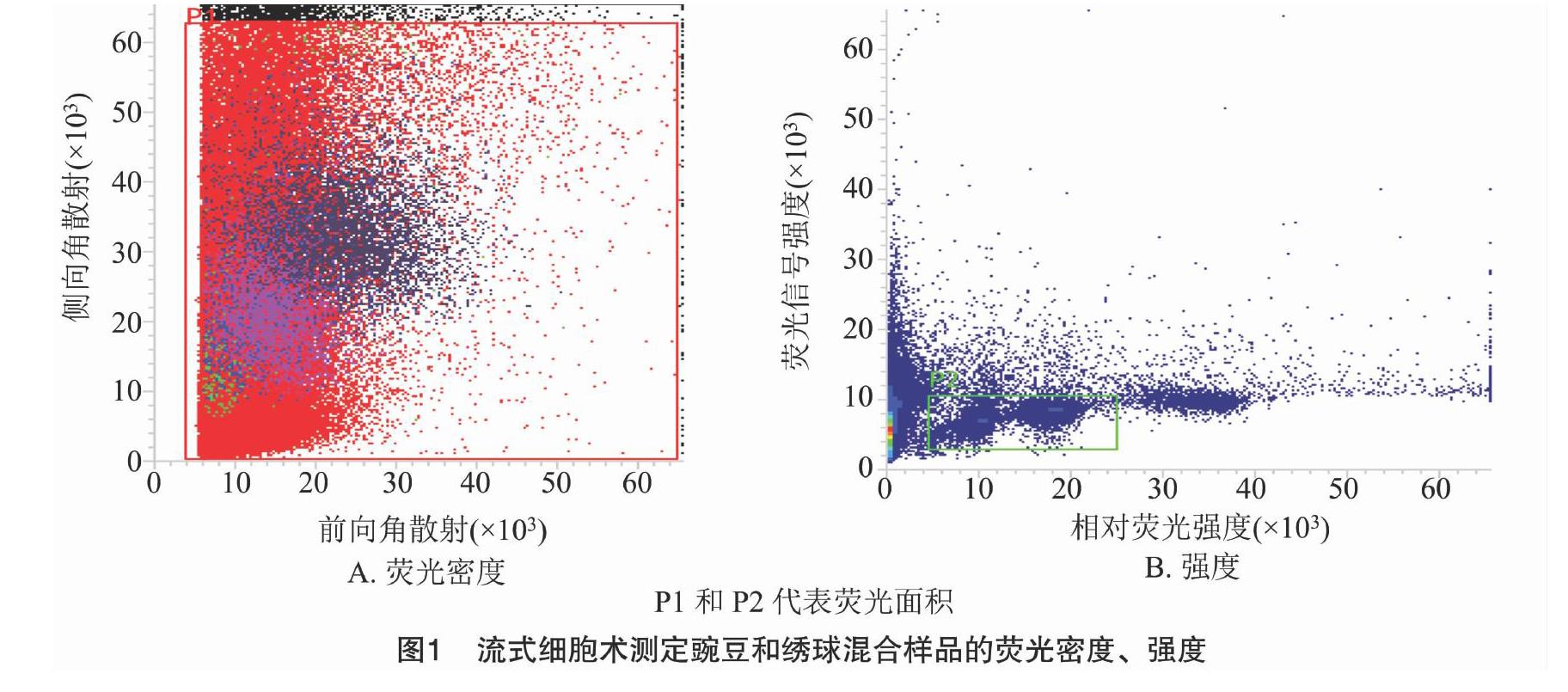
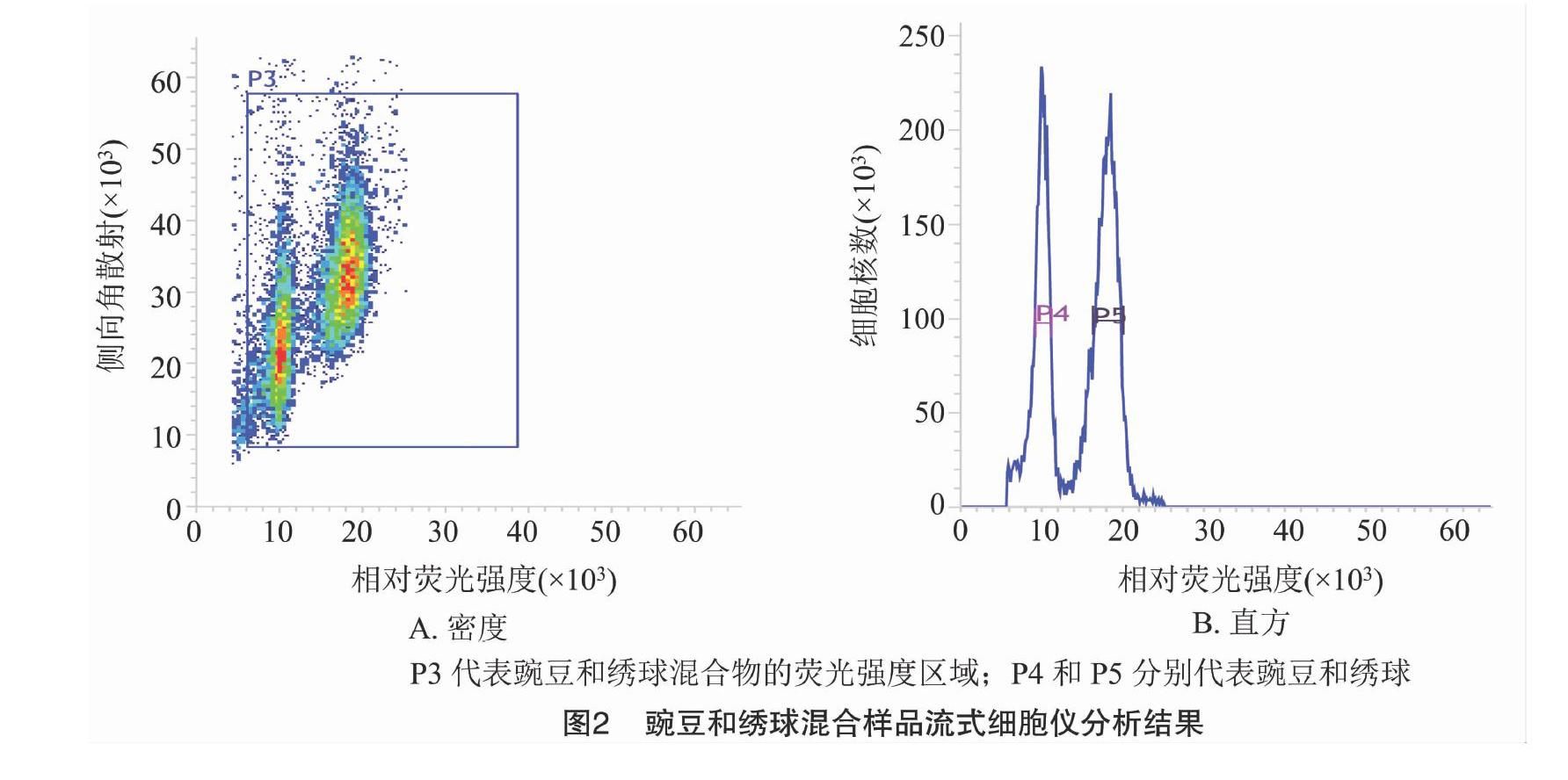
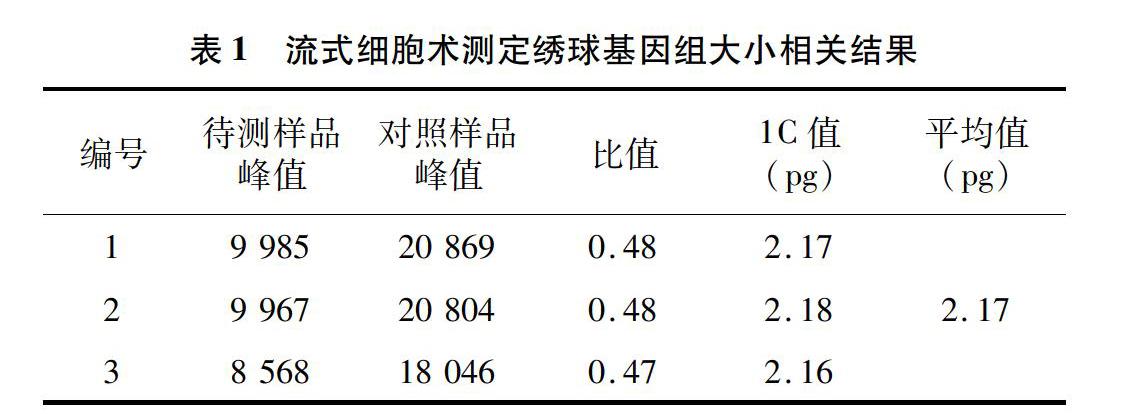
当变异系数控制在5%以内时,待测样品与对照样品的离子清晰集中,并且可以同时检测到混合样品的颗粒簇(图1),因此,解离液LB01和对照样品豌豆对于估算绣球基因组比较适宜,保证了利用豌豆作为对照估算绣球基因组大小的准确性。利用豌豆(2C=9.09 pg)作为对照样品,根据混合样品PI荧光强度以及待测样品与对照样品峰值的倍数关系,计算绣球基因组1C值为2.17 pg(图2、表1)。
2.2 基因组Survey与质量评估
利用Illumina Hiseq PE测序平台对构建的3个插入片段为350 bp的DNA文库(DES01984、DES02239和DES02238)进行双末端测序,经过滤和修正后,获得212.41 Gb的测序数据。测序质量评估显示,这3个文库Q20值分别为96.04%、96.64%、96.99%,Q30值分别为90.8%、92.12%、92.83%(表2),测序错误率均小于0.03%,表明测序质量较好。此外,取每个文库的部分有效测序数据比对到NCBI核苷酸数据库(NT)进行比对,在DES01984、DES02239和DES02238文库中,排名前3的物种分别为粗齿绣球/珙桐(Davidia involucrata Baill.)/大花绣球、大花绣球/粗齿绣球/山茱萸(Cornus officinalis Sieb. et Zucc.)、大花绣球/粗齿绣球/葡萄(Vitis vinifera L.)。根据这些结果,认为序列比对结果为同源比对,样本不存在污染现象(表3)。
2.3 K-mer分析
将获得的有效数据(212.41 Gb)用于“Bailer”K-mer分析,并估测基因组大小、杂合度及序列重复率。从图3可以看出,横坐标表示K-mer出现的次数,纵坐标表示出现的频率;K-mer分布曲线成峰情况较好,呈双峰分布,在50和85附近各有1个峰值。根据survey分析,推测depth=85附近为主峰值,即K-mer的期望深度,K-mer总数为168、564、374、328(图3、表4)。结合公式(基因组大小=K-mer-number/depth)估算得出“Bailer”基因组为1 983.11 Mb,修正后的基因组大小为 1 964.82 Mb(约1.96 Gb,表4)。从图3还可以看出,在主峰的1/2位置处有明显的杂合峰,而且K-mer分布曲线有严重的拖尾,这可能是“Bailer”基因组杂合度和重复序列含量均较高所致。根据公式计算,Bailer基因组杂合度和重复率分别高达1.97%、72.8%。
2.4 基因组组装
利用Soap denovo软件对所获得的有效数据(clean data)进行denovo拼接组装,选择K-mer=41得到最优的拼接效果。组装结果显示,Contigs 总数为7 418 139,N50长度为249 bp,总读长为 1.49 Gb;进一步组装后,Scaffolds 总数为7 071 975,N50和N90长度分别为289 bp和113 bp,总读长为1.52 Gb(表5)。
2.5 GC含量分布
根据GC含量与测序深度相关性分析,Bailer的GC含量为38.75%(图4)。GC-depth分析显示,测序无明显偏向趋势;GC深度分布被分为2层,这可能与基因组杂合度高有关。此外, 取低深度区域的序列与NT数据库比对,未比对上细菌序列,因此可以排除此区域受细菌污染的可能性。
3 讨论与结论
植物基因组大小估测不仅对于物种本身基因组测序具有重要意义,而且可为相关蛋白组、转录组以及代谢产物研究提供不可或缺的基础资料[25-26]。本研究采用流式细胞术和基于K-mer分析的基因组Survey测序估测绣球主栽品种Bailer的基因组大小,为进一步进行基因组测序和相关基因功能研究提供了更准确的信息。
自1983年以来,流式細胞术已成为分析植物基因组大小的标准方法,应用于多种植物基因组大小(C值)的预测[16,24,27-29]。本研究中预测Bailer的1C值为2.17 pg,这与已有报道大花绣球1C值(2.15 pg)接近[16]。但与Jones等所报道的结果不同,该研究中大花绣球二倍体品种的1C值在2.23~2.49 pg之间,其中Bailmer(即Bailer)1C值为 2.37 pg[17]。流式细胞术中采用材料类型、荧光染料、裂解液的化学成分、内标的选择、处理环境等均有可能影响同一物种基因组大小的测定结果[13]。结合已有报道,造成绣球基因组大小差异的原因可能是材料类型和荧光染料不同造成的。本研究利用PI作为荧光染料估测Bailer基因组大小,PI可通过简单的化学计量插入到双链核酸中,无碱基偏好。Cerbah等研究中对绣球1C值估测采用的是溴化乙锭(与PI类似,对细胞计数具有相同特异性)、AT碱基特异性染料Hoechst和GC碱基特异性染料mithramycin作为细胞核荧光染料,但是该研究中没有明确所测品种[16];而Jones等研究采用的是具有AT碱基高度亲和力的染料4′,6′-diamidino-2-phenylindole (DPAI)[17]。
本研究还利用了基于Illumina Hiseq测序平台的K-mer分析技术进一步验证并估测绣球基因组大小。根据3个不同文库的测序数据,使用K-mer分析,修正后的Bailer的基因组大小约为 1 964.82 Mb(1.96 Gb)。根据细胞核DNA含量与基因组大小的关系(1 pg=978 Mb),流式细胞术估测绣球基因组大小为2.17 pg,换算为 2 122.26 Mb,即2.12 Gb。显然,以上2种方法估测的绣球基因组大小不一致,流式细胞术比K-mer分析估测结果大约157.44 Mb。流式细胞术估测基因组较大可能是由于估测结果是参考已知基因组大小的对照样品,而基于K-mer分析的基因组信息是基于数学计算,可能更加全面、准确[20,24,27]。
据报道,兰科蝴蝶兰(Phalaenopsis equestris)基因组杂合度为1.2%[28],康乃馨(Dianthus caryophyllus L.)基因组杂合度为0.2%[30],铁皮石斛(Dendrobium officinale)基因组杂合度为0.48%[31],而本研究基因组杂合度评估显示“Bailer”基因组杂合度则高达1.97%;Bailer基因组序列重复率估测为72.8%,与黄石斛(Dendrobium catenatum Lindl.)接近(78.1%)[32],然而,蝴蝶兰、铁皮石斛和牵牛(Ipomoea nil)基因组仅含有62.00%、63.30%和59.74%的重复序列,康乃馨基因组序列仅有33%的重复率。这些结果可能与基因组大小相关,如黄石斛基因组大小为1.1 Gb[33],蝴蝶兰基因组大小为1.2 Gb[32],铁皮石斛基因组大小为1.3 Gb[31],而康乃馨基因组大小只有Bailer的2/3,为622 Mb。因此,可以推测基因组大小与基因组杂合度和重复率相关。此外,与其他观赏植物如木槿(Hibiscus syriacus,34.04%)[34]、蝴蝶兰(Phalaenopsis cultivar ‘KHM190,30.7%)[28]、康乃馨(36%)[30]相比,Bailer基因组还有较高的GC含量(38.75%)且GC深度分布被分为2层,可能是由基因组的高杂合率引起。根据测序数据组装得到的基因组中,Contigs、Scaffolds总长度分别为1.49、1.52 Gb,其中N50长度分别为249、289 bp,基因组杂合度高可能导致N50值较低[22,31]。显然,绣球基因组是杂合度较高的复杂基因组。
本研究首次利用流式细胞术和K-mer分析的方法测定了绣球基因组大小,并对相应的参数进行了初步评估,主要结论如下:(1)大花绣球Bailer基因组大小估测为1.96~2.12 Gb;(2)绣球基因组具有较高的杂合度(1.97%)和重复率(72.8%),属于复杂基因组范畴;(3)由于绣球基因组杂合率较高,导致有较高的GC含量(38.75%)。本研究结果可为绣球全基因组测序及相关研究提供理论依据。
参考文献:
[1]邓衍明,韩 勇,齐香玉,等. 绣球属植物种质资源分析及其花色可调性和叶斑病抗性比较[J]. 植物资源与环境学报,2018,27(4):90-100.
[2]Ma J F,Ryan P R,Delhaize E. Aluminium tolerance in plants and the complexing role of organic acids[J]. Trends in Plant Science,2001,6(6):273-278.
[3]Schreiber H D,Jones A H,Lariviere C M,et al. Role of aluminum in red-to-blue color changes in Hydrangea macrophylla sepals[J]. Biometals,2011,24(6):1005-1015.
[4]Schreiber H D,Swink A M,Godsey T D. The chemical mechanism for Al3+ complexing with delphinidin:a model for the bluing of hydrangea sepals[J]. Journal of Inorganic Biochemistry,2010,104(7):732-739.
[5]孫晓波,苏家乐,陈双双,等. 大花绣球‘无尽夏组培苗叶片再生植株的研究[J]. 中国农学通报,2020,36(16):67-72.
[6]吴可鹏,徐炜杰,谢丽丽,等. 绣球属植物引种及适应性试验[J]. 浙江农业科学,2020,61 (3):549-551.
[7]贾新平,孙晓波,梁丽建,等. 绣球SSR-PCR反应体系的建立与优化[J]. 华北农学报,2016,31(4):68-73.
[8]Negishi T,Oshima K,Hattori M,et al. Tonoplast-and plasma membrane-localized aquaporin-family transporters in blue Hydrangea sepals of aluminum hyperaccumulating plant[J]. PLoS One,2012,7(8):e43189.
[9]Negishi T,Oshima K,Hattori M,et al. Plasma membrane-localized Al-transporter from blue Hydrangea sepals is a member of the anion permease family[J]. Genes to Cells,2013,18(5):341-352.
[10]龚仲幸,何 勇,杨 静,等. 外源硫酸铝调节八仙花花青苷组成和含量变化的分子生物学机制[J]. 植物营养与肥料学报,2017,23(3):821-826.
[11]Chen H X,Lu C P,Jiang H,et al. Global transcriptome analysis reveals distinct aluminum-tolerance pathways in the Al-accumulating species Hydrangea macrophylla and marker identification[J]. PLoS One,2015,10(12):e0144927.
[12]陈海霞,范 适,胡春梅. 铝胁迫下八仙花HmVALT基因表达的差异[J]. 西北农林科技大学学报(自然科学版),2017,45(5):147-152.
[13]李志奇,陈海霞. 八仙花NRAT1基因的克隆及表达分析[J]. 福建农业学报,2019,34(6):646-651.
[14]Ishih A,Miyase T,Suzuki T,et al. Seasonal variation in the content of a febrifugine and isofebrifugine alkaloid mixture in aerial parts of Hydrangea macrophylla var. Otaksa,with special reference to its antimalarial activity[J]. Journal of Natural Medicines,2006,61(2):213-216.
[15]Funamoto T,Tanaka R. Karyomorphological studies in some taxa of Hydrangea from Japan[J]. Kromosomo,1988(2):1583-1594.
[16]Cerbah M,Mortreau E,Brown S,et al. Genome size variation and species relationships in the genus Hydrangea[J]. Theoretical and Applied Genetics,2001,103(1):45-51.
[17]Jones K D,Reed S M. Analysis of ploidy level and its effects on guard cell length,pollen diameter,and fertility in Hydrangea macrophylla[J]. HortScience,2007,42(3):483-488.
[18]Rinehart T A,Scheffler B E,Reed S M. Ploidy variation and genetic diversity in Dichroa[J]. HortScience,2010,45(2):208-213.
[19]Peter H,Annette H,Conny T. Molecular reconstruction of an old pedigree of diploid and triploid Hydrangea macrophylla genotypes[J]. Frontiers in Plant Science,2018,9:429-442.
[20]Doleel J,Greilhuber J,Suda J. Estimation of nuclear DNA content in plants using flow cytometry[J]. Nature Protocols,2007,2(9):2233-2244.
[21]Yagi M. Recent progress in whole genome sequencing,high-density linkage maps,and genomic databases of ornamental plants[J]. Breeding Science,2018,68(1):62-70.
[22]Doleel J,Barto J. Plant DNA flow cytometry and estimation of nuclear genome size[J]. Annals of Botany,2005,95(1):99-110.
[23]弓 娜,田新民,周香艷,等. 流式细胞术在植物学研究中的应用——检测植物核DNA含量和倍性水平[J]. 中国农学通报,2011,27(9):21-27.
[24]Wang C R,Yan H D,Li J,et al. Genome survey sequencing of purple elephant grass (Pennisetum purpureum Schum ‘Zise) and identification of its SSR markers[J]. Molecular Breeding,2018,38(7):94-104.
[25]Bennett M D,Leitch I J. Nuclear DNA amounts in angiosperms:targets,trends and tomorrow[J]. Annals of Botany,2011,107(3):467-590.
[26]Bourge M,Brown S C,Siljak-yakovlev S. Flow cytometry as tool in plant sciences,with emphasis on genome size and ploidy level assessment[J]. Genetics and Applications,2018,2(2):1-12.
[27]霍恺森,赵冬兰,陈艳丽,等. 甘薯属耐盐植物马鞍藤基因组大小及特征分析[J]. 植物遗传资源学报,2019,20(3):728-735.
[28]Cai J,Liu X,Vanneste K,et al. The genome sequence of the orchid Phalaenopsis equestris[J]. Nature Genetics,2014,47(1):65-72.
[29]齐香玉,陈双双,冯 景,等. 3种瓣型茉莉基因组大小测定与比较[J]. 江苏农业科学,2020,48(19):40-44.
[30]Yagi M,Kosugi S,Hirakawa H,et al. Sequence analysis of the genome of carnation (Dianthus caryophyllus L.)[J]. DNA Research,2014,21(3):231-241.
[31]Yan L,Wang X,Liu H,et al. The genome of Dendrobium officinale illuminates the biology of the important traditional chinese orchid herb[J]. Molecular Plant,2015,8(6):922-934.
[32]Zhang G Q,Xu Q,Bian C,et al. The Dendrobium catenatum Lindl. genome sequence provides insights into polysaccharide synthase,floral development and adaptive evolution[J]. Scientific Reports,2016,6(1):1-10.
[33]Huang J Z,Lin C P,Cheng T C,et al. The genome and transcriptome of Phalaenopsis yield insights into floral organ development and flowering regulation[J]. PeerJ,2016,4:e2017.
[34]Kim Y M,Kim S,Koo N,et al. Genome analysis of Hibiscus syriacus provides insights of polyploidization and indeterminate flowering in woody plants[J]. DNA Research,2017,24(1):71-80.
