抗-HIV ELISA检测窗口期献血者的1例追踪随访分析
2021-07-29温丽玲梁佩贤余玉婷卓创近招淑文
温丽玲,梁佩贤,余玉婷,卓创近,招淑文
广东省佛山市中心血站,广东佛山 528000
获得性免疫缺陷综合征是由人类免疫缺陷病毒(HIV)感染所导致的以免疫系统功能缺陷为特征的致命性疾病。输血是HIV传播的重要途径之一,采供血机构开展HIV抗原抗体等检测后,输血安全性有了较大的提高,但由于酶联免疫吸附试验(ELISA)检测窗口期漏检、病毒变异、试剂的灵敏度低、免疫静默感染和人工失误等原因[1],仍然存在输血传播HIV的残余风险。本血站在进行常规血液筛查时发现,某献血者的ELISA检测各项指标均为阴性,6人份混样核酸检测(NAT)结果为HIV-RNA反应性,在征得献血者的知情同意后,先后进行了4次追踪检测,免疫印迹法由早期的阴性、不确定到后期确认为HIV-1抗体阳性,最终确证该献血者为1例低浓度HIV窗口期献血者,现将该献血者的追踪检测情况报道如下。
1 资料与方法
1.1一般资料 无偿献血者,男,50岁,工人,离异。2018年4月22日在本站捐献机采血小板2个治疗量。采用真空管留取献血者静脉血3管,分别用于核酸检测、ELISA检测和单采血小板捐献前的血型、血常规、丙氨酸氨基转移酶检测,用于核酸检测的标本管4 h内离心,保存于2~8 ℃冰箱。
1.2仪器与试剂 ELISA检测采用全自动酶免加样仪(Microlab STAR 8CH,瑞士Hamilton公司);全自动酶免后处理器(FAME 24/20,瑞士Hammer公司);核酸定性检测采用Cobas′s 201核酸血液筛查系统(瑞士罗氏公司);核酸定量检测采用CAP/CTM 96全自动病毒载量检测系统(瑞士罗氏公司);免疫印迹法使用Tecan PROFIBLOTT48 非温控全自动蛋白印迹仪;抗-HIV ELISA检测试剂盒(北京万泰生物药业股份有限公司);HIV-Ag/Ab ELISA检测试剂盒(美国伯乐公司);MPX v2.0-HIV(1+2型)PCR荧光法核酸检测试剂盒(瑞士罗氏公司);核酸定量检测试剂Roche COBAS AmpliPrep/COBAS TaqMan HIV-1 test,version 2.0(瑞士罗氏公司);HIV抗体确认采用HIV 1+2型抗体检测试剂盒(免疫印迹法,新加坡安倍生物医学亚太私人有限公司)。
1.3方法
1.3.1检测策略 血液标本进行一遍国产试剂、一遍进口试剂的ELISA检测,对于检测结果为双试剂阴性和单试剂反应性的标本,进行瑞士罗氏MPX v2.0 HIV(1+2型)PCR荧光法核酸检测,按照罗氏核酸检测系统要求,为6人份混检模式。对有反应性的6混样标本进行拆分,拆分后判断标本有无反应性;对于检测双试剂反应性的标本送佛山市疾病预防控制中心进行确认试验。
1.3.2献血者HIV阳性确认 对ELISA双试剂反应性、ELISA双试剂无反应性或者ELISA单试剂反应性而核酸定性有反应性的标本送佛山市疾病预防控制中心进行HIV抗体确认试验。
1.3.3献血者追踪检测 在征得献血者知情同意后,于初次献血后每间隔一周随访追踪和采集标本,并对每次采集的标本进行HIV抗原/抗体ELISA检测和核酸的定性、定量检测及HIV确证试验。
1.3.4T淋巴细胞计数检测 在HIV抗体确认检测不确定时,对随访标本进行T淋巴细胞计数检测。
2 结 果
献血者追踪检测 对献血者采取间隔一周随访,追踪随访结果。献血者从献血初次检测ELISA双试剂阴性、NAT阳性、病毒载量为48 copy/mL,1周后随访,进口4代试剂HIV-Ag/Ab转为阳性、病毒载量迅速上升至1.15×106copy/mL;2周后随访,国产4代试剂HIV Ag/Ab转为阳性、病毒载量上升至>1.00×107copy/mL;3周后随访,病毒载量开始下降,免疫印迹法确证试验出现了不确定条带;4周后随访,免疫印迹法确证试验判为阳性。见表1。
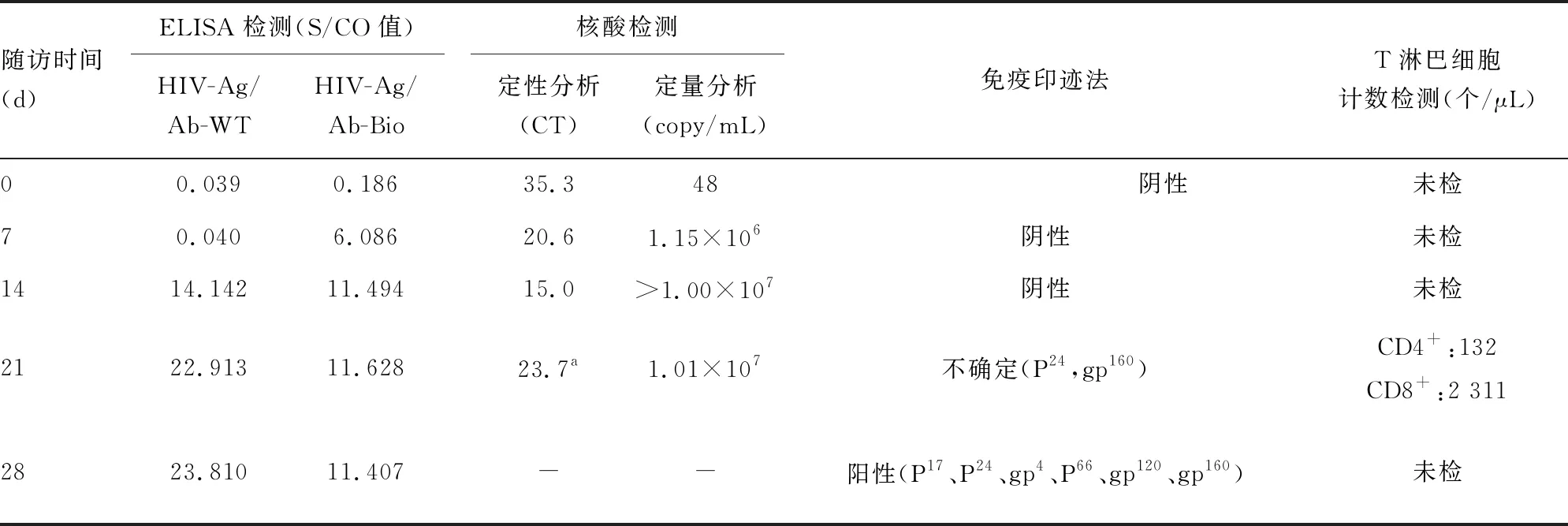
表1 献血者追踪检测结果
3 讨 论
本病例是本站自开展献血者血液NAT工作以来,首次出现NAT阳性、HIV-Ag/Ab阴性的HIV感染窗口期献血者,并连续对该献血者进行的一次追踪随访,最终免疫印迹法确证试验为阳性。对献血者进行了连续跟踪随访,确认其为HIV窗口期感染者,此过程符合HIV感染者体内病毒和抗体的变化规律;其感染标志物的检出次序,NAT>进口4代ELISA>国产4代ELISA>免疫印迹法,也与研究报道一致[2]。有研究显示,HIV抗体和抗原检出时间最短为第19天,使用NAT能缩短至第3天[3]。NAT可将病毒抗体或抗原阴性的慢性携带者及病毒株发生变异的感染者检测出来,除了大幅度缩短血液筛查的窗口期外,也弥补了血清学方法的不足,有效降低了经输血传播HIV的残余风险,提升了输血的安全性[4-7]。
血站在检测HIV抗原抗体的基础上全面开展HIV-RNA检测,4代ELISA试剂可以同时检测HIV的抗原和抗体[8],采供血机构HIV感染标志物的检测应采用NAT和4代ELISA试剂同步检测的模式,一方面可缩短ELISA检测“窗口期”对血液安全的影响,另一方面还可避免因病毒滴度降低、病毒感染株核酸序列变异及标本采集、保存、运输不当等造成的NAT假阴性结果。表1显示,在检测本例标本时,进口4代HIV-Ag/Ab试剂的灵敏度更优于国产试剂,有报道认为HIV-Ag/Ab 4代试剂中国产试剂与进口试剂比较,在批间精密度和最低检出量上尚存在差距[9]。因此,采供血机构在选用4代ELISA试剂时,要尽可能使用一次进口试剂,一次国产试剂,即选用“NAT+4代ELISA进口试剂+4代ELISA国产试剂”检测模式可有效降低输血传播HIV残余风险。
表1显示,献血后21 d追踪随访,CD4+T淋巴细胞数量明显减少,CD4+T淋巴细胞是HIV损害的主要靶细胞,HIV可引起CD4+T淋巴细胞进行性丢失与功能受限;CD8+T淋巴细胞出现反应性升高,并发挥着重要的抑制病毒复制的作用[10];CD4+/CD8+比值下降,当比值<0.20时,HIV感染者机会性感染率会明显增加[11],提示该献血者应该要尽快接受正规治疗,进而防止疾病的2代传播。
目前NAT技术已经大大缩短了HIV检测的窗口期,但仍然没有完全消除窗口期的检测方法。因此,血站在献血前宣传时,应鼓励有高危行为的献血者延迟献血,实施献血后主动自我排除,即保密性弃血[12],同时,也只有确保核酸检测标本的质量才能最大限度保证低浓度标本的检出。
