经典名方化肝煎总黄酮、多糖、无机盐三大类成分及5 种有效成分的含量测定
2021-07-29郭中华李更生其木格张志平刘伟伟王晓冰
郭中华 李更生 其木格 张志平 刘伟伟 王晓冰
1.河南太龙药业股份有限公司研发部,河南郑州 450001;2.河南省中医药研究院科教科,河南郑州 450001
化肝煎是《古代经典名方目录(第一批)》中疏肝解郁、清肝泻火的代表方剂,收载于《景岳全书》(明·张景岳),全方由青皮、陈皮、炒栀子、芍药、丹皮、泽泻、浙贝母七味药配伍而成,用于治疗气逆动火、郁怒伤肝等,效果较好,临床应用广泛[1-2]。
目前有关化肝煎的研究多集中在临床应用及药理作用方面[3-4],而有关其质量研究方面的报道较少,仅有文献[5]报道其指纹图谱测定方法及3 种成分含量测定方法,其可控成分含量占比约3.05%,虽对评价化肝煎质量提供了一定方法,但仍有很多物质基础组成无法整体了解。结合化肝煎中各药味化学成分及药理作用,本研究采用紫外-可见分光光度法(UV-Vis)[6]法测定其总黄酮[7-8]、多糖[9-10]及无机盐三大类成分含量,分析化肝煎物质基础组成,摆脱了定量须先分离的束缚,实现了未能完全分离的复方大类成分的定量;此外还采用高效液相色谱法(HPLC)[5]同时测定化肝煎中没食子酸、栀子苷、芍药苷、芸香柚皮苷、橙皮苷的含量,通过测定复方中大类成分及多种有效成分的含量,以期为化肝煎质量控制提供试验依据。
1 材料与方法
1.1 材料
1.1.1 仪器 Ultimate 3000 高效液相色谱仪、DAD-3000 二极管阵列检测器(赛默飞世尔科技有限公司);TU-1900 紫外-可见分光光度计(北京普析通用仪器有限责任公司);MS105DU 型电子分析天平(梅特勒-托利多仪器上海有限公司);KQ-300E 型超声波清洗器(昆山市超声仪器有限公司)等。
1.1.2 试剂与试药 乙腈、甲醇,色谱纯(默克化工技术有限公司);磷酸,色谱纯(天津市科密欧化学试剂有限公司);无水乙醇、乙酸乙酯,分析纯(天津市科密欧化学试剂有限公司);苯酚,分析纯(天津市富宇精细化工有限公司)等;对照品橙皮苷(批号:110721-201818,质量分数为96.2%)、栀子苷(批号:110749-201718,质量分数为97.6%)、芍药苷(批号:110736-201943,质量分数为95.1%)、没食子酸(批号:110831-201605,质量分数为90.8%)、D-无水葡萄糖(批号:110833-201908,质量分数为99.8%)均购于中国食品药品检定研究院;芸香柚皮苷对照品(批号:250107-201812,质量分数≥98%)购于上海鸿永生物科技有限公司;将化肝煎所用饮片按浸出物高配高、低配低进行组合,依次编号为S1~S16。
1.2 总黄酮含量测定方法
1.2.1 对照品溶液的制备 精密称取橙皮苷对照品适量,加甲醇制成0.2553 mg/mL 的橙皮苷对照品溶液。
1.2.2 供试品溶液的制备 精密称取冻干粉0.25 g 置具塞锥形瓶中,加水25 mL 超声使溶解,摇匀,精密量取20 mL 置分液漏斗中,加乙酸乙酯振摇提取3 次,每次20 mL,合并乙酸乙酯液蒸干,残渣加70%乙醇溶解于20 mL 量瓶,以70%乙醇定容,摇匀,精密吸取2 mL 于50 mL 量瓶中,以70%乙醇定容,摇匀即得。
1.2.3 测定波长的选择 精密量取橙皮苷对照品溶液0.6 mL 置10 mL 量瓶中,以70%乙醇定容,对对照品和供试品进行全波长扫描(190~800 nm),选最大吸收波长283 nm 为测定波长。
1.2.4 标准曲线的制备 精密量取橙皮苷对照品溶液0.2、0.4、0.6、0.8、1.0、1.2 mL,分别置10 mL 量瓶中,以70%乙醇定容,70%乙醇为空白,在283 nm 处测吸光度,以浓度对吸光度进行线性回归。
1.2.5 测定法 吸取供试品溶液,测定吸光度,并根据标准曲线计算供试品中橙皮苷含量。
1.3 多糖含量测定方法
1.3.1 对照品溶液的制备 精密称取D-无水葡萄糖对照品适量,加水制成0.1033 mg/mL 的D-无水葡萄糖溶液。
1.3.2 供试品溶液的制备 精密称取冻干粉0.25 g 加水20 mL,超声处理30 min,摇匀,精密量取1 mL 置离心管后加入乙醇25 mL 摇匀,冷藏4 h 取出,离心5 min,弃去上清液,沉淀挥干乙醇,加热水使溶解,转移至50 mL 量瓶中放冷,以水定容,摇匀即得。
1.3.3 显色反应 精密量取供试品溶液1 mL、D-无水葡萄糖对照品溶液0.2、0.4、0.6、0.8、1.0、1.2 mL,分别置具塞试管中,加水补至2 mL,精密加入1 mL 5%苯酚溶液摇匀,迅速精密加入5 mL 硫酸摇匀,放置10 min,置45℃水浴中保温10 min,取出迅速冷却至室温。
1.3.4 测定波长的选择 精密量取对照品、供试品溶液0.6、1.0 mL,分别置具塞试管中,按“1.3.3”项下显色,对两者进行全波长扫描(190~800 nm),选最大吸收波长490 nm 为测定波长。
1.3.5 标准曲线的制备 精密量取D-无水葡萄糖对照品溶液0.2、0.4、0.6、0.8、1.0、1.2 mL,分别置于具塞试管中,水为空白,按“1.3.3”项下显色,在490 nm 处测吸光度,以浓度对吸光度进行线性回归。
1.3.6 测定法 测定显色后供试品溶液吸光度,并根据标准曲线计算供试品中D-无水葡萄糖含量。
1.4 无机盐含量测定方法
精密称取冻干粉2.00 g,参照2015 版《中华人民共和国药典》[11]“四部”通则2302 灰分测定法进行试验,无机盐不做方法学考察。
1.5 5 种有效成分含量测定方法
1.5.1 对照品溶液制备 精密称取没食子酸、栀子苷、芍药苷、芸香柚皮苷、橙皮苷对照品适量,加甲醇制成浓度分别为301.27、1031.63、504.41、297.53、247.62 μg/mL的对照品溶液,再分别精密量取适量,加甲醇稀释成浓 度 分 别 为60.25、154.74、50.44、59.51、49.52 μg/mL的对照品溶液。
1.5.2 供试品溶液制备 精密称取冻干粉2.00 g 置锥形瓶中,加水50 mL 煎煮30 min,放冷滤过,精密量取滤液5 mL 蒸干,残渣加70%乙醇适量,转移至20 mL量瓶中超声处理15 min,以70%乙醇定容,摇匀滤过,取续滤液即得。
1.5.3 色谱条件 色谱柱为Kromasil 100-5-C18(250 mm×4.6 mm,5 μm);柱温30℃;流速0.9 mL/min;检测波长230 nm;流动相为乙腈(A)-0.05%磷酸溶液(B),进行梯度洗脱(0~20 min,5%~15%A;20~35 min,15%~20%A;35%~45 min,20%~30%A;45~60 min,30%~45%A;60~61 min,45%~5%A;61~90 min,5%A);供试品进样5 μL,对照品进样10 μL;理论塔板数按橙皮苷峰计算应不低于3000。
精密量取各对照品溶液适量,加甲醇稀释制成混合对照品溶液,该色谱条件下对照品与供试品HPLC图谱见图1。
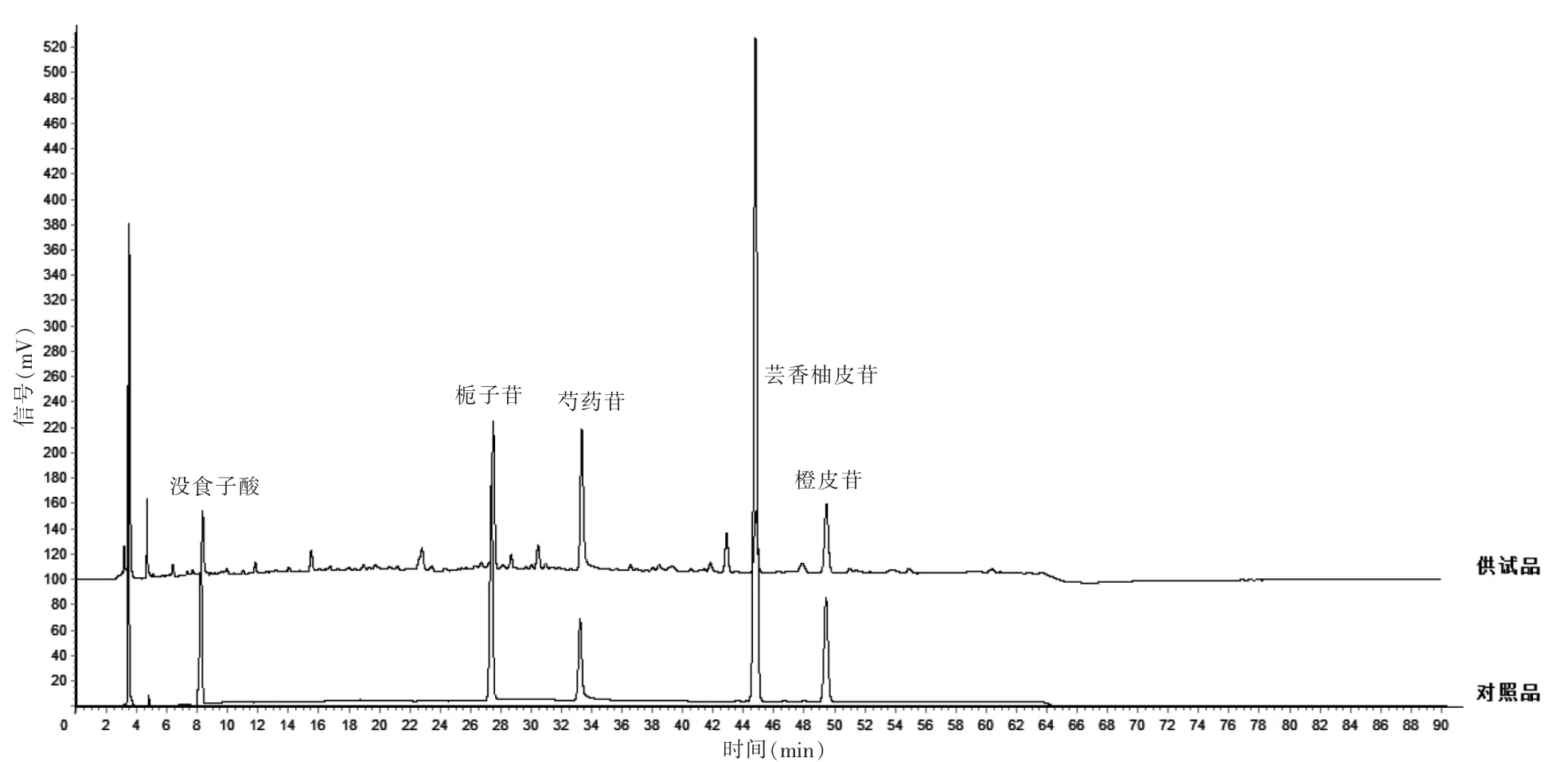
图1 对照品与供试品图谱
2 结果
2.1 总黄酮、多糖方法学考察
2.1.1 线性关系考察 分别按“1.2.4”“1.3.5”下项制备标准曲线,得橙皮苷、D-无水葡萄糖线性回归方程分别为A=10.2275C+0.0018(r=0.9992)、A=8.2694C-0.0056(r=0.9991),提示橙皮苷、D-无水葡萄糖分别在0.0051~0.0306、0.0103~0.0620 mg/mL 浓度范围内线性关系良好。
2.1.2 精密度试验 精密量取两种对照品溶液各0.6 mL,制备相应溶液并分别连续测定吸光度各6 次,计算橙皮苷、D-无水葡萄糖吸光度RSD 值分别为0.55%、0.64%,提示仪器精密度良好。
2.1.3 重复性试验 精密称取S1 冻干粉0.25 g,总黄酮、多糖供试品溶液各平行制备6 份,分别测定吸光度,计算其吸光度RSD 值分别为1.72%、1.66%,提示方法重复性好。
2.1.4 稳定性试验 精密称取S1 冻干粉0.25 g,总黄酮、多糖供试品溶液制备后分别于0、10、20、30、40、50、60 min 测定吸光度,计算其吸光度RSD 值分别为1.58%、1.41%,提示供试品溶液在1 h 内稳定。
2.1.5 加样回收率试验 精密称取0.20 g S1 冻干粉18 份,9 份添加等量橙皮苷对照品溶液,9 份添加等量D-无水葡萄糖对照品,供试品溶液制备后分别测定吸光度,计算含量及加样回收率,数据见表1,提示准确度良好。

表1 总黄酮、多糖加样回收率数据
2.1.6 样品含量测定 取16 批化肝煎样品,制备相应供试品并测定吸光度,计算16 批样品中总黄酮、多糖、无机盐的含量。结果示16 批样品中总黄酮、多糖、无机盐含量范围分别为2.61%~3.52%、11.65%~16.49%、7.10%~10.20%,平均含量分别为2.99%、13.92%、8.55%,见表2,提示不同批次样品中各大类成分的含量存在一定差异。

表2 16 批化肝煎中总黄酮、多糖、无机盐的含量(%)
2.2 5 种有效成分方法学考察
2.2.1 线性关系考察 分别精密量取“1.5.1”项下稀释前对照品溶液适量,加甲醇分别配制成6 个质量浓度,进样测定,记录色谱图及峰面积,以质量浓度对峰面积进行线性回归,绘制标准曲线,见表3。提示各成分在各自浓度范围内线性关系良好。
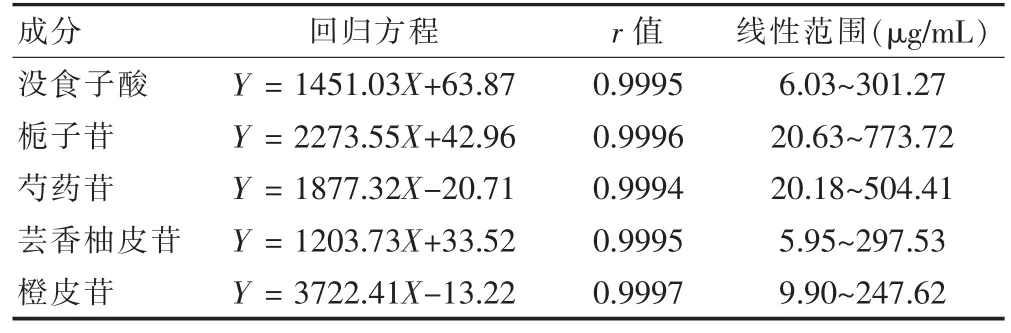
表3 线性关系结果
2.2.2 精密度试验 取“1.5.1”项下稀释后对照品溶液,进样测定,分别连续进样6 次,计算没食子酸、栀子苷、芍药苷、芸香柚皮苷、橙皮苷峰面积RSD 值分别为0.26%、0.15%、0.09%、0.20%、0.18%,提示仪器精密度良好。
2.2.3 重复性试验 精密称取S1 冻干粉2.00 g,平行制备6 份供试品并测定,计算没食子酸、栀子苷、芍药苷、芸香柚皮苷、橙皮苷峰面积RSD 值分别为1.15%、1.36%、0.95%、0.88%、0.65%,提示方法重复性好。
2.2.4 稳定性试验 取化肝煎供试品溶液S1,分别在0、2、4、8、12、24 h 进样测定,计算没食子酸、栀子苷、芍药苷、芸香柚皮苷、橙皮苷峰面积RSD 值分别为1.02%、1.24%、1.39%、0.93%、0.79%,提示供试品溶液在24 h 内稳定。
2.2.5 加样回收率试验 精密称取0.4 g S1 冻干粉9 份,添加适量一定质量浓度的5 种对照品溶液,制备供试品,测定含量并计算各成分加样回收率,数据见表4。
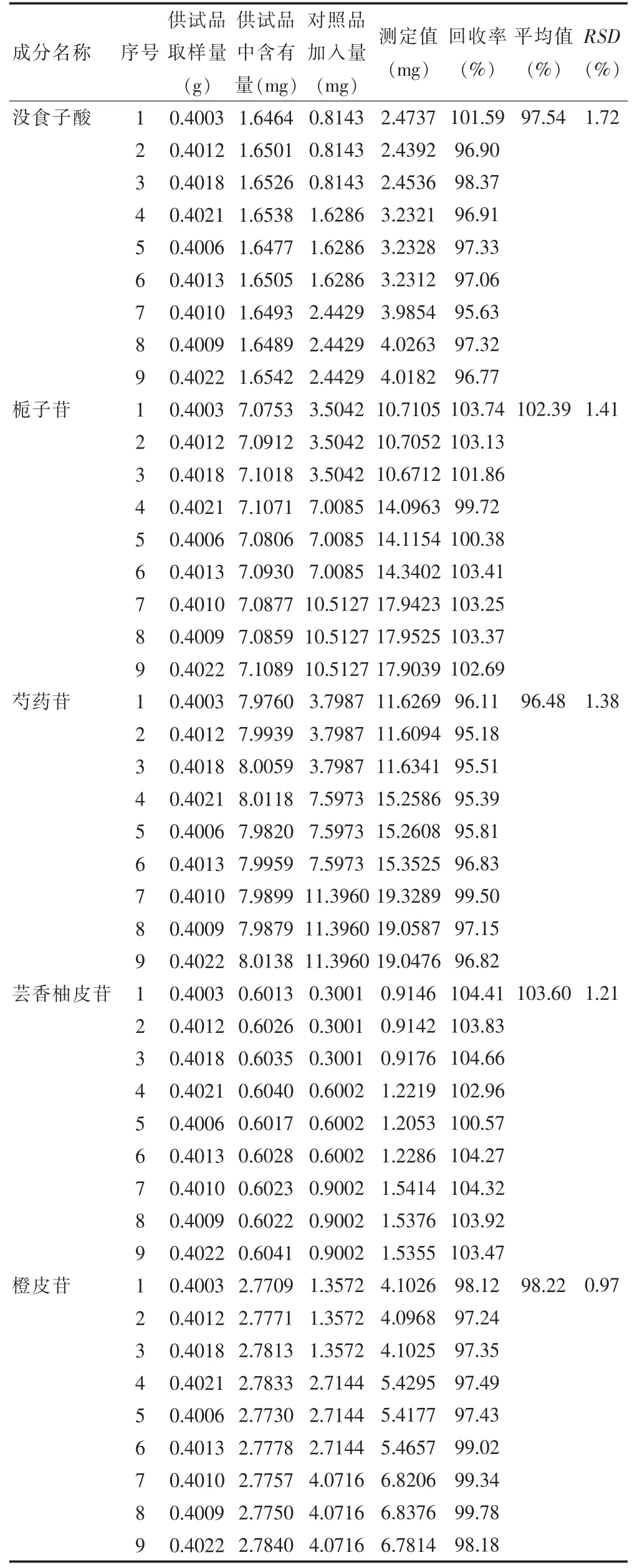
表4 5 种成分加样回收率数据
2.2.6 化肝煎样品含量测定 制备16 批化肝煎供试品并测定,计算样品中没食子酸、栀子苷、芍药苷、芸香柚皮苷、橙皮苷的含量,其质量分数分别为0.36%~1.12%、1.40%~3.01%、1.73%~4.58%、0.12%~0.51%、0.62%~1.62%,平均含量分别为0.56%、1.94%、2.37%、0.22%、0.89%,见表5,提示不同批次样品中各成分含量存在一定差异。

表5 16 批化肝煎中5 种成分的质量分数(%)
3 讨论
3.1 大类成分含量测定成分及测定方法的确定
单味中药及中药复方发挥功效是由于其中多种有效成分共同作用,也是中药多靶点效应的物质基础,从控制有效性上来讲,测定复方总成分含量要比测定单一成分效果好,更科学。因此,测定大类成分含量对保证化肝煎质量意义重大。
化肝煎中青皮[12]主要含黄酮类、挥发油等;陈皮[13]主要含黄酮类、挥发油、微量元素等;炒栀子[14]主要含环烯醚萜苷类、黄酮类等;白芍[15-16]主要含单萜及其苷类、黄酮类、多糖、有机酸类、微量元素等;牡丹皮[17]主要含单萜及其苷类、有机酸类、多糖等;泽泻[18]主要含黄酮类、多糖等;浙贝母[19]主要含生物碱等。
化肝煎中君药陈皮、青皮,臣药炒栀子、白芍、牡丹皮中均含黄酮类化合物,这类化合物在自然界广泛存在,药理作用广,如抗氧化、抗炎等,常作为质量控制指标[20-22]。通常运用UV-Vis 法测定总黄酮含量,化肝煎君药中起主要药效的成分是橙皮苷,2015 版《中华人民共和国药典》[11]将橙皮苷作为陈皮、青皮的含量测定指标,结合文献,最终确定以橙皮苷为指标来测定总黄酮的含量[7-8]。总黄酮含量测定方法有直接测定法、三氯化铝显色法、碱液显色法、硝酸铝显色法等[23-26],通过对比分析上述常用的4 种方法对于化肝煎的适用性,以此得到较为准确的检测方法,对对照品及供试品进行全波长扫描发现,直接测定法中橙皮苷对照品和供试品光谱扫描曲线相似度较高,特征峰重叠较好,附近无过多干扰峰,相较于其他方法干扰较小、效果要好,且该方法操作简便,根据试验结果选择283 nm 为检测波长,故为了最大限度地测定以橙皮苷为主的黄酮类化合物的含量,本研究采用干扰相对较小、较为接近真实值的直接测定法,更加科学准确的判断要在更多黄酮单品经精确测定之后才能得出。
臣药白芍、牡丹皮中均含有大分子物质多糖,白芍多糖[27]具抗氧化作用,牡丹皮多糖[28]在免疫调节方面具有一定作用。多糖含量测定通常采用UV-Vis法,选用D-无水葡萄糖作为对照品,经查阅文献[9-10],其测定多采用苯酚-硫酸法,本研究也采用此法进行测定。
化肝煎多种药味均含常量元素,且陈皮、白芍中还含微量元素,这些无机盐是人体不可或缺的营养素,也具一定药理作用,如陈皮中微量元素有一定强心、抗休克[13]作用。中药灰分来源主要为中药经灰化后遗留的不挥发性无机盐,是衡量中药材质量的重要指标,故采用灰分测定法进行测定。
本研究主要测定总黄酮、多糖、无机盐的含量,涵盖了化肝煎所具有的大类物质基础,三大类成分含量总计约25.46%,可以反应出化肝煎物质基础组成,为其质量评价提供依据。
3.2 多成分含量测定成分的确定
橙皮苷、芸香柚皮苷是君药陈皮、青皮的主要活性成分;栀子苷是臣药炒栀子的主要活性成分;芍药苷、没食子酸是臣药白芍、牡丹皮的主要活性成分,因此本研究选取起主要药效的橙皮苷、栀子苷及起次要药效的芸香柚皮苷、芍药苷、没食子酸作为含量测定指标,建立同时测定其含量的HPLC 法并进行方法学考察。
综上,本研究通过采用测定化肝煎大类成分的含量与测定单一成分的含量相结合的方法,既能涵盖该品种所具有的大类物质基础,也能控制起主要药效的化学成分的含量,可以更充分反应化肝煎的质量,5 种有效可控成分总含量约5.98%,大类成分及单一成分含量总计约31.44%,占比相对较高,能较好体现化肝煎物质基准物质基础的组成,可为化肝煎质量评价提供较为全面的方法和依据,也可为后续复方制剂的质量控制研究提供参考。
