富硫双金属氧化物制备及其对水体铅的去除
2021-07-29龚娴彭港谌宇楠张凌杰蔡悦章萍1b
龚娴,彭港,谌宇楠,张凌杰,蔡悦,章萍,1b
(1.南昌大学a.资源环境与化工学院;b.鄱阳湖环境与资源利用教育部重点实验室,江西 南昌 330031;2.江西省南昌生态环境监测中心,江西 南昌 330038)
随着铅蓄电池、矿业和电镀等行业发展,含Pb2+废水导致的水体污染问题日益严重。含铅废水因其铅浓度高、酸性强及生物难降解等特性,已成为当前水污染控制领域中的热点问题[1-2]。目前,含铅废水的处理方法主要有化学沉淀法[3-4]、离子交换法[5]、吸附法[6-7]、膜分离法[8-9]、电化学处理技术[10]等,其中吸附法因其成本低、效率高、操作简单等优点而被广泛应用[11]。
层状双金属氧化物(layered double oxides,LDOs),是由层状双金属氢氧化物(layered double hydroxide,LDHs)煅烧而成的一类金属氧化物[12]。因其具有丰富的金属氧化物、大量的活性位点以及独特的“记忆效应”等特性,作为水体重金属吸附材料已引起了广泛的关注[13]。Yang等[14]采用煅烧法制备的Ni/Al-LDO纳米片实现了对水中As5+的去除,吸附容量高达180.9 mg·g-1。Long等[15]采用原位氧化聚合法制备的PANI/LDOs对水中Cr6+的吸附容量为409.77 mg·g-1。Hou等[16]采用水热法合成的Mag-LDO/C有效地去除水中Cu2+、Cd2+和Pb2+。目前,借助元素掺杂、构建多维结构等可进一步提高吸附材料的吸附性能,其中负载硫基团可明显促进改性材料对水体中Pb2+的吸附性能。硫基团具有软碱性质,Pb2+具有软酸性质,基于软硬酸碱定理,作为软酸的Pb2+对硫基团等软碱具有高的亲和力[17-18]。然而,目前有关富硫双金属氧化物(S-LDO)除Pb2+的研究甚少。
本文以课题组前期采用的十二烷基硫酸钠(SDS)为软模板剂成功制备的含硫有机LDHs[19]为前驱体,在高温条件下煅烧制得富硫层状双金属氧化物(S-LDO),将其用于对Pb2+的去除行为研究。考察静态吸附实验中投加量、Pb2+初始浓度和反应时间等因素对S-LDO去除Pb2+的影响,并结合XRD、SEM对反应前后的固体产物进行表征,探究其吸附机制,以期为富硫功能化材料去除重金属离子的应用提供理论基础和技术支持。
1 实验方法
1.1 实验材料和仪器
试剂:九水合硝酸铝;六水合硝酸镁;尿素;硝酸铅;十二烷基硫酸钠;去离子水。试剂纯度均为分析纯。
仪器:场发射扫描电子显微镜(JSM6701F,日本电子株式会社);X射线粉末衍射仪(D8ADVANC,德国BRUKER公司);红外光谱分析仪(NICOLET5700,美国Thermo公司);数显恒温水浴振荡器(SHA-R,天津赛得利斯实验分析仪器制造厂);数控超声波清洗器(KQ3200D,昆山市超声仪器有限公司);数显鼓风干燥箱(GZX-9140MBE,上海博讯实业有限公司医疗设备厂);高速离心机(TG16G,北京华瑞科学器材);电子天平(AR224CN,奥豪斯仪器(常州)有限公司);电感耦合等离子体原子发射光谱仪(PerkinElmer Optima DV 2000 ICP-AES)。
1.2 S-LDO材料的制备
按n(Mg2+):n(Al3+):n(H2NCONH2)=1:2:10,称取0.20 g Mg(NO3)2·6H2O、0.15 g Al(NO3)3·9H2O和0.24 g H2NCONH2溶解于50 mL去离子水中,并立即加入30 mL SDS溶液(0.1 mol·L-1)快速混合搅拌,超声30 min,最后将混合液移至反应釜内中,150 ℃下水热6 h,室温下陈化24 h。所得产物经离心、洗涤、干燥、研磨后于马弗炉中700 ℃煅烧4 h,即得S-LDO。
1.3 S-LDO对Pb2+吸附实验
称取一定量S-LDO样品投加至Pb(NO3)2溶液中,置于恒温振荡器中,以150 r·min-1的转速振荡,待反应结束后,取样离心分离,采用ICP-AES测定上清液中Pb2+质量浓度,并按式(1)、式(2)分别计算平衡吸附量qe和去除率E:
qe=(C0-Ce)V/m
(1)
E=(C0-Ce)/C0×100%
(2)
式中:C0为Pb2+的初始质量浓度,mg·L-1;Ce为Pb2+的平衡质量浓度,mg·L-1;V为溶液体积,L;m为S-LDO的质量,g。
2 结果与讨论
2.1 S-LDO的结构表征
图1为S-LDO的XRD图谱。可知,S-LDO样品在2θ=31.28°、36.90°、45.06°、59.82°及65.58°处出现MgAl2O4的特征衍射峰,分别对应其(220)、(311)、(400)、(511)及(440)晶面[20-21]。同时在2θ=23.09°、24.66°、25.23°、33.95°、39.07°、50.42°和51.89°处出现的特征衍射峰,与MgSO4标准图谱(JCPDS No.21-0546)一致。上述结果表明煅烧后有机三维LDH可形成晶态良好的三维S-LDO。
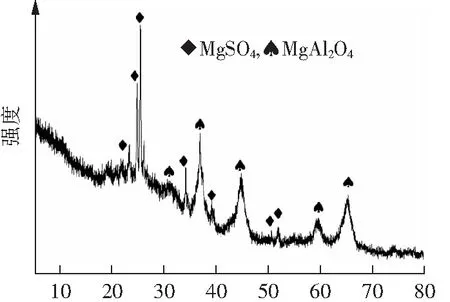
2θ/(°)图1 S-LDO的XRD图谱Fig.1 XRD pattern of S-LDO


σ/cm-1图2 S-LDO的红外光谱图Fig.2 FT-IR spectra of S-LDO

图3 S-LDO的SEM图Fig.3 SEM image of S-LDO
2.2 S-LDO除铅行为
2.2.1 S-LDO投加量对去除性能的影响
在温度为25 ℃,反应时间为12 h的条件下,将不同投加量ρ(0.25、0.50、1.00、2.50、5.00 g·L-1)的S-LDO投至质量浓度为1 000 mg·L-1的Pb2+的溶液中,探究投加量对Pb2+的吸附效果影响,结果如图4所示。
可知,当S-LDO投加量从0.25 g·L-1增加到1.00 g·L-1时,Pb2+的去除率E从40%显著提升至96%,此后随着投加量的增加,去除率缓慢增加并趋于稳定。相反,Pb2+的吸附量随着S-LDO投加量的增加逐渐降低。这可能是由于过量的S-LDO使得活性吸附位点的利用率降低所导致的。综合考虑去除成本以及去除效率选择1.00 g·L-1为S-LDO吸附Pb2+的最佳投加量。

ρ/(g·L-1)图4 投加量对S-LDO吸附Pb2+的影响趋势图 Fig.4 Effect of dosage on the adsorption of Pb2+by S-LDO
2.2.2 初始Pb2+质量浓度对去除性能的影响
在25 ℃、反应时间为12 h、S-LDO的投加量为1.00 g·L-1的条件下,对不同初始质量浓度的Pb2+(10、200、500、1 000、1 500、1 800、2 000 mg·L-1)进行等温吸附实验,实验结果如图7所示。随着Pb2+初始浓度的增加,对Pb2+的吸附量先迅速上升,在初始浓度为1 500 mg·L-1达到吸附平衡。分析原因可能是在初始浓度较低时,吸附位点未达到饱和,单位质量吸附剂与Pb2+碰撞概率随浓度增大而增加,从而使得吸附量增加。之后吸附剂的吸附位点达到饱和,吸附量达到平衡。
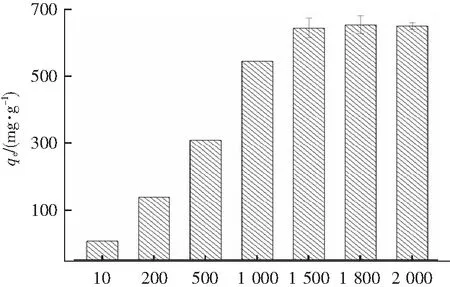
C0/(mg·L-1)图5 S-LDO对Pb2+的吸附等温线Fig.5 Adsorption isotherms for the adsorption of Pb2+on S-LDO
为进一步探究S-LDO对Pb2+的去除行为,分别采用Langmuir和Freundlich等温吸附模型对吸附过程进行拟合,模型方程式如式(3)和式(4):
(3)
(4)
式中:qe为平衡吸附量,mg·g-1;qm为最大吸附量,mg·g-1;Ce为Pb2+的平衡质量浓度,mg·L-1;KL为Langmuir等温模型常数,L·mg-1;KF为Freundlich等温模型常数,L·mg-1;n为Freundlich吸附强度。
表1为Langmuir和Freundlich模型拟合相关参数,拟合曲线如图6所示,通过对比两种模型拟合结果的相关系数(R2)可知,Langmuir模型能更好描述S-LDO对Pb2+的吸附过程(R2> 0.999),表明S-LDO对Pb2+的吸附是单分子层吸附。

表1 S-LDO对Pb2+的吸附等温方程拟合特征值Tab.1 Eigenvalue of Langmuir and Freundlich for Pb2+on S-LDO

Ce/(mg·L-1)(a) Langmuir
2.2.3 反应时间对去除性能的影响及吸附动力学
为探究反应时间对S-LDO吸附Pb2+的影响,在25 ℃下将1.0 g·L-1的S-LDO投至100 mg·L-1的Pb2+溶液中反应。如图7所示,在反应前1 min,S-LDO对Pb2+的吸附量迅速达到86 mg·g-1,随后吸附速率趋于平缓并在30 min时达到平衡,平衡吸附量为95 mg·g-1。

t/min图7 S-LDO对Pb2+的吸附动力学曲线Fig.7 Kinetics curves for the adsorption of Pb2+ on S-LDO
为进一步揭示S-LDO对Pb2+的吸附机制,采用准一级动力学方程(式(5))和准二级动力学方程(式(6))对动力学数据进行拟合。
ln(qe-qt)=lnqe-k1t
(5)
(6)
式中:qe为动力学反应平衡时S-LDO对Pb2+的吸附量,mg·g-1;qt为t时刻S-LDO对Pb2+的吸附量,mg·g-1;t为反应进行时间,min;k1为准一级反应动力学方程速率常数,min-1;k2为准二级反应动力学方程速率常数,g·mg-1·min。
S-LDO对Pb2+的动力学拟合结果如图8所示,模型拟合相关参数见表2。可知,与准一级动力学模型相比,准二级动力学模型具有更高的相关性(R2>0.999),且通过准二级动力学模型拟合得到的qe,cal更接近实验值qe,exp,因此S-LDO对Pb2+的吸附过程更符合准二级动力学,说明该吸附过程主要受化学作用影响。

表2 S-LDO对Pb2+的吸附动力学方程拟合特征值Tab.2 Eigenvalue of the kinetic sorption equation for Pb2+ on S-LDO
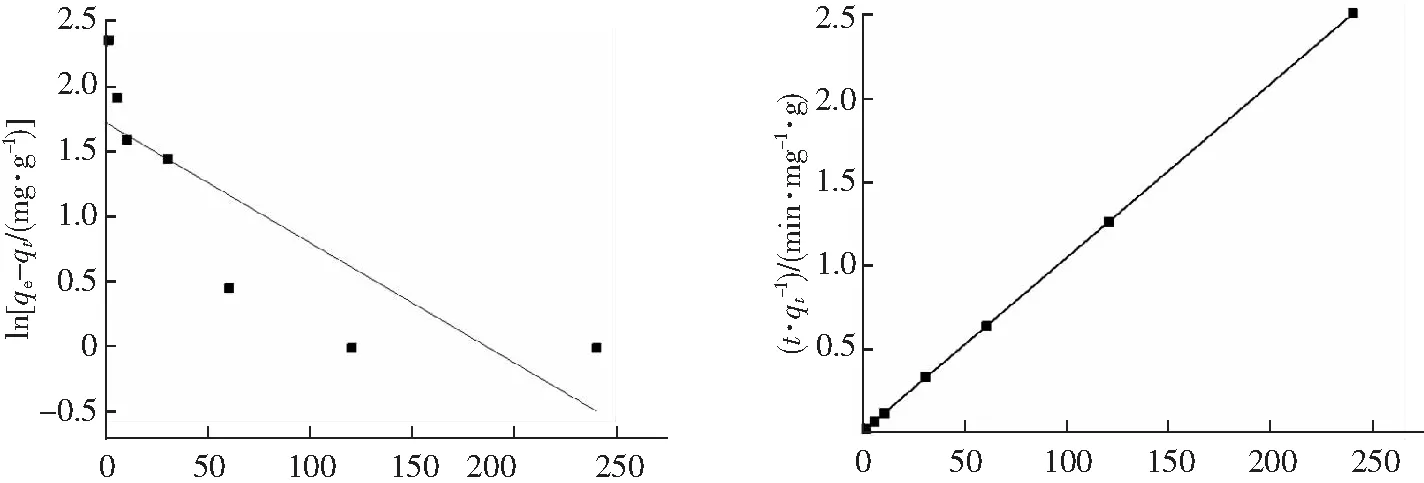
t/min t/min
2.3 机制探讨

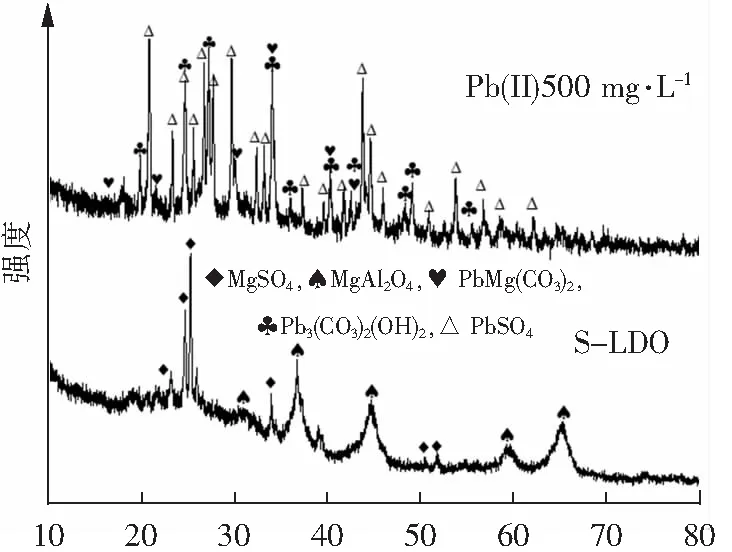
2θ/(°)图9 S-LDO与Pb2+反应前后的XRD图谱Fig.9 XRD of S-LDO before and after Pb2+ adsorption


图10 S-LDO与Pb2+反应后的SEM图谱Fig.10 SEM of S-LDO before and after Pb2+ adsorption
3 结论

2) S-LDO对Pb2+具有良好的吸附性能,其等温吸附过程符合Langmuir模型,吸附量为653.4 mg·g-1;S-LDO对Pb2+的吸附动力学符合准二级动力学方程。

