电沉积FeCoNiCr高熵合金镀层工艺参数优化
2021-07-29杨海泊于金库郭燕青郭富钰肖静静
杨海泊,于金库,*,郭燕青,乔 琪,郭富钰,肖静静
(1.燕山大学 材料科学与工程学院,河北 秦皇岛 066004;2.燕山大学 亚稳材料制备技术与科学国家重点实验室,河北 秦皇岛 066004)
0 引言
近年来,高熵合金受到材料研究工作者的广泛关注。传统合金的设计主要以一种或两种元素为主,添加少量其他元素改善合金性能[1]。高熵合金通常是由5种及5种以上元素所构成的等摩尔比或近似等摩尔比的高熵合金体系[2],高熵合金打破了传统设计理念的束缚,通过增加组元数来获得优异的性能,成为近年来的研究热点。自从2004年我国台湾学者叶均蔚初次提出高熵合金的概念[3-6],至今被广泛引用。目前,世界许多学者及科研单位对高熵合金进行了大量研究工作,取得许多令人惊喜的成果。由于有较高的混合熵,高熵合金具有许多优异的性能,比如良好的高温强度[5-6]、较高的耐腐蚀性[7]和耐磨性[8-9]。2011年有学者发现,等摩尔比的四主元合金也具有和五主元合金相似的性质,于是又将高熵合金扩展为具有4种及4种以上[10-11]元素组成的合金。高熵合金研究工作者已经总结了高熵合金一些设计理论,高熵合金设计原则即是通过使组成元素按一定比例相互溶合形成FCC(面心立方)、BCC(体心立方)或HCP(密排六方)的简单固溶体结构,一般要避免金属间化合物或其他非金属夹杂物的形成。
高熵合金存在“鸡尾酒”效应[12],可以通过调节合金中的成分来获得所需要的性能,满足不同工作环境的要求。Fe、Co、Ni、Cr原子半径及电负性相近,容易形成结构简单的单一的FCC结构,Co、Ni、Cr等致钝化元素的加入可提高其耐蚀性[13],同时引发晶格发生畸变,从而获得本征强化,得到高强度、高硬度以及耐蚀性良好的FeCoNiCr高熵合金镀层。目前对于高熵合金制备大多采用磁控溅射法、机械合金化法、激光熔覆法等[14-16],但这些方法生产成本较高,且不便于工业化生产。
同一种成分,由于制备方法或加工方式不同,所得到的材料性能也大不相同。电沉积法制备的合金镀层具有成本低、操作简单、沉积速率快、对环境友好等优点。因此,可以通过电沉积的方法在工件表面镀覆一层高熵合金镀层,提高工件的耐蚀性和力学性能等。目前利用电沉积法制备高熵合金镀层的研究较少,没有成熟的镀液配方,因此,有必要对电沉积制备FeCoNiCr高熵合金镀层进行深入研究。本文从FeCoNiCr高熵合金镀层制备、工艺参数优化,通过正交实验的方法探究电流密度、温度、pH值、硫酸铬浓度对镀层的沉积速率和Cr含量的影响,确定电沉积制备FeCoNiCr高熵合金镀层的最佳配方及工艺参数,并对其形貌、微观结构、镀层成分和耐蚀性进行了表征。
1 试样制备与检测
1.1 涂层制备
本实验采用的基体材料是纯铜片。材料大小为12 mm×12 mm×1 mm。预处理流程:粗磨—碱洗—去离子水清洗—酒精清洗—强酸抛光—去离子水清洗—活化—去离子水清洗—施镀。本文在酸性条件下,采用直流电沉积方法制备了FeCoNiCr高熵合金镀层,镀液成分如表1所示,镀覆工艺参数为:pH值1.5~3.5,温度20~60 ℃,电流密度15~35 A/dm2,镀覆时间30~60 min,搅拌速度100 r/min。实验中所用试剂均为去离子水和分析纯试剂配制。
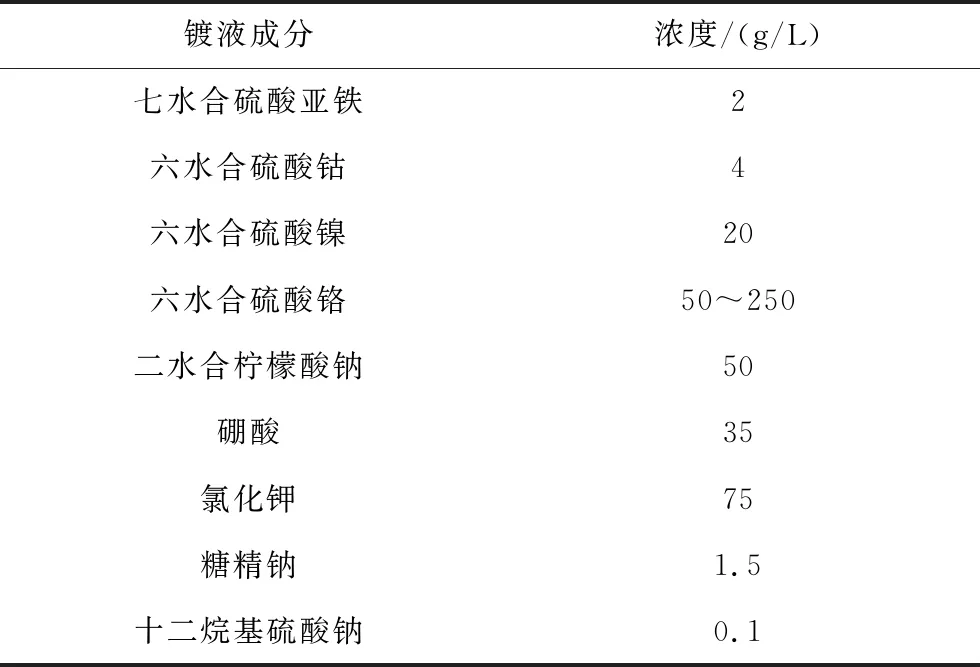
表1 FeCoNiCr高熵合金镀层镀液成分Tab.1 Composition of FeCoNiCr high entropy alloy plating solution
将预处理后的基体纯铜片接直流电源的负极,石墨片接阳极,放入镀槽中。镀液中硫酸铬的浓度分别为50 g/L、100 g/L、150 g/L、200 g/L、250 g/L;pH值分别为1.5、2.0、2.5、3.0、3.5;电流密度为15 A/dm2、20 A/dm2、25 A/dm2、30 A/dm2、35 A/dm2;温度分别为20 ℃、30 ℃、40 ℃、50 ℃、60 ℃。打开直流电源并调节为恒流模式,电镀时间约60 min,电镀结束后取出铜片。
本研究采用正交实验法,探究了电流密度、温度、pH值、硫酸铬浓度对镀层沉积速率和Cr含量的影响,分别用A、B、C、D表示,每个因素选取5个水平变量,不考虑各因素之间的相互作用,选用L25(54)正交实验表,如表2所示。
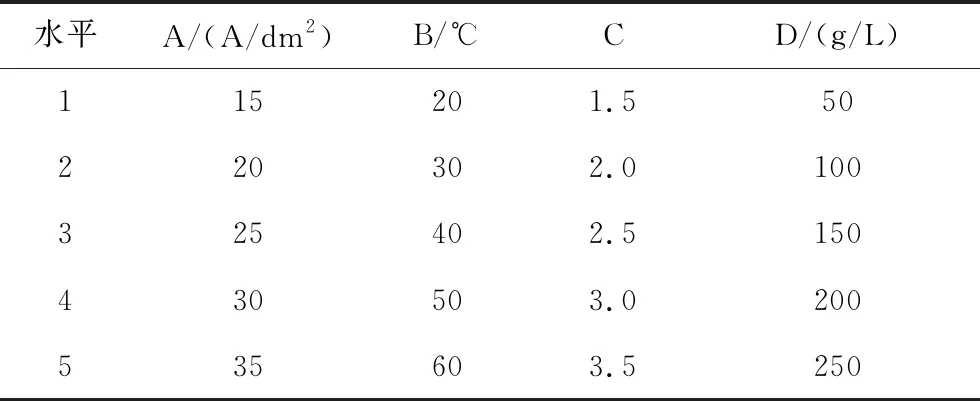
表2 正交实验设计的因素及水平Tab.2 Factors and levels of orthogonal experimental design
1.2 镀层性能表征及组织观察
采用重量法测定镀覆速度;用HITACHI S-4800的场发射扫描电子显微镜和随带的EMAX-250型号能谱仪测定镀层表面形貌特征和化学成分;用日本理学公司生产的D/MAX2500HB+/PC型X射线衍射仪检测镀层的相结构。
采用标准三电极体系进行电化学分析,饱和甘汞电极为参比电极,铂片为辅助电极,工作电极为FeCoNiCr高熵合金镀层试样。腐蚀介质为3.5%(质量分数)NaCl溶液。采用CHI660E型电化学工作站对三电极体系进行极化曲线测试,扫描电位范围选取为-800 mV~800 mV,扫描速率为1 mV/s。
2 实验结果及分析
2.1 正交实验结果
正交实验考查了电沉积FeCoNiCr高熵合金镀层的沉积速率、镀层Cr含量,实验结果如表3所示。对于同一试样,镀层厚度与镀层质量成正比,镀层质量和镀层的沉积速率成正比,因此可以用一定时间内单位面积上镀层的质量来表征镀层的沉积速率(v)。
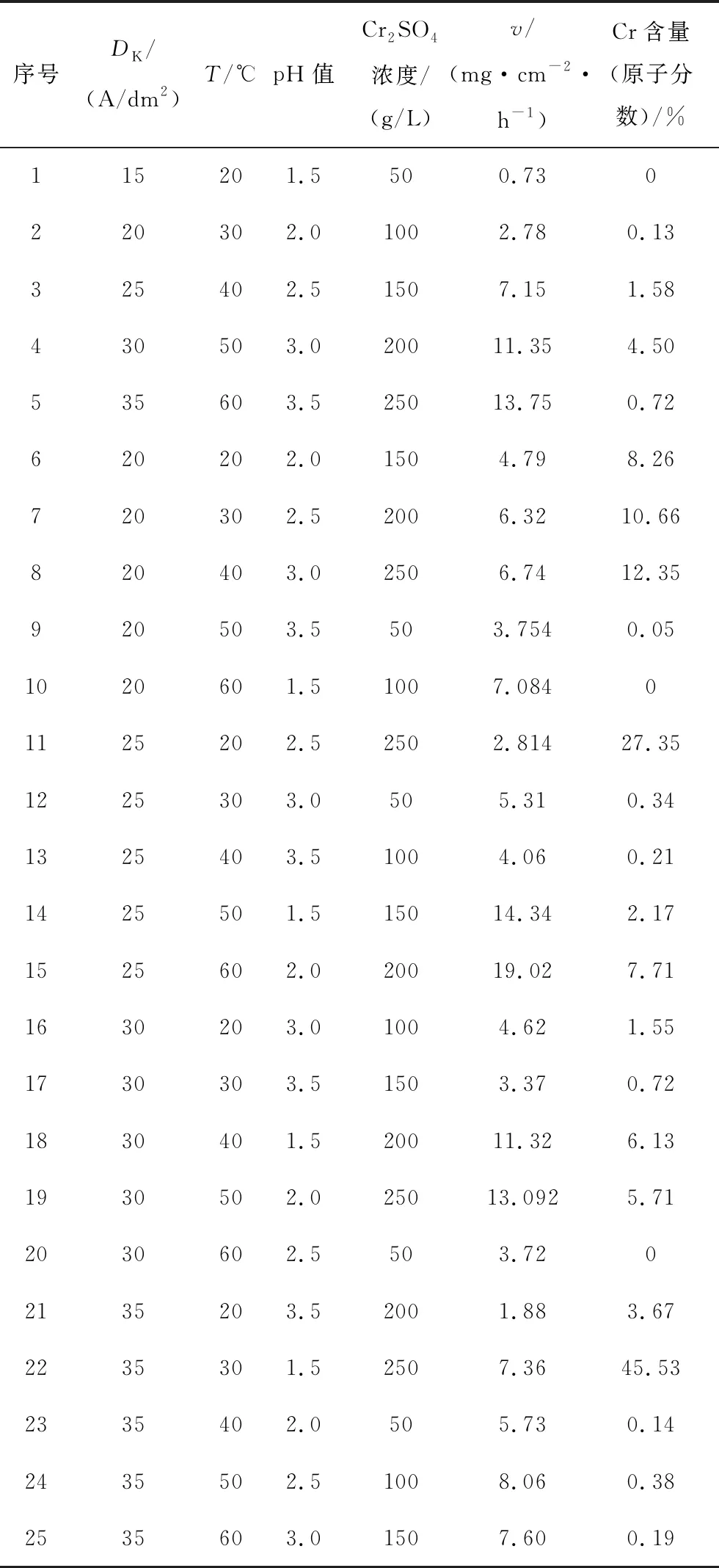
表3 正交实验结果Tab.3 Orthogonal experimental results
2.2 工艺参数及硫酸铬含量对FeCoNiCr高熵合金镀层沉积速率的影响
由不同因素、水平条件下FeCoNiCr高熵合金沉积层的正交实验结果,经计算得到积层沉积速度的均值与极差见表4所示。
从表4中可以看出,各个因素对沉积层沉积速率作用从大到小依次为:B>D>C>A,即在该实验条件下,溶液温度对镀层沉积速度的作用最大。沉积速率在A因素作用下时3水平的均值为最大值;在B因素影响下时5水平均值达到最高;在C因素影响下时2水平均值达到最高;在D因素影响下时4水平均值达到最高。由此可知,电沉积FeCoNiCr高熵合金镀层沉速率达到最大时的工艺参数是:DK为25 A/dm2,T为60 ℃,镀液pH值为2.0,硫酸铬质量浓度为200 g/L。

表4 镀层沉积速率均值与极差Tab.4 Deposition rate (v) average of coating and range (R)
该实验条件下,镀液温度对镀层的沉积速率的影响最大,镀液温度为60 ℃时沉积速率最大为10.24 mg·cm-2·h-1。镀液温度低时,Fe2+、Co2+、Ni2+、Cr3+等离子扩散到电极表面的速率相对缓慢,随着镀液温度的上升,试剂在镀液中的溶解能力和导电能力上升。同时Fe2+、Co2+、Ni2+、Cr3+等离子迁移速率加快,电解液活度增大,电流效率提升,FeCoNiCr高熵合金沉积层的沉积速率增大。但各离子对温度的敏感性不同,因此沉积到镀层中的含量变化趋势也不相同。继续提高溶液的温度,由于镀液挥发严重,导致溶液稳定性下降,沉积层表面开始出现粗糙,并且存在发白、发雾的情况,镀层边缘部发黑,使光亮区域变窄,镀层晶粒逐渐变得粗大。
硫酸铬含量对高熵合金镀层沉积速率的影响也较为明显。随着硫酸铬含量增加,镀层的沉积速率先升高,后又下降。当硫酸铬含量为200 g/L时,镀层沉积速率达到最大值为9.98 mg·cm-2·h-1。硫酸铬含量小于200 g/L时,镀层的沉积速率随硫酸铬含量的增大而增大,因为镀液中硫酸铬含量较少时,阴极表面Cr3+浓度较低,使得沉积速率也相对降低;随着硫酸铬含量的增添,镀液中Cr3+浓度也升高,使得阴极极化增大,从而沉积速率增大。当硫酸铬含量大于200 g/L时,沉积速率反而降低,因为硫酸铬含量过高,造成了羟桥基聚合反应[17],生成的聚合物黏着在试样上面,从而导致沉积层的沉积速度下降。
2.3 工艺参数及硫酸铬含量对FeCoNiCr高熵合金镀层Cr含量的影响
由不同因素、水平条件下FeCoNiCr高熵合金沉积层正交实验结果,经计算得到镀层中Cr含量(原子分数,%)均值与极差见表5所示。
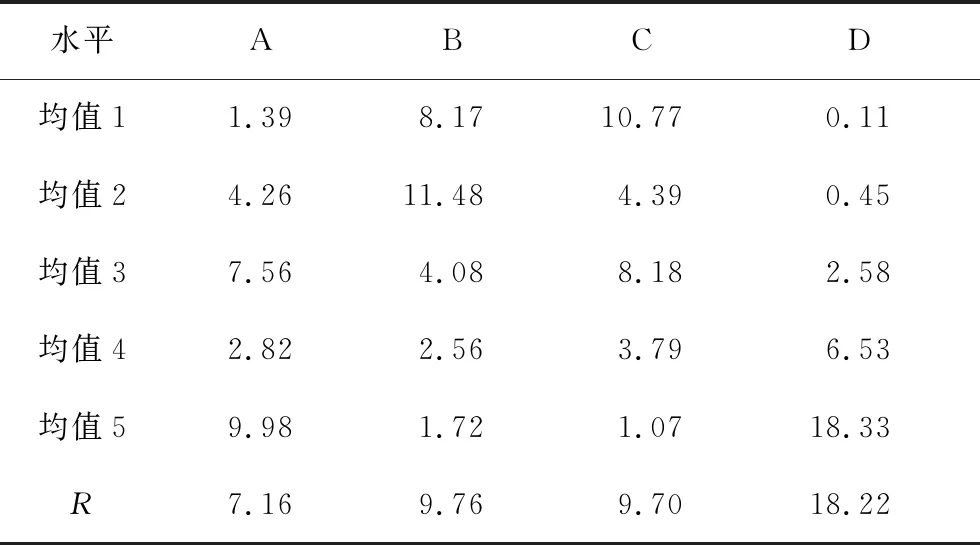
表5 镀层Cr含量均值与极差RTab.5 Cr content mean of coating and range (R) %
从表5可以看出,各个因素对镀层中Cr原子分数的影响从大到小依次为:D>B>C>A。在该实验参数下,镀液中硫酸铬用量对镀层中Cr原子分数的作用最为显著。镀层中Cr原子分数在A因素作用下时5水平的均值为最大;在B因素影响下时2水平均值最高;在C因素影响下时1水平均值最高;在D因素影响下时5水平均值最高。即FeCoNiCr高熵合金镀层中Cr原子分数最大时的工艺参数为:DK为35 A/dm2、T为30 ℃、pH值为1.5,硫酸铬含量为250 g/L。
本实验条件下,硫酸铬用量较小时,不利于FeCoNiCr高熵合金共沉积,硫酸铬含量较低时镀层中Cr原子分数很低,甚至为零。随着镀液中硫酸铬含量的增加,Cr3+浓度升高,而镀液中其他3种离子含量不变,Cr3+极化程度增加,析出电位正向移动,使Cr3+与Fe2+、Co2+、Ni2+在电位较低时共沉积。当硫酸铬浓度达到一定值时,镀层表面光亮度下降,继续增加硫酸铬浓度,镀层质量开始变差,表面出现黑色物质。此现象的原因是镀液中硫酸铬用量增加而配位剂用量保持不变,镀液中柠檬酸根的含量不够满足完全络合Cr3+时,镀液中存在大量游离的Cr3+,造成Cr3+的羟桥基聚合反应变的加剧[17],从而产生了大量的聚合物附着在试样表面,阻碍沉积的继续进行。因此,硫酸铬浓度并不是越高越好。
镀液温度在20~60 ℃范围内变化时,对镀层中Cr含量的影响也较大,随溶液温度上升,镀层中Cr含量整体呈降落趋势,在20~30 ℃范围内,镀层中Cr含量相对较高。镀液的pH值在1.5~3.5区域内变化时,对镀层的质量影响较大,镀液pH值较低时,镀层中会出现气孔和裂纹,但镀液pH值过高会使Cr3+发生羟桥基聚合反应[17]。综上所述,结合镀层的质量,镀液中硫酸铬含量为200 g/L,电流密度为25 A/dm2,温度为20 ℃,pH值为2.5。
2.4 FeCoNiCr高熵合金镀层微观结构、形貌和成分
在DK为25 A/dm2,T为20 ℃,pH值为2.5,Cr2(SO4)·6H2O为200 g/L条件下,制备样品,电沉积时间为60 min。FeCoNiCr高熵合金镀层的XRD衍射图、SEM图和元素分布,如图1所示。
从图1(a)中看出,FeCoNiCr高熵合金镀层在2θ=45°附近出现宽化衍射峰,此时沉积层为非晶态镀层。从图1(b)中可以看到,镀层仅含有Fe、Co、Ni、Cr四种元素,因此镀层为FeCoNiCr合金镀层,且镀层表面均匀、平整。

图1 FeCoNiCr高熵合金镀层XRD图, SEM图和元素分布图Fig.1 XRD,SEM and elements distribution of FeCoNiCr alloy coatings
3 FeCoNiCr高熵合金的耐蚀性能
图2为FeCoNiCr高熵合金镀层在3.5 %(质量分数)NaCl溶液中的极化曲线和腐蚀后的表面形貌。由图2(a)极化曲线可以看出,FeCoNiCr高熵合金镀层表现为活性溶解特征,腐蚀电流密度出现突增现象,说明FeCoNiCr高熵合金镀层在3.5%(质量分数)NaCl溶液中发生腐蚀,该结果与图2(b)合金镀层腐蚀后的表面形貌一致。
利用外延法得到自腐蚀电位(Ecorr)和自腐蚀电流密度(icorr)分别为-0.45 V、1.73×10-6A/cm2。由图2(b)可以看到,FeCoNiCr高熵合金镀层经3.5%(质量分数)NaCl溶液腐蚀后,表面出现点状分布的腐蚀坑,因此在该溶液中,FeCoNiCr高熵合金镀层的腐蚀机制为点蚀。根据腐蚀电化学理论,金属的耐蚀能力和自腐蚀电位呈负相关,其腐蚀速率与自腐蚀电流密度呈正相关,即Ecorr值越大,金属的耐蚀性越好,icorr值越小,金属的腐蚀速率越小。由实验结果可以看出,电沉积法制备的FeCoNiCr高熵合金镀层在3.5%(质量分数)NaCl溶液中,比真空热压烧结制备的CoCrFeNi高熵合金涂层的自腐蚀电位(-1.08 V)高,比真空热压烧结制备的CoCrFeNi高熵合金涂层的自腐蚀电流密度(9.44×10-6A/cm2)低[18]。所以电沉积制备的FeCoNiCr高熵合金镀层耐蚀性更优。
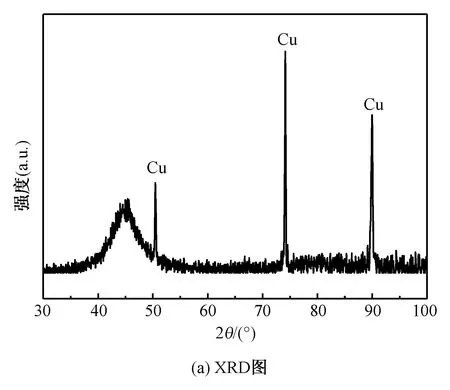

图2 FeCoNiCr高熵合金镀层在3.5 % (质量分数)NaCl溶液中的极化曲线和腐蚀后的形貌Fig.2 Polarization curve and corrosion morphology of FeCoNiCr high entropy alloy coating in 3.5%(mass fraction) NaCl solution
4 结论
本实验使用了直流电沉积方式制备了FeCoNiCr高熵合金镀层,对FeCoNiCr高熵合金镀层形貌、镀层成分、微观结构和耐蚀性进行了表征,得到以下结论:
1) 对FeCoNiCr高熵合金镀层沉积速率的影响程度,从大到小依次为:镀液温度>硫酸铬浓度>pH值>电流密度,即在该实验条件下,镀液温度对镀层沉积速率的影响程度最大。
2) 对FeCoNiCr高熵合金镀层中Cr含量影响程度,从大到小依次为:硫酸铬浓度>镀液温度>pH值>电流密度,即在该实验条件下,镀液中硫酸铬浓度对镀层中Cr含量的影响程度最大。
3) 电沉积FeCoNiCr高熵合金的配方为:硫酸亚铁2 g/L,硫酸钴4 g/L,硫酸镍20 g/L,硫酸铬浓度200 g/L,硼酸35 g/L,氯化钾75 g/L,柠檬酸钠50 g/L,糖精1.5 g/L,十二烷基硫酸钠0.1 g/L。工艺参数为:电流密度为25 A/dm2,温度为20 ℃,pH值为2.5。该实验条件下,FeCoNiCr高熵合金镀层为非晶态,且镀层表面均匀、平整。
4) FeCoNiCr高熵合金镀层在3.5% (质量分数)NaCl溶液自腐蚀电位(Ecorr)和自腐蚀使电流(Icorr)分别为-0.45 V、1.73×10-6A/cm2。比真空热压烧结制取的CoCrFeNi高熵合金涂层的自腐蚀电位(-1.08 V)高,比其自腐蚀电流密度(9.44×10-6A/cm2)低,电镀制备的FeCoNiCr高熵合金镀层耐腐蚀性更优。
