Ca-Al层状双金属(氢)氧化物气凝胶的制备及其吸氯性能
2021-07-28王鹏飞
王鹏飞,罗 炫,杨 莉
(1.西南科技大学材料科学与工程学院,四川 绵阳 621000; 2.中国工程物理研究院激光聚变研究中心,四川 绵阳 621000)
1 前 言
由于经济发展,造成的诸如空气污染、土壤板结和水污染等环境问题日益突出[1-4]。在水污染中Cl-是最为常见的腐蚀性离子,它主要来自于工业生产,如石油化工、纺织、化学制药等[5]。当Cl-的浓度达到某一阈值时,便会在金属表面形成大量的原电池反应活性位点,从而使金属快速腐蚀[6]。所以如不对含氯废水进行有效处理而随意排放,会对人类的生产和生活带来众多危害。
目前国内外处理Cl-的方法主要有化学沉淀法、电化学法和离子交换法[7-8]。在离子交换法中,水滑石(Hydrtalcite)又称为层状双金属氢氧化物(Layered double hydroxide,LDH)是一种高性价比的吸附材料[9]。其结构与水镁石相似,化学表达式为 [M2+1-xM3+x(OH)2]x+[(An-)x/n·mH2O]x-,其中:M2+为二价金属阳离子,M3+为三价金属阳离子,x为M3+/(M2++M3+)的比例,An-为板层间的平衡阴离子[10],其层间平衡阴离子具有一定的迁移性及离子交换性,可被环境中的其他阴离子所置换[11]。因在不同的合成条件下,板层中的M2+会被粒子半径相近的M3+所同晶取代,从而会使LDH的板层组成发生相应的变化,即形成所谓的类水滑石(LDHs)。当LDHs在一定温度下焙烧时,晶体的层状结构会随层间阴离子的氧化而塌陷,使表面带有正电荷。水滑石高温焙烧后的产物被称作焙烧态水滑石(Calcined LDH,CLDH)[12],当CLDH放入到含有某种阴离子的水环境中时,阴离子会作为平衡阴离子快速穿插进入到板层间,进而恢复成原有的层状结构,这种特性被称为材料的“结构记忆效应”[13]。因LDHs及其焙烧产物能较为高效、快速地去除水中的阴离子、重金属离子和有机物[14],因此其在污水治理、耐腐蚀等方面的应用日益受到关注。
LDHs的主要制备方法是共沉淀法[15]。吕亮等[16]研究Mg-Al-LDHs制备方法的优点在于:分散性好、结晶完整且纯度高,但在制备中极易产生大量含有高浓度M2+和M3+的混盐废水。本研究中以钙盐和铝盐为对象,通过溶胶-凝胶法制备出具有高比表面积的LDHs[17-20],并将其焙烧产物CLDH作为吸附剂以去除水体中的Cl-。通过溶胶-凝胶法在制备材料过程中不存在混盐废水的产生,在提高比表面积的基础上,提高了原料利用率,解决了水体中Cl-的污染问题。
2 实 验
2.1 实验药品及仪器
所用试剂均为分析纯的硝酸(HNO3),硝酸钙(Ca(NO3)2·6H2O),硝酸铝(Al(NO3)3·9H2O),环氧丙烷,乙醇和铬酸钾(K2CrO4)。自制蒸馏水,酚酞和氯离子标准液。
主要试验设备有优普超纯水制造系统、磁力加热搅拌器79-1(JT)、数显恒温油浴锅HY-S、分析天平FA2004B、循环水式多用真空泵SHB-III、马弗炉KSL-1500X和1L乙醇超临界干燥装置等。
2.2 Ca-Al层状双金属(氢)氧化物气凝胶的制备
2.2.1Ca-Al层状双金属氢氧化物气凝胶的制备 使用溶胶-凝胶法制备Ca-Al层状双金属氢氧化物气凝胶。把4 mmol水合硝酸钙和2 mmol水合硝酸铝加入到称量瓶中,并加入4 mL去离子水和10 mL乙醇,搅拌溶解后,再加入5 mL环氧丙烷作为促凝剂,充分混合后,置于40 ℃恒温环境中,记录凝胶时间,待凝胶完成后,老化12 h。以乙醇为交换溶剂充分交换后,使用乙醇超临界干燥制备出密度为85 mg/cm3左右的Ca-Al层状双金属氢氧化物气凝胶。
2.2.2Ca-Al层状双金属氧化物气凝胶的制备 取少许上述的Ca-Al层状双金属氢氧化物气凝胶放入坩埚中置于马弗炉,在设定的升温程序(室温下1 ℃/min至300 ℃保温2 h,再1 ℃/min至570 ℃保温6 h)下高温焙烧。制备出密度为45 mg/cm3左右的Ca-Al层状双金属氧化物气凝胶。
2.3 样品表征
使用D/MAX-1A型X射线衍射仪(XRD)对所制得的样品进行物相分析,CuKα靶,Ni滤波;采用SU8010型扫描电镜(SEM)观察样品的形貌,15 kV,喷金(5 Pa,2 mA,10 s,20次);使用PoreMaster33IQ型压汞仪测定样品的比表面积等。
2.4 Ca-Al-CLDH吸附Cl-性能研究
取5份Ca2+∶Al3+=1∶1的样品0.2 g,对Cl-浓度分别为100,200,300,400和500 mg/L的100 mL氯化钠溶液进行平行吸附实验,室温搅拌吸附一定时间后抽滤,再测定吸附后滤液中Cl-的浓度。Ca2+∶Al3+=2∶1、3∶1和4∶1的样品也同上进行相应的吸附实验。相关吸附机理见图1。

图1 Ca-Al-CLDH吸附Cl-机理图示Fig.1 Adsorption mechanism of Cl- by Ca-Al-CLDH
Cl-测定方法参照GB/T 15453—2018国家标准。具体步骤为:用移液管量取5 mL吸附后的氯化钠滤液于锥形瓶中,加入两滴10 g/L乙醇酚酞指示液,若水样变红,再滴加几滴0.184 M稀硝酸以调节氯化钠滤液的pH值使得红色褪去。加入两滴50 g/L橙黄色铬酸钾溶液作为滴定终点指示剂,之后缓慢滴加2.85 mM硝酸银溶液直至氯化钠滤液产生的砖红色沉淀30 s不褪去,则到达滴定终点。
3 结果与分析
3.1 不同Ca-Al比例金属板层对样品微观形貌的影响
在进行Cl-吸附之前,首先使用溶胶-凝胶法合成不同Ca/Al比例金属板层二元体系的Ca-Al气凝胶类水滑石样品。
通过对比图2中不同Ca-Al硝酸盐比例合成的Ca-Al气凝胶水滑石样品,可以发现在硝酸铝含量偏高时(图2(a)),样品形貌以氧化铝纤维为主;从图2(b)可以看出,当Ca2+∶Al3+=2∶1时,得到以六边形晶粒为骨架的Ca-Al气凝胶水滑石;当钙盐的含量升高时,Ca-Al水滑石晶粒会有明显的团聚现象(图2(c));当Ca2+∶Al3+=4∶1时(图2(d))Ca-Al钙铝水滑石晶粒会团聚成无孔的连续相。

图2 不同比例Ca-Al气凝胶水滑石样品的SEM图像 (a)-(d)分别为Ca2+∶Al3+=1∶1、2∶1、3∶1和4∶1,(e)为传统水热法制备的Ca2+∶Al3+=2∶1粉体)Fig.2 SEM images of Ca-Al-LDHs aerogel samples with different ratios (a)-(d) were Ca2+∶ Al3+=1∶1, 2∶1, 3∶1 and 4∶1, respectively and (e) was Ca2+∶Al3+=2∶1 powder prepared by traditional hydrothermal method)
通过对比溶胶-凝胶法和传统水热法所制备的Ca-Al水滑石可以看出,在Ca2+∶Al3+=2∶1时,使用溶胶-凝胶法所制备的Ca-Al水滑石气凝胶,在晶粒尺寸上比传统水热法所制备的水滑石要小,且结晶相对不完整,但是Ca-Al水滑石在溶胶-凝胶过程中晶粒彼此相连,形成以Ca-Al气凝胶水滑石晶粒为骨架的多孔结构,这表明可以成功得到所需的目标产物。
3.2 Ca-Al气凝胶水滑石样品的孔结构分析
在使用溶胶-凝胶法制备Ca-Al-LDHs气凝胶样品后,为表征相对于传统水热法所制备的Ca-Al-LDHs粉体在比表面积上是否有所提升,对样品进行了氮气吸附-脱附测试(BET),如图3所示。
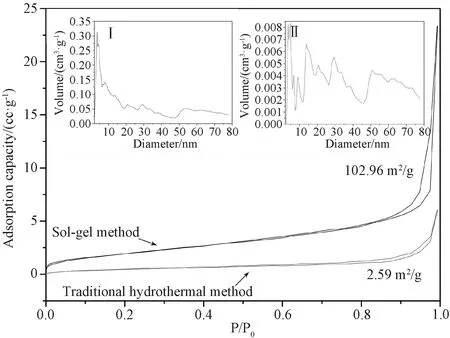
图3 钙铝气凝胶水滑石样品BET图(I.溶胶凝胶法气凝胶;II.传统水热法粉体)Fig.3 BET curves of Ca-Al aerogel LDHs sample (I. Sol-gel method aerogel; II. traditional hydrothermal method powder)
从图可见,使用溶胶-凝胶法制备的Ca-Al-LDHs气凝胶样品和使用传统水热法所制备的Ca-Al-LDHs粉体,均呈现大孔的吸附-脱附平衡曲线。结合孔容和孔径表征分析,结果显示Ca-Al-粉体材料孔容仅为0.008 cm3/g,平均孔径为62.615 nm,而经过溶胶-凝胶法制备的Ca-Al-LDHs气凝胶孔容可达0.286 cm3/g,平均孔径为73.239 nm,所以两种材料均呈现标准的大孔平衡曲线,在接近大气压时会有明显的液化现象。从图中还可以看出Ca-Al-LDHs粉体比表面积仅有2.59 m2/g,而Ca-Al-LDHs气凝胶样品在比表面上可以高达102.96 m2/g,这是由于在使用溶胶-凝胶法制备所需样品时,形成了以Ca-Al-LDHs纳米片层为核的Ca-Al气凝胶水滑石多孔骨架结构,所以气凝胶样品比表面积有了很大的提升。
3.3 Ca-Al气凝胶水滑石样品的物相分析
图4为分别采用传统水热法和溶胶-凝胶法制备的Ca-Al水滑石的XRD图谱。

图4 Ca-Al水滑石样品的XRD图谱Fig.4 XRD patterns of Ca-Al aerogel LDHs sample
通过对比观察发现,使用传统水热法所制备的Ca-Al水滑石要比使用溶胶-凝胶法所制备的衍射峰的峰型更窄、更尖锐;使用溶胶-凝胶法所制备的Ca-Al水滑石气凝胶,具有LDHs材料典型的(003)、(006)和(009)特征衍射峰,但由于结晶相对较小且生长相对不太完整,所以材料的半高宽较大。又因为气凝胶样品在制样时样品高度较高、晶粒生长边界存在应力且易形成水合氢氧化物使得晶粒生长相对不完整,所以峰位置也有所偏移。
3.4 高温焙烧态水滑石(Ca-Al-CLDH)对Cl-吸附性能研究
从图5可以看出,当Ca2+∶Al3+=2∶1时,Ca-Al-CLDH对Cl-的吸附具有最高的单位吸附量(35.63 mg/g)。当Ca2+∶Al3+=1∶1时,材料表面被氧化铝纤维所覆盖,以致单位吸附量不佳。结合SEM观察分析可以得到,随着Ca2+含量的增高,富钙板层材料趋于团聚结块,在吸附过程中不能充分和溶液中的Cl-交换,从而使得吸附性能明显下滑。

图5 Ca/Al比例和溶液pH值对Cl-的单位吸附量的影响Fig.5 Effects of ratio of Ca/Al and pH of solution on the unit adsorption of Cl-
同样也易看出,当溶液的pH=6~8时,Ca-Al-CLDH具有最佳的吸附性能。这是因为Ca-Al-CLDH属于金属氧化物,所以当pH<6时,板层会和溶液中的H+发生反应,使板层发生溶解,从而影响材料对Cl-的吸附;同样在pH>8时,材料对Cl-的单位吸附量也出现了明显的下滑,这是由于溶液中同时存在Cl-和OH-,这两种阴离子会存在一个竞争反应[16],争相作为平衡阴离子插入板层中间,又由于OH-和板层的-OH存在较强的氢键作用,所以OH-作为平衡阴离子插入板层的能力要强于Cl-,因此在OH-存在的水环境中,材料对Cl-的吸附能力会出现一个明显的下滑趋势。
图6为不同温度和Cl-初始浓度下Ca-Al-CLDH对Cl-吸附的平衡等温线。从图可见,材料对Cl-的单位吸附量随Cl-初始浓度的增高而增大,这是由材料对Cl-的吸附机理所决定的。吸附机理分为两个步骤:①由于材料表面呈正电,Cl-吸附在材料表面,使材料呈电中性。②利用材料的结构记忆效应,Cl-作为平衡阴离子快速穿插进入材料的阴离子层,恢复Ca-Al-CLDH的结构,所以当Cl-的浓度升高时,Cl-和材料接触和碰撞的几率也就会上升,从而提升了材料的单位吸附量。另外,随温度的升高,Cl-的吸附量也随之增大。

图6 溶液初始浓度和温度对Cl-的单位吸附量的影响Fig.6 Effects of initial concentration and temperature on the unit adsorption of Cl-
图7为利用LDHs的“记忆效应”,在室温下吸附时间和对应单位吸附量的关系曲线。从图中可以看出材料的吸附效率随时间的延长而上升,在180 min后趋于平衡,材料对Cl-的吸附达到饱和(最大值34.86 mg/g)。同样从曲线可以看出,在刚开始投入样品时(120 min前),材料对Cl-的吸附很快,这是由吸附机理和步骤决定的。而在120 min后,由于材料充分水合,已经吸附了大量的Cl-,从而趋于平衡,并且溶液呈现出碱性,OH-和Cl-会相互竞争进入板层,从而吸附效率从整体上呈现出平衡态势。

图7 吸附平衡时间对Cl-的单位吸附量的影响Fig.7 Influence of adsorption equilibrium time on unit adsorption of Cl-
Ca2+∶Al3+=2∶1时,溶胶-凝胶法可成功制备Ca-Al水滑石气凝胶。在气凝胶样品中LDHs晶粒彼此相连,形成以Ca-Al-LDHs纳米片为骨架的多孔结构,且比表面积由传统水热法制备粉体的2.59 m2/g提高到了102.96 m2/g。溶胶-凝胶法所制备的水滑石气凝胶衍射峰的半高宽较宽、峰高较矮且峰位有所偏移,这是由于气凝胶样品高度较高、晶粒生长边界存在应力且易形成水合氢氧化物,使得晶粒生长相对不完整所致。
Ca-Al-CLDH材料为金属氧化物,在pH<6时,板层会和溶液中的H+反应,使板层发生溶解,影响对Cl-的吸附;在pH>8时,溶液中的Cl-和OH-,存在一个竞争过程,从而影响材料对Cl-的吸附。当温度升高时,Cl-的吸附量也随之增大(41.3 mg/g,60 ℃)。同样,随着吸附时间的延长,材料对Cl-的吸附效率也呈现出上升的趋势,在180 min后基本达到吸附平衡。
