3种添加物抑制模拟体系中羟甲基糠醛(HMF)的形成
2021-07-27欧隽滢江楷煜高瑜悦张延杰黄才欢
欧隽滢,江楷煜,高瑜悦,张延杰,黄才欢
(1.暨南大学食品安全与营养研究院,广东广州 510632)(2.暨南大学食品科学与工程系,广东广州 510632)(3.中山洪力健康食品产业研究院有限公司,广东中山 528430)
热加工是食品制作的一种主要加工方式,但过度热加工不仅破坏营养素,而且产生有害物质,如5-羟甲基糠醛(HMF)、丙烯酰胺、杂环胺、氯丙醇、活泼羰基化合物、晚期糖基化终末产物(AGEs)等[1-5]。食品添加剂是为改善食品品质和色、香、味,以及为防腐、保鲜和加工工艺的需要而加入食品中的人工合成或者天然物质。基于安全考虑,食品添加剂对有害物质形成的影响近年报道较多。研究发现,食盐影响油脂产生氯丙醇:当添加量较低时,随着其浓度的增加,氯丙醇形成量增加;进一步增加氯化钠浓度,氯丙醇反而下降。在油酸甘油酯、猪油和鸡油的模拟反应体系中,食盐促进氯丙醇生成的最有效剂量分别是7.00%、20.00%和10.00%[6,7]。活泼羰基化合物如乙二醛、丙酮醛是丙烯酰胺和晚期糖基化终末产物(AGEs)形成的前体,膨松剂碳酸氢铵促进面包、曲奇等焙烤食品中乙二醛和丙酮醛的形成[8],并显著增加丙烯酰胺含量:当面包中碳酸氢铵添加量分别为0.40和1.60 g/100.00 g时,丙烯酰胺含量分别增加17.00和88.00倍[9]。碳酸氢钠同样促进丙烯酰胺的形成。在挤压膨化食品中(含水量22.00%~26.00%),添加0.10 g/100.00 g的碳酸氢钠使丙烯酰胺含量增加2.00~3.50倍[10]。
鉴于一些食品添加剂可能产生负面作用,国家对食品添加剂的管理越来越严格。如2014年,国家卫生计生委等5部门联合印发的《关于调整含铝食品添加剂使用规定的公告》,限制了硫酸钾铝、硫酸铝铵等膨松剂的应用范围。主要原因是长期摄入铝会对人体产生慢性毒作用,包括神经毒性、生殖毒性和肝脏毒性[11],影响人的神经系统和人的脑细胞等代谢,以及儿童生长和智力发育[12]。但是,基于食品添加剂影响有害物质形成而被限制使用的例子在国内还不多见。但欧洲要求更为严格,如欧洲食品安全局经过10多年的评估,2017年出台了食品中丙烯酰胺控制法规(Commission Regulation (EU) 2017/2158),要求食品企业减少碳酸氢铵等膨松剂用量或采用其替代品[13]。
5-羟甲基糠醛(HMF)是热加工食品中含量较高的一种内源有害物,广泛存在于焙烤食品、干果和焦糖制品中[1,14]。高剂量的HMF对人体横纹肌、内脏、基因和神经等具有毒副作用,对皮肤、眼睛、上呼吸道及粘膜具有刺激和损伤作用,并通过醛基与人体蛋白(DNA)的氨基或巯基反应,影响细胞功能和生长,影响正常代谢[15,16]。但低剂量的HMF却具有抗氧化、抗肿瘤细胞增殖、改善血液流变学、抗心肌缺血、调节Ca2+平衡、抗酪氨酸酶等生物活性[15]。10年前Monien等发现,磺基转移酶可将HMF转化为具有致癌活性和基因毒性的5-亚磺酰甲基糠醛[17],该酶广泛存在于人和动物体内。因此,摄入高剂量的HMF可能导致人体产生各种癌变,如肝癌、结肠癌等[18]。2015年欧洲食品安全局正式确认了5-亚磺酰甲基糠醛的致癌活性[19]。因此,近年来,食品中HMF的安全性问题成为国际研究热点。
焙烤、油炸、膨化等高温加工食品因其食用量大,HMF含量高而成为人体HMF的重要来源。目前人们对HMF的形成途径已基本清楚,主要来自己糖脱水,或丙酮醛和甘油醛通过羟醛缩合反应后产生HMF[20]。其形成受糖类、加工温度、pH、水分活度、二价或三价阳离子以及酚类物质等的影响[20],但有关食品䐍化剂等添加物的影响鲜见报道。
碳酸氢铵、碳酸氢钠是焙烤、膨化食品中常用的膨松剂;食盐可使面筋质地变细密,增强面筋的立体网状结构,易于扩展延伸,并作为咸味剂而广泛添加到面团中[21]。因此,本研究以焙烤、膨化食品的主要内源化学污染物HMF为对象,采用形成HMF的不同前体物质(葡萄糖、果糖和蔗糖)构建模拟反应体系,考察膨松剂碳酸氢铵和碳酸氢钠、食盐对HMF形成的影响,并以饼干为代表在食品中进行验证。硫酸铝钾和硫酸铝铵过去一直作为膨松剂允许在小麦粉及其制品、虾味片、焙烤食品、膨化食品等(GB2760-2011)或焙烤食品、油炸面制品、面糊、虾味片等(GB2760-2014)食品中使用[22,23],但国家卫生计生委等5部门联合印发的《关于调整含铝食品添加剂使用规定的公告》(2014年第8号)已禁止其在小麦粉及其制品(除油炸面制品、面糊、裹粉、煎炸粉外)中使用。为了进一步评价这两种含铝膨松剂的负面效果,为国家的规定提供更多依据,本研究一并将其纳入进行研究。
1 材料与方法
1.1 材料与仪器
低筋面粉(五得利面粉集团有限公司)、起酥油,购于广州市暨南大学兴安超市;葡萄糖、果糖、蔗糖、甘氨酸、食盐、碳酸氢钠、碳酸氢铵、硫酸铝钾、硫酸铝铵,分析纯,百灵威科技有限公司;羟甲基糠醛(HMF),99%纯度,百灵威科技有限公司;甲醇,色谱纯,Mallinckrodt Baker公司;不锈钢试管(25.00 mL)为实验室定制品。
LC-20AT高效液相色谱仪(配备SPD-M20A光电二极管阵列检测器),日本岛津有限公司;磁力加热搅拌器(DF-Ⅱ型集热式),江苏省金坛市医疗仪器厂;离心机(KDC-12),安徽中科中佳科学仪器有限公司。
1.2 实验方法
1.2.1 5种添加物对不同前体物质形成HMF的影响
按照Zhang等的方法设置4个模拟反应体系[24]:葡萄糖/甘氨酸(美拉德反应体系)、葡萄糖、果糖、蔗糖(各成分浓度均为1.00 mM),研究不同浓度的碳酸氢钠、碳酸氢铵和食盐(2.00、4.00、6.00、8.00、10.00 mg/mL),以及硫酸铝钾和硫酸铝铵(0.20、0.40、0.60、0.80、1.00 mg/mL)对HMF形成的影响。将总体积为5.00 mL的反应混合物置于不锈钢试管中,在160 ℃油浴中反应15 min,冰水浴冷却后用去离子水定容至10.00 mL,经0.45 μm水相微孔滤膜过滤,采用HPLC法测定HMF含量[25]。
HPLC色谱条件:色谱柱为ZORBAX SB-Aq(4.60×250.00 mm, 5.00 μm),流动相为甲醇-水(5:95,V/V),0.60 mL/min流速等度洗脱40 min,检测波长284 nm,柱温40 ℃,进样量10.00 μL。并以去离子水配制6.25~100.00 mg/L的HMF系列标准溶液,制作标准曲线,外标法定量。
1.2.2 五种添加物对饼干中HMF形成的影响
饼干制作:参考Van Der Fels-Klerx等[26]的方法制作饼干。面团配方:小麦面粉80.00 g,精炼棕榈油20.00 g,蔗糖35.00 g,水17.60 g。碳酸氢钠、碳酸氢铵、食盐、硫酸铝钾和硫酸铝铵的添加量见表1。首先在不锈钢盆中将蔗糖和添加物用水分别溶解,再与起酥油充分混合,加入面粉和剩余水制成面团,用压面机压面5次后,切成3.00 cm×5.00 cm×0.30 cm形状面饼片,190 ℃烘烤10 min后,将饼干取出置于干燥器中冷却。根据Zou等的方法[27]提取饼干中的HMF。取5.00 g饼干粉末,用20.00 mL 80%甲醇水溶液连续超声强化提取。每次提取30 min,样品液在3000.00 g下离心20 min,收集上清液;对沉淀进行第二次提取,重复三次后,合并上清液。在60 ℃下减压浓缩,除去水和甲醇,得残留物;加入2.00 mL蒸馏水溶解残留物,用0.45 μm滤膜过滤,按1.2.1中的方法,采用HPLC法检测HMF含量。

表1 饼干配方Table 1 Biscuit formulations
1.2.3 饼干水提液pH的测定
按Huang等[28]的方法获得饼干水提液。称取1.00 g饼干粉末于离心管中,加入5.00 mL水,超声提取20 min,3000.00 g离心20 min,取上清液,再加2.00 mL水重复提取2次,合并上清液,用pH计测定提取液样品的pH。
1.3 数据处理
以上各项测试均重复3次,采用SPSS 17.0软件系统进行统计学分析,实验数据以平均数±SD表示。在5.00%水平下,采用Duncan多重比较分析处理间显著性差异。
2 结果与分析
2.1 碳酸氢钠对模拟反应体系中HMF形成的影响
由图1可知,在美拉德和果糖反应体系中,碳酸氢钠显著抑制HMF形成,添加量为2.00 mg/mL时,体系中的的HMF的生成量分别为5.01、3.02 mg/L,与对照组相比分别下降3.06和8.68倍;随着添加量的增大,HMF生成量进一步降低。其原因可能是由于碳酸氢钠的水解,提高了体系的pH,不利于美拉德反应中间体薛夫碱的形成和3-脱氧奥苏糖脱水转化为HMF[29]。同时,碳酸氢钠的钠离子可能和钾离子相似,抑制HMF形成[21]。对于果糖体系,呋喃果糖阳离子是产生HMF的关键步骤,酸性条件下有利于其形成,而碱性的碳酸氢钠则抑制了呋喃果糖阳离子的产生,从而导致HMF含量下降。
在葡萄糖体系中,随着碳酸氢钠添加量的增加,HMF的生成量增加。碳酸氢钠添加量为6.00 mg/mL时HMF达到最高值17.23 mg/L,为对照(无添加物)的3.31倍。进一步增加碳酸氢钠添加量,HMF含量开始下降。当碳酸氢钠添加量为10.00 mg/mL时,HMF形成量与对照相当(图1)。其原因可能是在弱碱性环境下,有利于葡萄糖异构化为果糖,而果糖形成HMF的能力显著高于葡萄糖[21]。如前所述,如果碳酸氢钠添加过量,则使pH增高,从而抑制呋喃果糖阳离子的形成和3-脱氧奥苏糖的脱水,导致HMF形成下降。而蔗糖的水解需要在酸性条件下才能进行,碱性的碳酸氢钠不能促进蔗糖水解为果糖和葡萄糖,因而碳酸氢钠对蔗糖形成HMF无影响(图1)。
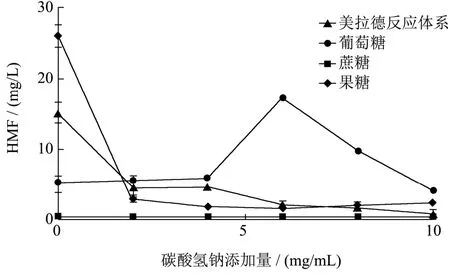
图1 碳酸氢钠对4个模拟反应体系中HMF形成的影响Fig.1 Effects of sodium bicarbonate on HMF formation in four model reaction systems
2.2 碳酸氢铵对模拟反应体系中HMF形成的影响
与无添加物的对照组相比,碳酸氢铵降低所有模拟反应体系中HMF含量(图2)。当添加量为2.00 mg/mL时,碳酸氢铵在美拉德、葡萄糖和果糖反应体系中都显著抑制HMF形成,HMF含量分别3.30、1.61和17.52 mg/L,下降4.64、3.28和1.49倍。碳酸氢铵对果糖体系中HMF的抑制效果呈剂量效应。但在美拉德和葡萄糖反应体系中,添加量为4.00~6.00 mg/mL时,碳酸氢铵会略微促进HMF形成(与2.00 mg/mL的添加量相比),而后含量下降。蔗糖体系中形成的HMF量很低,碳酸氢铵抑制其形成(图2)。碳酸氢铵水解后呈弱碱性,有利于葡萄糖烯醇化进而转化为果糖,促进HMF形成;但是,NH4+对HMF形成的抑制效果[29]可能发挥了主要作用,从而导致美拉德反应、葡萄糖和果糖模拟反应体系中的HMF含量下降。
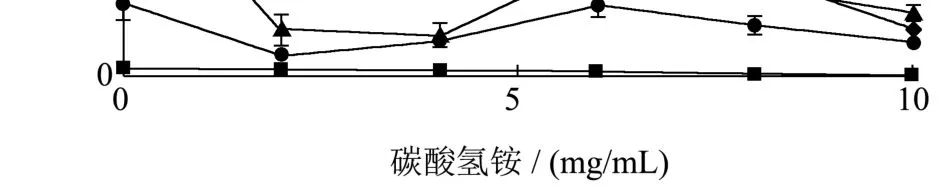
图2 碳酸氢氨对4个模拟反应体系中HMF形成的影响Fig.2 Effects of ammonium bicarbonate on HMF formation in four model reaction systems
2.3 食盐对模拟反应体系中HMF形成的影响
由图3可知,在美拉德、葡萄糖与果糖反应体系中,食盐的添加均抑制HMF的生成,且呈剂量依赖关系。当添加量为4.0 mg/mL时,HMF生成量分别为7.21、1.52和9.03 mg/L,分别比对照组下降52.88%、70.77%和65.40%。在蔗糖体系中,其pH值趋于中性,酸水解难以发生,因此该体系中HMF的生成量是四个体系中最低的(图3)。以上结果表明,食盐在焙烤食品中除改善口感和面团结构外,还具有抑制HMF形成的作用。

图3 食盐对4个模拟反应体系中HMF形成的影响Fig.3 Effects of table salt on HMF formation in four model reaction systems
2.4 铝盐对模拟反应体系中HMF形成的影响
由图4可知,硫酸铝钾在4个模拟反应体系中均显著促进HMF形成。在蔗糖模拟体系中,硫酸铝钾的促进效果最明显,且呈剂量效应;当添加量达到1.00 mg/mL时,HMF形成量为348.30 mg/L,是对照组的696.60倍。在其它3个反应体系中(美拉德、葡萄糖和果糖反应体系),HMF形成量在硫酸铝钾添加量为0.60 mg/mL时达到峰值,分别为80.52、13.00和265.03 mg/L,是对照组的5.26、2.50和10.15倍。硫酸铝铵也显著促进HMF的形成,且对蔗糖形成HMF的促进效应最强。当添加量为1.00 mg/mL时,HMF形成量是161.41 mg/L,是对照组的322.82倍。在其它3个反应体系中(美拉德、葡萄糖和果糖反应体系),HMF在硫酸铝铵添加量为0.60 mg/mL时达到峰值,分别为50.92、9.94和139.31 mg/L,是对照组的3.33、1.91和5.34倍。

图4 硫酸铝钾(a)和硫酸铝铵(b)对4个模拟反应体系中HMF形成的影响Fig.3 Effects of potassium aluminium sulphate (top) and ammonium aluminium sulphate on HMF formation in four model reaction systems
与碳酸氢钠、碳酸氢铵和食盐处理组比较,硫酸铝钾和硫酸铝铵大幅增加HMF生成量。在最低剂量组(2.00/0.20 mg/mL),硫酸铝钾处理组的HMF含量分别是碳酸氢钠、碳酸氢铵和食盐的4.22、6.39、2.05倍(美拉德反应体系),1.24、4.19、1.31倍(葡萄糖反应体系),29.00、4.97、8.13倍(果糖反应体系),300.60、250.50、250.50倍(蔗糖反应体系)。在最高剂量组(10.00/1.00 mg/mL),硫酸铝钾处理组的HMF含量分别是碳酸氢钠、碳酸氢铵和食盐处理组的46.55、11.64、14.22倍(美拉德反应体系),2.21、3.88、2.58倍(葡萄糖反应体系),64.28、48.70、27.71倍(果糖反应体系),696.60、1161.00、248.79倍(蔗糖反应体系)。在最低剂量组,硫酸铝铵处理组的HMF含量分别是碳酸氢钠、碳酸氢铵和食盐处理组的3.34、5.06、1.62倍(美拉德反应体系),1.00、3.38、1.06倍(葡萄糖反应体系),14.47、2.48、4.06倍(果糖反应体系),90.00、75.00、75.00倍(蔗糖反应体系)。在最高剂量组,硫酸铝铵处理组的HMF量分别是碳酸氢钠、碳酸氢铵和食盐处理组的22.18、5.55、6.78倍(美拉德反应体系),1.50、2.63、1.75倍(葡萄糖反应体系),38.96、29.52、16.79倍(果糖反应体系),322.80、538.00、115.29倍(蔗糖反应体系)。
硫酸铝钾和硫酸铝铵对HMF的促进机理可能源于两方面。一是它们都为强酸弱碱盐,水解后pH降低,而较低pH有利于HMF的形成且促进蔗糖在高温下水解[20]。二是Al3+的催化效果。由于三价阳离子铝比二价阳离子钙、镁对HMF的催化效率更高[20],因此Al3+的催化可能发挥更重要的作用。硫酸铝铵对HMF形成的促进效应小于硫酸铝钾,主要原因可能是NH4+对HMF形成的抑制作用[30]。
2.5 五种添加物对饼干中HMF形成的影响
图5 的结果表明,与无添加物的对照相比,食盐、碳酸氢铵和碳酸氢钠处理组的HMF含量都降低。其中,1.00g食盐+0.40 g碳酸氢铵与1.00 g食盐+0.80 g碳酸氢铵+0.80 g碳酸氢钠的处理降低最多,其含量分别为0.88和0.86 mg/kg,分别下降35.34%和33.83%。在硫酸铝钾和硫酸铝铵处理组中,尽管添加了对HMF具有抑制效果的食盐、碳酸氢铵和碳酸氢钠,HMF含量还是大幅升高。当硫酸铝钾添加量为0.05 g和0.10 g时,HMF含量分别2.11和2.16 mg/kg,增加58.65%和62.41%。在低添加剂量下(0.05 g),硫酸铝铵仅略微增加HMF含量,但高剂量(0.10 g)下HMF含量增加了55.64%。因此,从HMF形成角度看,限制含铝膨松剂在食品中的使用非常合理。添加0.10 g硫酸铝钾与硫酸铝铵后,饼干水提液的pH从9.60下降至6.50左右,pH的降低促进了己糖直接脱水形成HMF[20]。不过,铝盐中三价铝离子的催化效应可能是铝盐促进HMF形成的主要原因。研究表明,样品中的HMF 含量与配方有着重要的关系,由于不同的膨松剂的使用,使食品体系的pH值有着明显的差异,从而影响HMF 的含量。Kukurova′证实,若用碳酸氢铵(1.00 g/80.00 g面粉)作为膨松剂制作曲奇时,体系的pH值约在7.82,其HMF含量在焙烤过程中出现明显上升;若只采用碳酸氢钠(2.00 g/80.00 g面粉)作为膨松剂时,可使食品中HMF的含量从2.96 mg/kg降至1.30 mg/kg,降低了56.08%;主要是因为碳酸氢钠可使体系的pH控制在8.10~10.00,从而抑制蔗糖形成呋喃果糖阳离子和3-脱氧奥苏糖[31];但碳酸氢钠添加过多会使制品中碱味较大[32]。
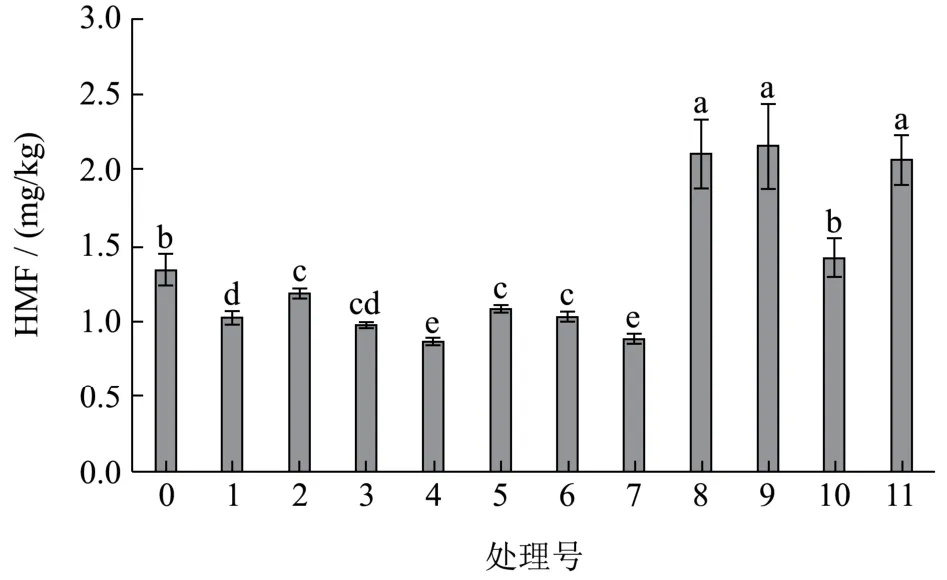
图5 五种添加物对饼干中HMF形成的影响Fig.5 Effect of five additives on HMF formation in biscuits
3 结论
探讨添加物对食品有害物形成的影响是目前国内外的研究热点。本研究发现,焙烤食品的添加物食盐和膨松剂碳酸氢钠、碳酸氢铵在模拟反应体系中能显著降低HMF含量,当碳酸氢钠添加量为2.00 mg/mL时,美拉德(葡萄糖/甘氨酸)和果糖反应体系中HMF的生成量分别为5.01、3.02 mg/L,较对照组下降3.06和8.68倍;加入相同量的碳酸氢铵时,美拉德、葡萄糖和果糖反应体系中HMF含量分别为3.30、1.61和17.52 mg/L,分别比对照组下降4.64、3.28和1.49倍;当食盐添加量为4.00 mg/mL时,HMF生成量分别为7.21、1.52和9.03 mg/L,降幅达52.88%、70.77%和65.40%。而被禁用的膨松剂硫酸铝钾和硫酸铝铵,则显著增加HMF含量,最高可达310.13和139.31 mg/L,增幅达620.26和197.00倍。该结果在饼干中得到验证:添加食盐、碳酸氢钠和碳酸氢铵降低饼干中HMF含量,浓度在0.86~0.88 mg/kg之间,降幅为33.83%~35.34%。但是,即使在添加了食盐、碳酸氢钠和碳酸氢铵的情况下,硫酸铝钾和硫酸铝铵仍使饼干中HMF含量为2.11和2.16 mg/kg,增幅为58.65%和62.41%。由于HMF在体内可转化为致癌物质5-亚磺酰甲基糠醛,而焙烤、油炸食品食用量大,HMF含量高而成为人体HMF的重要来源,本研究结果进一步支持了国家限制含铝膨松剂使用的合法性。
