以豌豆荚为碳源制备氮掺杂碳点及应用研究
2021-07-26韩爱霞王玉环谢亚典谢荣荣吴瑞鑫刘兴亮
韩爱霞,王玉环,谢亚典,谢荣荣,杨 欢,吴瑞鑫,刘兴亮
(青海大学化工学院, 青海 西宁 810016)
碳点(Carbon Dots,CDs)以其优异的荧光性能、激发/发射可调、细胞毒性低、水溶性好、应用广泛等优点受到越来越多的关注[1]。而在CDs中等效掺杂一些杂原子,并在其结构中引入电子施主或受主,赋予了CDs不同于纯CDs的一些新的性能[2]。如Xu等[3]通过水热法合成N掺杂CDs(NCDs),然后用于亚硝酸盐的检测和多色细胞成像。Zhou等[4]合成了一种P掺杂CDs (P-CDs),具有量子产率高达25%、细胞毒性低、生物标记能力突出的特点。其中,N掺杂CDs的使用最多,因为N原子与C原子有一定的相似性,且N原子中的孤对电子以及在CDs内部结构中引入的缺陷位点,可以改变NCDs的电子环境,有效提高其荧光性能[5]。
汞离子(Hg2+)是一种有毒的重金属离子,容易通过食物聚集在人体内,会对人体神经系统、免疫系统、肾脏、肝脏[6]等造成损害。同时,因其不能迅速被生物降解也造成了严重的环境问题。因此,对微量Hg2+的检测是非常必要的。常用的Hg2+测定分析技术有原子吸收/发射光谱(AAS/AES)、紫外-可见光谱(UV-Vis)、X射线吸收光谱(XAS)、电感耦合等离子体质谱(ICP-MS)和极谱等[7-8]。但是,这些方法在准确检测Hg2+方面都存在一定的缺陷。近年来,各种基于CDs/NCDs的荧光探针被开发用于测定Hg2+。
本文以生物质废弃物豌豆荚和乙二胺分别作为碳前体和氮前体,通过简单的水热合成方法,制备了一种新型的NCDs。对制备的NCDs用多种仪器分析技术进行结构表征和性能测试并将其成功用于Hg2+的测定。
1 实验部分
1.1 试剂与仪器
豌豆荚(购于青海省西宁市小桥农贸市场)使用前先用超纯水彻底超声清洗,榨汁备用。尿素、乙二胺、二乙醇胺、三聚氰胺均购自天津市大茂化学试剂厂,所有试剂均为分析纯;实验全程使用超纯水。
Shimadzu UV-2550分光光度计(日本Shimadzu公司); Perkin Elmer Spectrum Ⅱ光谱仪(美国Perkin Elmer 公司);Cary Eclipse 荧光分光光度计(美国Agilent公司);Rigaku D/Max 2500 PC X射线衍射仪(日本Rigaku公司);JEOL JEM-1200EX透射电镜(日本电子株式会社JEOL);Thermo scientific ESCALABTM 250Xi X 射线光电子能谱仪(美国Thermo公司);Milli-Q Direct 16 超纯水系统(德国Merck Millipore公司);聚四氟乙烯反应釜;101F3-D 恒温干燥箱(上海申光公司);冷冻干燥机(上海普若迈德公司);H2050R-1 型高速离心机(湖南湘仪公司);MWCO=1 kD的透析袋。
1.2 NCDs的制备与提纯
将5 mL豌豆荚汁、1.33 mL乙二胺加到50 mL 的聚四氟乙烯内衬中,再加入超纯水至30 mL,搅拌均匀并超声赶走气泡。将聚四氟乙烯内衬密封进反应釜中,拧紧釜盖,放入预热好的200 ℃恒温干燥箱中,水热反应20 h后将反应釜自然冷却至室温。取上清液离心 (12 000 r/min,20 min),所得清液用MWCO=1 kD 的透析袋透析(25 ℃,60 r/min搅拌,8 h换水) 24 h,收集透析袋内液体,得到纯化的碳点溶液。将纯化的碳点溶液预冷冻成冰状,放入预冷好的真空冷冻干燥机中冻干,可得碳点粉末。
1.3 NCDs对重金属离子的检测
配制NCDs溶液(0.05 g/L,3.0 mL);配制0.1 mol/L的金属离子(Hg2+、Ba2+、Ca2+、Cd2+、Co2+、Cu2+、Mg2+、Mn2+、Pb2+)硝酸盐溶液作为测试液。
第一组实验中,将3.0 μL金属离子硝酸盐溶液分别添加到NCDs溶液中,混合均匀后在419 nm处检测NCDs荧光强度的变化。
第二组实验中,在竞争离子存在的NCDs溶液中加入Hg2+,检测Hg2+与其他金属离子的竞争能力,测定NCDs的荧光强度变化。
2 结果与分析
2.1 NCDs形貌的表征
通过XRD图谱和TEM图像表征NCDs形貌的特征。NCDs的XRD图谱如图1a所示,在21.5°附近有一个较宽的衍射峰,由布拉格公式计算可得晶面间距d为0.41 nm,对应为石墨无定形结构[9]。图1b为NCDs的TEM图像,其内嵌图为NCDs的粒径分布,统计520个NCDs的粒径可知平均粒径为2.42 nm,粒径主要分布在1.59~3.96 nm内,由此可知以豌豆荚为碳源制备的碳点粒径很小,很均匀。

图1 NCDs的XRD图谱和TEM图像Fig.1 XRDFigure and TEM image of NCDs
2.2 NCDs元素与官能团的表征


图2 NCDs元素与官能团的表征Fig.2 Characterization of NCDs elements and functional groups

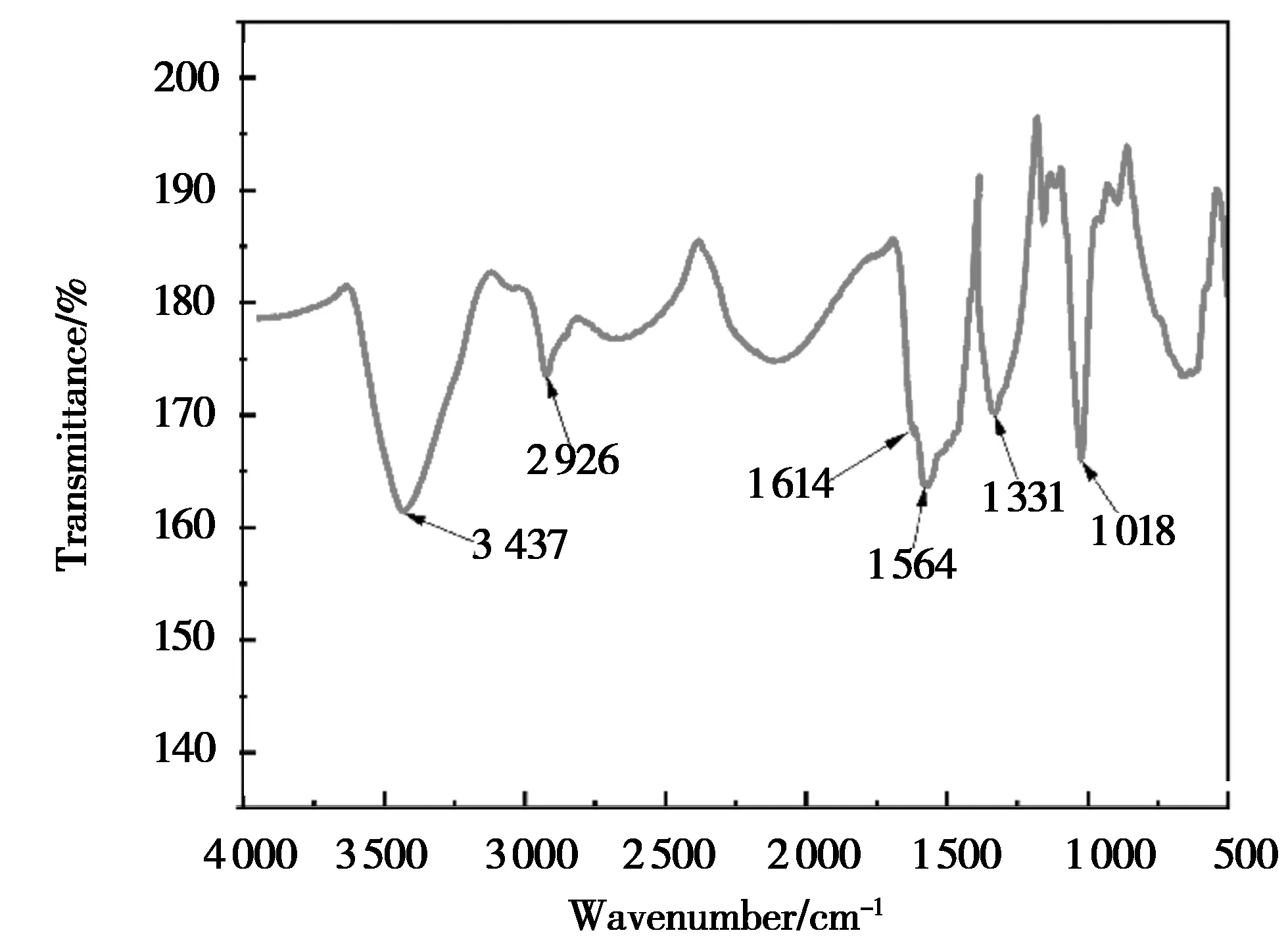
图3 NCDs的FTIR光谱 Fig.3 FTIR spectrum of NCDs

2.3 NCDs光学性能的表征及检测机理

为测试合成的NCDs有无其他碳点具有的激发波长依赖特性,在不同激发波长激发下扫描其发射光谱,结果如图4b所示。NCDs的激发波长从300 nm增至420 nm时,其最大发射波长从417 nm红移至485 nm,荧光强度先升高后降低,在340 nm激发时荧光强度达到最高,NCDs具有激发波长依赖性[14]。
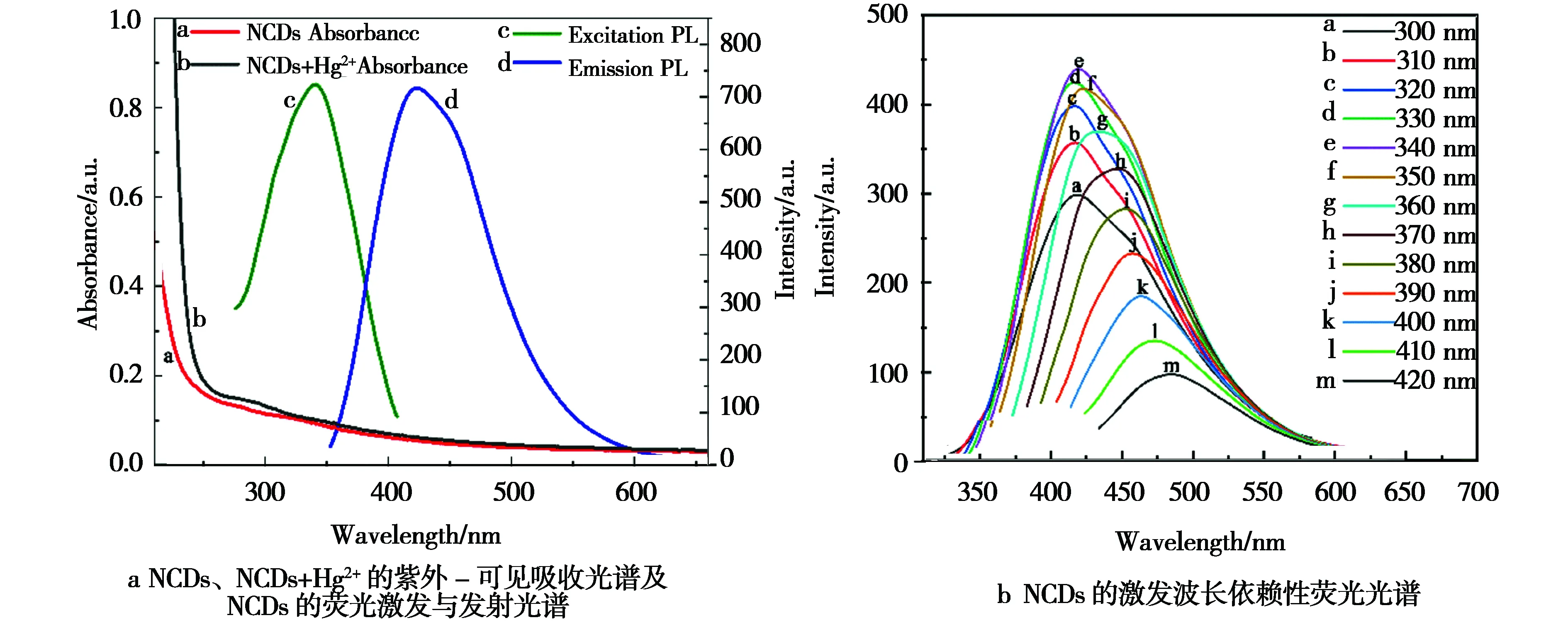
图4 NCDs光学性能的表征Fig.4 Characterization of optical properties of NCDs
2.4 NCDs对重金属Hg2+的检测
2.4.1 选择性和竞争性
如图5a所示,在Hg2+、Ba2+、Ca2+、Cd2+、Co2+、Cu2+、Mg2+、Mn2+、Pb2+等金属离子中, Hg2+淬灭NCDs的荧光效果明显,这表明NCDs 对Hg2+测定的选择性比较高。
从图5b可以看出,将Hg2+分别加入竞争金属离子存在的NCDs溶液中,NCDs的荧光淬灭程度与Hg2+单独加入NCDs溶液时的荧光淬灭程度几乎一致,这说明Hg2+与其他金属离子相比有较强的竞争能力。

图5 NCDs对不同金属离子的响应结果及在其他金属离子存在时对Hg2+的响应结果Fig.5 Response of NCDs to different metal ions and Hg2+in the presence of other metal ions
2.4.2 工作曲线及检测限测定
测定NCDs原溶液的荧光光谱,然后加入Hg2+溶液,并在340 nm激发波长下扫描每次加入Hg2+溶液后的荧光光谱,如图6a所示。取其峰值 (419 nm) 处的荧光强度 (FL) 与加入Hg2+溶液的浓度 (c) 作图并拟合可得工作曲线,结果显示Hg2+溶液的浓度(0~300 μmol/L)与荧光强度之间成良好的线性关系(图6b),通过拟合及计算可得其线性关系表达式:FL=-8.11×c+421.28。根据检出限(LOD)的计算公式LOD=3σ/K(σ是11次空白测定的标准偏差,K是工作曲线的斜率),计算得到检出限为2.36 μmol/L。

图6 NCDs对Hg2+的荧光滴定光谱及工作曲线Fig.6 Fluorescence titration spectrum and working curve of NCDs for Hg2+
3 讨论与结论
本文以豌豆荚和乙二胺为前体,采用水热法合成了NCDs,通过荧光淬灭可以在0~300 μmol/L线性范围内选择性检测重金属Hg2+,检出限低至2.36 μmol/L。目前已有一些NCDs用于检测Hg2+的文献报道,Li等[15]以橙汁和乙二胺为原料合成NCDs,该NCDs的荧光强度比在4.0~32.0 μg/mL范围内与Hg2+浓度成正比,加标样品的回收率为102.0%~103.0%。Singh等[16]用柠檬酸和二氨基吡啶为原料合成了一种NCDs,对Hg2+测定的线性范围在0.2~1.2 μmol/L,检出限低至 0.08 μmol/L。与以上研究相比,本研究为NCDs的制备提供了新原料,给Hg2+的检测提供了新材料,实现了对生物质废弃物豌豆荚的高效利用,符合绿色环保可持续发展的理念。
