酚类化学品在好氧污水处理系统中归趋特征
2021-07-18周林军范德玲刘济宁石利利徐炎华
周林军,古 文,冯 洁,范德玲,郭 敏,刘济宁,石利利,徐炎华
(1.南京工业大学 生物与制药工程学院,江苏 南京 211800;2.生态环境部南京环境科学研究所 国家环境保护农药环境评价与污染控制重点实验室,江苏 南京 210042;3.苏州化工职业病防治院,江苏 苏州 215000;4.南京工业大学 环境科学与工程学院,江苏 南京 211800)
酚类化学品(PCs)主要为人工合成化学品,被广泛用作增塑剂、工业洗涤剂、农药乳化剂、纺织整理剂等[1]。PCs常用于合成烷基酚聚氧乙烯醚(APEOs),同时也会作为APEOs的分解产物存在于环境当中。目前PCs在欧盟以及美国被视为高产量化学品,其中壬基酚、辛基酚以及其合成的聚氧乙烯醚类物质在全球市场占据主要比例[2]。
多项研究证实APEOs 与PCs均属于内分泌干扰物[1,3-4],此类物质能打破生物体原有的内分泌平衡从而影响有机体的正常生长、行为和繁殖,即使远低于理论安全浓度仍然会影响野生动物生殖系统和胚胎发育[3,5-6]。由于较强的内分泌干扰效应(EDC),联合国环境保护署以及美国、加拿大等已经出台了相关的管理政策和禁限用规定[7],近年来欧盟REACH法规也将对特辛基酚、4-庚基苯酚、4-叔丁基苯酚列入高关注物质清单。
由于PCs潜在的EDC特性及水生急、慢性毒性效应[8-10],研究其环境归趋及暴露将对评估环境风险具有重要意义[11]。有研究表明PCs在我国地表水及水生生物中被普遍检出[12-18],主要来源为污水处理厂(STP)排放的污水[7]。PCs在工业生产、使用和消费过程中,将不可避免地随工业废水和生活污水排入STP,因此STP是化学品进入环境的最后一道关口,也是化学品环境归趋重要的中转站:挥发性化学品在好氧曝气过程中重新进入大气,吸附性化学品吸附在剩余污泥中通过污泥农用等方式进入农田,未处理完全的化学品随二级出水排入地表水。因此,PCs在STP好氧污水处理系统中的归趋与去除研究是环境暴露水平评估的重要内容。然而,目前国内外对PCs的安全性评估焦点仍然为壬基酚、辛基酚、聚氧乙烯醚、四溴双酚A等[19-24],由于PCs种类众多,且污水处理工艺众多,大部分PCs在STP中的归趋仍然未得到充分的评估[25-26]。
化学品在STP中的归趋评估方法有室内批次试验、室内模拟试验、STP实测验证及模型预测方法。室内批次试验可采用经济合作与发展组织(OECD)化学品测试导则的快速生物降解性试验[27-28]。快速生物降解性指化学品在水体好氧环境下被微生物彻底的降解为CO2和H2O的潜力,其不添加任何碳源,也不进行微生物驯化,降解条件非常严苛,达到通过水平即可认为能在环境中被微生物有效地降解[29]。室内模拟试验可采用OECD 303A试验方法[30],在实验室搭建小型试验装置模拟测定化学品在STP中的去除效率,目前常采用好氧生化处理方法[31]。STP实测验证方法可以研究处理工艺、运行工况对去除效率的变异性影响[32]。模型预测方法则是基于化学品在STP中的吸附、挥发、气提和降解机制以及环境介质平流和扩散流过程而开发的数学模型,常用的预测软件有Simple Treat[33]、STPWIN[34]以及C-STP[35],这些模型都采用传统的好氧活性污泥工艺[36]。
化学品在STP中的归趋评估方法是一种层级评估策略,从简单到复杂,从保守到精准,从不同方位提供不同的信息。如室内批次试验可以评估化学品在环境中的最终矿化能力,并可得到降解动力学信息。室内模拟试验可以提供化学品在STP中的去除信息以及最佳去除条件。STP实测验证可以得到化学品在环境真实条件和处理工艺下的去除以及化学品的暴露水平。而模型预测可以揭示化学品的挥发、吸附和生物降解归趋机制以及去除贡献率。
本文利用上述4种归趋评估方法,系统地研究18种PCs的快速生物降解性,研究PCs在污水模拟系统中的去除效率以及在STP中的去除效率及暴露水平,并使用模型研究PCs在STP中的归趋机制,以期为PCs的环境暴露评估、持久性评估及风险防控提供基础。
1 试验
1.1 主要仪器与试剂
生化需氧量(BOD)测定仪(OXITOP CONTROL 12型,德国WTW),好氧生化污水处理模拟系统(KLD4N/SR型,德国BEHR LABOR-TECHNIK GMBH),可控恒温培养箱(ET99636型,德国LOVIBOND),高效液相色谱-串联质谱仪(LC-MS/MS,液相色谱为1290型,美国AGILENT,质谱为QTRAP 4500型,美国AB SCIEX),总有机碳(TOC)分析仪(N/C 3100型,德国ANALYTIKJENA)。
PCS标准品,分析纯,上海百灵威;甲醇和乙腈,色谱纯,德国MERCK;固相萃取柱(HLB,500 MG/6ML),美国WATERS;快速生物降解性试验和室内模拟试验使用的活性污泥均采自南京城东污水处理厂曝气池。
1.2 快速生物降解性试验
采用OECD的快速生物降解性试验的测压呼吸计量法[37]。通过测定密闭试验瓶中因化学品生物降解消耗O2导致的气体压力的变化,来测定快速生物降解性。该方法具有连续测量、适用性广且适用于难水溶解性和挥发性化学物质的优点。
向500 mL BOD瓶中添加297 mL无机培养基、3 mL活性污泥悬浮液 (3 g/L) 以及约9 mg PCs,使活性污泥质量浓度为30 mg/L,PCs质量浓度为30 mg/L。此外,设置不含PCs的接种空白对照,含苯胺的程序对照用于指示污泥活性。所有瓶子在22 ℃±2 ℃下密闭恒温搅拌28 d,28 d内的氧消耗通过BOD分析仪测定。PCs的生物降解率(B)按照式(1)计算。
(1)
式中:QT和QC分别为PCs和空白对照样品的氧消耗质量浓度(mg/L),ρ为受试物质量浓度(mg/L),ThOD为PCs的理论需氧量(mg/mg)。
1.3 室内模拟试验
1.3.1 系统运行
参考OECD 303A试验方法[30],将活性污泥接种于生物降解模拟系统的曝气罐中,使悬浮污泥质量浓度(MLSS)稳定在5~8 g/L(以干质量计),连续充氧驯化。用乙醇配制10 g/L的PCs混合储备液,添加到合成污水中。试验期间,含有PCs(1 mg/L)的合成污水(TOC为100 mg/L)以固定流速进入曝气罐中。按照表1运行条件,分a、b和c 3个试验阶段调节水力停留时间(HRT)以及曝气罐中的MLSS。
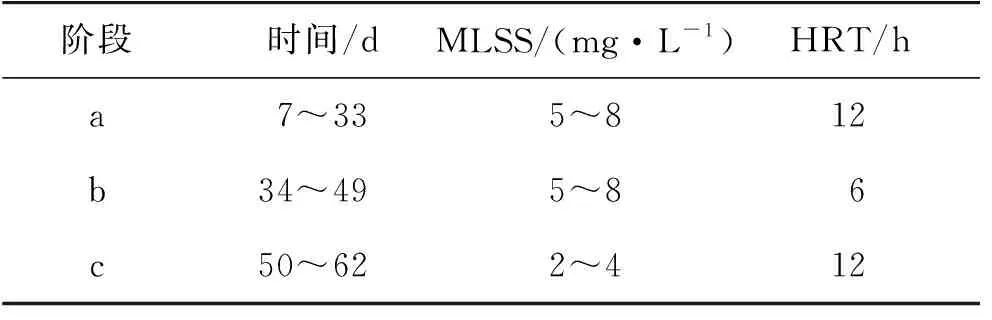
表1 模拟系统运行条件控制Table 1 Parameters setting of simulation test
1.3.2 水质参数测定
试验期间,定期测定曝气罐中活性污泥的溶解氧质量浓度、温度和pH,确保溶解氧质量浓度大于2 mg/L,温度保持在20~25 ℃,pH为7.5±0.5。
定期采集进出水样品,过0.45 μm滤膜,弃去前期5 mL滤液,进TOC分析仪测定有机碳含量。
采集100 mL曝气罐污泥悬浮液(采样前充分搅拌),8 000 r/min离心5 min后弃去上清液,将下层污泥团称质量后置于105 ℃烘箱中烘干,再次称质量,用差值法计算混合液中的MLSS。
1.3.3 PCs浓度测定
水样测定:定期采集原水或二沉池出水10 mL(采样前对进水罐和出水盛水罐充分搅拌),用甲醇稀释1倍,超声15 min,过0.22 μm滤膜,弃去前期2 mL滤液,剩余滤液进LC-MS/MS分析PCs浓度。
剩余污泥中PCs浓度分析:从二沉池开关阀处取适量污泥,混合均匀后离心分离,取5 g离心后的湿污泥,加入10 mL甲醇超声20 min,在8 000 r/min下离心5 min,收集上清液。重复两次,合并上清液,过0.22 μm滤膜,弃去前期2 mL滤液,取剩余滤液进LC-MS/MS分析PCs浓度。
1.3.4 仪器分析方法
采用电喷雾离子源(ESI)、负电离模式、多反应离子监测扫描定量分析目标物。色谱柱为ZORBAX Eclipse Plus C18(3.5 μm,2.1 mm×150 mm),进样量5 μL,18种PCs分3组进行测定。流动相条件和质谱条件参考许晶晶[38]及丁洁等[39]的研究,母离子质荷比、子离子质荷比、色谱保留时间以及分析结果见表2。

表2 酚类化学品的质谱条件和方法性能Table 2 Mass spectrometric conditions for the analysis of the target PCs and performance
由表2可得:仪器分析方法标曲线性相关系数大于0.995,线性良好,回收率为62%~115%,检出限为0.1~5.0 μg/L。
1.4 STP实测验证
从上海、广州选择6家企业的STP(基本情况见表3)采集进出水样品,使用3 L棕色玻璃瓶保存水样。用浓盐酸将水样pH调节至3以下并在4 ℃暗处保存。测定进出水样品中PCs的质量浓度。PCs去除率(R)按照式(2)计算。

表3 现场采样的STP基本情况Table 3 Conditions of STP for field tests
(2)
式中:ρi和ρe分别为进水和出水样品中PCs的质量浓度(μg/L)。
1.5 STP模型预测与分析
课题组前期开发了基于我国典型污水处理工艺和环境参数的C-STP(O)预测模型[35],该模型是基于质量守恒原理,为污染物在不同处理阶段的质量流建立了稳态方程,可有效评估化学品在污水处理阶段的暴露和归趋。C-STP(O)将初沉池、曝气池和二沉池按照水相、悬浮颗粒相、污泥相及空气相划分成9箱概念模型。模型包括输入、计算、输出过程,输入参数包括化学品固有特性(如分子量、水溶解度、吸附系数(lgKoc)或分配系数(lgKow)、蒸汽压以及快速生物降解性数据等)和环境场景参数(模型默认);模型预测可得废水经STP处理后化学品的大气挥发去除率、污泥吸附去除率和生物降解去除率。
目前欧盟和美国根据快速生物降解性及固有生物降解性测试结果,制定了外推标准以获得化学品在STP中的降解速率(k)[40]。本文中,PCs的理化数据来自OECD echemportal数据库[41],k值根据本文快速生物降解性试验结果用欧盟外推标准获得。
2 结果与讨论
2.1 PCs的快速生物降解性试验结果
18种PCs的快速生物降解性试验结果见表4,10 d观察期生物降解率达到60%即表示可快速生物降解。由表4可见:11种PCs的10 d观察期降解率>60%。此外,4-(1,1,3,3-四甲基丁基)苯酚仅发生了一定程度生物降解,28 d生物降解率为48%。其余物质28 d生物降解率均<10%,表明不可快速生物降解。四溴双酚A和五溴苯酚28 d生物降解率分别为-15%和-60%,表明在28 d试验期间,不仅没有生物降解而好氧,反而对微生物的正常呼吸作用造成了抑制,使其氧消耗量低于空白对照,导致计算的降解率为负值。这种微生物毒性效应常见于含卤素的化合物[10,42]。
由表4可得:PCs的快速生物降解性与其取代基种类、数量有关。从烷基取代基种类来看,甲基、乙基、丙基、丁基和仲丁基、庚基等烷基取代都可快速生物降解,叔丁基、叔戊基取代不可生物降解。甲基、乙基、丙基几乎没有降解停滞期,而仲丁基、庚基都有较长的停滞期。因此,取代烷基碳链越短,越容易快速生物降解。从取代的丁基结构可以看出,取代基支链越少越容易快速生物降解。取代基数量较多时也不能快速生物降解,如4-(1,1,3,3-四甲基丁基)苯酚、4-仲丁基-2,6-二叔丁基苯酚、2,4-二叔戊基苯酚。综上可得,多取代烷基或取代基团较大时,由于位阻效应降低了微生物利用度,从而抑制了生物降解作用。有研究表明微生物更易于利用邻位、对位基以及基团较小的化学品,间位基化学品由于苯环上的氢原子有较低的负电离域作用[43]而不易被作为碳源利用,因此较为稳定。
由表4还可得:从卤代数量和种类来看,单卤、双卤、三卤苯酚可快速生物降解,如4-溴苯酚、2-氟-4-溴苯酚、2,4-二溴苯酚、2,4,6-三溴苯酚,但是需要较长的停滞期(适应期),分别为10、14、20、7 d。而四溴和五溴取代的苯酚则不能快速生物降解,如四溴双酚A和五溴苯酚,这是由于卤原子吸电子能力很强,多卤取代导致微生物及其酶的亲电攻击性大大降低,微生物活性受到了抑制。类似的吸电子能力较强的取代基团还有—NO2、—Cl、—Br等[10,44]。

表4 18种PCs快速生物降解性结果Table 4 Ready biodegradation results of 18 PCs
2.2 室内模拟试验中PCs的去除
2.2.1 系统运行情况
在STP室内模拟试验中,不同阶段曝气池MLSS、二沉池出水悬浮颗粒物质量浓度(SS)以及系统TOC去除率见图1。由图1可得:阶段a和b系统平均MLSS为6.5 g/L,阶段c系统平均MLSS为3 g/L。当曝气池HRT为12 h(阶段a和c)时,二沉池出水SS在9~34 mg/L间波动,均值为20 mg/L,符合水质排放一级B标准;当HRT为6 h(阶段b)时,由于流速加快,污泥在二沉池的停留时间由原来的6 h缩短为3 h,SS显著变高,在33~55 mg/L之间,均值达40 mg/L。系统平均TOC去除率均能维持在75%~97%,去除率比较平稳。综上表明,STP室内模拟系统运行良好。
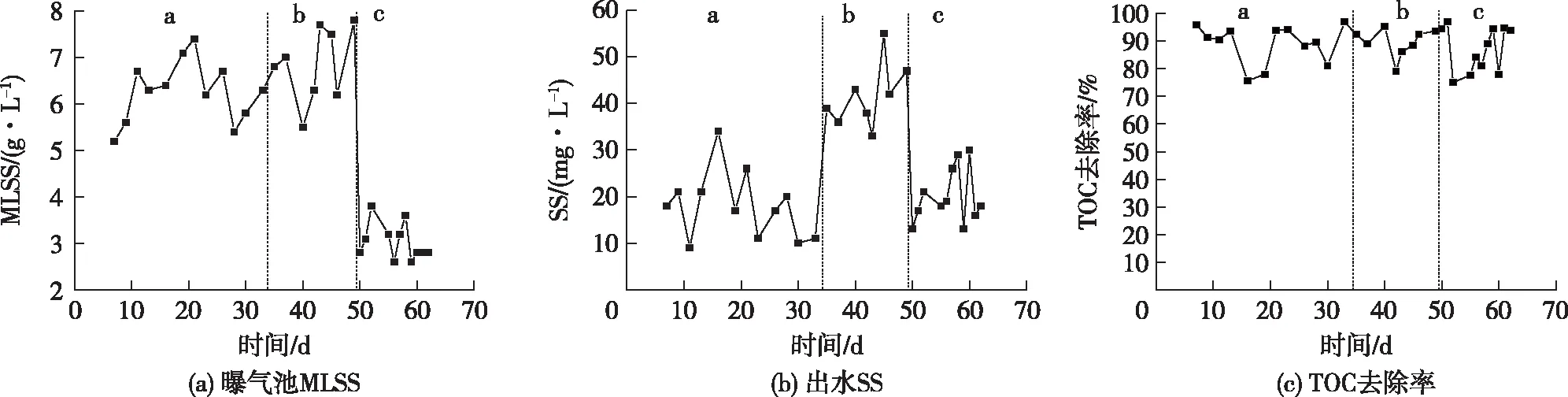
图1 STP模拟系统运行情况Fig.1 Performance of STP simulation systems
2.2.2 PCs去除率结果
试验期间,定期采集进出水样品,使用LC-MS/MS测定18种PCs的残留浓度,比较不同运行阶段PCs的去除率变化情况。图2为STP室内模拟试验中PCs去除率随时间变化曲线。
由图2可得:阶段a,只有四溴双酚A和五溴苯酚平均去除率小于70%,其余16种物质的平均去除率都大于85%。2-甲基-5-异丙基苯酚、2-氟-4-溴苯酚、4-(1,1,3,3-四甲基丁基)苯酚、2,4,6-三溴苯酚试验初期(7~15 d)的去除率逐步上升,表明这类物质在模拟系统中存在适应期,微生物对其适应后可有效去除。阶段b,HRT下调为6 h,4-异丙基苯酚、2-氨基-4-溴苯酚、2,4,6-三溴苯酚、4-丁基苯酚去除率显著降低,这4个物质的去除率在阶段c(HRT=12 h)时,又有一定程度提升。HRT影响化学品与污泥的接触时间,即生物降解接触时间,因此这类物质在模拟系统中的去除与生物降解作用紧密相关。

图2 STP室内模拟系统中的PCs去除率曲线Fig.2 Curves of PCs removal rates in STP simulation systems
试验期间,对剩余污泥中PCs检测发现,4-(1,1,3,3-四甲基丁基)苯酚、4-仲丁基-2,6-二叔丁基苯酚、四溴双酚A、五溴苯酚、2,4-二叔戊基苯酚的检出较高,对应含量分别为14~72、34~69、177~316、77~130、194~275 g/kg,对应的lgKoc分别为4.00、4.92、5.43、4.38、4.54,皆大于3.30,表明污泥中PCs浓度与lgKoc呈显著正相关性。说明这类PCs的去除不仅与生物降解有关,也与污泥吸附有关。在整个室内模拟试验期间,四溴双酚A和五溴苯酚去除率都不高,可见难生物降解的PCs在室内模拟试验中的去除以污泥吸附为主。
对快速生物降解性试验结果和STP室内模拟试验3个阶段结果进行综合分析后发现,有8种PCs可快速生物降解,在STP室内模拟系统各试验阶段去除率都能>85%,分别为4-乙基苯酚、2-甲基-5-异丙基苯酚、1-萘酚、4-仲丁基苯酚、4-n-庚基苯酚、4-溴苯酚、4-异丙基苯酚、4-丁基苯酚;有7种PCs不可快速生物降解,但其中4种在STP室内模拟系统各试验阶段去除率也较高(>90%),分别为4-仲丁基-2,6-二叔丁基苯酚、2,4-二叔戊基苯酚、4-叔丁基苯酚和4-(1,1,3,3-四甲基丁基)苯酚,另3种PCs在STP室内模拟系统各试验阶段去除率不高,且波动较大,分别为四溴双酚A(去除率为61%~71%)、五溴苯酚(去除率为25%~51%)、2-氨基-4-溴苯酚(去除率为68%~97%),表明不可快速生物降解的PCs,在STP室内模拟试验中的去除具有不确定性。2,4-二溴苯酚、2,4,6-三溴苯酚和2-氟-4-溴苯酚可快速生物降解,但在STP室内模拟系统中,HRT=6 h时去除率有限,HRT需12 h才能达到80%以上去除。
2.3 PCs在实际STP中的暴露及去除
采集上海、广州的生活污水和工业废水STP进出水样,分析PCs的暴露水平(表5)和去除率(表6)。由表5可知:五溴苯酚的检出率较低,其他PCs在STP进水中的检出率较高,大部分PCs检出率可达100%。PCs在进水和出水样品中检出质量浓度分别为未检出(ND)~13 635 ng/L和ND~289 ng/L。
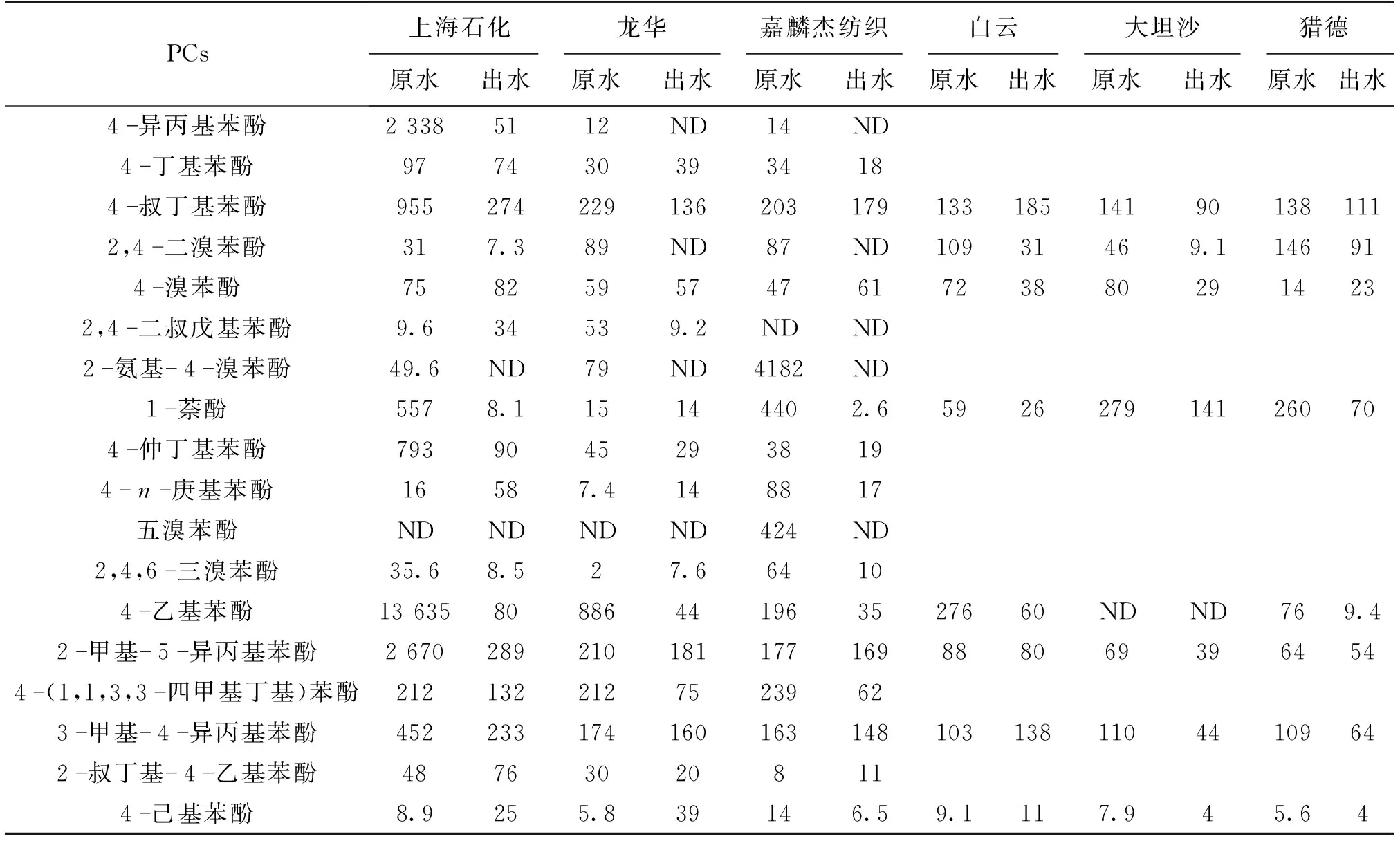
表5 STP中PCs的质量浓度Table 5 Mass concentration of PCs in sevage treatment plant ng/L
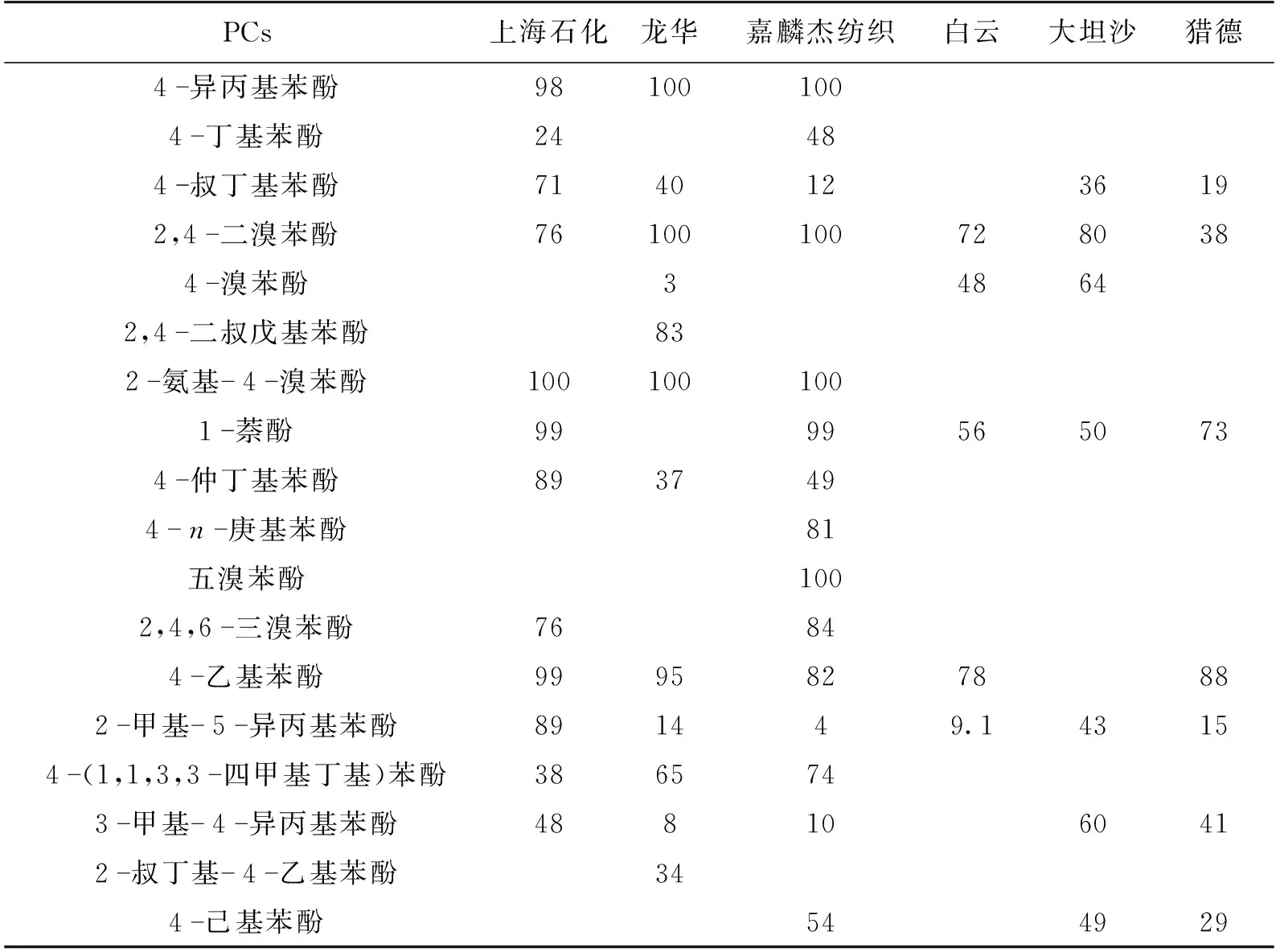
表6 STP中PCs去除率Table 6 Removal rate of PCs in sewage treatment plant %
Liu等[45]研究发现我国进水、出水以及污泥中2,4-(1,1,3,3-四甲基丁基)苯酚的含量分别为155±27 ng/L、31±7 ng/L以及196±21.3 ng/g,去除率为80%,这与本文的监测结果较为接近。
由表6可知:2-氨基-4-溴苯酚在各家STP不同处理工艺中均能完全去除,4-乙基苯酚、4-异丙基苯酚去除率皆较高,可达75%以上,与其快速生物降解性相关。2-甲基-5-异丙基苯酚、4-溴苯酚、4-丁基苯酚虽然可快速生物降解,但是STP的实际去除率却不高,分别为4%~89%、3%~64%、24%~48%,表明STP工艺、废水来源、运行条件显著影响化学品的去除率。
4-(1,1,3,3-四甲基丁基)苯酚、4-叔丁基苯酚不能快速生物降解,STP中去除率分别为38%~74%、12%~71%,去除主要由污泥吸附所致。
此外,部分化学品出水浓度高于进水浓度,显示出异常,出现该异常的PCs和异常的STP次数分别为:2,4,6-三溴苯酚(1次)、3-甲基-4-异丙基苯酚(1次)、2-叔丁基-4-乙基苯酚(2次)、4-n-庚基苯酚(2次)、4-溴苯酚(3次)、4-叔丁基苯酚(1次)、4-丁基苯酚(1次)、4-己基苯酚(3次),2,4-二叔戊基苯酚(1次)。出水浓度高于进水浓度预示着这些化学品可能是其他化学品的降解产物,如多溴苯酚经降解可能生成4-溴苯酚,Liu等[45]也观察到了类似的现象。
2.4 STP模型预测与试验结果比较
2.4.1 PCs在STP中的归趋预测
使用C-STP(O)模型预测18种PCs在不同HRT和MLSS参数下STP中的归趋,挥发、吸附和生物降解对总去除率的贡献见图3。PCs在STP中的分布同它们的理化性质有着紧密的关联,可快速生物降解的PCs可以得到较高的去除率(>70%)。四溴双酚A、4-仲丁基-2,6-二叔丁基苯酚、2,4-二叔戊基苯酚和五溴苯酚的lgKoc较高,分别为5.43、4.92、4.54和4.38,不能快速生物降解,预测结果表明这4种物质主要通过污泥吸附方式去除,去除率分别为75%、58%、53%、34%。Lu等[46]研究了加拿大不同污水处理厂中PCs等分布和归趋,结果也表明除了生物降解外,生物质吸附是PCs的主要去除机制。
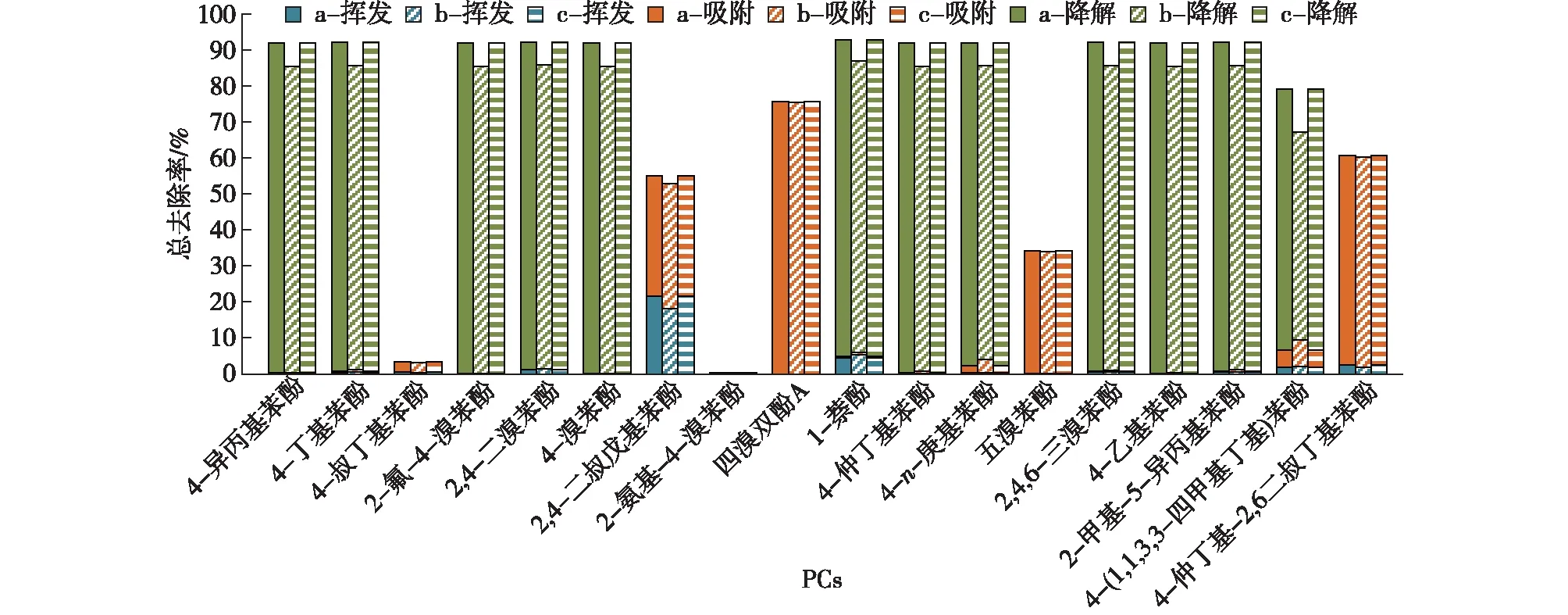
图3 C-STP(O)模型预测的PCs在STP中的归趋Fig.3 Predicted fate of PCs using C-STO(O) model
由图3可得:2,4-二叔戊基苯酚亨利常数为24.3 Pa·m3/mol,预测结果显示3个阶段该物质在曝气过程中的挥发去除率分别为22%、18%和22%,还有1-萘酚、4-(1,1,3,3-四甲基丁基)苯酚、4-仲丁基-2,6-二叔丁基苯酚也可通过挥发去除,但挥发去除贡献较小。4-叔丁基苯酚、2-氨基-4-溴苯酚由于挥发性和吸附性皆较小,且不能快速生物降解,因此去除率非常低。
总体而言,模型预测与输入的化学物质理化参数有关,其使用简单,而且可以阐明不同阶段不同归趋过程对总去除率的贡献,显示出极大的优越性。
2.4.2 不同方法得到的PCs去除率结果比较
室内模拟、STP实测和模型预测得到的PCs去除率结果见图4。由图4可以看出:总体上,室内模拟试验得到的去除率最高,且数值离散度低。这主要是因为室内模拟相对于实际STP,条件易于控制。实际STP去除率偏低,且不同STP变异性较大,主要是因为实际STP在废水来源、温度、进水中PCs含量、运行工况等因素都相差较大。因此,在风险评估中,应该考虑不同STP对化学品去除率的变异性。
C-STP(O)模型预测的大部分PCs(13个)的去除率稍低于室内模拟试验,极差小于20%,4-溴双酚A的预测去除率稍高于室内模拟试验结果,极差也保持在20%以内。4-叔丁基苯酚、2,4-二叔戊基苯酚、2-氨基-4-溴苯酚的模型预测去除率显著低于室内模拟试验和STP实测的,4-仲丁基-2,6-二叔丁基苯酚的模型预测去除率也显著低于室内模拟试验的。主要是因为上述4个物质不能快速生物降解,C-STP(O)模型预测时,使用的降解速率为0,导致其预测得到的生物降解对总去除率的贡献也为0。但是由于快速生物降解性严苛的测试条件,未达到快速生物降解通过水平,并不意味着其不能在STP中降解,而是需要开展更高层级的研究,如室内模拟试验和STP实测研究。事实上从这4个物质的结构也可以初步推断,由于不含强吸电子基团,如—F、—Cl、—NO2,不应该特别难生物降解。总体上可以认为C-STP(O)模型可以得到比较保守的预测结构,可用于筛选阶段评估化学品的环境风险。
3 结论
1)可快速生物降解性PCs在室内模拟试验中去除率较高,其中8种PCs去除率>85%;另外3种PCs(2,4-二溴苯酚、2,4,6-三溴苯酚和2-氧-4-溴苯酚)在HRT=6 h时去除率有限,在HRT=12 h时能达到80%以上。
2)不可快速生物降解的PCs,在STP室内模拟试验中去除具有不确定性。其中,4种PCs(4-仲丁基-2,6-二叔丁基苯酚、2,4-二叔戊基苯酚、4-叔丁基苯酚、4-(1,1,3,3-四甲基丁基)苯酚)在STP室内模拟试验中去除率较高(>90%);3种PCs(四溴双酚A、五溴苯酚、2-氨基-4-溴苯酚)在STP室内模拟试验中去除率不高且波动较大,为25%~97%。
3)STP模型通过预测化学品的挥发、吸附和降解去除,可以有效揭示PCs的归趋机制,能补充好氧模拟试验结果。
4)PCs在实际STP中的去除率偏低,且变异性较大,可能与废水波动性、运行工况有关,在风险评估中,应该考虑这种变异性。同时现有STP应该增加深度处理工艺,以有效去除PCs等化学品。
