镁合金与Q235钢在罐底水溶液下的电偶腐蚀行为
2021-07-15李卓远孙东旭赵志龙
李卓远,谢 飞,吴 明,孙东旭,赵志龙
(1.辽宁石油化工大学 石油天然气工程学院,辽宁 抚顺113001;2.中国石油抚顺石化公司 石油二厂,辽宁 抚顺113001)
储油罐是石油行业中的必要设施之一,超过80%的储罐事故是由储罐底板腐蚀引起的,底板腐蚀严重威胁了储罐的运行安全[1]。随着储罐防腐蚀技术的发展,储罐在一定程度上延长了使用寿命,但仍达不到预期设想[2]。储罐设计寿命长,施工成本高,维护工作复杂,因此储罐设备运行的好坏直接关系到石油化工的生产效率和安全[3]。目前对金属腐蚀的控制主要采用涂料防护和阴极保护[4]。经过多年的研究和应用,阴极保护是防止钢质储罐腐蚀最常用的方法之一,储罐罐底板的阴极保护是决定储罐运行寿命的关键技术[5]。相比其他金属,镁合金的电极电位低,利用这一特点和电化学原理,镁合金可作为牺牲阳极[6],镁合金牺牲阳极已广泛应用于石油、天然气、煤气管道和储罐等设备的腐蚀防护中[7-8]。储罐的阴极保护的标准国内外有所不同[9-10],但一般是根据国家和行业标准[11-13]进行设计和施工,其中所需镁合金的数量和与阴阳极的比例大小是根据预期的使用年限计算得到,这种根据预估保护年限确定阳极数量的设计方式会出现与现实阳极的消耗速率不相符的情况。同时阴阳极面积比也对阴极保护年限有着至关重要的影响,是影响电偶腐蚀速率的一个重要因素[14]。因此,研究镁合金与Q235钢在罐底水溶液下的电偶腐蚀行为,得到电偶腐蚀速率与阴阳极面积比的关系,有助于确定合理的牺牲阳极面积,避免资源和资金的浪费,为罐底牺牲阳极保护提供理论依据和参考。
国内外许多学者就牺牲阳极的电偶腐蚀进行了多方面的研究。H.H.Wang等[15]研究了两种不同牺牲阳极在海水中的电化学性能,判断了两种牺牲阳极的优劣。H.X.Wan等[16]采用电化学、浸泡和表面分析等方法,研究了海泥状态对AlˉZnˉInˉ MgˉTi牺牲阳极行为的影响,发现AlˉZnˉInˉ MgˉTi牺牲阳极在模拟海水中的腐蚀速率高于在模拟海泥中的腐蚀速率,并且随海泥粒径的增大,其腐蚀速率也增大。N.Zidane等[17]对含氯储罐阴极保护牺牲阳极AZ31镁合金腐蚀性能进行了评价,综合失重和电化学数据表明,随着NaCl质量浓度的增加和温度的升高,镁合金的腐蚀速率增大。Q.L.Cheng等[18]研究了Q235B碳钢在原油沉积水中的腐蚀行为,结果表明碳钢被碳酸钙为主的氧化物覆盖,在沉积水中电偶腐蚀导致局部溶解。M.Grabowski等[19]研究了AM 50镁合金在除冰盐溶液中的阴极保护,结果表明AM 50镁合金在除冰盐溶液中无法实现阴极保护,而是沿晶界发生局部溶解。虽然目前国内外学者对于阴极保护的研究已经有了一定进展,但多是针对影响电偶腐蚀的因素,对于牺牲阳极的大小、最佳的阴阳极面积比、牺牲阳极的使用寿命方面的研究却鲜有报道,在储罐阴极保护方面也少有研究,对于阴极保护系统设计的指导意义较差。
本文以Q235钢为阴极,镁合金为阳极组成电偶对,以大榭油库罐底水模拟溶液为腐蚀环境,利用失重法、电化学实验、显微形貌观察等方法,研究罐底水溶液中的Q235钢/镁合金电偶对在不同阴阳极面积比下的电偶腐蚀行为,讨论了不同阴阳极面积比对电偶腐蚀速率的影响,为储罐牺牲阳极阴极保护的设计方案、最佳阴阳极面积比提供科学的参考和理论指导。
1 实验部分
1.1 材料与介质
以大榭油库储罐钢制罐底所使用的Q235钢为阴极材料,AZ31B镁合金为牺牲阳极材料。大榭油库301罐底水中含Clˉ16 000 mg/L、341 mg/L、1 185 mg/L、198 mg/L,溶液p H为8.1[20]。实验溶液以此罐底水的模拟水溶液为介质溶液,用NaCl、MgSO4、NaHCO3、Na2CO3和去离子水配制实验室所用的罐底模拟溶液,具体离子质量浓度如表1所示。
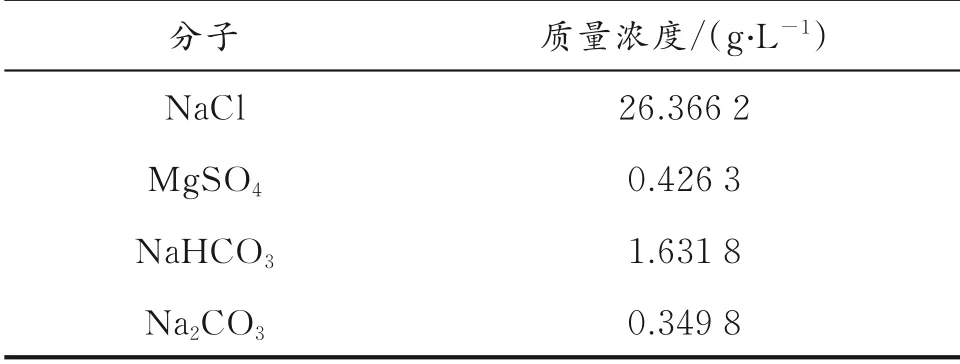
表1 模拟溶液的组成Table 1 Composition of simulated solution
1.2 浸泡实验
Sc表示Q235钢(阴极)面积,Sa表示镁合金(阳极)面积,Sc/Sa表示阴极与阳极的面积之比。
将Q235钢材料加工成尺寸大小为50 mm×25 mm×2 mm的试件,再将镁合金块分别加工成与Q235钢成一定比例的外形尺寸,Sc/Sa分别为1.0、2.0、3.0,用以进行对照实验,经过处理后逐一利用电子天平进行称重,在半小时内进行实验,并做好记录(精确到0.000 1 g),以防止外界因素影响实验结果。利用绝缘夹子将Q235钢与镁合金块紧密贴合不发生相对位移,之后将其固定在已经加工好且有足够空间的容器中,实验时间为15 d(360 h)。Q235钢与镁合金块均不能与容器壁接触,模拟溶液需浸没整个试件,在容器开口处进行密封处理,以防止空气进入到容器中,对每个容器进行标签区别记录。清洗过的镁合金块用滤纸吸去表面的水分后,放入由200 g三氧化铬(CrO3),10 g硝酸银(AgNO3),20 g硝酸钡[Ba(NO3)2]和去离子水配成的1 000 mL溶液中,放置1 min以清除剩余的腐蚀产物。用滤纸将清洗过的Q235钢表面的水分吸干,放入由500 mL密度为1.19 g/mL的盐酸、3.5 g六次甲基四胺与去离子水配制成的1 000 mL溶液中,静置10 min,观察除锈不够彻底则可适当延长静置时间[21]。将严格按要求处理后的试件放入干燥器中放置24 h后用电子天平称重并计算各试件的平均腐蚀速率,然后采用金相显微镜观察试件微观腐蚀形貌。在室温下,共进行3组平行实验,选取一组实验结果进行分析,其余实验结果用误差棒表示。
通过浸泡实验研究镁合金与Q235电偶对的腐蚀行为、阴阳极腐蚀情况,以及在不同Sc/Sa下的腐蚀速率变化情况。
利用失重法计算试件的平均腐蚀速率Vc,如式(1)所示[22]:
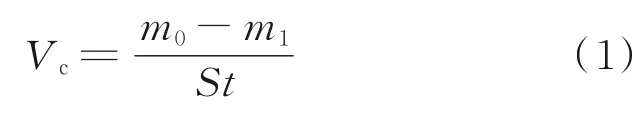
式中,m0为试件的初始质量,g;m1为试件经清除腐蚀产物后的质量,g;S为试件的表面积,m2;t为浸泡时间,d;Vc为平均腐蚀速率,g/(m2·d)。
1.3 电偶腐蚀实验
实验选取Q235钢为阴极材料,AZ31B镁合金为牺牲阳极材料,实验溶液如表1所示。将Q235钢加工成外形尺寸为1 cm×1 cm×2 mm的试件,再将镁合金块分别加工成与Q235钢成一定比例的外形尺寸,Sc/Sa分别为0.5、1.0、2.0,即未封装的试件的阳极工作面积分别为2.0、1.0、0.5 cm2,用以进行对照实验。
实验过程中采用三电极体系和PARSTAT 2273电化学工作站。其中,Q235钢为工作电极,镁合金为辅助电极,饱和甘汞电极(SCE)为参比电极。将准备好的电极与仪器的导线按要求接好,置于500 mL容量烧杯所盛的模拟溶液中(溶液未除氧),注意将3个电极正对处于同一水平面上且距离固定在3~5 cm,固定后先静置30 min,以消除扰动影响。电偶腐蚀实验电偶电流曲线测量时,设置实验时间为12 h(43 200 s),每个点间隔时间为10 s。画出相应的时间-电偶电流关系曲线,并将溶液的电偶腐蚀实验数据导出进行分析,采用金相显微镜观察试件微观腐蚀形貌。在室温下,共进行3组平行实验,选取一组实验结果进行分析,其余实验结果用误差棒表示。
通过电偶电流曲线,研究不同阴阳极面积比的电偶电流与腐蚀程度的规律。利用电偶电流,通过理论计算得到腐蚀速率,回归出腐蚀速率与阴阳极面积比的关系曲线。
腐蚀电流与腐蚀速率的相关公式为[22]:
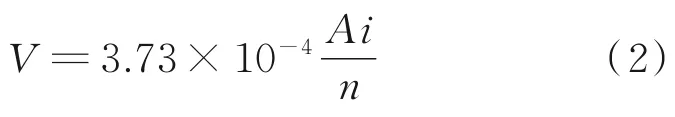
式中,V为腐蚀速率,g/(m2·h);i为腐蚀电流密度,μA/cm2;n为价数,即金属阳极反应方程式中的电子数;A为金属的相对原子质量。
2 结果与分析
2.1 浸泡实验结果
2.1.1 平均腐蚀速率 不同Sc/Sa的Q235钢/镁合金块在模拟溶液中浸泡360 h,实验前后统计的数据如表2所示。
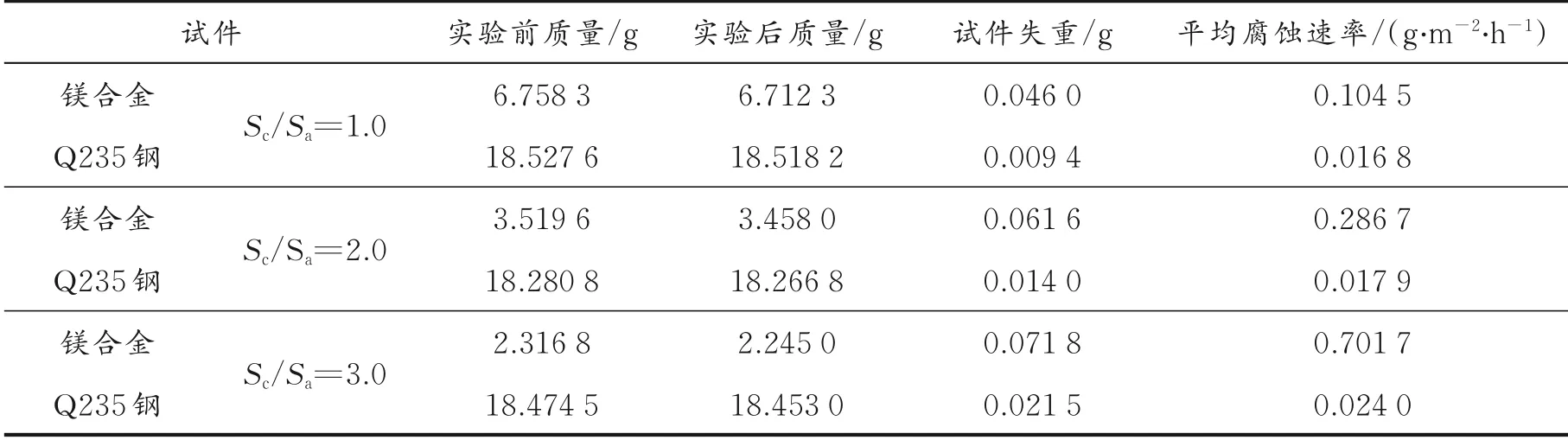
表2 各组试件实验前后数据统计Table 2 Data statistics of each gr oup befor e and after the experiment
由表2数据可以看出,镁合金和Q235钢都发生了腐蚀,二者均有失重。每一组镁块所损失的重量高于该组Q235钢所损失的重量,这表明镁合金所发生的腐蚀要比Q235钢严重。相同Sc/Sa时阴阳极的平均腐蚀速率也反应了阴阳极腐蚀情况的不同,二者的腐蚀速率相差很大,阳极腐蚀情况严重,Q235钢几乎未受到腐蚀,这种平均腐蚀速率的差距在Sc/Sa为3.0时最大,镁合金的腐蚀速率达到了0.701 7 g/(m2·h),而Q235钢只有0.024 0 g/(m2·h)。所以Q235与镁合金组成的电偶对会发生明显的电偶腐蚀,镁合金遭到严重腐蚀而Q235钢则腐蚀轻微,这是由于添加了镁合金后,镁合金相较于Q235钢有更低的电位,镁合金作为阳极被消耗,而Q235钢作为阴极被保护。实验结果验证了牺牲阳极的阴极保护是有效的。
图1为不同Sc/Sa下镁合金与Q235钢的平均腐蚀速率柱状图。由图1可以看出,不同的Sc/Sa,阴极、阳极的平均腐蚀速率是不同的。对镁合金而言,当Sc/Sa为1.0时,镁合金的平均腐蚀速率为0.104 5 g/(m2·h),当Sc/Sa为3.0时,镁合金的平均腐蚀速率达到了0.701 7 g/(m2·h)。镁合金的腐蚀速率随着Sc/Sa的增大而增大,且增加幅度明显。反观Q235钢,在Sc/Sa为1.0时平均腐蚀速率为0.016 8 g/(m2·h),Sc/Sa为3.0时为0.024 0 g/(m2·h),相较于镁合金来说增长幅度很小。虽然随着Sc/Sa的增大,无论是Q235钢还是镁合金块的失重均逐渐增加,但随着Sc/Sa的增大,镁合金块的平均腐蚀速率的增长速度要远大于Q235钢的平均腐蚀速率。总体来看,镁合金的平均腐蚀速率随着Sc/Sa的增大而明显增大,而Q235钢的腐蚀速率则增长较小,说明阴阳极面积比的增加更多地影响了阳极的腐蚀情况,加剧了阳极的腐蚀,使阳极溶解速度加快,相较于阳极来说,阴极还是处于被保护的状态。
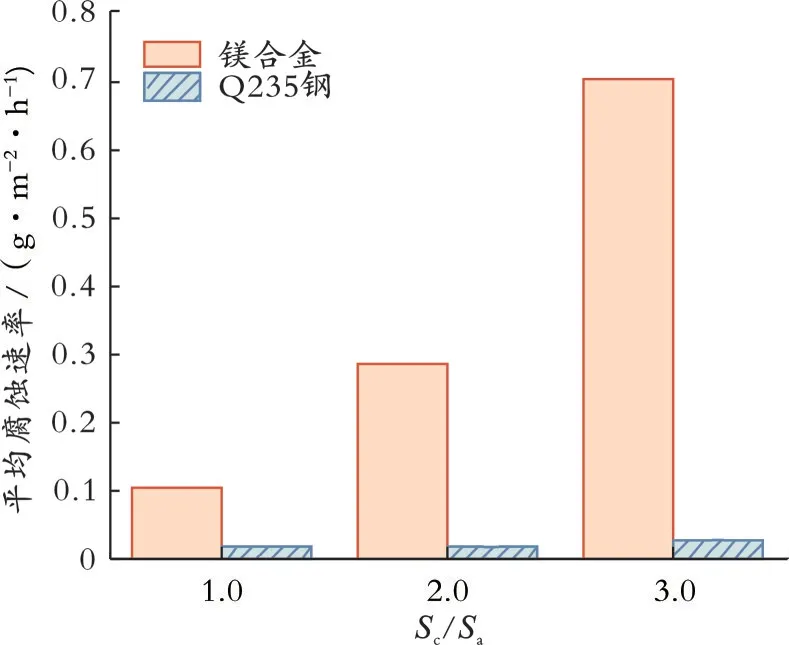
图1 不同S c/S a的镁合金与Q235钢平均腐蚀速率柱状图Fig.1 Histogram of average corrosion rate of magnesium alloy and Q235 steel with different S c/S a
2.1.2 微观腐蚀形貌 不同Sc/Sa的Q235钢/镁合金块在模拟溶液中浸泡后,镁合金块、Q235钢的微观腐蚀形貌分别如图2所示。由图2可知,当Sc/Sa为1.0时,镁合金块腐蚀轻微,试件表面仅有少量点蚀坑,能看到大部分裸露的基体;当Sc/Sa为2.0时,腐蚀与未腐蚀的部分面积基本相等;而当Sc/Sa为3.0时,几乎看不见裸露的基体部分,基体被大片的点蚀坑腐蚀,表面被大量的腐蚀产物覆盖。相较于Sc/Sa=2.0而言,Sc/Sa为3.0的腐蚀情况明显加重。由此可知,随着Sc/Sa的增大,镁合金块试件表面腐蚀状况由局部腐蚀形成的点蚀变成全面腐蚀,镁合金块试件的裸露可视基体的面积越来越少。

图2 浸泡实验中不同S c/S a的镁合金与Q235钢的微观腐蚀形貌Fig.2 Micro corrosion morphology of magnesium alloy and Q235 steel with different S c/S a in immersion experiment
当Sc/Sa为1.0时,Q235钢试件表面基本未发生腐蚀,试样表面机加工痕迹清晰可见,仅有零星点蚀坑;当Sc/Sa为2.0时,机加工痕迹依旧存在,但变得不太清晰,腐蚀渐渐变得严重,看到更多点蚀坑出现;当Sc/Sa为3.0时,腐蚀程度已经很严重,看不见加工痕迹的存在,点蚀坑非常密集,点蚀坑直径变大,基体表面已经全部被腐蚀。随着Sc/Sa的增大,Q235钢试件表面的点蚀坑越来越多,越来越密集;点蚀坑的直径越来越大。
Q235钢自身存在自腐蚀,所以尽管有镁合金作为牺牲阳极对其进行保护,但Q235表面还是会由于自腐蚀作用的影响而发生腐蚀。相较于镁合金来说,Q235钢的腐蚀不明显,镁合金块基体已经被严重腐蚀,腐蚀产物布满整个表面。可见,当Q235钢与镁合金组成电偶对时,会有明显的腐蚀发生,且相较于阴极来说阳极的腐蚀发生得更为剧烈、更加严重。作为阴极的Q235钢,未发生明显的腐蚀,处于被保护的状态,随着Sc/Sa的增大,阳极腐蚀加重且在Sc/Sa=3.0时最为严重。
2.2 电偶腐蚀实验结果
2.2.1 电偶电流曲线 采用三电极体系测试并绘制了不同Sc/Sa的Q235钢/镁合金电偶对在模拟溶液中偶接时发生电偶腐蚀时的电偶电流随时间变化的曲线,电偶电流的大小可以反映金属的腐蚀情况[23-26]。依据牺牲阳极与Q235钢偶合后的电极动力学,电偶电流Ig为阳极主导时牺牲阳极实际流出的电流量,即电偶电流的大小可以表示由电偶效应引起的腐蚀速度的大小。图3为不同Sc/Sa的Q235钢/镁合金电偶对在模拟溶液中的电偶电流。由图3可知,不同Sc/Sa的Q235钢/镁合金电偶对的电偶电流随时间变化呈下降的趋势,并且曲线振荡频率及幅度比较大。一方面是因为Q235钢/镁合金电偶对的表面状态不断发生变化,从而造成电偶电流的波动;另一方面是因为Q235钢/镁合金电偶对的表面在溶液中形成的腐蚀产物膜被破坏,文献[27ˉ29]认为腐蚀产物膜膜层破坏是由于腐蚀产物膜膜层不稳定,容易产生点蚀,之后腐蚀产物膜进行自我修复或者再次生成,所以出现腐蚀产物膜形成、破坏、再形成的反复过程,从而引起电偶电流的波动。
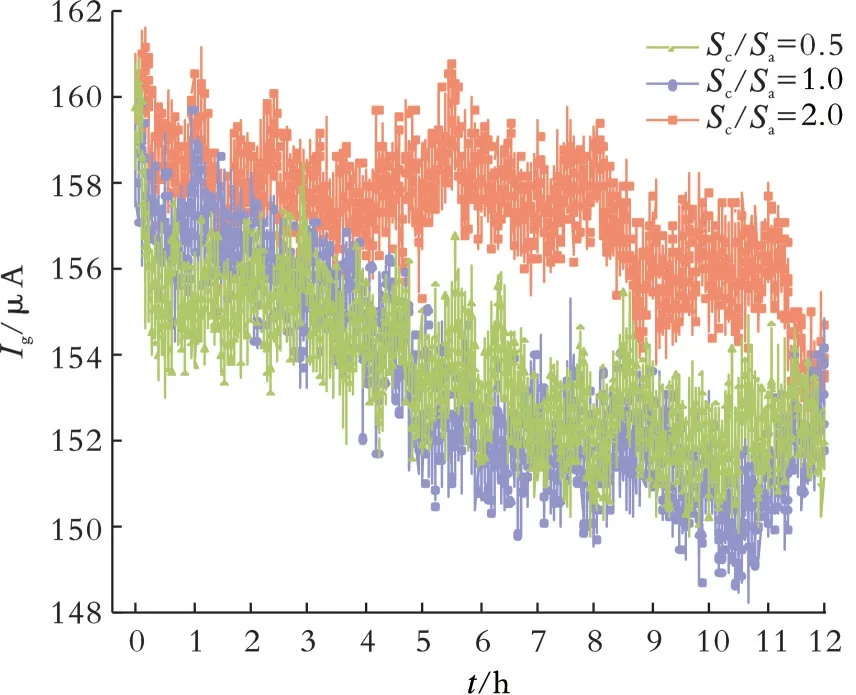
图3 不同S c/S a的Q235钢/镁合金块电偶对在模拟溶液中的电偶电流Fig.3 Galvanic curr ent of Q235 steel magnesium alloy block couple with different S c/S a in simulated solution
由图3可以看出,当Sc/Sa为0.5时,电偶电流从161μA左右快速下降到153μA左右,在t为3.0 h前曲线虽稍有降低但整体平稳,在t为3.0 h之后曲线下降趋势增大,从152μA左右降到150μA左右,在t为8.0 h之后曲线变得平稳。发生这种变化的原因:在腐蚀刚开始,发生腐蚀速率较大的点蚀;之后曲线下降是腐蚀产物膜的形成减缓了腐蚀的进行,所以电偶电流降低;最后由点蚀转为平稳的均匀腐蚀,曲线也转为平稳。Sc/Sa为1.0时曲线的总体趋势与Sc/Sa为0.5时相似,在t为4.0~6.0 h时,电偶电流下降的速度要大于Sc/Sa为0.5时的下降速度,在t为11.6 h时电偶电流达到最低148μA左右。Sc/Sa为2.0时电偶电流相较于另外两个面积比时的电偶电流有明显的增大,整条曲线均在其余两条曲线的上方,Sc/Sa为2.0时曲线总体较为平稳,在t为8.0~9.0 h有一个短时间的快速降低,但Sc/Sa为2.0时的曲线要比其余两个曲线平稳许多,电偶电流也没有明显的降低。在Sc/Sa为2.0时,电偶电流值最大,此时腐蚀程度最严重。
另一方面可以看出,当Sc/Sa由2.0变为1.0时,电偶电流的减小较为明显。当Sc/Sa为0.5时电偶电流的减小基本与Sc/Sa为1.0时一致,即增大牺牲阳极面积有助于降低阴极的腐蚀程度。由图3还可以看出,即使阳极面积增大,即Sc/Sa由1.0变为0.5,但对阴极的保护作用的提升并不是很明显,可知增加阳极面积对于增强阴极保护的效果是不合理的。在实际工程应用中,可以通过了解Sc/Sa和腐蚀速率之间的规律找到一个合适的牺牲阳极大小,而不是单纯地加大阳极面积来增强阴极保护的效果。
2.2.2 微观腐蚀形貌 不同Sc/Sa的Q235钢/镁合金电偶对在模拟溶液中电偶腐蚀实验后的微观腐蚀形貌如图4所示。

图4 电化学实验中不同S c/S a的镁合金与Q235钢的微观腐蚀形貌Fig.4 Micro corrosion morphology of magnesium alloy and Q235 steel with different S c/S a in electrochemical experiments
在图4中,当Sc/Sa为0.5时,镁合金块试件表面仍能观察到大部分未被腐蚀的基体表面,发生了小块的局部腐蚀,腐蚀程度很轻微;当Sc/Sa为1.0时,镁合金块表面点蚀坑连接成片,蚀坑的直径和深度都有所增加。当Sc/Sa为2.0时,能观察到试件表面发生了全面的腐蚀,腐蚀程度非常严重,表面能看到腐蚀产物的覆盖以及明显的深度点蚀坑。
相对于镁合金块的腐蚀情况,Q235钢的腐蚀情况要轻微。镁合金作为添加的保护金属,有更低的电位。相比于Q235,镁合金作为保护的金属构件的阳极,利用其容易失电子的特性,保护Q235不失去电子被氧化,达到保护Q235的作用。镁合金在Sc/Sa为1.0时,镁合金块已经发生较严重的腐蚀,Q235钢的点蚀坑虽然比较密集,但并未成片出现。当Sc/Sa为2.0时,Q235钢的腐蚀情况比较严重,出现大量蚀坑,蚀坑深度和直径明显增大,但总体来说作为阴极的Q235钢腐蚀不明显。
通过观察微观形貌,可以看到作为阳极的镁合金被严重腐蚀,作为阴极的Q235钢被保护,同时随着Sc/Sa的增大,镁合金的腐蚀程度加重,在Sc/Sa为2.0时,腐蚀产物已经遍布整个合金表面,腐蚀情况十分严重。
2.2.3 平均腐蚀速率 根据电偶腐蚀实验得到电偶电流,可以计算得到阳极的平均腐蚀速率,并用其来验证浸泡实验得到的平均腐蚀速率的准确性。计算得到的阳极平均腐蚀速率如表3所示。由表3可知,通过电偶电流计算得到的平均腐蚀速率同样随着Sc/Sa的增大而增大。当Sc/Sa为0.5时,腐蚀速率最小,为0.344 3 g/(m2·h),腐蚀速率随着Sc/Sa的增大逐渐增大,在Sc/Sa为2.0时达到最大值,为1.410 3 g/(m2·h)。电偶电流计算得到的腐蚀速率结果和浸泡实验得出的结果虽然在数值上有一定的误差[30-35],但在不同Sc/Sa对腐蚀速率影响的趋势和规律上有着良好的一致性。

表3 不同S c/S a下电化学计算得到的平均腐蚀速率Table 3 Average corrosion rate calculated by electrochemical method under differ ent Sc/Sa
为进一步探究Sc/Sa对Q235钢/镁合金电偶对在罐底水溶液下腐蚀的影响,探明Sc/Sa与腐蚀速率的关系,将表3中的数据进行拟合得到直线,方程为Y=0.711 88ˉ0.016 06(Sc/Sa),拟 合 方 程R2=0.999 68,接近于1,P=0.008 03(<0.05),因此拟合方程总体拟合效果较好(见图5)。3个数据点基本都在拟合出的直线上,说明该方程可以很好地反映出Sc/Sa和腐蚀速率的线性规律变化。图5表明,Sc/Sa与腐蚀速率呈线性关系,随着Sc/Sa的增大,腐蚀速率也逐渐增大,进一步证实了浸泡实验所得到的不同Sc/Sa下的腐蚀规律的正确性以及电偶电流反映出的不同Sc/Sa对腐蚀程度的影响规律的正确性。

图5 不同S c/S a对平均腐蚀速率的影响Fig.5 Effect of different S c/S a on average corrosion rate
通过所得到的线性规律,可以确定腐蚀速率和阴阳极面积比的关系,在储罐的设计中可以根据设计参数,通过线性方程计算得到合适的阴阳极面积比,从而得到合适的牺牲阳极的合理使用面积。
3 结 论
(1)Q235钢与镁合金块组成的电偶对在大榭油库罐底水模拟溶液中有明显的电偶腐蚀发生。作为阳极的镁合金腐蚀严重,Q235钢作为阴极受到保护,腐蚀并不明显。得到了不同Sc/Sa对镁合金、Q235钢电偶腐蚀的影响规律,即阳极的腐蚀速率随Sc/Sa的增大而增大。
(2)电偶电流曲线反应出的腐蚀程度随Sc/Sa的变化规律与浸泡实验一致,随着Sc/Sa的增大,电偶电流增大,腐蚀程度加重。Sc/Sa为0.5时,腐蚀电流较大,电偶电流无明显下降。Sc/Sa为1.0、2.0时,腐蚀电流较小,电偶电流下降明显。电偶电流计算得到腐蚀速率的规律与电偶电流和浸泡实验的规律一致。利用计算得到的结果拟合出不同Sc/Sa对腐蚀速率的关系图,可知腐蚀速率随着Sc/Sa的增大呈线性增长趋势,并得到了相应的拟合方程。
