臭氧催化氧化去除煤化工高盐废水难降解有机物工艺研究
2021-07-14王吉坤陈贵锋李文博何毅聪
王吉坤,陈贵锋,李 阳,刘 敏,李文博,何毅聪
(1.煤炭科学技术研究院有限公司,北京100013;2.煤炭资源高效开采与洁净利用国家重点实验室,北京100013)
煤化工废水“零排放”过程中,会产生大量高盐废水,废水成分复杂、色度大、化学需氧量(COD)及溶解性总固体(T D S)高,其中COD达100 mg/L~5 000 mg/L,TDS达10 000 mg/L~200 000 mg/L[1-2]。高盐废水中有机物易导致“零排放”过程中膜的污堵、蒸发结晶盐品质差、杂盐率高等问题[3],因此必须有效去除煤化工高盐废水中的有机污染物,降低其对后续系统的影响,保证膜及蒸发结晶单元的正常运转。
去除废水中难降解有机物的方法有生物法[4]、电解法[5]、化学氧化法[6-7]及高级氧化法[8]等。其中生物法、电解法及化学氧化法在去除废水中难降解有机物的同时会产生二次污染;而高级氧化法是通过产生羟基自由基(·OH)的方式,氧化去除水中难降解有机污染物,且不会产生二次污染。高级氧化法包括紫外芬顿氧化法、化学芬顿氧化法、光催化氧化法及臭氧催化氧化法等,其中臭氧催化氧化法利用臭氧在催化剂作用下产生的高活性·OH与难降解有机污染物快速反应,高效去除难降解物质,具有操作简单、氧化效率高的优点[9]。臭氧催化氧化法的核心为臭氧催化剂,高效的臭氧催化氧化剂可提高生成·OH的速率,进而提高难降解有机物的去除率。
Y.Z.P I等[10]以C uO/A l2O3为臭氧催化剂氧化降解草酸溶液,与纯臭氧氧化相比,其对总有机碳(T O C)的去除率提高了30%;陈炜彧等[11]以Fe2O3为活性组分制备臭氧催化剂降解煤化工废水,研究了不同工艺条件对COD去除率的影响;R.R OS A L等[12]以MnO2/A l2O3为臭氧催化剂氧化降解非诺贝酸,其中·OH产生速率是单独臭氧氧化时的8倍;陈志伟等[13]以MnO2/陶粒为臭氧催化剂氧化降解废水,COD去除率达40%。上述研究表明,臭氧催化氧化技术对废水中难降解有机物具有良好的去除效果,但关于其在煤化工高盐废水难降解有机物的去除方面仍缺乏探索。
为探索臭氧催化氧化法降解煤化工高盐废水有机物的规律,本文采用浸渍-焙烧法制备催化剂,研究载体[14]、活性组分对COD去除率的影响,优选出最佳臭氧催化剂;并以某煤化工企业高盐废水为实验水样,探讨不同工艺参数(有无催化剂、臭氧通气量、臭氧浓度、催化剂投加量)对COD去除率的影响,确定最佳工艺条件;最后探讨臭氧催化氧化反应的动力学,确定反应速率常数,以期为臭氧催化氧化技术在煤化工高盐废水中的广泛应用提供技术参考和借鉴。
1 实验材料与方法
1.1 主要仪器、试剂和原料
仪器:臭氧发生器、蠕动泵、反应柱、COD测定仪、pH计、分析天平等。
试剂:活性氧化铝、陶粒、COD测定专用试剂(连华科技)、硝酸锰(分析纯)、硝酸铁(分析纯)。
活性氧化铝、陶粒均为济南汇锦川商贸有限公司生产,其物性参数分别见表1、表2。实验水采用内蒙古某煤化工企业高盐废水,水质指标分析见表3。

表1 活性氧化铝的物性参数

表2 陶粒的物性参数
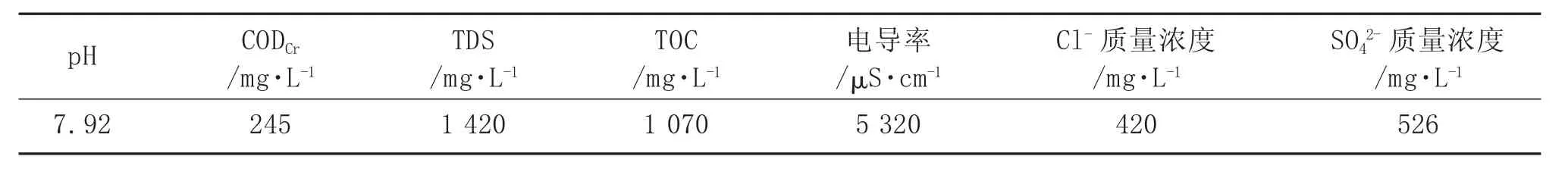
表3 高盐废水水质指标分析
1.2 催化剂制备流程
采用等体积浸渍的方式,将100 mL活性氧化铝分别浸渍至硝酸铁(浓度1 mol/L、体积100 mL)、硝酸锰(浓度1 mol/L、体积100 mL)和二者混合物(硝酸铁溶液浓度1 mol/L、体积50 mL,硝酸锰溶液浓度1 mol/L、体积50 mL)的3种溶液中,室温下在恒温振荡器内以150 r/min的速度振荡24 h,使其完全混匀,过滤后将活性氧化铝置于恒温烘干箱(105℃)中干燥12 h,再将其置于马弗炉内进行焙烧,采用程序升温方式升温:以3℃/min的升温速率由室温升至150℃,恒温30 min,随后以3℃/min的升温速率升至300℃,恒温30 min,再以3℃/min的升温速率升至550℃,恒温2 h,随后自然降至室温。焙烧后的催化剂分别为铁基、锰基和铁锰基活性氧化铝基催化剂。将催化剂制备过程中的活性氧化铝换成陶粒基,其他步骤相同,制备出含不同活性组分的陶粒基催化剂。
1.3 实验装置及处理流程
煤化工高盐废水脱除难降解有机物采用的臭氧催化氧化实验装置示意图如图1所示。废水中有机物在有机玻璃反应柱(尺寸为Φ40 mm×1 200 mm)中降解,煤化工高盐废水为实际水样,空气为臭氧发生器提供氧气源,臭氧从反应柱的底部进入,经曝气盘与臭氧催化剂接触生成·OH,并快速降解废水中的难降解有机物。未反应的臭氧经尾气出口排出,采用臭氧气体浓度检测仪检测臭氧浓度,采用循环水泵实现水样的循环处理。定时从出水口取样并分析COD含量。
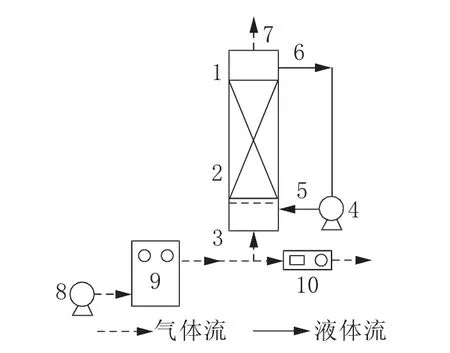
图1 臭氧催化氧化实验装置示意图
2 结果与讨论
2.1 最佳臭氧催化剂的选择
2.1.1 最佳活性组分的选择
采用制备的3种不同活性组分的活性氧化铝基催化剂在相同条件下分别开展臭氧催化氧化实验。实验条件:臭氧质量浓度200 mg/L,废水处理量2 L/h,催化剂投加量0.8 L/L,臭氧通气量1.5 m3/h,实验进行60 min后取样并分析COD含量。实验结果如图2所示。
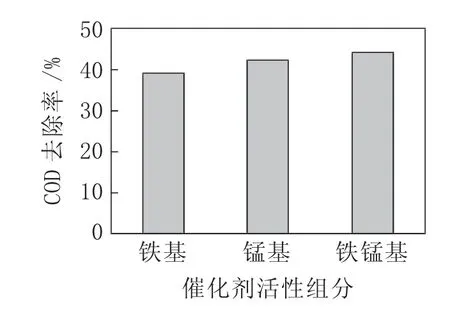
图2 催化剂活性组分对COD去除率的影响
由图2可看出,活性组分对COD的去除率影响较大,COD去除率由大到小时催化剂的活性组分依次为铁锰基、锰基、铁基,分析其原因为:锰、铁活性组分存在多种价态,金属氧化物价态变化所转移的电子能有效促进臭氧分解产生·OH,进而降解水中有机物。
2.1.2 最佳载体的选择
采用铁基活性氧化铝基催化剂、铁基陶粒基催化剂在相同条件下分别开展臭氧催化氧化实验。实验条件:臭氧质量浓度200 mg/L,废水处理量2 L/h,催化剂投加量0.8 L/L,臭氧通气量1.5 m3/h,实验进行60 min后取样并分析COD含量。实验结果如图3所示。
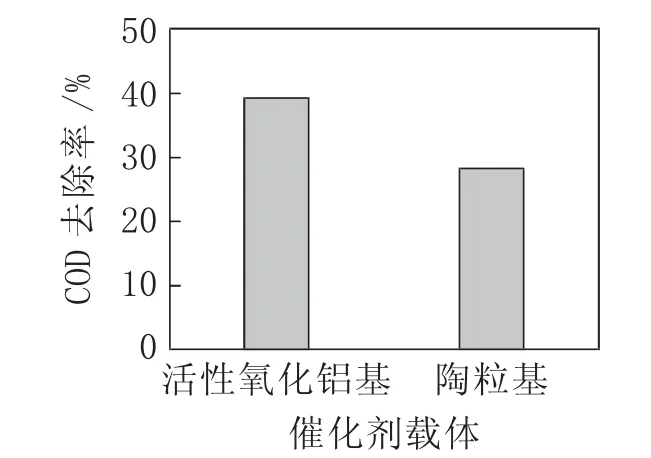
图3 催化剂载体类型对COD去除率的影响
由图3可看出,载体对COD的去除率影响较大,COD去除率由大到小时采用的载体依次为活性氧化铝、陶粒,分析原因为活性氧化铝的比表面积远大于陶粒,使得活性组分可以均匀充分地负载于活性氧化铝载体表面,从而提高了·OH的生成速率,进而促进水中有机物的降解。
综合活性组分及载体对COD去除率的考察,确定最佳臭氧催化剂为:活性氧化铝负载铁锰双组分氧化物的催化剂。
2.2 工艺条件对COD去除率的影响研究
对优选出的最佳催化剂采用单因素实验法开展臭氧催化氧化实验。分别在实验进行0、30 min、60 min、90 min、120 min、150 min、180 min时取样,水样经0.45μm膜过滤后分析COD含量,计算COD去除率。影响COD去除率的实验因素有:有无臭氧催化剂、臭氧通气量、催化剂投加量和臭氧浓度。
2.2.1 有无臭氧催化剂对COD去除率的影响
实验条件:臭氧质量浓度200 mg/L,废水处理量2 L/h,催化剂投加量分别为0、0.8 L/L,臭氧通气量1.5 m3/h,定时取样分析COD含量,结果如图4所示。
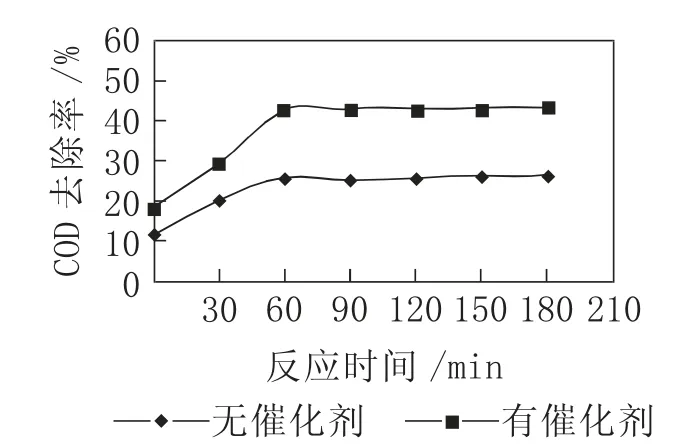
图4 有无催化剂对COD去除率的影响
由图4可看出,有无催化剂对COD去除率影响较大,在反应60 min后,COD去除率基本不再增加,此时,加入催化剂的COD去除率比未加入催化剂的COD去除率高15个百分点,分析原因为在催化剂的作用下,臭氧产生·OH的速率远高于无催化剂时的速率,从而可以更加高效地降解水中有机物。
2.2.2 臭氧通气量对COD去除率的影响
实验条件:臭氧质量浓度200 mg/L,废水处理量2 L/h,催化剂投加量0.8 L/L,臭氧通气量0.5 m3/h~2.0 m3/h,定时取样分析COD含量,结果如图5所示。
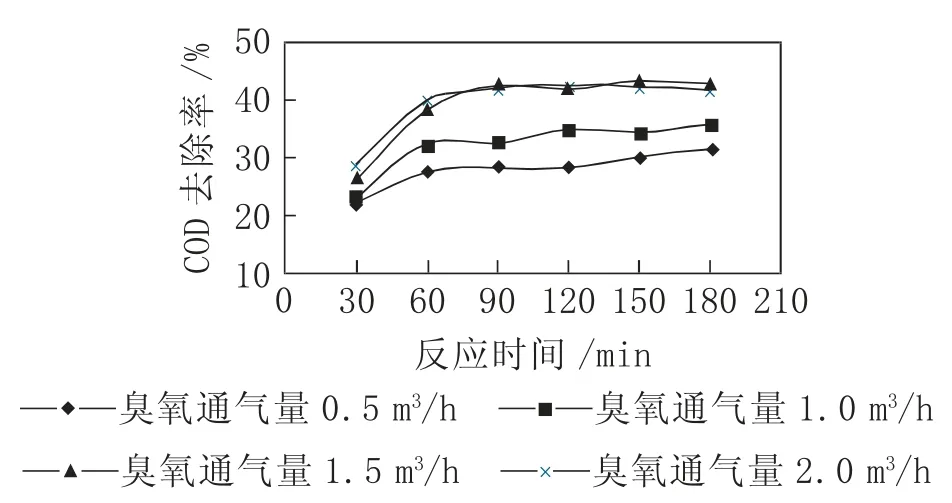
图5 臭氧通气量对COD去除率的影响
由图5可看出,臭氧通气量对COD去除率的影响显著,臭氧通气量越大,COD去除率越高,这是因为臭氧通气量越大,·OH产生量越多,进而可以更加快速地去除难降解有机物,提高COD去除率。在反应时间为180 min时,臭氧通气量分别为0.5 m3/h、1.0 m3/h、1.5 m3/h、2.0 m3/h时对应的COD去除率分别为31.5%、35.9%、42.2%、42.3%。考虑COD去除率及臭氧通气量成本,臭氧通气量选择1.5 m3/h。
2.2.3 臭氧浓度对COD去除率的影响
实验条件:废水处理量2 L/h,催化剂投加量0.8 L/L,臭氧通气量1.5 m3/h,臭氧质量浓度100 mg/L~300 mg/L,定时取样分析COD含量,结果如图6所示。
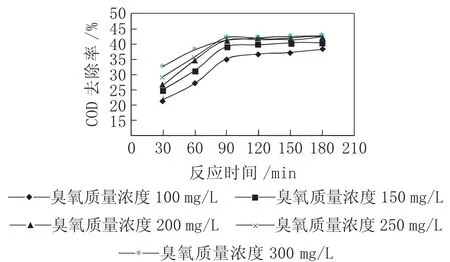
图6 臭氧浓度对COD去除率的影响
由图6可知,臭氧浓度对COD去除率影响显著,臭氧浓度越高,COD去除率越高,这是因为臭氧浓度越大,·OH生成量越多,进而可以更加快速地去除难降解有机物,提高COD去除率。在反应时间为180 min时,臭氧质量浓度分别为100 mg/L、150 mg/L、200 mg/L、250 mg/L、300 mg/L时对应的COD去除率分别为38.3%、40.5%、42.1%、42.5%、42.2%。考虑COD去除率及臭氧浓度成本,臭氧质量浓度选择200 mg/L。
2.2.4 催化剂投加量对COD去除率的影响
实验条件:臭氧质量浓度200 mg/L,废水处理量2 L/h,臭氧通气量1.5 m3/h,催化剂投加量0.5 L/L~1.0 L/L,定时取样分析COD含量。
由实验数据可知,催化剂投加量越大,COD去除率越高。这是因为催化剂投加量增加,催化活性位点数增加,·OH生成速率加快,进而可以更加快速地去除难降解有机物,提高COD去除率。在反应时间为180 min时,催化剂投加量分别为0.5 L/L、0.6 L/L、0.7 L/L、0.8 L/L、0.9 L/L、1.0 L/L时对应的COD去除率分别为29.5%、36.2%、40.7%、42.4%、42.6%、42.2%。考虑COD去除率及催化剂成本,催化剂投加量选择0.8 L/L。
2.3 臭氧催化氧化反应动力学研究
根据文献调研发现[15-16],臭氧催化氧化有机物的过程模型为一级动力学模型,因此通过反应动力学模型可计算不同臭氧催化剂降解有机物的反应速率。反应速率方程式见式(1)。

式中:C0为COD初始浓度,mg/L;C为反应一定时间后COD浓度,mg/L;k为反应速率常数;t为反应时间,min。
铁锰基陶粒基催化剂、铁锰基活性氧化铝基催化剂的一级反应动力学曲线模型如图7所示。由图7可知,陶粒基催化剂的反应速率常数为0.003 5(动力学方程为:y=0.003 5x,R2=0.662 7),活性氧化铝基催化剂的反应速率常数为0.004 1(动力学方程为:y=0.004 1x+0.245 5,R2=0.953 8),纯臭氧氧化(无催化剂)的反应速率常数为0.001 4(动力学方程为:y=0.001 4x+0.074 5,R2=0.983 4),其中陶粒基催化剂的反应速率常数是纯臭氧氧化的2.50倍,活性氧化铝基催化剂的反应速率常数是纯臭氧氧化的2.93倍。由反应动力学模型的拟合结果可知,臭氧催化氧化可有效提高降解有机物的反应速率,并提高COD去除率。

图7 不同臭氧催化氧化下的有机物反应速率常数
3 结 论
3.1 活性氧化铝基催化剂的催化效率高于陶粒基催化剂,铁锰基催化剂的催化效率高于铁基和锰基催化剂。最终选择的催化剂以活性氧化铝为载体,铁锰双组分为活性组分。
3.2 有催化剂时对COD的去除率比无催化剂时的高15个百分点;臭氧通气量越大、臭氧浓度越高、催化剂投加量越大,COD去除率越高;考虑COD去除率及运行成本,取最佳的臭氧催化氧化反应条件为:臭氧通气量1.5 m3/h,臭氧质量浓度200 mg/L,催化剂投加量0.8 L/L。
3.3 添加铁锰基陶粒基催化剂的反应速率常数是纯臭氧氧化的2.50倍,添加铁锰基活性氧化铝基催化剂的反应速率常数是纯臭氧氧化的2.93倍,即臭氧催化氧化可有效提高难降解有机物的反应速率,并提高COD去除率。
