PMP柱前衍生化-HPLC法分析不同生长年限黄芪中6种单糖的含量
2021-07-12余亦婷皮文霞谢辉曹丽娟李西文李霞陆兔林严国俊
余亦婷 皮文霞 谢辉 曹丽娟 李西文 李霞 陆兔林 严国俊


摘 要 目的:分析并比较不同生长年限黄芪中6种单糖的含量。方法:取来自3个产地的2~4年生黄芪药材,经水提醇沉、Sevage除蛋白后制得黄芪多糖;将上述多糖经三氟乙酸水解和1-苯基-3-甲基-5-吡唑啉酮衍生化后,采用高效液相色谱法测定其中甘露糖、鼠李糖、半乳糖醛酸、葡萄糖、半乳糖、阿拉伯糖等6种单糖的含量。以Symmetry C18为色谱柱,以磷酸盐缓冲液(pH 6.8)-乙腈(84 ∶ 16,V/V)为流动相,流速为1.0 mL/min,检测波长为245 nm,柱温为35 ℃,进样量为20 ?L。结果:黄芪多糖中甘露糖、鼠李糖、半乳糖醛酸、葡萄糖、半乳糖、阿拉伯糖的含量分别为0.50~0.94、0.76~1.60、3.35~7.86、87.33~275.77、1.95~8.96、2.35~14.04 mg/g,2、3、4年生黄芪中上述单糖的总含量分别为98.26~139.92、173.81~295.71、122.37~182.41 mg/g。3年生黄芪中葡萄糖的含量与2、4年生黄芪有显著差异(162.71~275.77 mg/g vs. 87.33~107.70、111.54~167.26 mg/g,P<0.05)。结论:2、3、4年生黄芪中均检出上述6种单糖,其中葡萄糖含量最高,且3年生黄芪中葡萄糖含量显著高于2、4年生黄芪。
关键词 黄芪;多糖;单糖;柱前衍生化;高效液相色谱法
ABSTRACT OBJECTIVE: To analyze and compare the contents of 6 kinds of monosaccharide in Astragalus membranaceus from different growth years. METHODS: 2-4 years old A. membranaceus from three areas were extracted with water extraction and alcohol precipitation, Sevage deproteinization to obtain A. membranaceus polysaccharide. The samples were firstly hydrolyzed with trifluoroacetic acid (TFA) and then derivatized by 1-phenyl-3-methyl-5-pyrazolone(PMP). HPLC analysis was adopted to determine the contents of 6 kinds of monosaccharide as mannose, rhamnose, galacturonic acid, glucose, galactose, arabinose. The determination was performed on Symmetry C18 column with phosphate buffer solution (pH 6.8)-acetonitrile (84 ∶ 16, V/V) as mobile phase at the flow rate of 1.0 mL/min. The detection wavelength was 245 nm, and column temperature was 35 ℃. The sample size was 20 ?L. RESULTS: The contents of mannose, rhamnose, galacturonic acid, glucose, galactose and arabinose were 0.50-0.94, 0.76-1.60, 3.35-7.86, 87.33-275.77, 1.95-8.96, 2.35-14.04 mg/g, respectively. Total contents of monosaccharide from 2, 3, 4 years old A. membranaceus were 98.26-139.92, 173.81-295.71, 122.37-182.41 mg/g, respectively. There was significant difference in the contents of glucose between 3 old years A. membranaceus and 2, 4 old years A. membranaceus (162.71-275.77 mg/g vs. 87.33-107.70, 111.54-167.26 mg/g, P<0.05). CONCLUSIONS: Above 6 monosaccharides are detected in 2, 3, 4 years old A. membranaceus, among which the content of glucose is the highest. The content of glucose in 3 years old A. membranaceus is higher than that in 2 and 4 years old A. membranaceus.
KEYWORDS Astragalus membranaceus;Polysaccharides;Monosaccharides;Pre-column derivatization;HPLC
黃芪为豆科植物蒙古黄芪Astragalus membranaceus(Fisch.)Bge. var. mongholicus(Bge.)Hsiao或膜荚黄芪Astragalus membranaceus(Fisch.)Bge.的干燥根[1],主产于我国山西、内蒙古等地[2]。作为常用传统中药之一,黄芪味甘、性平,具有补气固表、利水生津、托毒排脓、敛疮生肌等功效,临床上主要用于治疗气虚乏力、食少便溏、中气下陷、久泻脱肛、血虚萎黄、内热消渴等症[1,3]。现有研究指出,黄芪具有调节免疫、保护心血管与神经系统、抗肿瘤、护肝等药理作用,其主要化学成分包括黄酮类、皂苷类、多糖类化合物[4-5]。
作为大宗药材之一,黄芪在临床上使用较广,已有研究表明不同生长年限黄芪药材的成分含量存在较大差异,其中黄酮类和皂苷类成分的含量随生长年限的延长而逐年升高,而多糖类成分的含量则变化趋势不一[6-9]。黄芪药材中的黄芪多糖是一种重要的生物活性物质,具有抗氧化、抗肿瘤、降血糖、抑制人肝癌细胞增殖、调节免疫等作用[10-13]。由于非专属且可控性不强,黄芪多糖未能作为质控指标以评价黄芪种质资源[14]。多糖的生物活性与其单糖组成密切相关,且单糖组成及其含量测定是进行多糖质量控制的重要依据[15]。近年来对黄芪多糖的探索研究也成为了医学界的研究热点之一。目前,研究者多利用紫外分光光度法测定总多糖含量,并以此作为药材品质评价的手段,然而总多糖含量缺乏特异性,故2020年版《中国药典》(一部)并未收载黄芪多糖的相关检测标准[16]。为此,本研究对不同生长年限黄芪药材中的黄芪多糖进行水解,并对其进行柱前衍生化处理;再基于文献[15,17-20]的研究结果,采用高效液相色谱法(HPLC)对黄芪药材中甘露糖、鼠李糖、半乳糖醛酸、葡萄糖、半乳糖和阿拉伯糖等6种单糖的含量进行测定,考察黄芪药材中这6种单糖含量随生长年限变化的规律,旨在为不同生长年限黄芪药材的质量评价提供科学参考。
1 材料
1.1 主要仪器
本研究所用主要仪器包括Waters e2695型HPLC仪及配套的四元泵、柱温箱、自动进样器和Empower 3工作站(美国Waters公司),RE-52A型旋转蒸发器(上海亚荣生化仪器厂),HWS-24型电热恒温水浴锅(上海一恒科学仪器有限公司),BSA-124S型分析天平(赛多利斯科学仪器有限公司),DHG-9140A型电热恒温鼓风干燥箱(上海精宏实验设备有限公司),X-30R型高速冷冻离心机(美国Beckman Coulter公司)等。
1.2 主要药品与试剂
无水葡萄糖、鼠李糖、半乳糖、甘露糖、阿拉伯糖对照品(批号分别为YG8510、YR8080、YG8010、YG8420、YA8500,HPLC均大于98%)均购自南京翼飞雪生物科技有限公司;半乳糖醛酸对照品(批号B21894,HPLC大于98%)、1-苯基-3-甲基-5-吡唑啉酮(PMP,分析纯)均购自上海源叶生物科技有限公司;三氟乙酸(TFA,分析纯)购自上海麦克林生化科技有限公司;氢氧化钠(NaOH,批号20181113,分析纯)、三氯甲烷(批号20191216,分析纯)、正丁醇(批号20210119,分析纯)均购自国药集团化学试剂有限公司;乙腈(色谱纯)购自德国Merck公司;其余试剂均为分析纯,水为超纯水。
9批黄芪药材分别产自我国山西、甘肃、内蒙古等地,经南京中医药大学药学院陆兔林教授鉴定为蒙古黄芪A. membranaceus(Fisch.)Bge. var. mongholicus(Bge.)Hsiao的干燥根,其来源信息见表1。
2 方法与结果
2.1 黄芪多糖的提取
称取黄芪药材约20 g,加10倍量(mL/g,下同)水,于100 ℃下提取2 h,滤过;药渣加5倍量水同法提取30 min,滤过;合并滤液浓缩至50 mL,再加入Sevage试剂(氯仿-正丁醇=4 ∶ 1,V/V)10 mL以除去蛋白质(下层)。取上清液,以8 000 r/min离心10 min,除去不溶物,再加无水乙醇至总体积的90%,静置12 h,以8 000 r/min离心10 min,弃去上清液,收集沉淀并置于45 ℃鼓风干燥箱内干燥,即得黄芪多糖,得率见表2。
2.2 黄芪多糖的水解
称取“2.1”项所得黄芪多糖约0.25 g,精密称定,用水定容于5 mL量瓶中,摇匀,制成黄芪多糖供试液。量取上述黄芪多糖供试液1 mL,加入2 mol/L的TFA溶液2 mL,封口后于110 ℃鼓风干燥箱内水解6 h,取出,放冷,水浴蒸干,残渣加入甲醇1 mL,搅拌,蒸干以去除TFA,共重复3次,残渣加水溶解并转移至5 mL量瓶中,用水定容,摇匀,即得黄芪多糖水解溶液。
2.3 单糖对照品的衍生化
分别精密称取甘露糖对照品2.45 mg、鼠李糖对照品2.45 mg、半乳糖醛酸对照品2.05 mg、无水葡萄糖对照品260.15 mg、半乳糖对照品2.10 mg和阿拉伯糖2.15 mg,分别用水溶解后定容至2 mL量瓶中,充分摇匀,得各成分单一对照品溶液。量取上述单一对照品溶液各1 mL,置于同一10 mL量瓶中,加水定容,摇匀,即得混合对照品溶液。分别量取该混合对照品溶液100 μL、0.5 mol/L的PMP-甲醇溶液50 μL、0.3 mol/L的NaOH溶液50 μL,搖匀,于70 ℃水浴下反应30 min,冷却至室温,加入0.3 mol/L的盐酸(HCl)溶液50 μL进行中和,再加入氯仿1 mL进行萃取,以10 000 r/min离心10 min,弃去有机层,共重复萃取3次,得上层水相溶液,经0.22 ?m微孔滤膜滤过后,取续滤液,备用。
2.4 黄芪多糖水解样品的衍生化
精密吸取“2.2”项下黄芪多糖水解溶液400 μL、0.5 mol/L的PMP-甲醇溶液200 μL、0.3 mol/L的NaOH溶液200 μL,混匀,于70 ℃水浴下反应30 min,冷却至室温,加入0.3 mol/L的HCl溶液200 μL进行中和,再加入氯仿400 μL进行萃取,以10 000 r/min离心10 min,弃去有机层,共重复萃取3次,得上层水相溶液,经0.22 ?m微孔滤膜滤过后,取续滤液,备用。
2.5 色谱条件与系统适用性试验
以Symmetry C18(250 mm×4.6 mm,5 μm)为色谱柱,以磷酸盐缓冲液(pH 6.8)-乙腈(84 ∶ 16,V/V)为流动相,流速为1.0 mL/min,检测波长为245 nm,柱温为35 ℃,进样量为20 ?L。
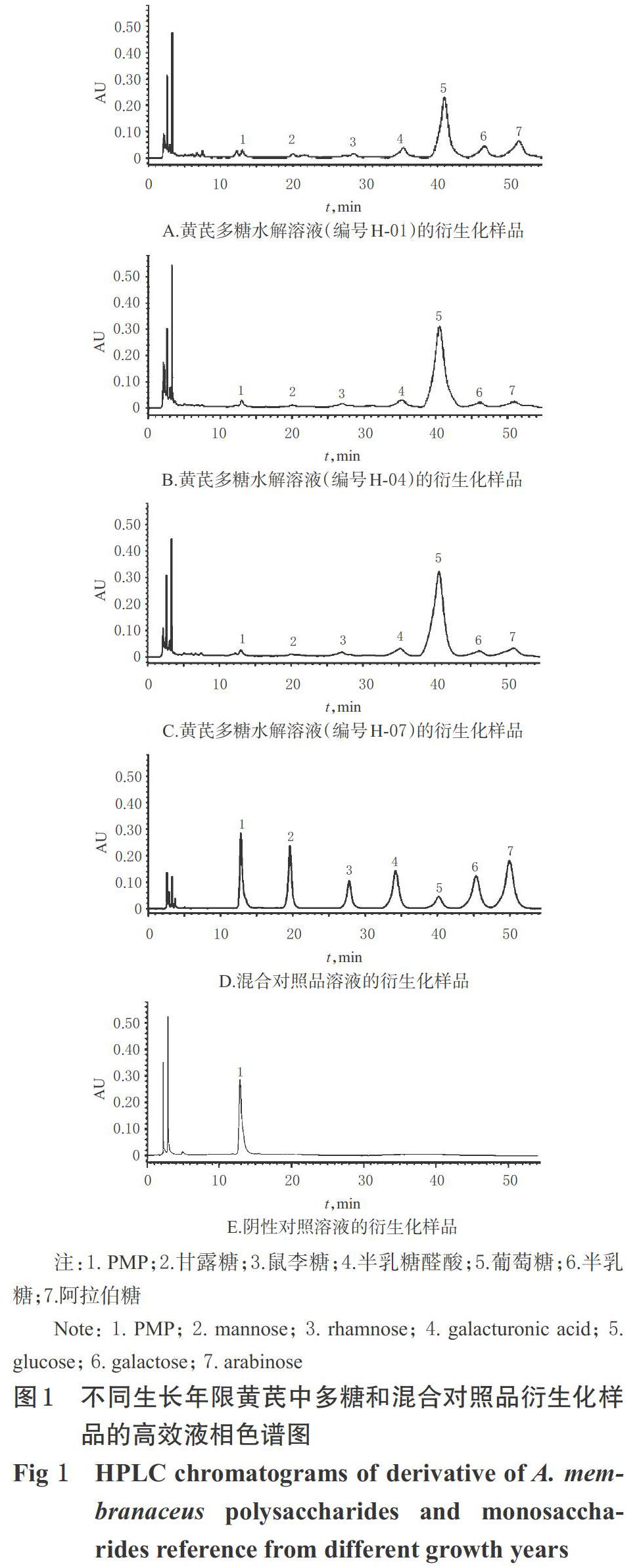
取衍生化后的2、3、4年生黄芪药材的多糖水解溶液和混合对照品溶液、阴性对照溶液(水),按上述色谱条件进样测定,记录色谱图。结果,不同生长年限黄芪药材中多糖的色谱图与混合对照品相似,各单糖成分的分离度良好,理论板数均大于2 500,阴性对照对单糖的测定无干扰,详见图1。
2.6 线性关系考察
精密吸取“2.3”项下甘露糖、鼠李糖、半乳糖醛酸、葡萄糖、半乳糖、阿拉伯糖单一对照品溶液各1 mL,置于同一10 mL量瓶中,加水定容,摇匀。分别吸取上述混合溶液800、400、200、100、80、40、20 ?L,置于4 mL离心管中,加水稀释至500 ?L,置于安瓿瓶中,按“2.3”项下方法进行衍生化处理(衍生化试剂加入量等比例增加,下同),制備成系列质量浓度的标准溶液,然后按“2.5”项下色谱条件进样测定,记录峰面积。以6种单糖的质量浓度(x,?g/mL)为横坐标、相应峰面积(y)为纵坐标进行回归分析。结果,甘露糖、鼠李糖、半乳糖醛酸、葡萄糖、半乳糖、阿拉伯糖在各自检测质量浓度范围内的线性关系均良好(R 2均大于0.999 0),详见表3。
2.7 稳定性试验
取衍生化后的黄芪多糖水解溶液(编号H-01),分别在室温下放置0、4、8、12、16、24 h时按“2.5”项下色谱条件进样测定6次,记录峰面积。结果,甘露糖、鼠李糖、半乳糖醛酸、葡萄糖、半乳糖、阿拉伯糖峰面积的RSD分别为1.37%、1.24%、0.95%、1.77%、1.12%、1.62%(n=6),表明衍生化后的黄芪多糖水解溶液在室温下放置24 h内稳定性良好。
2.8 重复性试验
精密称取同一编号(编号H-01)黄芪药材样品共6份,依次按“2.1”“2.2”“2.4”项下方法处理后,再按“2.5”项下色谱条件进样测定,记录峰面积并代入回归方程计算单糖含量。结果,样品中甘露糖、鼠李糖、半乳糖醛酸、葡萄糖、半乳糖、阿拉伯糖含量的RSD分别为2.13%、1.96%、2.38%、1.64%、1.99%、1.82%(n=6),表明本方法重复性良好。
2.9 加样回收率试验
取“2.2”项下已知含量的供试品溶液(编号H-01)共6份,每份1 mL,每份加入各单糖对照品溶液(取“2.3”项下各单糖单一对照品500 μL,分别定容至10 mL量瓶中,即得)1 mL,按“2.3”项下方法进行衍生化处理后,再按“2.5”项下色谱条件进样测定,记录峰面积并代入回归方程计算含量,再计算加样回收率和RSD值。结果,样品中甘露糖、鼠李糖、半乳糖醛酸、葡萄糖、半乳糖、阿拉伯糖的平均加样回收率分别为96.65%、99.56%、95.92%、101.48%、93.87%、99.80%,RSD分别为1.85%、1.12%、1.05%、0.95%、0.83%、0.44%(n=6),表明本方法准确度好。
2.10 精密度试验
取“2.3”项下衍生化后的单糖混合对照品溶液适量,按“2.5”项下色谱条件连续进样测定6次,记录峰面积。结果,甘露糖、鼠李糖、半乳糖醛酸、葡萄糖、半乳糖、阿拉伯糖峰面积的RSD分别为1.67%、1.08%、1.29%、1.81%、1.42%、1.92%(n=6),表明仪器精密度良好。
2.11 黄芪多糖中单糖含量的测定
分别称取9批黄芪药材约20 g,依次按“2.1”“2.2”“2.4”项下方法处理后,再按“2.5”项下色谱条件进样测定,记录峰面积并代入回归方程计算单糖含量,结果见表4。
由表4可以看出,黄芪多糖中各单糖的含量为0.50~275.77 mg/g;各批黄芪药材中黄芪多糖均含有甘露糖、鼠李糖、半乳糖醛酸、葡萄糖、半乳糖、阿拉伯糖等6种单糖,其中葡萄糖含量最高。采用Excel 2016软件对2、3、4年生黄芪药材中各单糖含量进行两两t检验,发现仅3年生黄芪药材中葡萄糖含量显著高于2、4年生黄芪(P<0.05),其他单糖含量均无显著差异(P>0.05)。同时,3个产地黄芪药材中黄芪多糖含量不一致,其中山西省产含量最高。
3 讨论
本研究采用水提醇沉法提取了黄芪多糖,并建立了测定其中6种单糖含量的PMP柱前衍生化-HPLC法。该方法的灵敏度高、分离效果好,线性范围宽,精密度、重复性、稳定性和回收率良好,操作简便,结果稳定可靠,可用于黄芪药材中多糖的单糖定量测定,为药材中多糖的组成研究提供了参考。
在流动相比例的选择中,本课题组前期考察了不同流动相比例[磷酸盐缓冲液-乙腈(85 ∶ 15、84 ∶ 16、83 ∶ 17,82 ∶ 18,V/V)]对单糖测定色谱峰分离效果的影响,结果显示,当乙腈与磷酸盐缓冲液的体积比为16∶84时,各单糖成分的分离效果较好,且整体保留时间较为适中,基线相对平稳且峰形良好。故综合考虑,本研究最终选择磷酸盐缓冲液-乙腈(84 ∶ 16,V/V)为流动相。
本课题组比较了各单糖在 Symmetry C18(250 mm×4.6 mm,5 ?m)、Hedera ODS-2 C18(200 mm×4.6 mm,5 ?m)两种不同类型色谱柱上的分离效果,结果发现,短柱上各单糖未能实现基线分离,峰面积小;长柱基线相对平稳,各主要峰之间能够基本实现基线分离,且峰形良好,可见长柱的分离效果比短柱好,故选择长柱对单糖进行定量分析。
生长年限是影响中药材质量的重要因素[7]。本研究以来自于山西、甘肃、内蒙古等3个产地不同生长年限的黄芪药材为对象,采用PMP柱前衍生化-HPLC法在上述黄芪药材中均检出了甘露糖、鼠李糖、半乳糖醛酸、葡萄糖、半乳糖和阿拉伯糖,其中葡萄糖含量最高。可见,单糖的含量和组成比例有一定差异,说明药材的生长年限对黄芪多糖的单糖组成有一定影响。就含量最高的葡萄糖而言,3年生黄芪药材中葡萄糖含量均显著高于2、4年生黄芪,推测原因可能是由于药材产地的土壤、气候等因素以及不同生长年限的影响导致药材质量发生变化。至于不同生长年限的黄芪多糖的药理活性是否存在差异,有待进一步研究。
参考文献
[ 1 ] 国家药典委员会.中华人民共和国药典:一部[S]. 2020年版.北京:中国医药科技出版社,2020:315.
[ 2 ] 曹庆伟,张瑞,李科,等.蒙古黄芪质量评价及商品规格等级研究进展[J].山西医科大学学报,2019,50(6):854- 859.
[ 3 ] 姜辉,顾胜龙,张玉婷,等.黄芪化学成分和药理作用研究进展[J].安徽中医药大学学报,2020,39(5):93-96.
[ 4 ] 刘靖丽,于海东,梁艳妮.中药黄芪中黄酮类化合物抗氧化活性的DFT研究[J].化学与生物工程,2019,36(1):36-40.
[ 5 ] 王青,赵林华,邸莎.黄芪的临床应用及其用量探究[J].吉林中医药,2018,38(12):1450-1454.
[ 6 ] 储成俭,金雅.基于一测多评法对不同生长年限黄芪中黄酮类成分的分析研究[J].中药材,2019,42(8):1777- 1780.
[ 7 ] 辛博,谢景,王文全.不同生长年限黄芪药材中总多糖和总黄酮含量的测定[J].中医药信息,2015,32(5):31-34.
[ 8 ] 张秋海,丁家欣,李树莉,等.不同生长年限黄芪中黄芪甲苷和多糖含量比较[J].中国中医药信息杂志,2014,21(11):79-82.
[ 9 ] 张善玉,朴惠顺,宋成岩.不同生长年限黄芪中总皂苷、黄芪甲苷、总黄酮及多糖含量比较[J].延边大学医学学报,2005,28(2):87-89.
[10] 劳军,王楠楠.探究影响黄芪多糖抗氧化活性的因素[J].中国食品,2020(14):121-122.
[11] 毛倩倩,林久茂.黃芪多糖抗肿瘤作用的研究进展[J].中医药通报,2020,19(4):69-72,34.
[12] 杜芳,董立江.黄芪多糖抑制人肝癌细胞增殖的作用机制研究[J].华西药学杂志,2020,35(4):402-406.
[13] 芮雯,李婵艺,陈宏远.黄芪多糖的结构表征与生物活性研究进展[J].中药新药与临床药理,2019,30(2):264- 270.
[14] 曹宇欣,李科,秦雪梅,等.基于多糖受体理论的黄芪多糖质量控制研究思路[J].中草药,2019,50(9):2201-2209.
[15] 吴岩斌,张秀才,易骏,等.柱前衍生化HPLC法测定不同基源金线莲多糖的单糖组成[J].中国药房,2015,26(15):2116-2119.
[16] 高凡茸,李科,郝霞,等.基于单糖指纹图谱技术的速生黄芪与野生黄芪的鉴别[J].中草药,2015,46(14):2134- 2142.
[17] 赖戈娜,贾文玉,罗思婉,等.猪苓多糖的PMP柱前衍生化-HPLC指纹图谱研究[J].中国药房,2020,31(7):788- 793.
[18] 周彦强,吴光斌,陈发河. PMP柱前衍生化HPLC法测定黄秋葵多糖的单糖组成[J].食品科学,2019,40(4):266- 271.
[19] 符梦凡,赵一帆,阎卫东.柱前衍生化HPLC法分析枸杞多糖中单糖组成[J].食品科学,2018,39(18):186-191.
[20] 陈虎虎,孙静,杨金颖,等.柱前衍生化-高效液相色谱法测定蒙古黄芪多糖中单糖的组成[J].现代药物与临床,2012,27(5):468-470.
(收稿日期:2021-01-06 修回日期:2021-05-06)
(编辑:邹丽娟)
