中药材小血藤质量标准研究
2021-07-11张静雅刘春花马雪王爱民李勇军王永林孙佳
张静雅 刘春花 马雪 王爱民 李勇军 王永林 孙佳


【摘 要】 目的:建立小血藤药材质量标准。方法:采集来自贵州六批次小血藤药材,参考2015版《中国药典》和2003版《贵州省中药材、民族药材质量标准》对小血藤的质量控制方法进行研究,包括性状鉴别、显微鉴别、薄层色谱建别、水分检查、总灰分检查及浸出物检查。结果:六批小血藤的性状特征相似,显微特征明显;薄层色谱斑点清晰、分离度好、专属性强;水分为8.90%~10.08%,平均值9.52%;总灰分为11.1%~12.7%,平均值11.8%;水溶性浸出物为12.83%~16.55%,平均值14.93%。结论:该方法操作简单,重复性好,可为小血藤质量控制提供实验依据。
【关键词】 小血藤;显微鉴别;薄层色谱鉴别;质量标准
【中图分类号】R284.1 【文献标志码】 A 【文章编号】1007-8517(2021)08-0045-06
Abstract:Objective The aim of this study is to establish the quality standard of Rubiae alatae Radix et Rhizoma. Methods Six batches of Rubiae alatae Radix et Rhizoma from Guizhou were collected. According to pharmacopoeia 2015, the quality control methods of Rubiae alatae Radix et Rhizoma were studied, including character, microscopic and thin layer chromatography (TLC) identification, water content, total ash inspection and water-soluble extract determination. Results The characters of the six batches of Rubiae alatae Radix et Rhizoma were similar, and their microscopic characteristics were obvious. The spots in TLC are clear, possessing good resolution and specificity.The range of water content of the six batches of samples was 8.90%~10.08% and the average value was 9.52%; the total ash content ranged from 11.1% to 12.7% with an average value 11.8%; and the content of water-soluble were 12.83%~16.55% with a mean value 14.93%. Conclusion This method is simple, accurate and reliable, which can provide experimental basis for the quality control of Rubiae alatae Radix et Rhizoma.
Key words:Rubiae alatae Radix et Rhizoma; Microscopic Identification; Thin Layer Chromatography; Quality Control
小血藤为茜草科植物金剑茜草(Rubia alata Roxb.)、大叶茜草(Rubia schumanniana Pritzel)或钩毛茜草(Rubia oncotricha Hand.-Mazz.)的干燥根及根茎,为我国传统常用中药[1],亦为贵州省少数民族用药,小血藤为三种茜草的总称。其最早记载于秦汉时期的《神农本草经》,原名“茜根”,书中记载“茜根主寒湿,风痹,黄疽,补中,生山谷[2],关于茜草的药用历史在《名医别录》、《新修本草》《本草纲目》《中华本草》等历代本草中均有描述[2],其功效与作用是凉血止血、清热退黄、止痒止痛、消炎杀菌[3] 。小血藤主要在西南地区如云南、四川、贵州等地分布,其中金剑茜草在贵州分布较为广泛[4]。雖然三种茜草在植物形态、生态环境及分布上略有差异,但是在民间均采集其根及根茎,用于治疗吐血,衄血,崩漏,经闭,黄疸,支气管炎,跌扑损伤等疾病[5],具有良好的药用价值。
研究显示,茜草及同属植物的主要化学成分是蒽醌及其苷类[6],此外还含有萘醌类、萜类、环己肽类及多糖等成分[7-11] 。目前关于小血藤的质量控制尚不完善,在《贵州省中药材、民族药材质量标准》(2003版)中没有建立小血藤的定性鉴别和检查项等,质量标准相对简单,限制了其应用和开发。因此,本研究通过收集不同批次的小血藤药材(包括三种不同的茜草),通过开展三种不同茜草的性状研究,鉴别研究(显微、薄层),有关检查项目研究(水分、总灰分、浸出物),建立共性的小血藤药材质量标准,为完善小血藤的质量标准提供参考依据。
1 材料与仪器
1.1 仪器 超声波清洗仪(上海跃进医用光学器械厂),XTP-A500多功能粉碎机(永康市红太阳机电有限公司),EL204电子天平(梅特勒-托利多仪器有限公司),WP-MP-II-20实验室超纯水机(四川沃特尔科技发展有限公司),青岛海洋硅胶G板(青岛海洋化工厂分厂),烟台黄海江友硅胶G板(烟台黄海江友化工厂),青岛鼎康硅胶G板(青岛鼎康化工厂),REPROSTAR3薄层数码成像系统(瑞士CAMAG公司),DK-98-Ⅱ型水浴锅和DH600BII恒温箱(天津泰斯特仪器有限公司),ProskitPD-153游标卡尺购自上海宝工工具有限公司,微量滴定管3 mL(分度值0.01 mL)、扩散皿(标准)、镊子、载玻片、盖玻片、酒精灯等。
1.1 试剂 无水乙醇、95%乙醇、甲醇、水合氯醛、硼酸、碳酸钾、甘油及溴甲酚绿指示剂(国药集团化学试剂有限公司),三氯甲烷、冰醋酸、丙酮、正丁醇(上海试四赫维化工公司),茚三酮、甲基红指示剂(上海馨晟试化工科技有限公司),丙三醇购(天津市致远化学试剂有限公司),阿拉伯树胶(天津市科密欧化学试剂有限公司),盐酸(重庆川东化工(集团)有限公司),无水碳酸钠基准试剂(天津市化学试剂研究所有限公司),以上试剂均为分析纯。
1.2 试药 本品横切面和粉末性状的显微鉴别所用样本来至于贵州不同地区收集的6批小血藤药材样品,样品均由贵州医科大学药学院中药民族药标本馆龙庆德副教授鉴定为茜草科植物金剑茜草Rubia alata Roxb.、大叶茜草Rubia schumanniana Pritzel或钩毛茜草Rubia oncotricha Hand.-Mazz.的干燥根及根茎,凭证标本存放于贵州医科大学贵州省药物制剂重点实验室。来源见表1。(其中20170819作为对照药材)
2 方法与结果
2.1 原植物形态 小血藤为三种不同茜草的根及根茎,植物形态中叶片材质、叶基部形状、花序、果实颜色、大小等存在一定差异,根据中国植物志记载[12],总结其原植物的特征差异,见表2。
2.2 性状鉴定 参照2003版《贵州省中药材、民族药材质量标准》,对采集来的6批药材样品除去杂质、晒干后,采用标尺对小血藤的大小进行测量,用看、摸、闻、尝等方法对样品进行颜色、形状、表面、质地、气味、断面的外观鉴定。
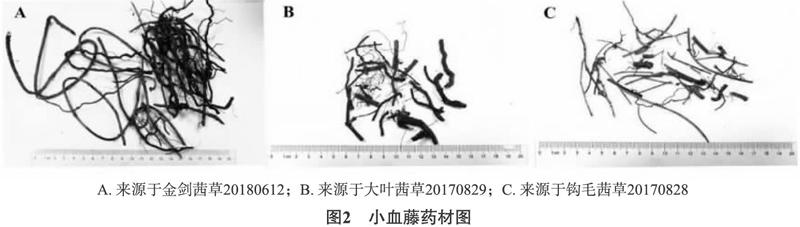
其药材在形状上相似,如图2所示。根茎结节状,丛生多条细根。根长圆柱形,略弯曲,长10~30 cm,直径0.2~1 cm;表面红棕色或暗棕色,具细纵皱及少数细根痕;皮部脱落处黄红色。质脆,易折断,断面平坦,皮部狭窄,紫红色,木部宽广,浅黄红色,可见多数小孔。气微,味微苦,久嚼刺舌。
2.3 显微鉴别 采用直接切片法,将根切到一层细胞的厚度,置于载玻片上,滴加水合氯醛透化,再滴加稀甘油。盖上盖玻片,置于显微镜下观察,拍照记录。筛选小血藤粉末少许在载玻片上,滴加水合氯醛加热透化,再滴加稀甘油。盖上盖玻片,置于显微镜下观察,拍照记录。通过观察多批小血藤根的横切面,选择其中有代表性的结果,如图3~4所示,但三种来源间的横切面的木栓层、木栓内层、韧皮部、木质部均存在差异,见表3。
根据对小血藤三种来源的粉末进行观察后,发现三者的粉末颜色都呈灰褐色,进行显微观察后,能明显的观察到草酸钙针晶、导管、木栓细胞等,如图4~5所示。但针晶、导管、木栓细胞等均存在差异,根据显微鉴别后总结出其异同点,见表4。
通过对多批样品的粉末进行观察和测量,其粉末的显微鉴别特征总结如下:本品粉末棕褐色。木栓细胞呈类方形或多角形,壁增厚。草酸钙针晶散在或成束,长20~250 μm。具缘纹孔导管多见,直径20~300 μm,如图5所示。
2.4 薄层色谱鉴别 取本品粉末0.5 g,加甲醇10 mL,超声处理30 min,滤过,滤液蒸干,残渣加甲醇1 mL使溶解,作为供试品溶液。另取小血藤对照药材0.5 g,同法制成对照药材溶液。照薄层色谱法(《中国药典》2015年版四部通则0502)试验,吸取上述两种溶液各2 μL,分别点于同一硅胶G板上,以石油醚-丙酮(8∶2)为展开剂,展开,取出,晾干,置紫外光灯(365 nm)下检视。供试品色谱中,在与对照药材色谱相应的位置上,显相同颜色的荧光斑点。按照拟定的的薄层色谱鉴别方法,对6批样品进行测定,结果图6所示,来源于金剑茜草、大叶茜草和钩毛茜草的小血藤的薄层色谱主斑点几乎一致,但也存在一定的差异,尤其是大叶茜草,提示其所含成分种类及含量存在差异,还有待进一步深入研究。
2.5 水分、总灰分及浸出物检查 取本品粉末(过二号筛)2 g,水分照《中国药典》2015年版通则0832水分测定法(第二法烘干法)测定。6批小血藤中含水量分为8.90%~10.08%,平均值9.52%,故暂定本品水分不得过12.0%。见表5。取本品粉末2 g,照《中国药典》2015年版通则2302灰分测定法测定。6批小血藤中总灰分为11.1%~12.7%,平均值11.8%,暂定本品总灰分不得过15.0%。见表5。
取本品粉末(过二号筛)2 g,精密称定,置100 mL的锥形瓶中,照《中国药典》2015年版四部通则2201浸出物测定法中,水溶性浸出物测定法-热浸法,采用水为溶剂进行浸出物测定,以浸出物作为本品质量控制指标之一。6批干小血藤水溶性浸出物为12.83%~16.55%,平均值14.93%,暂定本品水溶性浸出物不得少于12.0%。见表5。
3 讨论
中药显微鉴定是通过显微技术确定中药品种和质量的一种鉴定方法,是目前中药材鉴别的主要方法之一[12]。本研究通过对小血藤三种不同来源的根的横切面进行显微鉴定,发现其木栓层、木栓内层、韧皮部、木质部及薄壁细胞中的草酸钙针晶均有不同,粉末中的导管的大小也有明显的区别。上述差异有助于对三种茜草加以区别,进一步完善了小血藤药材的质量标准研究。
从性状研究来看,三种茜草根及根茎的性状无显著差异。为了方便小血藤药材的采集并对三种茜草加以区分,研究发现三种茜草在植物形态和显微鉴别上存在一定的差异。从植物形态上看,大叶茜草叶片较宽,呈厚纸质至革质;金剑茜草叶片呈薄革质,线形或披针状线形;钩毛茜草叶片近纸质,其主要特征是全株均密被灰色硬毛,毛的末端作弯钩状。
在薄层色谱研究中,还考察专属性和耐用性。分别考察青岛海洋硅胶G板、青岛鼎康硅胶G板和烟台黄海硅胶HSG板的展开效果,三个品牌的硅胶G板中,青岛海洋与青岛鼎康硅胶G板的分离度基本一致,说明其耐用性较好,烟台江友黄海硅胶HSG板是高效板,其分离开的斑点较其它两种普通硅胶G板多,从经济适用的角度选择普通硅胶G板。同时,分别以不同浓度硫酸调节的展开环境相对湿度为32%、52%、72%,在25℃温度下分别考察不同相对湿度展开的效果。结果显示,虽不同湿度下色谱图的条带清晰,Rf值有一定差异,但仍能较好鉴别药材,说明该湿度范围耐用性较好。分别在相对湿度58%的条件下,考察10 ℃、25 ℃、35 ℃不同温度对薄层展开的影响,结果显示,不同温度下色谱图的条带清晰,Rf值差异不明显,说明该药材受温度的影响不大。进一步对供试品的稳定性进行考察,将同一批次的本品粉末于3天前、2天前、1天前、当天按拟定的方法制备供试品溶液,分别点于同一硅胶G板上,展开,显色。结果显示,放置1~3天的供试品溶液展开后的色谱图基本一致,各斑点无差异。可见所建立的薄层色谱鉴别方法色譜斑点清晰、无干扰、专属性强、稳定性好、耐用性强。
在对水分、总灰分、浸出物和含量测定的限量测定中,6批小血藤的含水量平均值为9.52%,初步拟定本品水分不超过12.0%;总灰分的平均值为11.8%,初步拟定本品总灰分不超过15.0%;水溶性浸出物的平均值为14.93%,初步拟定本品水溶性浸出物不得少于12.0%。
综上,本实验系统地研究了小血藤性状特征、显微特征、薄层色谱特征、水分、总灰分和浸出物含量,为小血藤的质量控制提供参考依据。
参考文献
[1]崔玲.神农本草经[M].天津:天津古籍出版社,2009:21.
[2]张琳,胡本祥,安衍茹,等.茜草本草考证[J].吉林中医药,2018(3):317-320.
[3]国家药典委员会.中华人民共和国药典(一部)[M].北京:中国医药科技出版社,2015:234.
[4]中华本草编委会.中华本草苗药卷[M].贵阳:贵州科技出版社,2005:90.
[5]李安仁.中国植物志第七十一卷第二分册[M].北京:科学出版社,1998.
[6]陈毅,王海丽,薛露,等.茜草的研究进展[J].中草药,2017,48(13):2771-2779.
[7]李海峰,肖凌云,张菊,等.茜草化学成分及其药理作用研究进展[J].中药材,2016,39(6):1433-1436.
[8]李鹏,胡正海.茜草的生物学及化学成分与生物活性研究进展[J].中草药,2013,44(14):2009-2014.
[9]袁悦,董双双,冯文佩,等.茜草的化学成分及其生理活性研究进展[J].江西饲料,2016(4):14-18.[ZK)]
[10][ZK(#]汪哲,赵思蒙,曾广智,等.钩毛茜草的化学成分及其细胞毒活性研究[J].中国中药杂志,2018,43(22):4462-4468.
[11]李鹏,胡正海.茜草的生物学及化学成分与生物活性研究进展[J].中草药,2013,44(14):2009-2014.
[12]安丽敏,安丽华.中药显微鉴定常用制片方法概述[J].哈尔滨医药,2016,36(1):78-79.
(收稿日期:2020-10-07 编辑:程鹏飞)
