柠檬酸用量对浸渍法制备K2CO3/Al2O3吸附剂脱除CS2性能的影响
2021-07-05张现策周广林姜伟丽周红军
张现策,周广林,李 芹,姜伟丽,周红军
(中国石油大学(北京) 新能源与材料学院,北京 102249)
C5馏分油是石脑油高温裂解制乙烯过程的主要副产物,约占总产物的15%~25%[1]。C5馏分油约含有20多种组分,主要为异戊二烯、(双)环戊二烯和间戊二烯[2-3]。C5组分由于具有特殊的分子结构,可用于生产石油树脂、橡胶和黏合剂等高附加值产品[4-6],但却含有在后续过程中会导致贵金属催化剂失活的硫化物(如CS2),并严重影响高附加值产品的质量[7]。因此有效地脱除硫化物、降低对下游产品的影响,是C5组分有效利用的关键。目前,CS2的脱硫技术主要包括干法和湿法两种。干法常用的方法有化学转化吸收法、催化还原法、催化加氢法、催化水解法等[8-13]。Fiedorow等[14]对γ-Al2O3催化剂的活性中心进行研究,提出表面碱中心为水解中心。上官炬等[15]通过对负载铝基和铂基的γ-Al2O3催化剂进行碱性表征,发现弱和次弱两类碱性中心均参与了CS2与COS的水解。Ning等[16]采用溶胶-凝胶法制备了一系列金属氧化物负载的微波煤基活性炭催化剂,发现催化水解活性随碱性强度的增加而增加。Li等[13]使用共浸渍法制备了Cu/Ni/Fe类水滑石催化剂用于CS2催化水解,并进行CO2-TPD表征,发现合成催化剂时溶液的pH=10~11时,催化剂的脱硫活性最好,推断碱的引入可以产生更多有利于CS2催化水解的羟基,这些羟基是CS2水解的活性中心[17]。因此,碱性与载体的相互作用对吸附剂脱CS2性能的提升有很大的影响。
本课题组前期工作制备了K2CO3/Al2O3吸附剂,能够对C5中的CS2有效脱除[18]。吸附剂除主要活性组分外,通常引入助剂以改变吸附剂的吸附性能,提高吸附容量。本工作以K2CO3/Al2O3吸附剂为载体,采用浸渍法制备了不同含量柠檬酸溶液改性的CA-K2CO3/Al2O3吸附剂,并用于C5馏分油吸附脱硫实验中,考察添加柠檬酸对CAK2CO3/Al2O3吸附剂结构及对CS2的吸附脱除性能的影响,以期获得吸附性能高的实用型CAK2CO3/Al2O3吸附剂。
1 实验部分
1.1 主要试剂及原料
薄水铝石粉、田菁粉:工业级,山东淄博恒亿化工科技有限公司;稀硝酸:AR,北京北化精细化学品有限责任公司;柠檬酸:AR,天津市光复科技发展有限公司;K2CO3:AR,天津市大茂化学试剂厂;C5馏分油:工业级,山东淄博齐鲁乙烯鲁华化工有限公司。
1.2 吸附剂的制备
将拟薄水铝石粉100 g、2%(w)稀硝酸溶液40 g与田菁粉2 g混合,混捏三次并挤条,再经干燥、焙烧,制得活性氧化铝载体。分别称量0,0.7,1.4 g的柠檬酸与3 g的K2CO3溶解在10 mL去离子水中,配制成透明的溶液,用等体积法浸渍于已制备好的Al2O3上,浸渍时间12 h。之后,在120℃干燥2 h,空气气氛下于马弗炉中升温至500 ℃焙烧3 h,制得不同含量柠檬酸的CA-K2CO3/Al2O3吸附剂。根据柠檬酸含量的不同,分别记为CA0-K2CO3/Al2O3,CA0.07-K2CO3/Al2O3,CA0.14-K2CO3/Al2O3吸附剂。
1.3 吸附剂的脱硫性能评价
采用静态吸附法评价吸附剂吸附脱除CS2的性能,吸附剂用量5 g,反应温度30 ℃,C5馏分油(CS2,硫含量为1 200 μg/mL)用量50 mL。称取所制备吸附剂与模拟油在磨口锥形瓶中混合,并搅拌,每间隔一段时间,将固液两相分离,收集液相。
1.4 吸附剂的表征
采用泰州市启航石油分析仪器有限公司QH-2000SN型紫外荧光定硫仪测量硫含量,并制作静态吸附曲线;采用麦克仪器公司TriStarⅡ 3020型N2吸附-脱附仪测量吸附剂的比表面积(BET法计算)和总孔体积(BJH法计算),总孔体积由在相对压力为0.99时吸附的N2数量计算得到;采用麦克仪器公司Auto ChemⅡ 2920型多功能吸附仪对试样进行CO2-TPD表征,首先在氦气中将催化剂以500 ℃的温度净化1 h,冷却至室温,用流量为50 mL/min的纯CO2吸附饱和30 min,启动实验,升温速率为10 ℃/min,升温至800 ℃;采用铂金埃尔默公司Nicoleti S50型红外光谱仪对待测试样表面官能团的种类进行FTIR表征,KBr压片,波长范围为400~4 000 cm-1。
2 结果与讨论
2.1 CA-K2CO3/Al2O3吸附剂脱硫性能的评价
图1 为不同含量柠檬酸改性CA-K2CO3/Al2O3吸附剂脱硫的评价结果。由图1可知,柠檬酸的加入提高了CA0-K2CO3/Al2O3吸附剂对CS2的脱除能力。当柠檬酸的含量由0增至0.07 g/mL时,当反应时间为1 h时,C5馏分油中的硫含量由1 200 μg/mL降低至375 μg/mL,脱硫效果比未改性的吸附剂提升了322 μg/mL。并且CA0.07-K2CO3/Al2O3吸附剂在11 h内将C5馏分油中的CS2含量从1 200 μg/mL降低至50 μg/mL以内。然而,随着柠檬酸含量的进一步增加,脱硫活性却随之降低。当柠檬酸含量为0.14 g/mL时,C5馏分油中的硫含量在1 h内从1 200 μg/mL降低至563 μg/mL。脱硫效果在1 h时比0.07 g/mL柠檬酸改性的吸附剂降低了188 μg/mL。这表明柠檬酸的加入促进了OH-与载体的相互作用,从而有利于吸附剂脱硫活性的提高。柠檬酸添加过量可能改变了吸附剂的孔径结构,或者破坏了吸附剂表面的碱性基团,导致脱硫能力减弱。
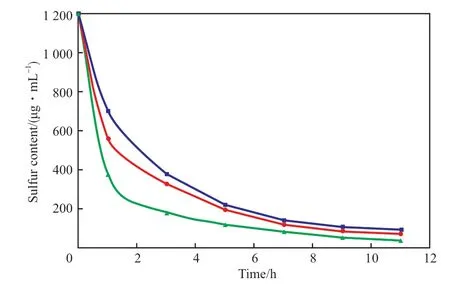
图1 不同含量柠檬酸改性CA-K2CO3/Al2O3吸附剂脱硫的评价结果Fig.1 Evaluation results of desulfurization of CA-K2CO3/Al2O3 adsorbent modified with different concentration of citric acid.
2.2 N2吸附-脱附表征结果
表1 为不同含量柠檬酸改性CA-K2CO3/Al2O3吸附剂的孔结构参数。由表1可知,与CA0-K2CO3/Al2O3吸附剂相比,加入柠檬酸的CAK2CO3/Al2O3吸附剂的比表面积和孔体积都有一定程度的增加,孔径略有减小,这可能是由于加入的柠檬酸增加了吸附剂的部分介孔,使比表面积、孔体积增加,平均孔径减小。CA0-K2CO3/Al2O3,CA0.07-K2CO3/Al2O3,CA0.14-K2CO3/Al2O3吸附剂的比表面积分别为181.01,196.54,210.14 m2/g。
图2 为不同含量柠檬酸改性CA-K2CO3/Al2O3吸附剂的N2吸附-脱附曲线及孔径分布。由图2a可知,各吸附剂的N2吸附-脱附曲线均呈IUPAC分类的Ⅳ型等温线[19],对应介孔固体,有助于吸附。各曲线在低压段(p/p0< 0.4)吸附量平缓增加,此时N2分子以单层到多层吸附在介孔的内表面。在中压段(p/p0=0.4~0.8)吸附量有一突增,代表在此处的中孔结构较为均一。在中压段和高压段(0.8 <p/p0< 1)都具有相同的H2型滞后环,且能够被N2完全填充,可认为是介孔材料孔径之间相互连通[20]。由图2b可知,各吸附剂以25 nm内的介孔为主,且孔径为4~6 nm的孔数量较多,有利于CS2水解反应。与CA0-K2CO3/Al2O3吸附剂相比,加入柠檬酸的吸附剂在4~6 nm的孔数量变多,结合表1中试样的比表面积和孔体积随着柠檬酸含量的增加而增大的现象,说明添加柠檬酸后可增加吸附剂的介孔。当柠檬酸含量为0.07 g/mL时,平均孔径约为4.8 nm,且分布均匀,此范围的孔径适合CS2的吸附,吸附脱硫效果最好。而随着改性的柠檬酸含量进一步增加,吸附剂的孔径过小,限制了CS2与活性位的接触,导致脱硫效果下降。

表1 不同含量柠檬酸改性CA-K2CO3/Al2O3吸附剂的孔结构参数Table 1 Pore structure parameters of CA-K2CO3/Al2O3 adsorbents modified by citric acid at different concentrations

图2 不同含量柠檬酸改性CA-K2CO3/Al2O3吸附剂的N2吸附-脱附曲线(a)及孔径分布(b)Fig.2 N2 adsorption and desorption curves(a) and pore diameter distribution(b) of CA-K2CO3/Al2O3 adsorbents modified by citric acid at different concentrations.
2.3 CO2-TPD表征结果
图3 为不同含量柠檬酸改性CA-K2CO3/Al2O3吸附剂的CO2-TPD曲线。在110 ℃与190 ℃出现两个CO2脱附峰,分别代表着弱碱中心和次弱碱中心,弱碱中心能够促进CS2与COS的水解反应[15]。与CA0-K2CO3/Al2O3吸附剂相比,CA0.07-K2CO3/Al2O3吸附剂110 ℃处CO2脱附峰面积明显增加,证明经0.07 g/mL柠檬酸改性后,吸附剂表面的弱碱中心明显增多,CA0.14-K2CO3/Al2O3吸附剂110 ℃处CO2脱附峰面积明显减小,证明经0.14 g/mL柠檬酸改性后,吸附剂表面的弱碱中心明显减少。640℃处的峰为吸附剂的强碱中心,强碱中心是CS2吸附和水解的主要活性位点。加入柠檬酸的CAK2CO3/Al2O3吸附剂640 ℃处的峰形基本相同,与CA0-K2CO3/Al2O3吸附剂相比,脱附峰面积整体减小。说明CA0-K2CO3/Al2O3吸附剂的碱性过强,会增加它对CO2和H2S等竞争组分的吸附,导致对CS2的吸附能力降低。柠檬酸自身含有一个羟基,改性后,能够在降低吸附剂碱性的同时,引入羟基。其中柠檬酸含量为0.07 g/mL时,弱碱中心最多,强碱中心适中,有助于CS2水解活性的提高[13]。而当柠檬酸含量增至0.14 g/mL时,吸附剂的弱碱和强碱中心都被破坏,不利于CS2的吸附水解,导致CA0.14-K2CO3/Al2O3吸附剂的脱硫活性低于CA0.07-K2CO3/Al2O3吸附剂。

图3 不同含量柠檬酸改性CA-K2CO3/Al2O3吸附剂的CO2-TPD曲线Fig.3 CO2-TPD curves of CA-K2CO3/Al2O3 adsorbents modified by citric acid at different concentrations.
2.4 FTIR表征结果
图4 为不同含量柠檬酸改性CA-K2CO3/Al2O3吸附剂的FTIR谱图。778 cm-1(AlO4)和582 cm-1(AlO6)两处的峰与Al—O—Al结构有关[21],是氧化铝的特征峰。在3 448 cm-1处发现—OH的特征峰[22],该—OH主要来自于吸附剂上负载的K2CO3和柠檬酸。—OH能够促进CS2吸附和水解反应的发生。柠檬酸改性的FTIR谱图中,—OH发生蓝移,说明柠檬酸与K2CO3发生反应,并引入部分羟基,从而增加羟基吸附和水解CS2的能力。1 396 cm-1和1 577 cm-1两处的峰分别是—COO和—C=O的特征峰[23],与负载的K2CO3和柠檬酸有关。—COO和—C=O能够促进H2S被氧化为S单质[24]。柠檬酸改性后,—COO的峰位置发生红移,—C=O的峰位置发生蓝移,两个峰的强度变大,峰形变尖锐。这主要是因为柠檬酸本身含有的三个羧基,改性后会引入—COO和—C=O基团,增加了—COO和—C=O在吸附剂表面的分布,提高了H2S的转化能力,进而提高CA-K2CO3/Al2O3吸附剂的脱硫活性。

图4 不同含量柠檬酸改性CA-K2CO3/Al2O3吸附剂的FTIR谱图Fig.4 FTIR spectra of of CA-K2CO3/Al2O3 adsorbents modified by citric acid at different concentrations.
3 结论
1)与CA0-K2CO3/Al2O3吸附剂相比,添加柠檬酸改性的吸附剂对C5馏分油中的CS2脱除能力有了很大提升。CA0.07-K2CO3/Al2O3吸附剂能够在1 h内将C5馏分油的硫含量由1 200 μg/mL降至375 μg/mL,比CA0-K2CO3/Al2O3吸附剂提高了322 μg/mL,。
2)添加柠檬酸会改变吸附剂的比表面积、孔径、碱性及官能团的分布。CA0.07-K2CO3/Al2O3吸附剂的比表面积为196.54 m2/g,平均孔径约为4.8 nm,弱碱中心增加,强碱中心适中,这些都有助于CS2的吸附水解。
